| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Carboxyl-terminal domain kinases, such as casein kinase II and cell cycle-dependent kinases (CDK)
|
|---|---|
| 体外研究 (In Vitro) |
在人结肠癌细胞中,5,6-二氯苯并咪唑核苷(10-80 μg/ml,72 小时)抑制 RNA 合成,导致 p53 依赖性死亡 [5]。通过调节 Mcl-1 和 BclxL,5,6-二氯苯并咪唑核苷(10-100 μM,72 小时)促进人 MCF-7 乳腺癌细胞凋亡。并对 caspase 家族成员进行剂量和时间依赖性激活 [6]。
腺苷类似物5,6-二氯-1-β-D-呋喃核糖基苯并咪唑(DRB)是体内和体外RNA聚合酶II转录的特异性抑制剂[Tamm+Sehgal(1978)Adv.Virus Res.22187-258;Zandomeni&Weinmann(1984)J.Biol.Chem.25914804-14811]。对RNA聚合酶II特异性转录的影响似乎是通过其对核酪蛋白激酶II的抑制来介导的[Zandomeni,Carrera Zandomini,Shugar&Weinmann(1986)J.Biol.Chem.2613414-3419]。抑制研究表明,DRB对酪蛋白是一种混合型抑制剂,对核苷酸磷酸供体底物是一种竞争性抑制剂。就ATP和GTP而言,小牛胸腺酪蛋白激酶II的DRB抑制常数为7微M[1] RNA聚合酶II对链延长的调节可以对基因表达产生重要影响(Bentley,D.(1995)Curr。Opin。基因。第5210-216页;Yankulov,K.、Blau,J.、Purton,T.、Roberts,S.和Bentley,D.(1994)《细胞》77749-759);然而,控制转录中这一步骤的机制尚不清楚。腺苷类似物5,6-二氯-1-β-D-呋喃核糖基苯并咪唑(DRB)长期以来一直被用作RNA聚合酶II延长的抑制剂,但其靶标尚不清楚。我们发现DRB是一种与一般转录因子TFIIH相关的Cdk活化激酶的强效抑制剂。该激酶的另外两种抑制剂H-7和H-8也抑制了转录延长。此外,TFIIH激酶特异性结合到单纯疱疹病毒VP16激活结构域,除了启动外,还刺激聚合酶II的延长(Yankulov,K.,Blau,J.,Purton,T.,Roberts,S.和Bentley,D.(1994)Cell 77749-759)。我们的研究结果表明,DRB通过抑制TFIIH相关激酶来影响转录,并且该激酶在RNA聚合酶II的伸长控制中起作用。[2] 大多数现代人类癌症的化疗和放疗都使用DNA损伤途径,该途径诱导p53反应,导致G1期阻滞或细胞凋亡。然而,这种治疗可能会诱导突变和易位,导致继发性恶性肿瘤或复发性疾病,由于对治疗的耐药性,这些疾病的预后往往较差。在这里,我们报告了5,6-二氯-1-β-D-呋喃核糖基苯并咪唑(DRB),一种CDK7 TFIIH相关激酶、CKI和CKII激酶的抑制剂,在早期伸长阶段阻断RNA聚合酶II,以转录非依赖的方式触发人结肠腺癌细胞中p53依赖性凋亡。DRB在不使用DNA损伤的情况下杀死肿瘤衍生细胞的事实,为开发一种新的替代化疗方法来治疗表达野生型p53的肿瘤提供了可能性,从而降低了与治疗相关的继发性恶性肿瘤的风险。[5] 癌症的有效治疗仍然是一个深刻的临床挑战,特别是由于许多患者不幸出现耐药性和转移。转录抑制剂5,6-二氯-1-β-D-呋喃核糖基苯并咪唑(DRB)作为细胞周期蛋白依赖性激酶9的选择性抑制剂,已被证明能有效诱导各种造血恶性肿瘤的细胞凋亡。然而,DRB对乳腺癌症的抗癌效果尚不清楚。在此,我们证明对癌症细胞系施用DRB可抑制细胞增殖并诱导凋亡细胞的典型迹象,包括膜联蛋白V阳性细胞的增加、DNA断裂以及胱天蛋白酶-7、胱天蛋白酶-9和聚ADP核糖聚合酶(PARP)的激活。DRB治疗导致髓细胞白血病1(Mcl-1)蛋白迅速下降,而其他抗凋亡蛋白的水平没有变化。Mcl-1的过表达降低了DRB诱导的PARP切割,而敲除Mcl-1增强了DRB对PARP激活的影响,表明Mcl-1缺失是DRB介导的MCF-7细胞凋亡的原因,但在T-47D中没有。此外,我们发现用AKT抑制剂(LY294002)或蛋白酶体抑制剂(MG-132)共同处理MCF-7细胞显著增强了DRB诱导的凋亡。这些数据表明,DRB与LY294002或MG-132联合使用可能对乳腺癌症细胞具有更大的治疗效力[6]。 |
| 酶活实验 |
蛋白激酶测定[2]
20μl反应包含50 mM KCl、20 mM Tris-HCl、pH 8.0、7 mM MgCl2、2 mM DTT、5 mM 2-甘油磷酸、1μM微囊藻毒素、3.3μg/ml EcoRI线性化pAdH3 DNA、100μg/ml牛血清白蛋白、7.5μM ATP、4μCi的[g32P]ATP、1μg/ml降氨酸、1μg/ml亮肽、1μg/ml胃蛋白酶抑制剂和100 ng VP16亲和柱级分5(图2A除外)或0.1μl纯化的TFIIH(BTF2)HAP级分(Gerard等人,1991)。pAdH3含有腺病毒2的2.1-k激酶SmaI-HindIII片段,包括主要的晚期启动子。底物浓度如下:GST-CTD为40μg/ml,TFIIF为45μg/ml,以及TFIIE为60μg/ml。在这些重组底物中未检测到激酶活性。样品在30°C下用5μM未标记的ATP(和抑制剂,如有指示)预孵育30分钟,然后加入底物和[g-32P]ATP。在30°C下孵育1小时。在这些条件下,激酶反应在3小时以上呈线性。通过加入5μl 5×SDS负载缓冲液终止反应。通过磷光成像仪对固定的干燥凝胶进行定量。 先前描述了从爪蟾卵中免疫沉淀的CAK的蛋白激酶测定(Poon等人,1994)。激酶反应分别与50μg/ml的GST-CTD或GST-Cdk2(K33R)反应。 蛋白激酶底物[2] 免疫亲和纯化的小牛胸腺pol II(Thompson等人,1990)是J.Greenblatt的礼物。含有小鼠CTD的所有52个七肽重复的GST-CTD由pGCTD(Peterson等人,1992)或其衍生物pET21a-GCTD生产。TFIIE p34和p56由R.Tjian博士提供的载体产生。通过将编码His6标签的寡核苷酸插入NdeI位点来修饰p34表达载体。在Ni2+琼脂糖上纯化之前,通过在冰上混合含有两个亚基的细菌细胞裂解物20分钟来分离p56-His6-p34复合物。TFIIF(rap74-rap30)由Z.Burton博士提供的载体表达。通过在NcoI位点插入His6标签来修饰rap74载体,并分离出针对TFIIE的His6-rap74-rap30复合物。激酶缺陷型Cdk2底物GST-Cdk2(K33R)之前已有描述(Poon等人,1994)。 ATP酶测定 ATP酶测定在蛋白激酶反应条件下进行。将0.2μl TFIIH HAP组分、300 ng VP16组分5或5μg HeLa核提取物在30°C下孵育2小时。在这些条件下,ATP酶反应在3小时以上呈线性。通过在7 mM H3P04中加入0.8 ml冰冷的5%活性炭(Sigma)终止反应。将混合物离心,通过计数上清液的等分试样来测量释放的无机磷酸盐。 体外转录[2] 已经描述了RNA酶保护、重组GAL4-AH和GAL4-VP16以及质粒pSPVA(腺病毒VA1)和pGal5-HIV2-CAT的纯化(Yankulov等人,1994)。转录反应(20μl)包含250ng超螺旋质粒pGal5-HIV2-CAT和pSPVA、80μg HeLa核提取物(Dignam等人,1983)、100ng GAL4-AH或GAL4-VP16、1mM MgCl2、1mM亚精胺、4%聚乙二醇8000、0.5mM NTPs、50mM KCl、12mM Hepes、pH 7.9、10μM ZnCl2、2mM DTT、20mM磷酸肌酸、0.01%Nonidet P-40、15单位RNAguard(Pharmacia)。反应在30°C下孵育1小时,通过加入α-鹅膏蕈碱(5μg/ml)、1 mM CaCl2和2μl RQ-DNase I(Promega)停止。在30°C下10分钟后,加入SDS(0.4%)和蛋白酶K(400μg/ml),在37°C下孵育10分钟。使用HIV2和VA的反义探针对反应进行RNase保护处理(Yankulov等人,1994)。 |
| 细胞实验 |
蛋白质印迹分析[5]
细胞类型: LS174T、HT29、SW48 测试浓度: 80 μg/ml 孵育时间: 24 小时 实验结果: [5,6-3H] 尿苷掺入减少,p53 蛋白水平增加。 细胞活力测定[6] 细胞类型: MCF-7、T-47D 测试浓度: 10、50、75,100 μM 孵育时间: 72 小时 实验结果: 以剂量依赖性方式抑制细胞生长。在浓度为 75 μM 时,导致较高的早期凋亡群体(5.7 ± 1.1 vs. 2 ± 0.4%)和晚期凋亡群体(15.9 ± 2.4 vs. 7.7 ± 0.9%)。 蛋白质印迹分析[6] 细胞类型: MCF-7 测试浓度: 75 μM 孵育持续时间:0.5、2、6、10小时 实验结果:以时间依赖性方式降低Mcl-1蛋白水平,并在6小时后增加p53水平。 |
| 参考文献 |
|
| 其他信息 |
RNA聚合酶II转录抑制剂。该化合物通过选择性抑制RNA合成,使转录提前终止。它被用于研究细胞调控的潜在机制。
FIIH激酶在体外可磷酸化RNA聚合酶II的C端结构域(CTD)、TATA结合蛋白以及TFIIF和TFIIE的大亚基(Ohkuma和Roeder,1994;图2B)。这些磷酸化对转录延伸的相对重要性尚未确定。已知延伸因子TFIIF的修饰可能通过稳定其与不稳定的RNA聚合酶II的相互作用来促进转录的持续性(Price等,1989)。 CTD在延伸过程中发挥作用的推测可由以下观察结果得出:RNA聚合酶II在进入起始前复合物以及起始后不久暂停时处于低磷酸化状态,而活跃延伸状态下则处于高磷酸化状态(Lu et al., 1991; O'Brien et al., 1994; Payne et al., 1989; Weeks et al., 1993)。因此,CTD磷酸化的时机似乎与5,6-二氯-1-β-D-呋喃核糖基苯并咪唑(DRB)发挥作用的时间相吻合,即在起始过程中或起始后立即发生(Cisek and Corden, 1989; Kephart et al., 1992)。此外,5,6-二氯-1-β-D-呋喃核糖基苯并咪唑 (DRB) 在体内抑制 CTD 磷酸化(Dubois 等,1994a,1994b)。这些数据与 TFIIH 对 CTD 的磷酸化是 5,6-二氯-1-β-D-呋喃核糖基苯并咪唑 (DRB) 敏感的修饰这一观点相符(Marshall 和 Price,1992;Roberts 和 Bentley,1992;Bentley,1995),该修饰可刺激 pol II 的延伸。[2] |
| 分子式 |
C12H12N2O4CL2
|
|---|---|
| 分子量 |
319.14068
|
| 精确质量 |
318.017
|
| CAS号 |
53-85-0
|
| PubChem CID |
5894
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.8±0.1 g/cm3
|
| 沸点 |
606.2±65.0 °C at 760 mmHg
|
| 熔点 |
222-224ºC
|
| 闪点 |
320.4±34.3 °C
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
| 折射率 |
1.750
|
| LogP |
2.05
|
| tPSA |
87.74
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
20
|
| 分子复杂度/Complexity |
364
|
| 定义原子立体中心数目 |
4
|
| SMILES |
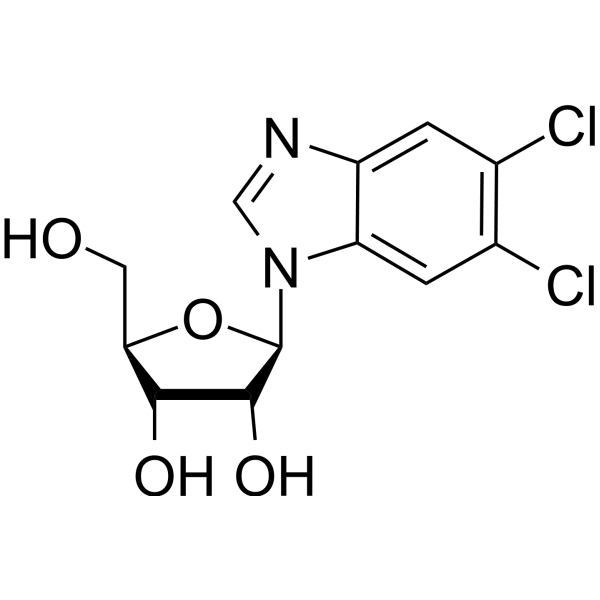
C1=C2C(=CC(=C1Cl)Cl)N(C=N2)[C@H]3[C@@H]([C@@H]([C@H](O3)CO)O)O
|
| InChi Key |
XHSQDZXAVJRBMX-DDHJBXDOSA-N
|
| InChi Code |
InChI=1S/C12H12Cl2N2O4/c13-5-1-7-8(2-6(5)14)16(4-15-7)12-11(19)10(18)9(3-17)20-12/h1-2,4,9-12,17-19H,3H2/t9-,10-,11-,12-/m1/s1
|
| 化学名 |
(2R,3R,4S,5R)-2-(5,6-dichlorobenzimidazol-1-yl)-5-(hydroxymethyl)oxolane-3,4-diol
|
| 别名 |
53-85-0; 5,6-Dichlorobenzimidazole riboside; DRB; Dichlororibofuranosylbenzimidazole; NSC 401575; 5,6-Dichloro-1-beta-D-ribofuranosylbenzimidazole; MFCD00036785; 5,6-Dichloro-1-Beta-D-Ribofuranosyl-1h-Benzimidazole;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~313.34 mM)
DMF : 100 mg/mL (~313.34 mM) Ethanol : ~7.69 mg/mL (~24.10 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (7.83 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (7.83 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (7.83 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.1334 mL | 15.6671 mL | 31.3342 mL | |
| 5 mM | 0.6267 mL | 3.1334 mL | 6.2668 mL | |
| 10 mM | 0.3133 mL | 1.5667 mL | 3.1334 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。