| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
ERK2 (IC50 = 0.6 nM)
C-X-C chemokine receptor type 2 (CXCR2) (Ki = 0.5 nM for human CXCR2; IC₅₀ = 0.9 nM for inhibiting CXCL8 binding to human CXCR2; IC₅₀ = 1.4 nM for inhibiting CXCR2-mediated calcium mobilization); >1000-fold selectivity over CXCR1 (Ki = 420 nM), CXCR3, CXCR4, CCR1, CCR2, CCR5, CCR7 (Ki > 1000 nM for all) [1][2] |
|---|---|
| 体外研究 (In Vitro) |
AZD0364 对 MAPK 途径上的直接下游底物表现出高细胞效力(例如,BRAFV600E 突变 A375 细胞中的磷酸化 p90RSK1 抑制,IC50 = 6 nM)。根据人未磷酸化-ERK2 的 SPR:pKd = 10; t1/2 = 277 分钟[2],该分子在蛋白质上的停留时间较长,是一种高选择性激酶抑制剂(测试的 10/329 个激酶在 1 µM 浓度下抑制率 > 50%)[2]。
CXCR2结合及选择性抑制:AZD-0364是一种二氢咪唑并吡嗪酮衍生物,对人CXCR2具有高结合亲和力(Ki = 0.5 nM),可竞争性阻断CXCL8(IL-8)与人CXCR2表达细胞的结合(IC₅₀ = 0.9 nM)。该化合物对CXCR1的交叉反应性较弱(Ki = 420 nM),浓度高达10 μM时仍未与其他趋化因子受体或G蛋白偶联受体产生显著结合,证实其对CXCR2的高选择性[1][2] - CXCR2功能抑制:在稳定表达人CXCR2的CHO细胞中,AZD-0364剂量依赖性抑制CXCL8诱导的钙流(IC₅₀ = 1.4 nM)和CXCL1介导的趋化(IC₅₀ = 1.7 nM);抑制人中性粒细胞向CXCL8的趋化,IC₅₀ = 2.0 nM,10 nM浓度下抑制率达88%[1] - 癌细胞抗增殖活性:AZD-0364抑制高CXCR2表达的人癌细胞系增殖,包括非小细胞肺癌(NSCLC:A549,IC₅₀ = 3.2 μM;H460,IC₅₀ = 4.5 μM)、结直肠癌(HT-29,IC₅₀ = 5.1 μM;HCT116,IC₅₀ = 6.3 μM)和胰腺癌(PANC-1,IC₅₀ = 4.8 μM)。蛋白质印迹分析显示,A549细胞经10 μM药物处理48小时后,切割型caspase-3和切割型PARP水平升高,表明诱导细胞凋亡[1][2] - 代谢稳定性:人肝微粒体中,AZD-0364的代谢半衰期为105分钟,内在清除率(CLint)为12 μL/min/mg蛋白[1] |
| 体内研究 (In Vivo) |
AZD0364 具有良好的跨物种口服药代动力学。 AZD0364 以剂量依赖性方式抑制异种移植模型肿瘤中的磷酸化 p90RSK1。在 KRAS 突变 NSCLC Calu 6 异种移植模型中,AZD0364 导致回归。在 KRAS 突变 NSCLC 异种移植模型中,AZD0364 也可以与 MEK1/2 抑制剂司美替尼 (selumetinib) 联合安全、成功地使用[2]。
人NSCLC异种移植模型(A549细胞裸鼠移植):口服给予AZD-0364(10、30、60 mg/kg,每日一次,持续21天),剂量依赖性减少肿瘤体积,较溶媒组分别减少42%、65%和78%;30 mg/kg剂量下,肿瘤内中性粒细胞浸润减少60%,微血管密度减少55%,且不影响小鼠体重。肿瘤组织分析显示,促血管生成因子(VEGF、bFGF)和促炎细胞因子(IL-6、TNF-α)表达降低[1][2] - 人结直肠癌异种移植模型(HT-29细胞裸鼠移植):口服给予AZD-0364(30 mg/kg,每日一次,持续28天),较溶媒组减少肿瘤体积62%、降低肿瘤重量58%;抑制肿瘤细胞增殖(Ki-67阳性细胞减少52%),并增强细胞凋亡(TUNEL阳性细胞增加2.3倍)[1] |
| 酶活实验 |
AZD-0364 使用 A375 磷酸化 p90RSK 测定和 ERK2 质谱法进行测量,IC50 值分别为 0.6 nM 和 5.7 nM。作为单一疗法,AZD-0364可以减缓多种癌细胞系(包括具有KRAS突变的A549、H2122、H2009和Calu6细胞系)的生长,而Selumetinib治疗可以进一步增强这种效果。
CXCR2放射性配体结合实验:制备表达人CXCR2的HEK293细胞细胞膜,悬浮于含三羟甲基氨基甲烷-盐酸、氯化镁和0.1%牛血清白蛋白的结合缓冲液中。将系列稀释(0.001–1000 nM)的AZD-0364与细胞膜悬液及氚标记CXCL8混合,25°C孵育90分钟后,通过玻璃纤维滤膜过滤分离结合态与游离态配体。滤膜用冷结合缓冲液洗涤后,液体闪烁计数器测量放射性强度,通过置换曲线的非线性回归分析计算Ki/IC₅₀值[1] - CXCR2介导钙流检测实验:表达CXCR2的CHO细胞用钙敏感荧光染料负载30分钟(37°C)。AZD-0364(0.001–100 nM)与细胞预孵育15分钟后,加入10 nM CXCL8刺激。酶标仪实时检测荧光强度(激发光340/380 nm,发射光510 nm),通过剂量-反应曲线推导IC₅₀值[1][2] - 受体选择性实验:按上述方法制备表达人CXCR1、CXCR3、CXCR4、CCR1、CCR2、CCR5或CCR7的细胞膜。AZD-0364测试浓度最高达10 μM,通过测定结合亲和力(Ki)评估对非靶标受体的选择性[1] |
| 细胞实验 |
KRAS 突变非小细胞肺癌 (NSCLC) A549、H2122、H2009 和 Calu6 细胞系接种于 384 孔黑色透明底板中,培养 18-24 小时,并用浓度不断增加的 AZD-0364 处理( 6×6 剂量基质中的 7.143 nM、61 nM、357 nM、2.143 μM 和 10 μM) 和 Selumetinib (0-10 μM)。细胞以一定密度播种,使得在测定结束时,未经处理的孔中的细胞大约达到 80% 汇合。 Sytox Green 终点用于计算治疗三天后的活细胞数量[1]。
人中性粒细胞趋化实验:通过密度梯度离心从人外周血中分离中性粒细胞,悬浮于RPMI 1640培养基。AZD-0364(0.1–100 nM)与中性粒细胞混合后加入Transwell插入物(5 μm孔径)上室,下室加入10 nM CXCL8,37°C、5% CO₂孵育2小时。血细胞计数板计数下室中的迁移中性粒细胞,计算相对于溶媒对照组的抑制率[1] - 癌细胞增殖实验:人癌细胞(A549、H460、HT-29、HCT116、PANC-1)以5×10³个细胞/孔接种到96孔板,孵育过夜。加入AZD-0364(0.1–40 μM)处理,孵育72小时。采用四唑盐比色法评估细胞活力,计算IC₅₀值[1][2] - 癌细胞凋亡实验:A549细胞以2×10⁵个细胞/孔接种到6孔板,孵育过夜。用AZD-0364(10 μM)处理48小时后,用含蛋白酶/磷酸酶抑制剂的RIPA缓冲液裂解细胞。蛋白质印迹法检测切割型caspase-3、切割型PARP及GAPDH(内参)的表达[1] |
| 动物实验 |
小鼠:A549 是一种人类非小细胞肺癌细胞系,携带 KRAS 基因的 G12S 突变,该突变会导致癌症。将每只雌性裸鼠的 5×10⁶ 个 A549 细胞(ATCC)皮下植入左侧腹部。通过计算肿瘤体积和每周两次的游标卡尺测量来追踪肿瘤生长。将动物分为 7-11 只一组,并采用持续联合用药方案治疗,包括 selumetinib(ARRY-142886,25 mg/kg,每日两次)和 AZD-0364(25 mg/kg,每日一次,在首次服用 selumetinib 四小时后服用)。两种药物均口服给药。给药开始后,每周测量两次肿瘤体积[1]。
人非小细胞肺癌异种移植研究:将2×10⁶个A549细胞皮下接种到雌性裸鼠(6-8周龄,每组n=7)体内。当肿瘤体积达到100-150 mm³时,小鼠通过灌胃给予溶于0.5%甲基纤维素的AZD-0364,剂量分别为10、30和60 mg/kg,每日一次,持续21天。对照组给予0.5%甲基纤维素。每3天测量一次肿瘤体积(V = 长 × 宽² / 2)。治疗结束后,处死小鼠;切除肿瘤以分析中性粒细胞浸润(免疫组织化学)、微血管密度(CD31染色)和细胞因子/VEGF表达(ELISA)[1][2] - 人结直肠癌异种移植研究:将2×10⁶个HT-29细胞皮下接种到6-8周龄的雌性裸鼠(每组n=6)体内。当肿瘤体积达到100-150 mm³时,每天一次通过灌胃给予小鼠AZD-0364(30 mg/kg)或载体,持续28天。每周测量两次肿瘤体积和体重。研究结束时,收集肿瘤组织进行 Ki-67 免疫组化(增殖标志物)和 TUNEL 检测(凋亡标志物)[1] - 大鼠药代动力学研究:雄性 Sprague-Dawley 大鼠(200–250 g,每个时间点 n=5)分别经口灌胃(10 mg/kg)或静脉注射(5 mg/kg)给予 AZD-0364。分别于给药后 0.25、0.5、1、2、4、8、12 和 24 小时采集血样。采用 LC-MS/MS 法测定血浆药物浓度,并使用非房室模型分析计算药代动力学参数[1] |
| 药代性质 (ADME/PK) |
在大鼠中:口服给药(10 mg/kg)可使血浆峰浓度(Cₘₐₓ)达到 2.3 μg/mL,达到 Cₘₐₓ 的时间(Tₘₐₓ)为 1.0 小时,末端半衰期(t₁/₂)为 7.8 小时,分布容积(Vd)为 2.9 L/kg,口服生物利用度为 65%。静脉注射(5 mg/kg)的清除率(CL)为 0.35 L/h/kg [1]
- 在犬中:口服(10 mg/kg)导致 Cₘₐₓ 为 2.8 μg/mL,Tₘₐₓ 为 1.2 小时,t₁/₂ 为 9.5 小时,Vd 为 2.6 L/kg,口服生物利用度为 72% [1] - 组织分布:在大鼠中,口服给药(10 mg/kg)2 小时后,AZD-0364 优先分布于肿瘤组织(组织与血浆比 = 2.4)、肺(2.8)、肝(2.6)、脾(2.2)和肾(2.0);脑组织浓度较低(组织/血浆比值 = 0.2)[1] - 体外代谢:在大鼠肝微粒体中,AZD-0364的代谢半衰期为112分钟;主要代谢途径包括氧化和葡萄糖醛酸化,未检测到毒性代谢物[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
血浆蛋白结合率:AZD-0364 在人血浆中的血浆蛋白结合率为 94%,在大鼠血浆中为 92%,在犬血浆中为 93%(通过超滤法测定)[1]
- 急性毒性:在大鼠和犬中,口服 LD₅₀ >300 mg/kg。在为期 7 天的急性研究中,剂量高达 150 mg/kg 时未观察到明显的毒性(体重减轻、惊厥、死亡)[1] - 亚慢性毒性:在为期 28 天的大鼠重复口服给药研究(10、30、100 mg/kg/天)中,AZD-0364 不会引起体重、血液学参数或肝肾功能的显著变化。主要器官(肝、肾、心、肺、脾)未发现组织病理学异常[1] - 药物相互作用:体外研究表明,浓度高达 10 μM 时,未观察到对细胞色素 P450 酶(CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP3A4)的抑制作用[1] |
| 参考文献 | |
| 其他信息 |
替扎特克是一种口服生物利用度高的细胞外信号调节激酶1 (ERK1) 和2 (ERK2) 抑制剂,具有潜在的抗肿瘤活性。口服后,替扎特克特异性靶向并结合丝氨酸/苏氨酸蛋白激酶ERK1和ERK2,抑制其活性,从而阻止ERK1/2底物的磷酸化以及丝裂原活化蛋白激酶 (MAPK)/ERK介导的信号转导通路的激活。这导致肿瘤细胞ERK依赖性增殖和存活受到抑制。MAPK/ERK通路,也称为RAS/RAF/MEK/ERK通路,由于上游靶基因突变,在多种肿瘤细胞类型中过度激活。它在肿瘤细胞的增殖、分化和存活中起着关键作用。
AZD-0364 是一种强效、高选择性、口服生物利用度高的 CXCR2 拮抗剂,属于二氢咪唑并吡嗪酮衍生物类,已在专利 WO2017080979A1 [1] 中公开。 - 作用机制:与人 CXCR2 竞争性结合,阻断促炎趋化因子(CXCL8、CXCL1)与受体的相互作用,从而抑制下游信号传导(钙动员、趋化性)并抑制中性粒细胞向肿瘤的募集。它还能诱导癌细胞凋亡,并通过降低促血管生成因子的表达来抑制肿瘤血管生成[1][2] - 预期治疗应用:具有高CXCR2表达或富含中性粒细胞的肿瘤微环境的癌症,包括非小细胞肺癌、结直肠癌和胰腺癌[1][2] - 药理学优势:口服生物利用度高(临床前动物模型中为65-72%),半衰期长(7.8-9.5小时),支持每日一次给药,靶组织(肿瘤、肺)分布,毒性低;对CXCR2的高选择性可最大限度地减少脱靶效应[1] |
| 分子式 |
C24H24F2N8O2
|
|
|---|---|---|
| 分子量 |
494.496570587158
|
|
| 精确质量 |
494.2
|
|
| 元素分析 |
C, 58.29; H, 4.89; F, 7.68; N, 22.66; O, 6.47
|
|
| CAS号 |
2097416-76-5
|
|
| 相关CAS号 |
2097416-77-6 (ethanesulonate);2097416-76-5;2097416-93-6 (hemiadipate);
|
|
| PubChem CID |
129116690
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
2
|
|
| tPSA |
103
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
9
|
|
| 可旋转键数目(RBC) |
7
|
|
| 重原子数目 |
36
|
|
| 分子复杂度/Complexity |
768
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
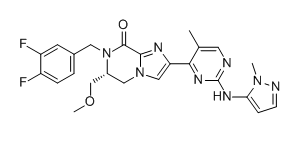
CC1=CN=C(N=C1C2=CN3C[C@@H](N(C(=O)C3=N2)CC4=CC(=C(C=C4)F)F)COC)NC5=CC=NN5C
|
|
| InChi Key |
HVIGNZUDBVLTLU-MRXNPFEDSA-N
|
|
| InChi Code |
InChI=1S/C24H24F2N8O2/c1-14-9-27-24(30-20-6-7-28-32(20)2)31-21(14)19-12-33-11-16(13-36-3)34(23(35)22(33)29-19)10-15-4-5-17(25)18(26)8-15/h4-9,12,16H,10-11,13H2,1-3H3,(H,27,30,31)/t16-/m1/s1
|
|
| 化学名 |
(6R)-7-[(3,4-difluorophenyl)methyl]-6-(methoxymethyl)-2-[5-methyl-2-[(2-methylpyrazol-3-yl)amino]pyrimidin-4-yl]-5,6-dihydroimidazo[1,2-a]pyrazin-8-one
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.21 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0222 mL | 10.1112 mL | 20.2224 mL | |
| 5 mM | 0.4044 mL | 2.0222 mL | 4.0445 mL | |
| 10 mM | 0.2022 mL | 1.0111 mL | 2.0222 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04305249 | Recruiting | Drug: ATG-017 Drug: ATG-017+Nivolumab |
Solid Tumor Hematological Malignancy |
Antengene Therapeutics Limited | August 15, 2020 | Phase 1 |