| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
human CB2 receptor ( Ki = 45.5 nM ); human CB1 receptor ( Ki = 48.3 nM ); rat CB1 receptor ( Ki = 55.4 nM )
Cannabinoid CB1 receptor (rat CB1: Kᵢ = 55.4 nM; human CB1: Kᵢ = 48.3 nM), Cannabinoid CB2 receptor (human CB2: Kᵢ = 45.5 nM) [1] - Human CB1 (hCB1) receptor (EC₅₀ = 46 ± 5 nM, efficacy = 39 ± 11% in cAMP assay) [2] |
|---|---|
| 体外研究 (In Vitro) |
3-[2-氰基-3-(三氟甲基)苯氧基]苯基-4,4,4-三氟-1-丁磺酸酯(BAY 59-3074)是一种新型的选择性大麻素CB1/CB2受体配体(Ki=55.4、48.3和45.5 nM,分别在大鼠和人大麻素CR1和人CB2受体上),在鸟苷5-[γ35S]-硫代磷酸三乙基铵盐([35S]GTPγS)结合试验中对这些受体具有部分激动剂特性[1]。
1. 在鸟苷5-[γ³⁵S]-三磷酸三乙铵盐([³⁵S]GTPγS)结合实验中,BAY 59-3074在大麻素CB1和CB2受体上表现出部分激动剂特性[1] 2. 在稳定表达hCB1受体的中国仓鼠卵巢(CHO)细胞的功能性cAMP实验中,BAY 59-3074的EC₅₀为46±5 nM,效能为39±11%(以完全激动剂CP55940的信号为参照)[2] 3. 分子对接、诱导契合和分子动力学(MD)研究显示,BAY 59-3074结合于hCB1的正构结合位点,其磺酰基区域通过水桥氢键与T197³·³³和W279⁵·⁴³相互作用,并与F268^ECL2、F170²·⁵⁷等芳香族残基发生π-堆叠[2] |
| 体内研究 (In Vivo) |
BAY 59-3074(0.3-3 mg/kg;口服;每日;持续 2 周;雄性 Wistar 大鼠)治疗可改善慢性神经性疼痛和炎性疼痛大鼠模型中针对热或机械刺激的抗痛觉过敏和抗异常疼痛作用。动物模型:雄性 Wistar 大鼠(160-250 g)[1] 剂量:0.3 mg/kg、1 mg/kg 和 3 mg/kg 给药方法:口服;口服;口服。日常的; 2个礼拜。结果:每日给药2周后,神经损伤模型仍能保持镇痛效果。对大麻素相关副作用的耐受性迅速发展(5 天内)。抗痛觉过敏和抗异常疼痛功效得以维持/增强。
BAY 59-3074(0.3-3mg/kg,口服)在慢性神经性(慢性收缩损伤、备用神经损伤、胫神经损伤和脊髓神经结扎模型)和炎性疼痛(卡拉胶和完全弗氏佐剂模型)的大鼠模型中诱导了对热或机械刺激的抗痛觉过敏和抗痛觉过敏作用。BAY 59-3074(1mg/kg,口服)在备用神经损伤模型中的抗异常性疼痛作用在每日给药2周后得以维持。然而,对大麻素相关副作用的耐受性迅速发展(5天内),这些副作用发生在1mg/kg以上的剂量下(如低温)。口服1至32mg/kg的剂量(每4天增加一倍的日剂量)可以防止此类副作用的发生,而抗痛觉过敏和抗痛觉过敏的疗效得以保持/提高。在每天口服1至10mg/kg的14次突然停药后,没有出现停药症状。结论是,BAY 59-3074可能为治疗各种慢性疼痛提供了一种有价值的治疗方法。[1] BAY 59-3074[3-[2-氰基-3-(三氟甲基)苯氧基]苯基-4,4,4-三氟-1-丁烷磺酸盐]是一种结构新颖的大麻素CB1/CB2受体部分激动剂,具有镇痛作用。本研究旨在通过高灵敏度的体内试验确认其受体结合谱。在28次训练后,大鼠(n=10)学会了以固定比例(10,食物强化双杠杆程序)区分BAY 59-3074(0.5mg/kg,口服,t-1h)和载体。BAY 59-3074呈全身剂量依赖性(ED(50):0.081mg/kg,口服),给药后0.25至4小时可检测到提示。选择性大麻素CB1受体拮抗剂SR 141716A[N-(哌啶-1-基)-5-(4-氯苯基)-1-(2,4-二氯苯基)-4-甲基-1H-吡唑-3-甲酰胺盐酸盐]阻断了BAY 59-3074的鉴别作用(ID50:1.79mg/kg,i.p.)。腹腔注射BAY 59-3074(ED50值:0.41 mg/kg)和参考大麻素BAY 38-7271[(-)-(R)-3-(2-羟基甲基茚基-4-氧基)苯基-4,4,4-三氟-1-丁磺酸酯,0.011 mg/kg]、CP 55940[(-”-顺-3-[2-羟基-4(1,1-二甲基庚基)苯基]-反-4-(3-羟基丙基)环己醇,0.013 mg/kg]、HU-210[(-WIN55212-2[(R)-4,5-二氢-2-甲基-4(4-吗啉基甲基)-1-(1-萘羰基)-6H-吡咯并[3,2,1-ij]喹啉-6-酮,0.41mg/kg]和(-)-Delta9-四氢大麻酚(0.41mg/kg)。具有镇痛作用的非大麻素,如吗啡、阿米替林、卡马西平、加巴喷丁和巴氯芬,并没有推广到这一线索。结论是BAY 59-3074的鉴别刺激作用是由大麻素CB1受体激活特异性介导的[3]。 1. 在大鼠慢性神经病理性疼痛模型(慢性压迫性损伤[CCI]、保留神经损伤[SNI]、胫神经损伤、脊神经结扎)和炎症疼痛模型(角叉菜胶、完全弗氏佐剂)中,BAY 59-3074(0.3-3 mg/kg,口服)对热/机械刺激诱导的痛觉过敏和异常性疼痛表现出剂量依赖性的拮抗效应[1] 2. 在SNI模型中,BAY 59-3074(1 mg/kg,口服)每日给药2周后,其抗异常性疼痛的疗效仍能维持;剂量超过1 mg/kg时出现的大麻素相关副作用(如体温过低)在5天内快速产生耐受,而将剂量从1 mg/kg逐步增至32 mg/kg(每4天加倍)可避免副作用,且抗痛觉过敏和抗异常性疼痛的疗效得以维持或增强[1] 3. 大鼠经14天每日口服1-10 mg/kg BAY 59-3074后突然停药,未观察到戒断症状[1] 4. 在大鼠热板实验中,BAY 59-3074的镇痛和体温过低效应可被CB1受体拮抗剂SR 141716A阻断;在药物辨别实验中,BAY 59-3074诱导的辨别线索也可被SR 141716A阻断[1] 5. 在大鼠药物辨别实验中,以口服0.5 mg/kg BAY 59-3074进行训练后,该药物的辨别线索呈现剂量依赖性泛化,口服ED₅₀为0.081 mg/kg,腹腔注射ED₅₀为0.41 mg/kg;SR 141716A对其辨别效应的阻断ID₅₀为1.79 mg/kg(腹腔注射)[3] 6. 参考大麻素类药物(BAY 38-7271、CP 55,940、HU-210、WIN 55,212-2、(-)-Δ⁹-THC)可完全泛化至BAY 59-3074的辨别线索,而非大麻素类镇痛药(吗啡、阿米替林、卡马西平、加巴喷丁、巴氯芬)无此交叉泛化现象[3] 7. C57BL6小鼠腹腔注射3 mg/kg BAY 59-3074后,其脑内最大浓度(Cmax)约为341 ng/mL,脑:血浆Cmax比值为0.40[2] |
| 酶活实验 |
放射性配体置换试验[2]
使用[3H]CP55940的放射性配体置换对21进行了进一步表征,并如前所述确定了平衡解离常数(Ki)值。报告的数据是3次测量的平均值,标准误差<30%。 1. 测定Kᵢ值的受体结合实验:将表达大鼠CB1、人CB1和人CB2受体的膜制剂与BAY 59-3074及放射性标记的大麻素受体配体共同孵育,通过检测放射性配体的置换程度,计算BAY 59-3074对各受体亚型的结合亲和力(Kᵢ)[1] 2. 检测激动活性的[³⁵S]GTPγS结合实验:将含CB1/CB2受体的膜制剂与BAY 59-3074、GDP及[³⁵S]GTPγS共同孵育,通过测定膜中[³⁵S]GTPγS的掺入量,评估BAY 59-3074在CB1和CB2受体上的部分激动活性[1] 3. 测定hCB1结合亲和力的放射性配体置换实验:将过表达hCB1的CHO细胞膜制剂与[³H]CP55940及系列稀释的BAY 59-3074共同孵育,通过检测放射性配体的置换情况,确定平衡解离常数(Ki)[2] |
| 细胞实验 |
cAMP积累测定[2]
使用Lance™检测试剂盒在标准细胞培养条件下(37°C,5%二氧化碳,含1%青霉素/链霉素和400µg/mL G418的DMEM培养基)培养的稳定表达人CB1受体(hCB1)的中国仓鼠卵巢(CHO)细胞中进行cAMP检测,并严格遵循制造商的说明。简而言之,制备了含有1X Hank's平衡盐溶液(HBSS)、5 mM HEPES、0.1%BSA稳定剂和0.5 mM最终IBMX的刺激缓冲液,并在室温下滴定至pH 7.4。将测试化合物和300 nM毛喉素的连续稀释液(均以刺激缓冲液中所需终浓度的4倍制备)加入96孔白色½面积微孔板中。CHO-hCB1细胞用非酶溶液提起,每个孔中加入4000个细胞。在室温下孵育30分钟后,按照制造商的说明加入Eu-cAMP示踪剂和uLIGHT抗-cAMP工作溶液。孵育1小时后,在CLARIO星型多模读板器上读取TR-FRET信号(例如337nm、em 620和650nm)。使用Prism软件分析数据。进行非线性回归分析以拟合数据并获得最大响应(Emax)、EC50、相关系数(r2)和其他参数。所有实验均重复进行2-3次,以确保再现性,除非另有说明,否则数据以平均值±平均值的标准误差报告。 1. CHO-hCB1细胞的cAMP积累实验:将稳定表达hCB1的CHO细胞在标准条件下(37 ℃、5% CO₂、含1%青霉素/链霉素和400 µg/mL G418的DMEM培养基)培养,用非酶溶液消化后接种于96孔板(4000个细胞/孔)。加入系列稀释的BAY 59-3074和福斯高林(300 nM),室温孵育30分钟后,加入Eu-cAMP示踪剂和uLIGHT-抗cAMP工作液,检测TR-FRET信号(激发光337 nm,发射光620/650 nm)以测定cAMP水平,评估BAY 59-3074的激动活性[2] |
| 动物实验 |
雄性Wistar大鼠(160-250克)
0.3毫克/千克、1毫克/千克和3毫克/千克 口服给药;每日;持续 2 周。 在大鼠中,BAY 59-3074 对大麻素 CB(1) 受体激动剂 (-)-(R)-3-(2-羟甲基茚基-4-氧基)苯基-4,4,4-三氟-1-丁烷磺酸盐 (BAY 38-7271) 在药物辨别程序中诱导的线索的泛化,以及其在热板试验中的降温和镇痛作用,均被大麻素 CB(1) 受体拮抗剂 N-(哌啶-1-基)-5-(4-氯苯基)-1-(2,4-二氯苯基)-4-甲基-1H-吡唑-3-甲酰胺盐酸盐 (SR 141716A) 阻断。 BAY 59-3074(0.3-3 mg/kg,口服)在慢性神经性疼痛(慢性压迫损伤、神经保留损伤、胫神经损伤和脊神经结扎模型)和炎症性疼痛(角叉菜胶和弗氏完全佐剂模型)大鼠模型中,对热刺激或机械刺激引起的痛觉过敏和异常性疼痛均表现出抗痛觉过敏和抗异常性疼痛作用。在神经保留损伤模型中,每日给药 2 周后,BAY 59-3074(1 mg/kg,口服)的抗异常性疼痛疗效仍得以维持。然而,超过 1 mg/kg 的剂量即可出现与大麻素相关的副作用(例如体温过低),这些副作用会在 5 天内迅速产生耐受性。将剂量从 1 mg/kg 递增至 32 mg/kg(每 4 天剂量加倍)可预防此类副作用的发生,同时维持或增强其抗痛觉过敏和抗异常性疼痛疗效。在连续14天每日口服1至10 mg/kg剂量后突然停药,未观察到戒断症状。由此得出结论,BAY 59-3074可能为治疗多种慢性疼痛提供一种有价值的治疗方法。[1] 药代动力学测试[2] 本实验室饲养雌性C57BL/6小鼠,并在约10周龄时用于药代动力学(PK)测试。每个时间点测试三只动物。所有药物均配制于2% NMP的菜籽油溶液中,并以3 mg/kg的剂量通过腹腔注射(IP)给药。分别于给药后0.5、1、2和4小时采集组织。在采集组织前,对动物进行全身生理盐水灌注。脑组织样本用50:50乙醇:水(1:5, v/v)匀浆。取40 µL匀浆、10 µL乙腈和150 µL浓度为100 ng/mL的利血平(溶于含0.1%甲酸的乙腈溶液)涡旋混匀后离心。血浆样品用10 µL乙腈和150 µL浓度为100 ng/mL的利血平(溶于含0.1%甲酸的乙腈溶液)稀释,涡旋混匀后离心。样品进行LC/MS/MS分析。标准品在空白样品中制备,用于绘制校准曲线。色谱柱为Phenomenex Luna C18柱。大鼠慢性疼痛模型方案(神经性疼痛:CCI、SNI、胫神经损伤、脊神经结扎;炎症性疼痛:角叉菜胶、CFA):对大鼠进行手术以诱导慢性神经性疼痛,或注射角叉菜胶/CFA以诱导炎症性疼痛。BAY 59-3074以0.3-3 mg/kg的剂量口服给药,并在特定时间点评估热痛觉过敏/机械痛觉过敏/异常性疼痛。对于SNI模型,BAY 59-3074(1 mg/kg,口服)每日给药2周以评估耐受性;在剂量递增研究中,剂量每4天加倍,从1 mg/kg口服至32 mg/kg [1] 2.大鼠药物辨别实验(参考文献1和3):训练大鼠在固定比例10、食物强化双杆实验中区分BAY 59-3074(0.5 mg/kg,口服,测试前1小时)和溶剂对照。训练后,用不同剂量的BAY 59-3074(口服/腹腔注射)或其他大麻素对大鼠进行测试,并记录其选择操作杆的情况以评估泛化效果。使用CB1受体拮抗剂SR 141716A阻断BAY 59-3074的辨别效应[1] 3. 大鼠热板实验:将大鼠置于温度固定的热板上,测量其舔爪/跳跃的潜伏期以评估镇痛效果。给予小鼠 BAY 59-3074 后,监测体温以评估其低体温效应;同时给予 SR 141716A 以确认 CB1 受体介导的效应 [1] 4. 小鼠药代动力学 (PK) 试验:雌性 C57BL/6 小鼠(约 10 周龄)腹腔注射 BAY 59-3074,剂量为 3 mg/kg(溶于 2% NMP 的菜籽油中)。分别于给药后 0.5、1、2 和 4 小时采集组织(脑/血浆)。将脑组织用 50:50 乙醇:水匀浆,并将血浆/脑匀浆液用乙腈和利血平内标进行处理,然后进行 LC/MS/MS 分析 [2] |
| 药代性质 (ADME/PK) |
1. 在腹腔注射3 mg/kg BAY 59-3074的C57BL6小鼠中:脑内最大浓度(Cmax)约为341 ng/mL,脑/血浆Cmax比值为0.40,且该化合物在测试时间点内逐渐在脑内积累[2]
|
| 毒性/毒理 (Toxicokinetics/TK) |
1. 在大鼠中,口服剂量超过 1 mg/kg 的 BAY 59-3074 会引起大麻素相关副作用(例如体温过低),并且每日给药 5 天内即可迅速产生耐受性 [1]
2. 将 BAY 59-3074 的剂量从 1 mg/kg 递增至 32 mg/kg(每 4 天将每日剂量加倍)可预防副作用(例如体温过低)的发生 [1] |
| 参考文献 |
|
| 其他信息 |
4,4,4-三氟-1-丁烷磺酸是一种芳香醚。
选择性调节外周大麻素受体 (CBR) 在多种疾病的治疗中具有潜在的应用价值,包括肥胖症、糖尿病、肝病、胃肠道疾病和疼痛。尽管人们已投入大量精力来开发 CBR 的选择性拮抗剂或完全激动剂,但关于部分激动剂的研发报道却十分有限。靶向外周 CBR 的部分激动剂可能具有理想的药理学特性,同时不会产生中枢介导的解离效应。拜耳公司曾报道,BAY 59-3074 是一种可穿透中枢神经系统、同时作用于 CB1 和 CB2 受体的部分激动剂,在神经性疼痛和炎症性疼痛的大鼠模型中显示出疗效。在本报告中,我们将展示我们合成类似物的努力,这些类似物旨在提高外周选择性,同时保持对 CB1 的部分激动作用。我们的研究最终鉴定出一种新型化合物,它是人CB1 (hCB1)受体的部分激动剂,与BAY 59-3074相比,其脑暴露量显著降低。[2] 化合物1(BAY 59-3074)的构效关系研究将有助于开发中枢神经系统渗透性更佳的化合物。近期hCB1的晶体结构以及与化合物1的分子对接研究表明,磺酸酯连接基靠近结合口袋的极性区域,因此可以用极性氢键供体连接基取代,以促进外周选择性类似物的开发。初步结果证实了这一点,但控制其效力水平仍然具有挑战性。效力和疗效受连接基、连接的基团以及核心取代模式的相互影响。虽然尚未明确化合物1开发外周部分激动剂的构效关系,但我们鉴定出了两种具有改进物理性质的hCB1部分激动剂。将核心取代模式由间位改为对位,并将磺酸酯连接基替换为酰胺基,得到苄酰胺 24,该化合物具有氢键供体,并且在 cAMP hCB1 测定中表现出部分激动剂活性。将连接基替换为磺酰胺基,并将烷基链替换为环己基,得到磺酰胺 21,该化合物在 cAMP hCB1 测定中也表现出部分激动剂活性。化合物 21 的物理性质已显著有利于其外周选择性(TPSA = 91,cLogP = 4.2,氢键供体 = 2)。药代动力学研究证实了这一点,结果表明该化合物的脑浓度显著低于化合物 1。基于化合物 21 和 24 的进一步构效关系研究有望为获得具有所需特性的化合物提供线索。这些化合物在 hCB2 上的活性和功效尚未得到检验,这将构成未来研究的基础,并可能进行体内效应检验。[2] 3-[2-氰基-3-(三氟甲基)苯氧基]苯基-4,4,4-三氟-1-丁烷磺酸盐 (BAY 59-3074) 是一种新型的选择性大麻素 CB(1)/CB(2) 受体配体(在大鼠和人大麻素 CB(1) 和人 CB(2) 受体上的 K(i) 分别为 55.4、48.3 和 45.5 nM),在鸟苷 5-[γ(35)S]-硫代磷酸三乙铵盐 ([(35)S]GTPγS) 结合试验中,对这些受体具有部分激动剂特性。在大鼠中,BAY 59-3074 对大麻素 CB(1) 受体激动剂 (-)-(R)-3-(2-羟甲基茚基-4-氧基)苯基-4,4,4-三氟-1-丁烷磺酸盐 (BAY 38-7271) 在药物辨别程序中诱导的线索的泛化,以及其在热板试验中的降温和镇痛作用,均可被大麻素 CB(1) 受体拮抗剂 N-(哌啶-1-基)-5-(4-氯苯基)-1-(2,4-二氯苯基)-4-甲基-1H-吡唑-3-甲酰胺盐酸盐 (SR 141716A) 阻断。[1] 1. BAY 59-3074是一种新型选择性大麻素CB1/CB2受体部分激动剂,具有抗痛觉过敏和抗异常性疼痛作用,可能为治疗多种慢性疼痛疾病提供一种有价值的治疗方法[1] 2. BAY 59-3074是一种可穿透血脑屏障的CB1/CB2受体部分激动剂;对其结构进行修饰以开发外周选择性类似物,从而减少其在大脑中的暴露[2] 3. BAY 59-3074在大鼠中的辨别性刺激效应特异性地由大麻素CB1受体激活介导,不会泛化至非大麻素类镇痛药[3] |
| 分子式 |
C18H13NO4F6S
|
|---|---|
| 分子量 |
453.35552
|
| 精确质量 |
453.047
|
| 元素分析 |
C, 59.99; H, 5.03; F, 4.52; N, 26.65; O, 3.81
|
| CAS号 |
406205-74-1
|
| PubChem CID |
10479060
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.496g/cm3
|
| 沸点 |
490.569ºC at 760 mmHg
|
| 闪点 |
250.488ºC
|
| 折射率 |
1.521
|
| LogP |
6.501
|
| tPSA |
84.77
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
11
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
30
|
| 分子复杂度/Complexity |
709
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O=S(CCCC(F)(F)F)(OC1=CC=CC(OC2=CC=CC(C(F)(F)F)=C2C#N)=C1)=O
|
| InChi Key |
LWUSZIVDPJPVBW-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C18H13F6NO4S/c19-17(20,21)8-3-9-30(26,27)29-13-5-1-4-12(10-13)28-16-7-2-6-15(14(16)11-25)18(22,23)24/h1-2,4-7,10H,3,8-9H2
|
| 化学名 |
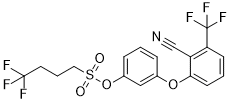
[3-[2-cyano-3-(trifluoromethyl)phenoxy]phenyl] 4,4,4-trifluorobutane-1-sulfonate
|
| 别名 |
BAY59-3074; BAY-593074; BAY-59-3074; BAY 59-3074; BAY 593074; BAY-59-3074; 1-Butanesulfonic acid, 4,4,4-trifluoro-, 3-(2-cyano-3-(trifluoromethyl)phenoxy)phenyl ester; BAY-593074; 5FO5Z101GU; CHEMBL1354658; 3-(2-Cyano-3-(trifluoromethyl)phenoxy)phenyl 4,4,4-trifluorobutane-1-sulfonate; BAY593074
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~91 mg/mL (~200.7 mM)
Ethanol: ~91 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.51 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2058 mL | 11.0288 mL | 22.0575 mL | |
| 5 mM | 0.4412 mL | 2.2058 mL | 4.4115 mL | |
| 10 mM | 0.2206 mL | 1.1029 mL | 2.2058 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。