| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Ionizable cationic lipid; siRNA delivery
D-Lin-MC3-DMA does not act through recognition of specific protein targets but rather through a physicochemical mechanism known as “endosomal escape,” enabled by its unique ionizable lipid properties. With a pKa value of approximately 6.2-6.4, the lipid is essentially neutral at physiological pH (7.4), which helps reduce non-specific interactions in the circulation and systemic toxicity. Upon cellular uptake via endocytosis, the acidic endosomal environment (pH ~5.0) protonates its tertiary amine group, conferring a positive charge. This positively charged lipid then interacts electrostatically with negatively charged endosomal membrane lipids, inducing a transition from a lamellar to a hexagonal phase that disrupts the endosomal membrane and releases the nucleic acid cargo into the cytoplasm. |
|---|---|
| 体外研究 (In Vitro) |
含LNP质粒的制备[1]
LNP-pDNA的制备如之前在J Phys Chem B,119(28)(2015),第8698-8706页中所述。将氨基脂质、辅助脂质、胆固醇和PEG-DMG以50/10/39/1的摩尔比溶解在乙醇中。将纯化的pCI-FLuc(表达萤火虫荧光素酶)或pCAX-eGFP(表达eGFP)溶解在pH 4至0.116mg/ml的25mM乙酸钠中。使用微型混合器混合溶液。对于大规模制剂,如Pharm Res,22(3)(2005),第362-372页所述,通过T型接头混合器进行混合。除非另有说明,否则所有制剂均以每μmol脂质0.029mg DNA的浓度生产(对应于N/P电荷比为6.0)。 含DNA脂质颗粒分析[1] 粒径、脂质浓度、pDNA包埋和总pDNA浓度如之前在J Phys Chem B,119(28)(2015),第8698-8706页和J Control Release,196(2014),第106-112页中所述进行测量。Zeta电位的测量方法如前所述,见《分子无机酸》,3(2014),第e210页。 含有二硬脂酰磷酸胆碱(DSPC)的脂质纳米粒(LNPs)和可电离的氨基脂质,如二氢吲哚甲基-4-二甲氨基丁酸酯(DLin-MC3-DMA),是体内有效的siRNA递送载体。在这里,我们探索了类似的LNP系统作为质粒DNA(pDNA)转染试剂的实用性。结果表明,用不饱和PC替代DSPC,用相关脂质DLin-KC2-DMA替代DLin-MC3-DMA,可在体外产生高效的HeLa细胞转染试剂。此外,这些制剂在各种哺乳动物细胞系中表现出优异的转染性能,在原代细胞培养中的转染效率接近90%。这些转染水平等于或大于Lipofectamine所达到的水平,毒性大大降低[1]。 在体外实验中,D-Lin-MC3-DMA主要表现为其作为核酸递送载体的功能活性。研究表明,包裹有D-Lin-MC3-DMA的脂质纳米颗粒能够将荧光素酶质粒DNA(pCI-FLuc)有效递送至HeLa细胞,在DNA浓度为0.75-6.0 μg/mL时观察到显著的荧光素酶表达。在登革热病毒研究中,装载抗DENV siRNA的D-Lin-MC3-DMA脂质体在HepG2细胞中显著降低了病毒滴度(siRNA工作浓度40 nM),同时未引起细胞毒性、溶血或促炎性细胞因子的释放。此外,将D-Lin-MC3-DMA共价偶联至siRNA后,在细胞培养中能够增强siRNA的内体逃逸能力,且不干扰RNA诱导沉默复合体的活性。有研究报道,含CD44靶向肽修饰的D-Lin-MC3-DMA脂质纳米颗粒(AKPC-LNP)在CD44高表达乳腺癌细胞中,可使YAP/TAZ siRNA的基因沉默效率达到70-80%。 |
| 体内研究 (In Vivo) |
有效的内部 siRNA 递送载体是含有可电离磷酸酯的磷酸盐纳米粒子 (LNP),例如二亚油基甲基-4-二甲基磷酸酯 (DLin-MC3-DMA) 和二硬脂基乙酰磷脂酰胆碱 (DSPC)。 LNP-siRNA 系统程序的摩尔比为 50/10/38.5/1.5 (PEG)-Pallet,经过调整,可在静脉注射后在肝细胞中实现最大的基因沉默功效。它包含DLin-MC3-DMA (MC3)、DSPC、溶液和聚合溶液。 DLin-MC3-DMA 改进的 pKa 值大大提高了功效 [1]。
在小鼠中,当siRNA剂量为1mg/kg时,与MC3的LNPs相比,ALC-0315的LNPs对FVII和ADAMTS13的敲除分别高出2倍和10倍。在高剂量(5mg/kg)下,ALC-0315 LNPs增加了肝毒性标志物(ALT和胆汁酸),而相同剂量的MC3 LNPs则没有。这些结果表明,ALC-0315 LNPs在小鼠肝细胞和HSC中实现了siRNA介导的靶蛋白的有效敲除,尽管在高剂量后可以观察到肝毒性的标志物。本研究提供了一个初步的比较,可能为开发具有最大疗效和有限毒性的可电离阳离子LNP疗法提供信息。[2] D-Lin-MC3-DMA是经过体内验证的最强效siRNA递送脂质之一。在小鼠凝血因子VII模型中,采用优化配方(摩尔比MC3/DSPC/胆固醇/PEG-脂质 = 50/10/38.5/1.5)的LNP-siRNA系统,其ED₅₀低至0.005 mg/kg,相比第一代脂质DLinDMA的效力提升了两个数量级以上。D-Lin-MC3-DMA共价偶联的siRNA在小鼠体内展现出与胆固醇偶联siRNA相似的组织分布特征,但更倾向于在血管区室中蓄积。靶向CD44的AKPC-LNP(含D-Lin-MC3-DMA)在斑马鱼异种移植模型中显著抑制乳腺癌生长,肿瘤负荷减少近100%,且未观察到明显毒性。此外,D-Lin-MC3-DMA也是首款获批siRNA药物Onpattro的核心脂质成分,临床证实能有效将patisiran递送至肝细胞以沉默TTR基因表达。 |
| 酶活实验 |
D-Lin-MC3-DMA并非典型的与酶或受体结合的化合物,它的功能依赖于脂质纳米颗粒的组装和物理化学性质。在非细胞体系中评价其性质时,主要关注其脂质特性:可将其溶解于无水乙醇(溶解度≥60 mg/mL)制备储存液。通过动态光散射(DLS)测定LNP的粒径(通常在80-120 nm)、多分散系数(PDI<0.2)和Zeta电位(生理pH下接近中性)。采用RiboGreen染料法测定siRNA的包封率(典型值>90%)。可电离特性的评估可通过监测不同pH值(从pH 4.0到pH 7.4)下脂质表面电荷的变化,或通过测定pKa值(约6.44)来完成。还可通过差示扫描量热法或荧光探针法考察脂质膜的流动性及与内体膜的融合能力。
|
| 细胞实验 |
培养细胞的体外转染研究[1]
HeLa、HepG2和Hep3B细胞在含有10%FBS的DMEM中培养。PC12和MCF7细胞在含有10%FBS的RPMI 1640中培养。LNPs以0.75-6.0μg/ml pDNA稀释到培养基中。治疗后24小时进行萤光素酶测定。在无血清治疗的情况下,LNP-pDNA系统仅稀释到培养基中。为了研究ApoE的作用,从杰克逊实验室购买了野生型(C57BL/6)和ApoE-/-(B6.129P2-Poetm1Unc/J)小鼠血清。将LNP-pDNA系统稀释到含有每种血清10%的培养基中。将测量的发光归一化为皮尔斯BCA蛋白测定法测量的蛋白质含量。 体外LNP摄取测量[1] 如前所述,进行了LNP制剂的细胞摄取。使用了29个用DiI-C18(总脂质0.2 mol%)标记的LNP pDNA。使用Cellomics Arrayscan VTI HCS阅读器对板进行成像。 D-Lin-MC3-DMA的体外细胞实验通常关注其作为核酸递送载体的效率。典型流程:1)采用微流控装置或乙醇注射法制备LNP:将D-Lin-MC3-DMA、DSPC、胆固醇和PEG-脂质以特定摩尔比(如50/10/38.5/1.5)溶解于乙醇中,与含核酸的柠檬酸缓冲液(pH 4.0)按3:1体积比快速混合。2)纯化:通过透析或超滤去除乙醇并置换缓冲液至PBS。3)细胞处理:将目标细胞(如HeLa、HepG2或乳腺癌细胞)接种于培养板(每孔约1×10⁴-1×10⁵个细胞),加入含LNP的培养基(核酸浓度0.75-6.0 μg/mL),37°C孵育24-48小时。4)效果评估:通过流式细胞术检测荧光报告基因表达,通过RT-qPCR或Western blot检测靶基因沉默效率(如YAP/TAZ下调70-80%)。 |
| 动物实验 |
通过注射LNP-pDNA进行体内转染[1]
将处于19-20期的白来航鸡胚胎用中性红染色,并在前肢胚外膜上撕开一个小口。使用Picospritzer II微量注射器(Parker Hannifin公司),将与约0.1%快绿染料混合的LNP制剂以10 μg/ml pDNA的浓度注射到远端前肢。将胚胎孵育过夜。冲洗胚胎并用4%多聚甲醛PBS溶液固定,然后使用Leica MZFLIII立体荧光显微镜记录GFP荧光。 原代胚胎间充质转染及试剂毒性分析[1] 取出处于24期的白来航鸡胚胎,并在Hanks平衡盐溶液(HBSS)中进行解剖。将前肢集中起来,用分散酶处理1小时以去除上皮外胚层。将肢体间充质组织解离,并重悬于含5%胎牛血清(FBS)和1%青霉素/链霉素的DMEM培养基中。将细胞以2 × 10⁵或2 × 10⁷个细胞/ml的密度接种于96孔板中,并用0-40 μg/ml的LNP-pDNA处理。按照制造商的说明书使用Lipofectamine进行转染。将细胞在37℃培养过夜,然后用PBS缓冲液重悬,使用BD LSRII流式细胞仪进行表达分析。在低密度培养物中,处理24小时后,通过计数PBS洗涤后剩余的贴壁细胞来评估细胞存活率。细胞活力基于单个视野(100倍)内所有贴壁细胞的平均计数,并以未处理培养物的细胞计数进行标准化来确定。 LNP-siRNA注射[2] siFVII、siADAMTS13和siLuc被封装在含有ALC-0315或MC3作为可电离阳离子脂质的LNP中。我们给小鼠注射1 mg/kg体重的siRNA用于基因敲低研究,注射5 mg/kg剂量用于毒性研究。1 mg/kg siRNA剂量是使用siRNA-LNP诱导肝细胞中蛋白质mRNA敲低的标准剂量,而5 mg/kg剂量则高于小鼠的常用剂量。3 ONPATTRO(临床批准的用于治疗hATTR的siRNA)的推荐剂量为0.3 mg/kg,根据体表面积换算,其在小鼠中的等效人剂量(HED)为3.69 mg/kg。给药一周后,采集肝组织和血液样本,分别检测靶mRNA和蛋白水平,并与siLuc处理组小鼠进行比较;血浆FVII和ADAMTS13的半衰期分别为3-6小时和2-3天23,24。mRNA和蛋白定量以及毒性研究将在下文进一步描述。 毒理学分析[2] 小鼠静脉注射PBS,或分别用ALC-0315(siLuc-ALC-0315)或MC3(siLuc-MC3)包封的siLuc脂质纳米颗粒(LNP),剂量为5 mg/kg(n = 4)。虽然任何LNP在10 mg/kg剂量下通常都会引起严重的毒性,例如炎症和肝坏死,但5 mg/kg剂量下的毒性取决于脂质配方26,27。注射5小时后,处死小鼠,并按上述方法采集血清样本。血清样本送至Idexx BioAnalytics进行毒理学检测。分析了天冬氨酸氨基转移酶(AST)、碱性磷酸酶(ALP)、丙氨酸氨基转移酶(ALT)、胆汁酸、总胆红素(TBIL)、血尿素氮(BUN)、肌酸(CREA)和γ-谷氨酰转移酶(GGT)的水平。需要注意的是,由于PBS组和siLuc-ALC-0315组各存在一个异常值(数据未显示),因此两组小鼠的胆汁酸水平数据样本量均为N=3。即使存在这些异常值,结论也不会改变;siLuc-ALC-0315组小鼠的胆汁酸平均值会更高,与PBS组小鼠的差异也更具统计学意义。异常值采用GraphPad Prism软件的ROUT方法进行识别,但同时也考虑到了样本量较小的局限性。胆汁酸水平通常在 0 至 6 μmol/L 之间;然而,我们的结果在生物学上可能是不可能的(>130 μmol/L)。 D-Lin-MC3-DMA的体内动物实验主要用于评估LNP-siRNA系统的药效和分布。标准流程:1)动物准备:使用6-8周龄雌性C57BL/6小鼠。2)LNP-siRNA配制:采用微流控技术制备含D-Lin-MC3-DMA的LNP(摩尔比MC3/DSPC/胆固醇/PEG-脂质=50/10/38.5/1.5),包载靶向特定基因的siRNA(如凝血因子VII或YAP/TAZ)。3)给药方式:通过尾静脉静脉注射,注射体积10 mL/kg,siRNA剂量范围0.005-1 mg/kg。4)检测终点:给药后24-72小时处死动物,收集肝脏等组织,通过RT-qPCR检测靶mRNA水平,或通过ELISA/Western blot检测蛋白表达。5)组织分布:可采用荧光标记的siRNA(如Cy5-siRNA)示踪,或通过LC-MS/MS测定组织中D-Lin-MC3-DMA的含量。 |
| 药代性质 (ADME/PK) |
D-Lin-MC3-DMA作为脂质纳米颗粒的组分,其药代动力学特性与普通小分子药物显著不同。当以LNP形式静脉注射后,颗粒主要被血浆中的载脂蛋白E调理,通过肝脏低密度脂蛋白受体介导的内吞作用主动靶向肝脏。该脂质在生理pH下呈电中性,有助于延长血液循环时间并减少非特异性摄取。在体内,D-Lin-MC3-DMA共价偶联的siRNA显示出与胆固醇偶联siRNA相似的组织分布特征,但独特地蓄积于血管区室。LNP的粒径通常在80-120 nm,这是避免肾脏快速清除并促进肝脏被动靶向的理想尺寸范围。关于D-Lin-MC3-DMA的终末半衰期和代谢途径,目前公开的数据有限,但该脂质被设计为可生物降解的,以避免在肝脏中过度蓄积。
|
| 毒性/毒理 (Toxicokinetics/TK) |
D-Lin-MC3-DMA及相关LNP制剂的毒性与配方组成、剂量、给药途径和靶组织密切相关。在临床前研究中,优化的D-Lin-MC3-DMA LNP(如Onpattro中的配方)在小鼠模型中ED₅₀低至0.005 mg/kg,在治疗剂量下未观察到显著毒性。然而,一项重要的毒理学发现是:当D-Lin-MC3-DMA共价偶联的siRNA在组织中蓄积水平较高时(>20 pmol/mg组织),会观察到非特异性的基因表达调控。这种效应很可能是由未结合的游离脂质引起,提示直接共价偶联策略存在潜在风险,需要在增强内体逃逸和降低毒性之间进行精细平衡。在体外实验中,装载siRNA的D-Lin-MC3-DMA脂质体(40 nM)未引起细胞毒性或溶血。D-Lin-MC3-DMA仅供科研使用,不得用于人体。
|
| 参考文献 | |
| 其他信息 |
含有二硬脂酰磷脂酰胆碱 (DSPC) 和可电离氨基脂质(例如二亚油酰甲基-4-二甲基氨基丁酸酯 (DLin-MC3-DMA))的脂质纳米颗粒 (LNP) 是体内有效的 siRNA 递送载体。本文探讨了类似 LNP 系统作为质粒 DNA (pDNA) 转染试剂的应用。结果表明,用不饱和磷脂酰胆碱 (PC) 替代 DSPC,用相关脂质 DLin-KC2-DMA 替代 DLin-MC3-DMA,可得到体外 HeLa 细胞高效转染试剂。此外,这些制剂在多种哺乳动物细胞系中均表现出优异的转染性能,在原代细胞培养中转染效率接近 90%。这些转染水平与 Lipofectamine 相当或更高,且毒性显著降低。最后,将 LNP-eGFP 显微注射到鸡胚肢芽中,实现了稳健的报告基因表达。结论是,含有可电离氨基脂质的脂质纳米颗粒(LNP)系统可作为高效、无毒的质粒DNA(pDNA)递送系统,用于体外和体内基因表达。总之,本研究结果表明,含有可电离阳离子脂质的pDNA LNP制剂可作为高效的体外转染试剂,其毒性显著低于Lipofectamine等商业试剂。含有DLin-KC2-DMA和不饱和辅助脂质的LNP系统也是体外和体内转染原代细胞的有效系统。预计这些系统在体外转染发育组织方面将具有重要应用价值,并具有基因编辑应用的潜力。[1]
可电离阳离子脂质对于脂质纳米颗粒(LNP)高效递送RNA至关重要。DLin-MC3-DMA(MC3)、ALC-0315和SM-102是目前唯一获临床批准用于RNA治疗的可电离阳离子脂质。 ALC-0315 和 SM-102 是结构相似的脂质,用于 SARS-CoV-2 mRNA 疫苗;MC3 则用于 siRNA 疗法,以敲低肝细胞中的转甲状腺素蛋白。肝细胞和肝星状细胞 (HSC) 是 RNA 疗法的理想靶点,因为它们合成多种血浆蛋白,包括影响血液凝固的蛋白。虽然脂质纳米颗粒 (LNP) 优先在肝脏中积累,但评估不同可电离阳离子脂质将 RNA 载体递送至不同细胞群的能力,对于设计肝毒性最小的 RNA-LNP 疗法至关重要。在此,我们直接比较了分别含有 ALC-0315 或 MC3 的 LNP 敲低肝细胞中凝血因子 VII (FVII) 和 HSC 中 ADAMTS13 的能力。在小鼠体内,以 1 mg/kg 的 siRNA 剂量注射 ALC-0315 脂质纳米颗粒 (LNP) 后,与 MC3 脂质纳米颗粒相比,ALC-0315 脂质纳米颗粒对 FVII 和 ADAMTS13 的敲低效果分别提高了 2 倍和 10 倍。在高剂量 (5 mg/kg) 下,ALC-0315 脂质纳米颗粒会增加肝毒性标志物(ALT 和胆汁酸),而相同剂量的 MC3 脂质纳米颗粒则不会。这些结果表明,ALC-0315 脂质纳米颗粒能够有效介导 siRNA 介导的小鼠肝细胞和肝星状细胞 (HSC) 中靶蛋白的敲低,尽管在高剂量下可能会观察到肝毒性标志物。本研究提供了一个初步的比较,可为开发具有最大疗效和最小毒性的可电离阳离子脂质纳米颗粒疗法提供参考。这项工作验证了可电离阳离子脂质纳米颗粒可用于靶向和敲低 HSC 特异性靶点(如 ADAMTS13)的概念。结果表明,MC3 和 ALC-0315 的疗效存在差异,这两种脂质是 LNP 递送平台中使用的三种临床批准的可电离阳离子脂质中的两种。这种直接比较的见解可能有助于优化基于 RNA 的药物,从而调节以前在体内无法获得的蛋白质的表达,用于研究和治疗目的。[2] |
| 分子式 |
C43H79NO2
|
|---|---|
| 分子量 |
642.0929
|
| 精确质量 |
641.611
|
| 元素分析 |
C, 80.43; H, 12.40; N, 2.18; O, 4.98
|
| CAS号 |
1224606-06-7
|
| 相关CAS号 |
1224606-06-7 ; 1258299-72-7 (deleted)
|
| PubChem CID |
49785164
|
| 外观&性状 |
Colorless to light yellow liquid
|
| 密度 |
0.886±0.06 g/cm3(Predicted)
|
| 沸点 |
670.2±43.0 °C(Predicted)
|
| LogP |
13.647
|
| tPSA |
29.54
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
36
|
| 重原子数目 |
46
|
| 分子复杂度/Complexity |
687
|
| 定义原子立体中心数目 |
0
|
| SMILES |
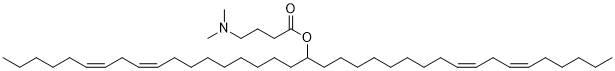
O(C(CCCN(C)C)=O)C(CCCCCCCC/C=C\C/C=C\CCCCC)CCCCCCCC/C=C\C/C=C\CCCCC
|
| InChi Key |
NRLNQCOGCKAESA-KWXKLSQISA-N
|
| InChi Code |
InChI=1S/C43H79NO2/c1-5-7-9-11-13-15-17-19-21-23-25-27-29-31-33-35-38-42(46-43(45)40-37-41-44(3)4)39-36-34-32-30-28-26-24-22-20-18-16-14-12-10-8-6-2/h13-16,19-22,42H,5-12,17-18,23-41H2,1-4H3/b15-13-,16-14-,21-19-,22-20-
|
| 化学名 |
(6Z,9Z,28Z,31Z)-Heptatriaconta-6,9,28,31-tetraen-19-yl 4-(dimethylamino)butanoate
|
| 别名 |
D-Lin-MC3-DMA; MC 3; RV-28; MC3; DLin-MC3-DMA; (6Z,9Z,28Z,31Z)-Heptatriaconta-6,9,28,31-tetraen-19-yl 4-(dimethylamino)butanoate; Q0J6FQ6FKP; D-Lin-MC3-DMA (Excipient); RV 28; MC-3; RV28; DLin-MC3-DMA; Dlin-mc3-dma
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
Ethanol : ~125 mg/mL (~194.68 mM)
DMSO : ~100 mg/mL (~155.74 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 6.25 mg/mL (9.73 mM) in 10% DMSO + 90% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
*生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 5 mg/mL (7.79 mM) in 5% DMSO + 40% PEG300 + 5% Tween80 + 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 View More
配方 3 中的溶解度: 5 mg/mL (7.79 mM) in 5% DMSO + 95% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 配方 4 中的溶解度: ≥ 2.5 mg/mL (3.89 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清的 DMSO 储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL 生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 5 中的溶解度: 2.5 mg/mL (3.89 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将100μL 25.0mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 6 中的溶解度: ≥ 2.5 mg/mL (3.89 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 配方 7 中的溶解度: ≥ 2.5 mg/mL (3.89 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若要配制1 mL工作液,可将100 μL 25.0 mg/mL 澄清DMSO 储备液加入到900 μL 玉米油中,混匀。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.5574 mL | 7.7871 mL | 15.5741 mL | |
| 5 mM | 0.3115 mL | 1.5574 mL | 3.1148 mL | |
| 10 mM | 0.1557 mL | 0.7787 mL | 1.5574 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。