| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| Other Sizes |
|
| 靶点 |
JAK2 (IC50 = 2.6 nM); JAK1 (IC50 = 2.8 nM); JAK3 (IC50 = 13 nM); Tyk2 (IC50 = 58 nM)
|
|---|---|
| 体外研究 (In Vitro) |
Delgocitin 在酶测定中有效抑制所有 JAK 亚型; JAK1、JAK2、JAK3 和 Tyk2 的 IC50 值分别为 2.8±0.6、2.6±0.2、13±0 和 58±9 nM。 Lineweaver-Burk 图表明,dexgocitinib 以与 ATP 竞争的方式抑制所有 JAK,JAK1、JAK2、JAK3 和 Tyk2 的 Ki 值分别为 2.1±0.3、1.7±0.0、5.5±0.3 和 14±1 nM。 Delgocitinib 阻断 IL-2、IL-6、IL-23 产生的 Stat 蛋白磷酸化的 IC50 值分别为 40±9、33±14、84±11、304±22 和 18±3 nM。这些基于细胞的细胞因子信号传导测试中的 GM-CSF 和 IFN-α。 delogocitinib 的效力与 CP-690550 (IC50=16 nM) 相似,同样以浓度依赖性方式抑制 IL-2 引起的 T 细胞增殖 (IC50=8.9±3.6 nM)[1]。
|
| 体内研究 (In Vivo) |
delognocitinib 可减少 IFN-γ 的产生;然而,一小时前治疗的效力大于六小时前给药的效力(ED50=0.24 vs 1.3 mg/kg)。当从第一天开始按处方服用时,德尔戈替尼可以抑制后爪水肿的发展以及滑膜细胞增生和炎症细胞浸润等组织学改变。 Delgocitinib 可防止放射线照相和组织学中观察到的骨和软骨退化。从第 15 天开始给药时,delocitinib 以剂量依赖的方式减少爪子肿胀。此外,在研究结束时的组织学和放射学检查中,Delgocitinib减少了软骨和骨的退化、滑膜细胞的增生以及炎症细胞的浸润[1]。
|
| 酶活实验 |
酶活性测定[1]
使用重组酶、生物素化底物和[33P]ATP进行激酶测定,如前所述,并进行了一些修改。用重组JAK1、JAK2、JAK3和Tyk2酶(分别为4、0.2、0.2和2μg/mL蛋白质)、10μM TK底物生物素、每种酶的Km特异性ATP(分别为40、10、2.5和40μM)、50mM HEPES(pH 7.0)、0.01%牛血清白蛋白(BSA)、0.02%NaN3、0.1mM原钒酸盐、5mM MgCl2、1mM二硫苏糖醇、50nM补充酶缓冲液和1%DMSO进行每种酶反应。 |
| 细胞实验 |
流式细胞术分析[1]
将hPBMCs(3×106个细胞/管)与受试化合物在37°C下孵育30分钟,然后用IL-2(100 ng/mL)、IL-6(100 ng/mL)、IL-23(100 ng/mL.)、IFN-α(100 ng/mL-)或GM-CSF(1 ng/mL)再处理15分钟。为了终止刺激,用固定缓冲液在37°C.下固定细胞10分钟。将固定细胞与Perm缓冲液II在冰上孵育30分钟,然后与荧光铬标记的抗CD3、抗CD4或抗磷酸化Stat抗体在室温下孵育30 min。使用Cytomics FC500对细胞因子诱导的Stat磷酸化进行分析和定量。在IL-23刺激的情况下,用10μg/mL植物血凝素(PHA)-M预培养hPBMC 3天,以增强其对IL-23的反应。 细胞测定[1] 为了测定IL-2诱导的T细胞增殖,将人T细胞用10μg/mL PHA-M预培养3天,并在存在或不存在各种浓度的JTE-052的情况下以1.0×104个细胞/孔的速度接种在96孔板中。在37°C下与化合物预孵育30分钟后,通过向每个孔中加入20 ng/mL重组人IL-2来刺激细胞,并在37°C.5%CO2下孵育3天。在培养期间加入[3H]胸苷(37kBq)。培养期结束后,用96孔采集器采集细胞,并在闪烁计数器中计数。 View More为了测定IL-21诱导的B细胞增殖,在存在或不存在JTE-052的情况下,将人B细胞以1×105个细胞/孔的速度接种在96孔板中。在与该化合物预孵育30分钟后,通过加入10ng/mL重组人IL-21和1μg/mL抗CD40抗体刺激细胞。然后将细胞培养3天,并如上所述测量[3H]胸苷摄取。 为了测定GM-CSF诱导的单核细胞产生的肿瘤坏死因子(TNF)-α,在存在或不存在JTE-052的情况下,将人单核细胞以1×105个细胞/孔的速度接种在96孔板中。与化合物预孵育30分钟后,通过添加0.03 ng/mL重组人GM-CSF刺激细胞16小时。然后将细胞与0.1 ng/mL脂多糖(LPS)在37°C下再培养6小时。收集上清液,用ELISA法测定TNF-α的分泌。 为了测定IL-4诱导的肥大细胞产生的TNF-α,在存在或不存在JTE-052的情况下,将人肥大细胞以2×105个细胞/孔的速度接种在96孔板中。在与该化合物预孵育10分钟后,通过加入10ng/mL重组人IL-4和1μg/mL免疫球蛋白(Ig)E刺激细胞5天。然后将细胞以1.2×105个细胞/孔的速度重新接种,并在37°C下用1μg/mL抗IgE再培养5小时。收集上清液,用ELISA法测定TNF-α的分泌。 为了测定细胞毒性,测量成纤维细胞增殖。在存在或不存在JTE-052而不添加细胞因子的情况下,将NHLF以1×103个细胞/孔的速度接种在96孔板中。然后将细胞培养3天,并如上所述测量[3H]胸苷摄取。 细胞在37°C、5%CO2下,在含有10%胎牛血清(T细胞、B细胞、单核细胞和NHLFs)的RPMI1640培养基或含有0.1%BSA、55µM 2-巯基乙醇和1%胰岛素转铁蛋白硒的Iscove改良Dulbecco培养基中培养,100x(肥大细胞)。 |
| 动物实验 |
IL-2诱导小鼠产生IFN-γ[1]
DBA/1J小鼠经口灌胃单次给药。给药后1小时或6小时,腹腔注射2 μg重组小鼠IL-2和10 μg生物素标记的抗小鼠IFN-γ捕获抗体。6小时后处死小鼠并采集血液。使用小鼠IFN-γ体内捕获检测试剂盒定量血清IFN-γ。 大鼠胶原诱导性关节炎[1] 大鼠胶原诱导性关节炎(CIA)的诱导方法如前所述,并进行了一些修改。简而言之,将II型胶原溶解于0.01 M乙酸中,浓度为2 mg/mL,并将该溶液与等体积的弗氏不完全佐剂乳化。在麻醉状态下,Lewis大鼠背部皮内注射10次,每次注射1 mL乳剂(含1 mg II型胶原蛋白)。第8天,在麻醉状态下,大鼠尾根部注射0.2 mL乳剂进行攻击。试验药物从第1天至第21天(预防性给药)或从第15天至第28天(治疗性给药)每日口服一次。关节炎诱导后,使用体积描记器通过排水法测量后爪体积。在第22天或第29天,处死大鼠,切取后爪进行X光检查或组织学评估。使用微焦点锥形束X射线CT扫描仪拍摄右后肢的X光片。骨破坏的严重程度采用 3 分制评分,分值范围为 0 至 2 分,评估以下五个关节的骨破坏程度:第二跖骨-第二跗间关节、第三跖骨-第三跗间关节、距骨-中央跗间关节、跟骨-第四跗间关节和距骨-胫骨关节。组织学分析方面,将福尔马林固定的左后肢切片,并用苏木精-伊红染色。跗关节的组织学评估基于初步检查中确定的以下参数:炎症细胞浸润、滑膜细胞增生、软骨破坏和骨破坏。每项组织学变化的严重程度均按 0 到 4 分的 5 分制进行评分。(0 分:正常;1 分:最小、孤立(且非常小)的病变;2 分:轻微、局灶性(且小)的病变;3 分:中度、散在的病变;4 分:严重的、广泛的病变)。 |
| 参考文献 | |
| 其他信息 |
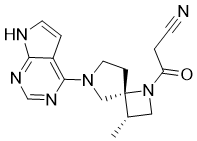
Delgocitinib 是一种吡咯并嘧啶类化合物,其结构为 7H-吡咯并[2,3-d]嘧啶,在 4 位被 (3S,4R)-1-(氰基乙酰基)-3-甲基-1,6-二氮杂螺[3.4]辛-6-基取代。它是一种泛 Janus 激酶 (JAK) 抑制剂,在日本获批用于治疗特应性皮炎 (AD)。它具有多种药理活性,包括 EC 2.7.10.2(非特异性蛋白酪氨酸激酶)抑制剂、抗炎药、抗银屑病药和抗脂溢药。它是一种吡咯并嘧啶、叔胺化合物、腈、氮杂螺环化合物、叔羧酰胺和N-酰基氮杂环丁烷。
Delgocitinib 正在临床试验 NCT03683719 中进行研究(一项 IIb 期剂量范围试验,旨在评估 Delgocitinib 乳膏 1、3、8 和 20 mg/g 与 Delgocitinib 乳膏赋形剂在治疗 16 周内对慢性手部湿疹成年患者的疗效)。 药物适应症 治疗皮炎和湿疹 |
| 分子式 |
C16H18N6O
|
|---|---|
| 分子量 |
310.35372209549
|
| 精确质量 |
310.15
|
| 元素分析 |
C, 61.92; H, 5.85; N, 27.08; O, 5.15
|
| CAS号 |
1263774-59-9
|
| 相关CAS号 |
2064338-33-4 (EtOH);1263774-59-9 (free);2064338-35-6 (CHCl3);
|
| PubChem CID |
50914062
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
1.1
|
| tPSA |
88.9Ų
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
23
|
| 分子复杂度/Complexity |
544
|
| 定义原子立体中心数目 |
2
|
| SMILES |
C[C@H]1CN([C@]12CCN(C2)C3=NC=NC4=C3C=CN4)C(=O)CC#N
|
| InChi Key |
LOWWYYZBZNSPDT-ZBEGNZNMSA-N
|
| InChi Code |
InChI=1S/C16H18N6O/c1-11-8-22(13(23)2-5-17)16(11)4-7-21(9-16)15-12-3-6-18-14(12)19-10-20-15/h3,6,10-11H,2,4,7-9H2,1H3,(H,18,19,20)/t11-,16-/m0/s1
|
| 化学名 |
3-[(3S,4R)-3-methyl-6-(7H-pyrrolo[2,3-d]pyrimidin-4-yl)-1,6-diazaspiro[3.4]octan-1-yl]-3-oxopropanenitrile
|
| 别名 |
LEO-124249; JTE-052; LEO 124249; JTE 052; LEO124249; JTE052
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ≥ 58 mg/mL (~186.89 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (8.06 mM) (饱和度未知) in 5% DMSO + 40% PEG300 + 5% Tween80 + 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
*生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (8.06 mM) (饱和度未知) in 5% DMSO + 95% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 0.5 mg/mL (1.61 mM) (饱和度未知) in 1% DMSO 99% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.2222 mL | 16.1108 mL | 32.2217 mL | |
| 5 mM | 0.6444 mL | 3.2222 mL | 6.4443 mL | |
| 10 mM | 0.3222 mL | 1.6111 mL | 3.2222 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
A phase 2b, double-blind, randomised, 5-arm, vehicle-controlled, dose-ranging trial to evaluate the efficacy and safety of twice daily topical application of delgocitinib cream 1, 3, 8, and 20 mg/g for 16 weeks in adult subjects with mild to severe chronic hand eczema
CTID: null
Phase: Phase 2 Status: Completed
Date: 2019-01-15