| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
- `Equilin (7-Dehydroestrone)` exhibits estrogenic activity, presumably targeting estrogen receptors (ERs) [1]
- `Equilin (7-Dehydroestrone)` activates NMDA receptors to promote cortical neuron growth, with an EC50 of ~10 nM for neuron survival promotion [2] - `Equilin (7-Dehydroestrone)` activates the NF-κB signaling pathway to increase monocyte-endothelial adhesion, with an EC50 of ~25 nM for NF-κB p65 nuclear translocation [3] |
|---|---|
| 体外研究 (In Vitro) |
结合马雌激素中的马烯蛋白通过 NF-κB 信号传导促进单核细胞与内皮细胞的粘附[3]。
- 在原代大鼠皮质神经元培养中,`Equilin (7-Dehydroestrone)`(1 nM-1 μM)处理72小时可剂量依赖性提高神经元活力:10 nM使活力升高35%,100 nM升高62%,1 μM升高78%(MTT法)。该效应可被MK-801(1 μM,NMDA受体拮抗剂)完全阻断 [2] - 在人脐静脉内皮细胞(HUVECs)与THP-1单核细胞共培养体系中,`Equilin (7-Dehydroestrone)`(1 nM-100 nM)处理24小时可提高单核细胞-内皮细胞黏附率:10 nM使黏附率升高41%,100 nM升高73%(流式细胞术)。Western blot显示100 nM `Equilin`可上调NF-κB p65(2.1倍)和ICAM-1(3.4倍)蛋白表达 [3] |
| 体内研究 (In Vivo) |
- 在去卵巢雌性大鼠(每组5只)中,皮下注射`Equilin (7-Dehydroestrone)`(0.1 mg/kg/天或0.5 mg/kg/天)14天,与溶剂组相比,子宫重量分别增加52%(0.1 mg/kg)和98%(0.5 mg/kg) [1]
- 在成年雄性小鼠(每组6只)中,腹腔注射`Equilin (7-Dehydroestrone)`(1 mg/kg)3天,肝糖原含量较溶剂组增加38% [1] - 在皮质神经元损伤的去卵巢雌性大鼠(每组6只)中,灌胃给予`Equilin (7-Dehydroestrone)`(0.3 mg/kg/天)21天,存活皮质神经元数量较溶剂组增加45%;该效应可被联合给予MK-801(0.1 mg/kg/天)消除 [2] |
| 酶活实验 |
- NMDA受体活性检测(验证`Equilin (7-Dehydroestrone)`靶点):原代大鼠皮质神经元以1×10⁵个/孔接种于24孔板,用`Equilin`(10 nM)±MK-801(1 μM)处理48小时。使用Ca²⁺敏感荧光染料检测胞内Ca²⁺浓度(激发光488 nm,发射光525 nm)。`Equilin`使Ca²⁺内流较对照组增加65%,而MK-801可使该增幅降低92% [2]
- NF-κB p65核转位检测:HUVECs用`Equilin (7-Dehydroestrone)`(100 nM)处理1小时后,提取核蛋白与胞质蛋白。通过ELISA(检测波长450 nm)定量核组分中的NF-κB p65蛋白,`Equilin`使核内p65较对照组增加2.8倍 [3] |
| 细胞实验 |
- 原代皮质神经元活力检测:从胚胎18天大鼠大脑分离皮质组织,解离为单细胞后,以5×10³个/孔接种于96孔板(神经基础培养基)。加入`Equilin (7-Dehydroestrone)`(0.1 nM-1 μM),培养72小时。加入MTT溶液(5 mg/mL)孵育4小时,加DMSO溶解甲瓒,在570 nm处测吸光度 [2]
- 单核细胞-内皮细胞黏附检测:HUVECs以2×10⁵个/孔接种于6孔板,用`Equilin (7-Dehydroestrone)`(1-100 nM)处理24小时。加入荧光染料标记的THP-1单核细胞(单核细胞:HUVECs=5:1),孵育1小时。洗去未黏附单核细胞,在荧光显微镜下计数黏附细胞 [3] |
| 动物实验 |
卵巢切除大鼠子宫重量测定:将雌性Sprague-Dawley大鼠(200-250 g)在麻醉下进行卵巢切除术。术后恢复7天,将大鼠分为3组(n=5):溶剂组(0.1%乙醇+0.9%生理盐水)、Equilin(7-脱氢雌酮)0.1 mg/kg组和Equilin(7-脱氢雌酮)0.5 mg/kg组。Equilin每日皮下注射一次,连续14天。处死大鼠,取出子宫并称重[1]
- 小鼠肝糖原测定:将雄性ICR小鼠(25-30 g)分为2组(n=6):溶剂组(0.1%乙醇+PBS)和Equilin(7-脱氢雌酮)1 mg/kg组。每天腹腔注射一次 Equilin,连续 3 天。将肝脏匀浆,并使用比色法试剂盒测定糖原含量 [1] - 卵巢切除大鼠皮层神经元保护试验:对卵巢切除的雌性大鼠(220-260 g)进行针刺皮层损伤。将大鼠分为 3 组(n=6):载体组(0.5% 羧甲基纤维素)、Equilin 0.3 mg/kg 组和 Equilin 0.3 mg/kg + MK-801 0.1 mg/kg 组。每天灌胃一次给药,连续 21 天。将脑组织切片,并通过尼氏染色计数存活的神经元 [2] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
吸收良好。 代谢/代谢物 肝脏 肝脏。 |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性总结
雌激素进入反应组织(例如,女性器官、乳房、下丘脑、垂体)的细胞,在那里它们与蛋白质受体相互作用,随后增加DNA、RNA和某些蛋白质的合成速率。雌激素可降低下丘脑促性腺激素释放激素的分泌,从而减少垂体卵泡刺激素 (FSH) 和黄体生成素 (LH) 的分泌。 蛋白结合 90% 与血浆蛋白结合 - 在大鼠中,皮下注射Equilin(7-脱氢雌酮)(剂量高达 0.5 mg/kg/天,持续 14 天)可引起子宫增生(生理性雌激素效应)[1] - 在人脐静脉内皮细胞 (HUVEC) 中,Equilin(7-脱氢雌酮)(浓度高达 1 μM,持续 24 小时)可维持细胞活力 >90%(CCK-8 检测)[3] |
| 参考文献 | |
| 其他信息 |
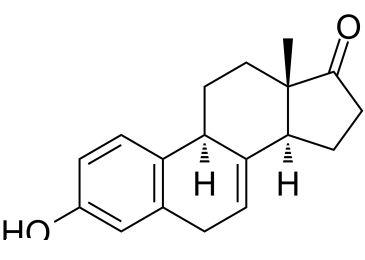
马尿素是一种17-氧代类固醇和3-羟基类固醇,来源于雌烷的氢化物。它是一种由马产生的雌激素类固醇,A环和B环上共有四个双键。妊娠母马的尿液中含有高浓度的马尿素。马尿素是一种天然存在的、具有雌激素活性的类固醇,提取自妊娠母马的尿液。它是一种由马产生的雌激素类固醇,A环和B环上共有四个双键。妊娠母马的尿液中含有高浓度的马尿素。马尿素是从马尿中分离出来的雌激素混合物中的一种,该混合物以普瑞马林(Premarin)的商品名销售。普瑞马林已成为美国最常用的激素替代疗法雌激素。雌酮是普瑞马林的主要雌激素(约占50%),马烯酮约占25%。雌酮是女性体内正常存在的主要雌激素。马烯酮通常不存在于女性体内,因此人们对马烯酮对人体的影响很感兴趣。普瑞马林中的雌激素主要以“结合物”的形式存在,这是一种经过修饰的化学形式,其中活性雌激素与硫酸盐等其他化学基团结合。硫酸雌酮通常是女性体内主要的雌激素形式。普瑞马林中的结合雌激素进入女性体内后,会转化为活性非结合雌激素或排出体外。雌酮可以转化为雌二醇,雌二醇被认为是女性体内主要的活性雌激素。
雌二醇是一种由马产生的雌激素类固醇。它的A环和B环共有四个双键。妊娠母马尿液中含有高浓度的雌激素。 药物适应症 用于治疗与更年期、萎缩性阴道炎、骨质疏松症、性腺功能减退引起的雌激素水平低下、去势、原发性卵巢功能衰竭、乳腺癌(仅用于姑息治疗)以及晚期雄激素依赖性前列腺癌(仅用于姑息治疗)相关的中度至重度血管舒缩症状。 作用机制 雌激素进入反应组织(例如,女性器官、乳房、下丘脑、垂体)的细胞,在那里与蛋白质受体相互作用,随后增加DNA、RNA和某些蛋白质的合成速率。雌激素可减少下丘脑促性腺激素释放激素的分泌,进而减少垂体卵泡刺激素 (FSH) 和黄体生成素 (LH) 的分泌。 药效学 马灵是普瑞马林(结合雌激素)的成分之一,普瑞马林是由雌酮、马灵、17α-二氢马灵和其他相关类固醇的硫酸酯水溶性盐组成的混合物,可能来源于妊娠马的尿液或山药和大豆植株。雌激素在女性生殖系统和第二性征的发育和维持中发挥着重要作用。它们促进阴道、子宫和输卵管的生长发育,以及乳房增大。雌激素间接参与骨骼的形成、泌尿生殖系统结构的张力和弹性的维持、长骨骨骺的变化(从而促进青春期生长突增及其终止)、腋毛和阴毛的生长以及乳头和生殖器的色素沉着。月经周期末期雌激素活性的下降可引发月经,尽管在成熟的排卵周期中,孕激素分泌的停止才是最重要的因素。然而,在排卵前或非排卵周期中,雌激素是月经来潮的主要决定因素。雌激素还会影响垂体促性腺激素的释放。结合雌激素的药理作用与内源性雌激素相似。 - 7-脱氢雌酮(Equilin)是从妊娠母马尿液中分离的一种天然雌激素,是结合雌激素(CEE,例如倍美力)的主要成分,用于雌激素替代疗法(ERT)[2][3]。 - 7-脱氢雌酮诱导皮层神经元生长的机制涉及NMDA受体的激活:它增加NMDA受体介导的Ca²⁺内流,从而激活下游存活信号通路(例如PI3K/Akt)[2]。 - 7-脱氢雌酮通过激活NF-κB促进单核细胞-内皮细胞黏附:它诱导NF-κB p65的磷酸化和核转位,从而上调黏附分子。 (例如,ICAM-1、VCAM-1)在内皮细胞上[3] - 在卵巢切除的大鼠中,马雌酮(7-脱氢雌酮)的雌激素活性弱于雌酮:0.5 mg/kg 的马雌酮引起的子宫重量增加约为 0.5 mg/kg 雌酮引起的子宫重量增加的 80%[1] |
| 分子式 |
C₁₈H₂₀O₂
|
|---|---|
| 分子量 |
268.35
|
| 精确质量 |
268.146
|
| CAS号 |
474-86-2
|
| 相关CAS号 |
Equilin-d4;285979-79-5
|
| PubChem CID |
223368
|
| 外观&性状 |
White to off-white solid
|
| 密度 |
1.2±0.1 g/cm3
|
| 沸点 |
459.1±45.0 °C at 760 mmHg
|
| 熔点 |
238-240ºC(lit.)
|
| 闪点 |
195.4±21.3 °C
|
| 蒸汽压 |
0.0±1.2 mmHg at 25°C
|
| 折射率 |
1.626
|
| LogP |
3.53
|
| tPSA |
37.3
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
0
|
| 重原子数目 |
20
|
| 分子复杂度/Complexity |
466
|
| 定义原子立体中心数目 |
3
|
| SMILES |
OC1C=C2CC=C3[C@@]4([H])[C@@](C(CC4)=O)(CC[C@]3([H])C2=CC=1)C
|
| InChi Key |
WKRLQDKEXYKHJB-HFTRVMKXSA-N
|
| InChi Code |
InChI=1S/C18H20O2/c1-18-9-8-14-13-5-3-12(19)10-11(13)2-4-15(14)16(18)6-7-17(18)20/h3-5,10,14,16,19H,2,6-9H2,1H3/t14-,16+,18+/m1/s1
|
| 化学名 |
(9S,13S,14S)-3-hydroxy-13-methyl-9,11,12,14,15,16-hexahydro-6H-cyclopenta[a]phenanthren-17-one
|
| 别名 |
7-Dehydroestrone; Equilin
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~100 mg/mL (~372.7 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (9.32 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (9.32 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (9.32 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.7265 mL | 18.6324 mL | 37.2648 mL | |
| 5 mM | 0.7453 mL | 3.7265 mL | 7.4530 mL | |
| 10 mM | 0.3726 mL | 1.8632 mL | 3.7265 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。