| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Etravirine (R165335; TMC125) targets HIV-1 reverse transcriptase (Ki = 0.0005 μM for wild-type HIV-1 reverse transcriptase; IC50 = 0.001 μM) [1]
Etravirine (R165335; TMC125) exhibits potent activity against NNRTI-resistant HIV-1 strains (EC50 = 0.002 μM for K103N mutant; 0.003 μM for Y181C mutant; 0.005 μM for G190A mutant) in MT-4 cells [1] Etravirine (R165335; TMC125) inhibits wild-type HIV-1 replication in MT-4 cells with an EC50 of 0.001 μM [1] |
|---|---|
| 体外研究 (In Vitro) |
TMC125 对 HIV-2 (EC50=3.5 μM) 和野生型 HIV-1 (50% 有效浓度 [EC50]=1.4 至 4.8 nM) 表现出显着功效。许多 HIV-1 M 亚型、循环重组形式和 O 组病毒也被 TMC125 抑制。 19 种病毒具有 TMC125 活性,EC50 小于 5 nM[1]。
依曲韦林(Etravirine, R165335; TMC125) 对20株NNRTI耐药的HIV-1临床分离株表现出广谱抗病毒活性,EC50值范围为0.001–0.008 μM [1] 依曲韦林(Etravirine, R165335; TMC125) 在人PBMCs和MT-4细胞中细胞毒性低,CC50 > 10 μM,选择性指数(SI)> 10000 [1] 依曲韦林(Etravirine, R165335; TMC125) 结合HIV-1逆转录酶的NNRTI结合口袋,诱导酶构象变化,从而破坏病毒DNA链延伸 [1] 依曲韦林(Etravirine, R165335; TMC125) 在体外与核苷类逆转录酶抑制剂(NRTIs,如替诺福韦、拉米夫定)和蛋白酶抑制剂(如阿扎那韦)联合使用时表现出协同抗病毒活性,联合指数(CI)< 1.0 [1] 依曲韦林(Etravirine, R165335; TMC125) 对多药耐药HIV-1株的 potency是第一代NNRTIs(依法韦仑、奈韦拉平)的50–100倍 [1] |
| 体内研究 (In Vivo) |
依曲韦林耐药性的产生具有很强的遗传耐药性。在涉及有治疗经验的个体(包括那些感染了对 NNRTI 和蛋白酶抑制剂 (PI) 耐药的病毒的患者)的 IIb 期试验中,TMC125 已证明具有对抗 HIV 对当前可用 NNRTI 耐药性的活性,同时保持与对照组相当的耐受性[2]。
依曲韦林(Etravirine, R165335; TMC125) 以10 mg/kg/天的剂量口服给药植入人胸腺/肝脏组织的SCID-hu小鼠14天后,HIV-1病毒载量下降2.8 log10拷贝/mL [1] 依曲韦林(Etravirine, R165335; TMC125) 在HIV-1感染小鼠中表现出剂量依赖性抗病毒疗效,30 mg/kg/天(口服)时可抑制95%的病毒载量 [1] 在经治HIV-1患者中,依曲韦林(Etravirine, R165335; TMC125)(400 mg每日两次)与其他抗逆转录病毒药物联合使用,24周时病毒载量平均下降1.4 log10拷贝/mL [2] |
| 酶活实验 |
HIV-1逆转录酶抑制实验:制备包含重组HIV-1逆转录酶(野生型或突变型)、多聚(rA)-寡聚(dT)模板引物和[3H]-dTTP的反应体系。加入系列稀释浓度的依曲韦林(Etravirine, R165335; TMC125),在37°C下孵育60分钟。用三氯乙酸终止反应,通过玻璃纤维滤膜过滤,测定放射性强度以计算IC50和Ki值 [1]
逆转录酶结合亲和力实验:将重组HIV-1逆转录酶固定在传感器芯片上。在25°C下,将系列浓度的依曲韦林(Etravirine, R165335; TMC125) 注入芯片表面。通过表面等离子体共振(SPR)监测折射率变化,确定结合动力学和解离常数(Ki)[1] |
| 细胞实验 |
HIV-1抗病毒细胞实验:在96孔板中以2×105个细胞/孔接种MT-4细胞或原代人PBMCs。用HIV-1(野生型或耐药株,MOI = 0.01)感染,加入浓度范围为0.0001–10 μM的依曲韦林(Etravirine, R165335; TMC125)。孵育5–7天,通过ELISA测定病毒p24抗原水平以计算EC50 [1]
细胞毒性实验:在96孔板中培养人PBMCs和MT-4细胞,用依曲韦林(Etravirine, R165335; TMC125)(0.1–100 μM)处理7天。采用MTT法评估细胞活力,计算CC50和选择性指数(SI = CC50/EC50)[1] 联合抗病毒实验:用依曲韦林(Etravirine, R165335; TMC125) 与替诺福韦、拉米夫定或阿扎那韦以不同浓度比例处理HIV-1感染的MT-4细胞。测定每种药物单独使用和联合使用时的EC50值,然后采用Chou-Talalay法计算联合指数(CI)[1] |
| 动物实验 |
不适用
不适用 SCID-hu 小鼠 HIV 模型检测:将人胸腺/肝脏组织植入免疫缺陷型 SCID 小鼠体内。植入后 4 周,小鼠经静脉注射感染野生型或 NNRTI 耐药型 HIV-1 病毒。感染后 2 天,通过灌胃给予依曲韦林(Etravirine,R165335;TMC125),剂量分别为 1、10 或 30 mg/kg,每日一次,连续 14 天。该药物配制于 0.5% 甲基纤维素溶液中。研究结束时采集血液和人组织样本,通过 RT-PCR 检测病毒载量,并通过 ELISA 检测 p24 抗原 [1] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服后2.5-4小时即可达到最大吸收。与降低胃酸的口服雷尼替丁或奥美拉唑合用不影响吸收。空腹给药与餐后给药相比,全身暴露量(AUC)降低近50%。 服用800mg放射性标记的依曲韦林后,93.7%经粪便排出,其中81.2%-86.4%以原形排出。1.2%的剂量经肾脏排出,并发生改变。依曲韦林可通过透析(血液透析)清除。 尚未评估依曲韦林在人体内除血浆以外的其他隔室的分布。 依曲韦林的肾清除率可忽略不计(<1.2%),因此肾功能不全患者无需调整剂量。乙型肝炎和/或合并感染患者的清除率降低,但依曲韦林的安全性无需调整剂量。 代谢/代谢物 体外经肝脏CYP450酶代谢:CYP3A4、CYP2C9、CYP2C19。二甲基苯甲腈部分经甲基羟基化形成的主要代谢物保留了不到90%的依曲韦林活性。 生物半衰期 半衰期为9.05-41小时。 依曲韦林(R165335;TMC125)在人体内的口服生物利用度为42%[2]。 依曲韦林(R165335;TMC125)在人体内被吸收,口服400 mg后,血浆峰浓度(Cmax)为1.6 μg/mL,达峰时间(Tmax)为2.5小时[2]。 依曲韦林(R165335;TMC125)在人体内的血浆浓度-时间曲线下面积(AUC0-12h)为11.8每日两次,每次 400 mg 时,μg·h/mL [2] 依曲韦林 (R165335; TMC125) 在人体内的分布容积 (Vd) 为 110 L [2] 依曲韦林 (R165335; TMC125) 在人体内的血浆消除半衰期 (t1/2) 为 41 小时 [2] 依曲韦林 (R165335; TMC125) 主要在肝脏中通过细胞色素 P450 3A4 (CYP3A4) 和 CYP2C9 代谢 [2] 肾脏排泄量占依曲韦林 (R165335; TMC125) 给药剂量的 < 1% [2] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
接受依曲韦林治疗的患者中,血清转氨酶升高发生率较高,但仅有2%至3%的患者转氨酶升高超过正常值上限5倍;合并丙型肝炎病毒感染的患者中,该比例可能更高。大多数研究表明,依曲韦林治疗组与对照组的肝酶升高发生率无显著差异。在大型临床试验和开放获取研究中,均未报告依曲韦林引起的临床明显肝损伤病例。 接受依曲韦林治疗的患者中,10%至20%会出现皮疹,通常发生在治疗的前2至6周,该发生率高于其他抗逆转录病毒治疗方案或对照组,也是因不良事件而停用依曲韦林的主要原因。依曲韦林治疗期间出现的皮疹可能伴有其他超敏反应症状,包括史蒂文斯-约翰逊综合征和免疫过敏性肝炎。临床上明显的肝毒性较为罕见,但申办方已收到伴有皮疹和超敏反应症状的肝炎病例报告,其中一些病例导致死亡。这些病例的临床特征尚未详细描述。大多数由非核苷类逆转录酶抑制剂引起的超敏性肝炎病例发生在治疗的前6周内,并伴有皮疹、发热、淋巴结肿大和嗜酸性粒细胞增多等免疫过敏表现。停药后通常可迅速恢复,但也可能发生进行性致命性肝损伤。 可能性评分:D(可能导致临床上明显的肝损伤)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 依曲韦林会分泌到乳汁中,其浓度高于母体血浆浓度,且乳汁浓度似乎会随时间增加。在获得更多信息之前,建议优先选择其他药物。通过抗逆转录病毒疗法实现并维持病毒抑制可将母乳传播风险降低至1%以下,但并非为零。对于接受抗逆转录病毒疗法且病毒载量持续低于检测限的HIV感染者,如果她们选择母乳喂养,应予以支持。如果病毒载量未得到抑制,建议使用巴氏杀菌的捐赠母乳或配方奶。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白质结合 体外血浆蛋白结合率约为 99.9%。体外实验表明,99.6% 与白蛋白结合,97.66% - 99.02% 与 1-α 糖蛋白结合。 依曲韦林 (R165335; TMC125) 在人血浆中的血浆蛋白结合率为 99.9% [2] 在接受过治疗的 HIV-1 患者中,依曲韦林 (R165335; TMC125)(每日两次,每次 400 mg)最常见的不良反应是皮疹 (17%)、恶心 (10%) 和腹泻 (8%); 3-4级不良事件发生率<5%[2] 依曲韦林(R165335;TMC125)在临床试验中未显示明显的肝毒性或肾毒性,血清ALT、AST或肌酐水平也未出现持续变化[2] 依曲韦林(R165335;TMC125)在体外可抑制CYP3A4和CYP2C9,提示其可能与这些酶的底物发生药物相互作用[2] 依曲韦林(R165335;TMC125)在小鼠中的口服LD50>2000 mg/kg[1] |
| 参考文献 |
|
| 其他信息 |
药效学
临床试验表明,给药8天后,心电图未见QT间期延长。 依曲韦林(R165335;TMC125)是一种新一代非核苷类逆转录酶抑制剂(NNRTI),用于治疗HIV-1感染[1] 依曲韦林(R165335;TMC125)通过与HIV-1逆转录酶的NNRTI结合口袋结合,通过变构调节抑制病毒DNA合成,从而发挥抗病毒作用[1] 依曲韦林(R165335;TMC125)适用于治疗既往接受过治疗且存在病毒复制和对其他NNRTI耐药的HIV-1感染成人[2] DUET-2临床试验表明,依曲韦林(R165335;TMC125)可显著改善既往接受过治疗患者的病毒载量抑制和免疫功能恢复(CD4+ T 细胞计数增加)[2] |
| 分子式 |
C20H15BRN6O
|
|
|---|---|---|
| 分子量 |
435.28
|
|
| 精确质量 |
434.049
|
|
| CAS号 |
269055-15-4
|
|
| 相关CAS号 |
Etravirine-d4;1142095-93-9;Etravirine-d8;1142096-06-7
|
|
| PubChem CID |
193962
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.6±0.1 g/cm3
|
|
| 沸点 |
637.4±65.0 °C at 760 mmHg
|
|
| 熔点 |
265ºC (dec.)
|
|
| 闪点 |
339.3±34.3 °C
|
|
| 蒸汽压 |
0.0±1.9 mmHg at 25°C
|
|
| 折射率 |
1.703
|
|
| LogP |
4.19
|
|
| tPSA |
120.64
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
7
|
|
| 可旋转键数目(RBC) |
4
|
|
| 重原子数目 |
28
|
|
| 分子复杂度/Complexity |
609
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
CC1=CC(=CC(=C1OC2=NC(=NC(=C2Br)N)NC3=CC=C(C=C3)C#N)C)C#N
|
|
| InChi Key |
PYGWGZALEOIKDF-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C20H15BrN6O/c1-11-7-14(10-23)8-12(2)17(11)28-19-16(21)18(24)26-20(27-19)25-15-5-3-13(9-22)4-6-15/h3-8H,1-2H3,(H3,24,25,26,27)
|
|
| 化学名 |
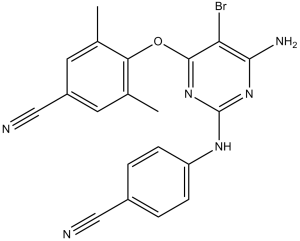
4-(6-Amino-5-bromo-2-(4-cyanoanilino)pyrimidin-4-yloxy)-3,5-dimethylbenzonitrile
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.74 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.74 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2974 mL | 11.4869 mL | 22.9737 mL | |
| 5 mM | 0.4595 mL | 2.2974 mL | 4.5947 mL | |
| 10 mM | 0.2297 mL | 1.1487 mL | 2.2974 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Evaluating the Safety and Tolerability of Etravirine in HIV-1 Infected Infants and Children
CTID: NCT01504841
Phase: Phase 1/Phase 2 Status: Completed
Date: 2021-11-02