| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
HSF1
HSF1A targets TRiC/CCT (chaperonin containing TCP-1) complex (subunits including Tcp1/CCT1, Cct2, Cct3, Cct4, Cct5, Cct8); no IC50/Ki/EC50 values provided [1] HSF1A targets TRiC/CCT complex; no IC50/Ki/EC50 values provided [2] HSF1A targets HSF1 (heat shock transcription factor 1); no IC50/Ki/EC50 values provided [3] HSF1A targets TRiC/CCT complex (CCT4/5 subunits); no IC50/Ki/EC50 values provided [4] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:HSF1A 是热休克转录因子 1 (HSF1) 的细胞渗透性小分子激活剂。 HSF1A 保护细胞免受应激诱导的细胞凋亡,在体内和体外结合 TRiC 亚基,并在不干扰 ATP 水解的情况下抑制 TRiC 活性。 TRiC 复合物的基因失活或耗竭会导致人类 HSF1 激活,并且 HSF1A 在体外抑制纯化的 TRiC 和 HSF1 之间的直接相互作用。热休克转录因子 1 (HSF1) 是一种进化上保守的转录因子,可保护细胞免受蛋白质错误折叠诱导的应激和细胞凋亡。激酶测定:使用补充有 1% Trition- 的生物素结合缓冲液(20 mM HEPES、5 mM MgCl2、1 mM EDTA、100 mM KCl、0.03% NP-40)从哺乳动物、酵母和大肠杆菌培养物中产生蛋白质提取物X100 和蛋白酶抑制剂。将大约 0.5 mg 蛋白质提取物与 100 μM HSF1A-生物素在 4°C 下孵育 4 小时,并用 NeutrAvidin 琼脂糖树脂捕获 HSF1A-生物素相关蛋白质。在生物素结合缓冲液中洗涤后,使用 50 μL 生物素洗脱缓冲液(100 mM Tris、150 mM NaCl、0.1 mM EDTA、2 mM D-生物素)洗脱蛋白质,在 4-20% SDS-PAGE 上解析并进行免疫印迹。对于纯化的 TRiC 和 Hsp70 分析,将 5 nM 蛋白质在生物素结合缓冲液+0.5% Triton X-100 中与 100 μM 生物素或 100 μM HSF1A-生物素在 4°C 下孵育 4 小时,并用 NeutrAvidin 树脂捕获。对于 NiNTA 纯化的酵母 Tcp1,将不同浓度的 Tcp1 0.5 μM、1 mM、2 mM、3 mM 和 4 mM 在 25 mM Hepes pH 7.5、150 mM NaCl 中与 0.5 μM 生物素或 HSF1A-生物素在 4° 下孵育 4 小时C 并用 NeutrAvidin 树脂捕获。细胞测定:HSF1A 保护细胞免受应激诱导的细胞凋亡,结合 TRiC 亚基并抑制 TRiC 活性,而不干扰 ATP 水解。 TRiC 复合物的基因失活或耗竭会导致人类 HSF1 激活,并且 HSF1A 在体外抑制纯化的 TRiC 和 HSF1 之间的直接相互作用。此外,使用 FITC 与 HSF1A 偶联的荧光各向异性实验表明,HSF1A-FITC 与 TRiC 的纯化 Tcp1 亚基结合,亲和力约为 600 nM。通过将纯化的 Tcp1 滴定到含有 500 nM 生物素或 HSF1A-生物素的结合反应中来定性验证这一点。通过计算含有聚集体的细胞数量作为细胞总数的函数进行定量,结果表明,在 HSF1A 浓度低至 2 µM 时,观察到含有聚集体的细胞数量减少。含有聚集体的细胞比例继续以剂量依赖性方式减少,因此用 12 µM HSF1A 预处理导致约 20% 的细胞表现出荧光显微镜可见的聚集体。将 PC12 细胞接种到 96 孔板(5×104 个细胞/孔)中,用浓度不断增加的 HSF1A(2、4、8 和 12 μM)处理 15 小时,此时通过在培养皿中孵育来刺激 httQ74-GFP 表达。 1 µg/mL 多西环素存在 5 d。通过 XTT 活力测定评估细胞活力
1. HSF1A(50 μM)预处理NIH3T3细胞15小时后,再用0.4 μg/ml衣霉素处理15小时,可保护细胞免受应激诱导的凋亡;免疫印迹检测显示Hsp70表达升高,caspase-3剪切水平降低 [1] 2. HSF1A(20 μM)预处理INS 832/13细胞15小时后,再用0.5 mM棕榈酸/BSA处理15小时,可保护细胞免于凋亡,同时Hsp70表达上调,caspase-3剪切水平降低 [1] 3. HSF1A(50 μM)预处理NIH3T3细胞15小时后,再用5 mM同型半胱氨酸处理15小时,可提升细胞活力(Cell Titer Glo法检测),并上调Hsp70表达 [1] 4. HSF1A(100 μM)可与HeLa细胞提取物中的TRiC亚基(Tcp1/CCT1、Cct2、Cct3、Cct4、Cct5、Cct8)结合(HSF1A-Biotin下拉实验+免疫印迹);可与纯化的牛源TRiC、重组Tcp1结合(荧光各向异性法、中性亲和素-琼脂糖下拉实验) [1] 5. HSF1A(200 μM)在体外可抑制TRiC介导的肌动蛋白重折叠(DNaseI-琼脂糖树脂捕获+放射自显影),且不影响TRiC的ATP水解活性(检测不同时间点ADP/ATP比值) [1] 6. HSF1A(200 μM)在体外可抑制纯化的TRiC与HSF1的直接相互作用(钴-琼脂糖树脂下拉实验+免疫印迹) [1] 7. HSF1A(10 μM)可在酵母中激活人源HSF1,促进酵母在含葡萄糖培养基中的生长(检测OD600值);可诱导HSF1多聚化(EGS交联+SDS-PAGE+免疫印迹) [2] 8. HSF1A(30/50/80 μM)处理HSF1+/+ MEFs细胞15小时,可上调Hsp70、Hsp25表达(免疫印迹);80 μM HSF1A处理6小时可升高Hsp70 mRNA水平(RNA印迹) [2] 9. HSF1A(80 μM)可促进MEFs细胞中HSF1的核转位(核/胞质组分分离+免疫印迹);与温和热休克(40℃处理1小时)协同作用可增强Hsp70表达 [2] 10. HSF1A(10 μM)预处理HD-Q74 PC12细胞15小时后,加入1 μg/ml强力霉素处理48小时,可减少httQ74-GFP聚集(可溶性/不可溶性组分免疫印迹、荧光显微镜观察;计数约800个细胞,p<0.01,p<0.001);4 μM HSF1A预处理PC12细胞15小时后,加入强力霉素处理5天,可提升细胞活力(XTT法检测,p<0.001) [2] 11. HSF1A(10 μM)预处理H9c2细胞2小时后,加入1 μM多柔比星(DOX)处理24小时,可稳定HSF1表达,下调IGF-IIR及活化型caspase-3水平(免疫印迹) [3] 12. HSF1A(100 μM)预处理HeLa细胞1小时,可抑制TcdB(5 pM)诱导的细胞圆缩(计数≥500个细胞,p<0.001)及Rac1糖基化(抗Rac1 MAB102抗体免疫印迹,p<0.05,p<0.01) [4] 13. HSF1A(50/100 μM)可抑制CCT4/5介导的热变性TcdB^GT糖基转移酶活性恢复(基于UDP-[¹⁴C]葡萄糖的GST-RhoA糖基化实验,p<0.001) [4] |
| 体内研究 (In Vivo) |
将 10 周大的 Wistar京都大鼠 (WKY) 饲养在恒温 (22°C)、12 小时光/暗循环下,并提供食物和自来水。将动物分为三组:WKY大鼠(对照组)、DOX大鼠和用HSF1A处理的DOX大鼠。每组包含五只动物。 DOX组连续6周腹腔注射DOX(5 mg/kg),以达到30 mg/kg的累积剂量,该剂量已被充分证明可实现心脏毒性。小分子HSF1激活剂HSF1A(100毫克/公斤/天)腹膜内注射。 HSF1A 增强 HSF1 活性,稳定 HSF1 表达并最大限度地减少阿霉素 (DOX) 引起的心脏损伤。 WKY大鼠用DOX(累积剂量:30mg/kgw)和DOX联合HSF1A(100mg/kgw/天)攻击。补充HSF1A可显着将心脏功能提升至对照组的水平。 HSF1A 已被证明可以刺激人类 HSF1 核易位、提高蛋白伴侣表达并改善神经退行性疾病模型中的蛋白错误折叠和细胞死亡。超声心动图结果表明,HSF1A 还可以减轻 DOX 引起的心功能衰竭。
1. HSF1A(5 mM)添加至W¹¹¹⁸果蝇饲料中,连续喂养3天,可上调果蝇体内Hsp70表达(免疫印迹) [2] 2. HSF1A(400 μM)添加至饲料中,可减轻UAS-MJDtrQ78 × gmr-GAL4果蝇(多聚Q介导的神经退行性疾病模型)的眼部形态缺陷/色素脱失 [2] 3. 向多柔比星(DOX)处理的大鼠给予HSF1A,可稳定大鼠心肌组织中HSF1表达,下调IGF-IIR、Gαq、活化型caspase-3及PARP水平(免疫印迹,n=4/组,p<0.05,p<0.01,p<0.001);减少心肌纤维化(Masson三色染色,n=4/组,p<0.05),改善左心室短轴缩短率(FS%,n=5/组,p<0.001);降低TUNEL阳性心肌细胞比例(对照组:10.43±2.14;DOX组:41.64±7.43;DOX+HSF1A组:21.32±7.32,n=4/组) [3] |
| 酶活实验 |
使用生物素结合缓冲液(20 mM HEPES、5 mM MgCl2、1 mM EDTA、100 mM KCl、0.03% NP-40),以及蛋白酶抑制剂和 1% Trition-X100、蛋白质提取物是从哺乳动物、酵母和大肠杆菌培养物中产生的。与 100 μM HSF1A-生物素在 4°C 下孵育 4 小时后,用 NeutrAvidin 琼脂糖树脂捕获约 0.5 mg 的蛋白质提取物,与 HSF1A-生物素的相关蛋白质相对应。一旦蛋白质在生物素结合缓冲液中得到净化,它们就会在 4–20% SDS-PAGE 上进行解析,并使用 50 μL 生物素洗脱缓冲液(100 mM Tris、150 mM NaCl、0.1 mM EDTA 和 2 mM D)进行免疫印迹。 -生物素)。为了分析纯化的 TRiC 和 Hsp70,将 5 nM 蛋白在含有 100 μM 生物素或 100 μM HSF1A-生物素的生物素结合缓冲液+0.5% Triton X-100 中于 4°C 孵育 4 小时。然后使用 NeutrAvidin Rinse 捕获蛋白质。将不同浓度的 Tcp1(0.5 μM、1 mM、2 mM、3 mM 和 4 mM)溶解在 25 mM Hepes pH 7.5、150 mM NaCl 中,与 0.5 μM 生物素或 HSF1A-生物素在 4°C 下孵育 4 小时,然后使用 NeutrAvidin 树脂捕获 NiNTA 纯化的酵母 Tcp1[1]。
1. TRiC介导的肌动蛋白重折叠实验:将纯化的TRiC与DMSO或200 μM HSF1A共处理,随后与变性肌动蛋白孵育;采用DNaseI-琼脂糖树脂捕获折叠态肌动蛋白,经SDS-PAGE分离后通过放射自显影定量,以此评估HSF1A对TRiC重折叠活性的抑制作用 [1] 2. TRiC ATP水解实验:将纯化的牛源TRiC与DMSO或200 μM HSF1A在不同时间点共孵育;检测ADP/ATP比值,判断HSF1A是否影响TRiC的ATP水解活性 [1] 3. TcdB^GT糖基转移酶活性恢复实验:将热变性(48℃,15分钟)的TcdB^GT与100 nM CCT4/5在含0.5 mM ATP的缓冲液中30℃孵育1小时(同时加入/不加入50/100 μM HSF1A);利用UDP-[¹⁴C]葡萄糖检测GST-RhoA的糖基化水平,通过放射自显影定量TcdB^GT活性,以此评估HSF1A对CCT4/5介导的TcdB^GT活性恢复的抑制作用 [4] |
| 细胞实验 |
将 PC12 细胞接种到 96 孔板(5 ×104 细胞/孔)中,用浓度递增的 HSF1A(2、4、8 和 12 μM)处理 15 小时。此后,在 1 µg/mL 强力霉素存在下将细胞孵育 5 天,刺激 httQ74-GFP 表达。 XTT 活力测定用于评估细胞活力[2]。
1. 凋亡保护实验(NIH3T3细胞):细胞经50 μM HSF1A预处理15小时后,用0.4 μg/ml衣霉素处理15小时;提取总蛋白进行免疫印迹,检测Hsp70、Bip、Erdj3及剪切型caspase-3(以GAPDH为内参),评估HSF1A的抗凋亡作用 [1] 2. 凋亡保护实验(INS 832/13细胞):细胞经20 μM HSF1A预处理15小时后,用0.5 mM棕榈酸/BSA处理15小时;提取总蛋白进行免疫印迹,检测Hsp70及剪切型caspase-3(以GAPDH为内参) [1] 3. 细胞活力实验(NIH3T3细胞):细胞经50 μM HSF1A预处理15小时后,用5 mM同型半胱氨酸处理15小时;采用Cell Titer Glo法检测细胞活力 [1] 4. HSF1A-TRiC结合实验(HeLa细胞):细胞提取物与100 μM HSF1A-Biotin孵育后,用中性亲和素-琼脂糖纯化结合蛋白,经SDS-PAGE分离后免疫印迹检测TRiC亚基(Tcp1、Cct2、Cct3、Cct4、Cct5、Cct8)及HSF1 [1] 5. HSF1A-Tcp1结合实验(大肠杆菌/纯化蛋白):含FLAG/His₆标签的Tcp1(全长/片段/突变体)的大肠杆菌提取物与100 μM HSF1A-Biotin(或Biotin作为对照)孵育后,用中性亲和素-琼脂糖纯化;通过抗FLAG/His标签抗体免疫印迹检测Tcp1与HSF1A的结合;采用荧光各向异性法检测HSF1A-FITC与纯化重组Tcp1的结合亲和力 [1] 6. HSF1激活实验(酵母):表达人源HSF1的酵母细胞经10 μM HSF1A或DMSO处理后,在96孔板培养4天;检测OD600值评估酵母生长情况;通过EGS交联+SDS-PAGE+免疫印迹检测HSF1多聚化 [2] 7. Hsp70表达实验(MEFs细胞):HSF1+/+和HSF1⁻/⁻ MEFs细胞经不同浓度HSF1A(30/50/80 μM)处理15小时,或经热休克(42℃处理2小时+恢复15小时);提取总蛋白免疫印迹检测Hsp70、Hsp25(以SOD1为内参);提取总RNA通过RNA印迹检测Hsp70 mRNA [2] 8. HSF1核转位实验(MEFs细胞):HSF1+/+ MEFs细胞经80 μM HSF1A处理不同时间,或经热休克(42℃处理2小时);分离核/胞质组分,免疫印迹检测HSF1(以c-fos为核标志物,SOD1为胞质标志物) [2] 9. 多聚Q聚集抑制实验(PC12细胞):HD-Q74 PC12细胞经10 μM HSF1A预处理15小时后,加入1 μg/ml强力霉素处理48小时;提取可溶性/不可溶性组分,抗GFP抗体免疫印迹检测httQ74-GFP;荧光显微镜计数含聚集物的细胞(每组约800个细胞);4 μM HSF1A预处理后加入强力霉素处理5天,采用XTT法检测细胞活力 [2] 10. TcdB诱导细胞圆缩实验(HeLa细胞):细胞经不同浓度HSF1A(0-100 μM)预处理1小时后,用5 pM TcdB处理;90分钟后显微镜观察细胞圆缩情况,计数≥500个细胞量化圆缩细胞百分比 [4] |
| 动物实验 |
实验动物:本研究采用10周龄的Wistar Kyoto大鼠(WKY)。大鼠饲养于温度恒定为22℃、12小时光照/12小时黑暗循环的笼舍内,并提供食物和自来水。实验分为三组:对照组、DOX组和DOX联合HSF1A处理组。每组5只大鼠。DOX组连续6周腹腔注射DOX(5 mg/kg),累积剂量达30 mg/kg,该剂量已被证实可引起心脏毒性。腹腔注射小分子 HSF1 激活剂 HSF1A(100 mg/kg/天)。
1. 果蝇喂养试验:将 W¹¹¹⁸ 果蝇饲喂添加了 DMSO、5 mM HSF1A 或 0.15 mM 格尔德霉素的食物 3 天;提取果蝇总蛋白进行免疫印迹分析,以检测 Hsp70(以肌动蛋白作为上样对照);将 UAS-MJDtrQ78 × gmr-GAL4 果蝇饲喂添加了 DMSO、400 μM HSF1A 或 5 μM 17-AAG 的食物,以评估眼部形态缺陷 [2] 2. 大鼠 DOX 诱导的心脏毒性试验:将大鼠分为对照组、DOX 处理组和 DOX + HSF1A 组; HSF1A用于减轻阿霉素(DOX)引起的心脏损伤(给药途径/频率/溶解配方未具体说明);采用超声心动图评估射血分数(FS%);收集心脏组织进行苏木精-伊红(HE)染色、Masson三色染色(用于定量心肌纤维化)、免疫印迹(检测HSF1、CHIP、IGF-IIR、Gαq、caspase-3、PARP)和TUNEL检测(用于定量TUNEL⁺心肌细胞)[3] |
| 参考文献 |
|
| 其他信息 |
1. HSF1A 是一种 HSF1 的小分子激活剂;它与 TRiC/CCT 复合物结合,抑制 TRiC-HSF1 相互作用,从而激活 HSF1 并上调 Hsp70,以保护细胞免受蛋白毒性应激[1]
2. HSF1A 的结构与其他 HSF1 激活剂不同;它不抑制Hsp90(与格尔德霉素/雷迪西醇/17-AAG不同),也没有不良的蛋白毒性活性[2] 3. HSF1A可改善表达polyQ的神经元前体细胞中的蛋白质错误折叠和细胞死亡,并在polyQ介导的神经退行性变果蝇模型中起到保护作用,防止细胞毒性[2] 4. HSF1A可稳定HSF1的表达,从而抑制IGF-IIR凋亡信号通路,最大限度地减少体外和体内DOX诱导的心脏损伤[3] 5. HSF1A通过抑制TRiC/CCT介导的毒素重折叠/活性恢复,阻断细菌糖基化毒素(TcdA/TcdB)的细胞毒性作用[4] |
| 分子式 |
C21H19N3O2S2
|
|
|---|---|---|
| 分子量 |
409.52
|
|
| 精确质量 |
409.092
|
|
| 元素分析 |
C, 61.59; H, 4.68; N, 10.26; O, 7.81; S, 15.66
|
|
| CAS号 |
1196723-93-9
|
|
| 相关CAS号 |
|
|
| PubChem CID |
44472508
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
6.117
|
|
| tPSA |
100.61
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
5
|
|
| 可旋转键数目(RBC) |
6
|
|
| 重原子数目 |
28
|
|
| 分子复杂度/Complexity |
595
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
C1(S(NC2N(C3=CC=CC=C3)N=C(C3SC=CC=3)C=2)(=O)=O)=CC=C(CC)C=C1
|
|
| InChi Key |
KJTITGSAONQVPY-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C21H19N3O2S2/c1-2-16-10-12-18(13-11-16)28(25,26)23-21-15-19(20-9-6-14-27-20)22-24(21)17-7-4-3-5-8-17/h3-15,23H,2H2,1H3
|
|
| 化学名 |
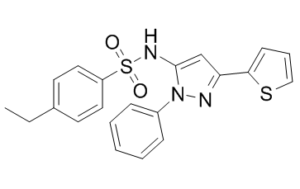
4-ethyl-N-(2-phenyl-5-thiophen-2-ylpyrazol-3-yl)benzenesulfonamide
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.10 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (6.10 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.10 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.4419 mL | 12.2094 mL | 24.4188 mL | |
| 5 mM | 0.4884 mL | 2.4419 mL | 4.8838 mL | |
| 10 mM | 0.2442 mL | 1.2209 mL | 2.4419 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。