| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
DP ( Ki = 0.57 nM ); TP Receptor ( Ki = 2.95 nM )
Laropiprant is a potent, selective antagonist of the DP receptor with Ki values for the TP Receptor and DP receptor of 2.95 nM and 0.57 nM, respectively.[1]. Although laropiprant (1 µM) significantly inhibits the aggregation, it still negates the strong inhibition brought on by BW245c (3 nM) and PGD2 (30 nM). Laropiprant inhibits P-selectin expression, GPIIb/IIIa activation, and in vitro thrombus formation in addition to the DP receptor-dependent increase in VASP phosphorylation. By activating the TP and EP3 receptors, laropiprant counteracts the increased platelet aggregation. Niacin and laropiprant (10 µM) both prevent thrombus formation in vitro[2]. |
|---|---|
| 体外研究 (In Vitro) |
Laropiprant 是一种有效的选择性 DP 受体拮抗剂,对 DP 受体和 TP 受体的 Ki 值分别为 0.57 nM 和 2.95 nM。[1]。 Laropiprant (1 µM) 会显着抑制聚集,但仍抵消 PGD2 (30 nM) 和 BW245c (3 nM) 引起的显着抑制。 Laropiprant 阻断 DP 受体依赖性 VASP 磷酸化增加,以及抑制 P-选择素表达、GPIIb/IIIa 激活和体外血栓形成。拉罗匹兰通过 TP 和 EP3 受体激活来拮抗血小板聚集增加。 Laropiprant (10 µM) 和烟酸抑制体外血栓形成[2]。
拉罗皮仑 (MK-0524) 在转染了 DP1 的 HEK293 细胞中,降低了由 DP1(一种 Gαₛ 偶联受体)产生的细胞内基础 cAMP 水平,证明了其反向激动剂活性。该降低作用在约 300 nM 时达到平台期,EC₅₀ 为 3.8 ± 0.3 nM。 拉罗皮仑 对 cAMP 的降低作用不会被百日咳毒素预处理所改变,表明其未诱导 DP1 与 Gαᵢ 蛋白偶联。 拉罗皮仑 对 DP1 的基础 ERK1/2 活化没有可检测的影响。 用 1 µM 拉罗皮仑 处理表达 Flag 标记 DP1 的 HEK293 细胞,可时间依赖性地增加 DP1 的细胞表面表达,2 小时后增加 25%,24 小时后增加 50%(与对照相比),表现出药理伴侣活性。 这种增加可被 Brefeldin A(一种抑制从内质网-高尔基体到质膜运输的抑制剂)所抑制。 免疫荧光共聚焦显微镜证实,用 拉罗皮仑 处理 24 小时可促进 DP1 从细胞内区室(与内质网标记物 calnexin 共定位)重新分布到质膜。 拉罗皮仑 促进了 DP1 与 ANKRD13C 蛋白之间的相互作用,该蛋白对受体具有类似伴侣蛋白的效应。 |
| 体内研究 (In Vivo) |
Laropiprant(0-100 mg/kg;口服和静脉注射;雄性 Sprague-Dawley 大鼠)表现出良好的药代动力学特征[3]。雄性 Sprague-Dawley 大鼠药代动力学分析[3] 途径剂量 (mg/kg) AUC0-∞ (μM·hr) Clp (mL/min/kg) Vdss (L/kg) T1/2 (hr) PO 1 22.7 1.9 0.7 7.4 PO 5 96.0 2.1 0.9 7.6 途径剂量 (mg/kg) AUC0-∞ (μM·hr) Cmax (μM) Tmax (hr) F(%) IV 5 52.6 15.6 1.2 /
|
| 细胞实验 |
Vena8Fluoro+ 生物芯片在 4°C 下用胶原蛋白 (200 µg/mL) 包被过夜,然后在室温下用牛血清白蛋白 (10 µg/mL) 封闭 30 分钟,然后进行清洗步骤。将收集在柠檬酸钠中的全血与 3, 3-二己基氧羰花青碘化物 (1 µM) 在黑暗中孵育 10 分钟。在灌注开始前 10 分钟添加 PGD2 (30 nM)、BW245c (3 nM),并在激动剂前 10 分钟添加 DP 拮抗剂 BWA868c 或 Laropiprant (1 µM)。在另一组实验中,全血用烟酸 (3 mM)、乙酰水杨酸 (1 mM) 或拉罗匹兰 (1 µM 和 10 µM) 处理 30 分钟。在灌注胶原蛋白涂层芯片前 2 分钟添加终浓度为 1 mM 的 CaCl2。灌注在 30 达因 cm2 的剪切速率下进行。记录血栓形成。 DucoCell 分析软件执行计算机图像分析,计算血栓覆盖的面积。数据以对照样本覆盖面积的百分比表示[2]。
cAMP 测定: 瞬时表达 Flag-DP1 的 HEK293 细胞接种于多聚赖氨酸包被的 96 孔板中。细胞用 IBMX(一种磷酸二酯酶抑制剂)预孵育 10 分钟,然后用配体(例如 1 µM 拉罗皮仑)刺激另外 10 分钟。使用商业酶免疫分析 (EIA) 试剂盒按照说明书测定细胞内 cAMP。对于百日咳毒素实验,细胞在配体刺激前用 1 µg/ml 百日咳毒素预处理 10 分钟。 ERK1/2 磷酸化: 表达 Flag-DP1 的 HEK293 细胞饥饿处理 30 分钟,然后用 1 µM 拉罗皮仑 或 PGD₂ 处理指定时间。用 SDS 上样缓冲液终止反应,超声处理,使用磷酸化特异性及总 ERK1/2 抗体通过 Western blot 分析蛋白。 细胞表面表达 ELISA: 转染了 Flag-DP1 的 HEK293 细胞接种于多聚赖氨酸包被的 24 孔板中。24 小时后,用配体(1 µM)处理不同时间。细胞固定,封闭非特异性结合,与抗 FLAG 一抗孵育,然后与碱性磷酸酶偶联的二抗孵育。加入显色底物,测定吸光度。 免疫荧光共聚焦显微镜: 在盖玻片上表达 Flag-DP1 的 HEK293 细胞用 1 µM 拉罗皮仑 或溶剂对照处理过夜。细胞固定、透化并封闭。然后用小鼠抗 FLAG 和兔抗 calnexin(内质网标记物)一抗孵育,随后用相应的荧光二抗孵育。使用共聚焦显微镜采集 Z-stack 图像。 免疫共沉淀: 共表达 Flag-DP1 和 ANKRD13C-myc 的 HEK293 细胞用 1 µM 拉罗皮仑 或溶剂对照处理 24 小时。细胞裂解,使用抗 FLAG 抗体和 protein G-agarose 珠免疫沉淀 Flag-DP1。免疫沉淀物和裂解液用抗 FLAG 和抗 Myc 抗体进行 Western blot 分析。 Brefeldin A 处理: 对于细胞表面 ELISA,细胞在用 1 µM 拉罗皮仑 处理 90 分钟前,先用 20 µM Brefeldin A 预处理 30 分钟。然后固定细胞并进行 ELISA 处理。 |
| 参考文献 |
|
| 其他信息 |
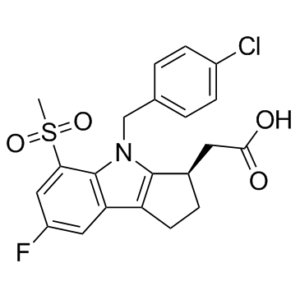
拉罗匹仑是一种吲哚羧酸。
拉罗匹仑是已被欧洲药品管理局(EMA)撤市的产品Pelzont的成分之一。 拉罗匹仑是一种前列腺素D2受体(DP1)拮抗剂,具有抑制烟酸诱导的血管舒张的作用。拉罗匹仑与G蛋白偶联受体DP1结合并抑制其活性。通过与前列腺素D2(PG D2)竞争DP1的结合位点,该药物可阻止PG D2诱导的血管舒张和血流量增加。由于烟酸主要在皮肤中诱导PG D2的合成,因此服用拉罗匹仑可能预防烟酸引起的皮肤血管舒张和面部潮红。 拉罗匹仑 (MK-0524) 是一种基于吲哚的乙酸衍生物。 它最初被认为是一种强效、选择性的DP1受体拮抗剂,可抑制PGD₂诱导的cAMP积累。 本研究将其重新归类为DP1介导的cAMP信号通路的反向激动剂,并发现了一种新的药理伴侣活性,可促进DP1的转运和细胞表面表达。 拉罗匹仑 已在临床上与烟酸联合使用,以抑制潮红症状。 该研究表明,其药理伴侣活性(增加表面受体)可能在某些治疗情况下抵消其拮抗剂/反向激动剂的作用,这可能具有临床意义。因其在血脂异常等疾病中的临床应用价值。[1] |
| 分子式 |
C21H19CLFNO4S
|
|---|---|
| 分子量 |
435.89600
|
| 精确质量 |
435.07
|
| 元素分析 |
C, 57.87; H, 4.39; Cl, 8.13; F, 4.36; N, 3.21; O, 14.68; S, 7.35
|
| CAS号 |
571170-77-9
|
| 相关CAS号 |
Laropiprant sodium; 572874-50-1
|
| PubChem CID |
9867642
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.5±0.1 g/cm3
|
| 沸点 |
710.0±60.0 °C at 760 mmHg
|
| 熔点 |
175∶ºC
|
| 闪点 |
383.2±32.9 °C
|
| 蒸汽压 |
0.0±2.4 mmHg at 25°C
|
| 折射率 |
1.664
|
| LogP |
3.82
|
| tPSA |
84.75
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
29
|
| 分子复杂度/Complexity |
721
|
| 定义原子立体中心数目 |
1
|
| SMILES |
O=S(C1=CC(F)=CC2=C1N(C3=C2CC[C@@H]3CC(O)=O)CC4=CC=C(Cl)C=C4)(C)=O
|
| InChi Key |
NXFFJDQHYLNEJK-CYBMUJFWSA-N
|
| InChi Code |
InChI=1S/C21H19ClFNO4S/c1-29(27,28)18-10-15(23)9-17-16-7-4-13(8-19(25)26)20(16)24(21(17)18)11-12-2-5-14(22)6-3-12/h2-3,5-6,9-10,13H,4,7-8,11H2,1H3,(H,25,26)/t13-/m1/s1
|
| 化学名 |
2-[(3R)-4-[(4-chlorophenyl)methyl]-7-fluoro-5-methylsulfonyl-2,3-dihydro-1H-cyclopenta[b]indol-3-yl]acetic acid
|
| 别名 |
MK-0524; Laropiprant; MK0524; MK 0524; Trade name: Cordaptive; Tredaptive
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~87 mg/mL (199.6 mM)
Ethanol: ~87 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.74 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.74 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2941 mL | 11.4705 mL | 22.9410 mL | |
| 5 mM | 0.4588 mL | 2.2941 mL | 4.5882 mL | |
| 10 mM | 0.2294 mL | 1.1471 mL | 2.2941 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT01126073 | Completed | Drug: Niacin/laropiprant Drug: Placebo |
Coronary Heart Disease | University Medical Centre Ljubljana |
September 2010 | Phase 4 |
| NCT00485758 | Completed | Drug: ER niacin/laropiprant Drug: Comparator : placebo (unspecified) |
Diabetes Mellitus Type 2 | Merck Sharp & Dohme LLC | July 2007 | Phase 3 |
| NCT01451619 | Completed | Drug: Laropiprant Drug: Placebo for Laropiprant |
Rosacea | Merck Sharp & Dohme LLC | November 2011 | Phase 1 |
| NCT00536510 | Completed | Drug: Comparator: placebo Drug: laropiprant/niacin (MK0524A) |
Hypercholesterolemia Hyperlipidemia |
Merck Sharp & Dohme LLC | April 2007 | Phase 3 |
| NCT01321034 | Completed | Drug: Niacin/Laropiprant | Hypercholesterolemia | Instituto Aragones de Ciencias de la Salud |
October 2011 | Phase 4 |
|
|
|
|