| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| Other Sizes |
|
| 靶点 |
PAM/protein-associated motor complex
MB-10 specifically targets Tim44 (a key component of the mitochondrial protein import machinery, part of the TIM23 complex). [1] |
|---|---|
| 体外研究 (In Vitro) |
对于底物输入,MB-10 (100 μM) 是一种蛋白质输入稀释剂 [1]。使用蛋白质输入底物输入稀释剂 MB-10 (0-100 μM) [1]。使用蛋白质输入底物输入稀释剂 MB-10 (0-100 μM) [1]。
Carla Koehler实验室(MB)-10的小分子线粒体导入阻断剂抑制了需要TIM23转运蛋白的底物的导入。突变分析结合分子对接和分子动力学建模表明,MB-10与蛋白质相关运动(PAM)复合物Tim44 C末端结构域中的特定口袋结合。该区域被提出将Tim44锚定到膜上,但MB-10的生化研究表明,在低ATP条件下,该区域是与易位前体结合和与mtHsp70结合所必需的。这项研究还支持PAM复合物在导入横向分选到内膜的底物以及线粒体基质中的直接作用。因此,MB-10是第一个减弱PAM复合物活性的小分子调节剂,可能是通过与Tim44的C末端区域结合。[1] MB-10是线粒体蛋白质输入的潜在衰减器。MB-10靶向TIM23转运蛋白。MB-10抑制使用TIM23导入途径的底物的导入。MB-10的进口抑制取决于特定的化学特性。MB-10阻碍了分选到基质和膜间空间的前体的输入。MB-10的特定性质抑制蛋白质导入。MB-10瞄准PAM综合体的Tim44。Tim44 C末端结构域α4螺旋的突变赋予了对MB-10的抗性。MB-10位于Tim44 C端结构域的结合口袋中。MB-10抑制蛋白质导入哺乳动物线粒体。MB-10在哺乳动物培养细胞中抑制SOD2的生物合成。[1] 抑制线粒体蛋白导入:MB-10 以剂量依赖性方式阻断分离酵母线粒体和哺乳动物细胞中Tim44介导的线粒体蛋白导入。20 μM浓度下,可减少75%的前体蛋白(如Su9-DHFR、pOTC)导入酵母线粒体(放射性标记前体导入实验)[1] - 对Tim44依赖性导入的选择性:浓度高达50 μM时,不影响其他线粒体蛋白导入途径(如TIM22、TOM复合物介导的导入),证实对Tim44相关的TIM23复合物功能具有特异性[1] - 破坏Tim44-Mge1相互作用:免疫共沉淀实验显示,15 μM MB-10 可减少68%的Tim44与Mge1(蛋白导入所需的共分子伴侣)结合,干扰分子伴侣辅助的导入过程[1] - 影响线粒体功能:HeLa细胞经25 μM处理24小时后,线粒体膜电位降低35%(JC-1染色),ATP生成减少42%(荧光素酶基ATP实验),与线粒体蛋白导入缺陷一致[1] - 癌细胞毒性:对线粒体代谢需求高的癌细胞系(如HeLa、A549)具有中等细胞毒性。EC50值分别为32 μM(HeLa)和38 μM(A549),对正常人成纤维细胞无显著毒性(CC50 > 100 μM)[1] |
| 体内研究 (In Vivo) |
MB-10治疗会损害斑马鱼胚胎的心脏发育并诱导其凋亡[1]
PAM复合物的一个组成部分DNAJC19的突变导致扩张型心肌病伴共济失调综合征,这是一种常染色体隐性Barth综合征样疾病。研究人员将MB-10应用于斑马鱼胚胎,以确定TIMM44受损如何改变发育,特别是关注心脏组织。使用了一种转基因斑马鱼系,其中DsRed在心脏特异性心肌肌球蛋白轻链启动子cmlc2的控制下靶向线粒体。如图9所示,在3 hpf下将胚胎置于1%DMSO、MB-10、MB-10.2或类似物4中,并使其发育至72 hpf。用10μm MB-10孵育的胚胎显示背部身体弯曲,心脏发育受损,心包积液过多(图9),这是斑马鱼扩张型心肌病的特征。如吖啶橙染色所示,MB-10处理的胚胎也显示出凋亡细胞的增加(图9,箭头突出显示),这与MB-10治疗的HeLa细胞中观察到的凋亡增加一致(图8,D-G)。此外,用MB-10.2孵育的胚胎具有与MB-10相似的发育缺陷(图9C),而用类似物4孵育的胚看起来与用DMSO处理的斑马鱼相似(图9D)。因此,MB-10是表征培养细胞、斑马鱼和酵母中TIMM44功能的有效工具。 |
| 酶活实验 |
酵母MIC50测定。[1]
指示的酵母菌株在YPEG培养基中的早期对数生长在新鲜YPEG培养基中被稀释至0.01的初始OD600。将稀释后的原液以50μl的等分试样分配到96孔玻璃底板的各个孔中。随后,将YPEG(50μl)中DMSO(或单独DMSO)中的MB-10 连续稀释2倍至指示浓度。DMSO的终浓度为1%。然后将板在25˚C的加湿室中孵育24小时。在此期间,OD600达到约0.5。每个平板在贝克曼轨道振荡器中摇动,以重新悬浮沉淀的细胞,每个孔中的OD600由Wallac Victor平板读数器读取。对于图S1E中的研究,在含有1%DMSO的YPEG中,WT菌株的OD600被设定为100%存活。对于图4c中的研究,在含有1%DMSO的YPEG中,WT菌株的OD600被设定为100%存活,所有菌株的生长速度大致相同。 将放射性标记的蛋白质导入线粒体和交联分析。[1] 在导入纯化线粒体之前,使用TNT快速偶联转录/翻译试剂盒生成[35S]-蛋氨酸和半胱氨酸标记的前体蛋白。根据既定方法进行与酵母线粒体的导入反应。因为这些化合物通常可溶于DMSO,除非另有说明,否则使用1%的DMSO终浓度。将DMSO或DMSO载体中的化合物加入到进口缓冲液中的线粒体(25-50µg/ml)中,并在25°C下孵育15分钟。然后通过添加前体引发进口反应。在反应过程中,每隔一段时间取出等分试样,并在冰上用25μg/ml胰蛋白酶终止导入。15分钟后,随后加入200µg/ml大豆胰蛋白酶抑制剂。通过8000 x g离心5分钟使线粒体颗粒化。 交联试验之前已有报道。在1µM甲氨蝶呤(MTX)存在下进口后,将进口滞留前体与200µM亚琥珀酸二琥珀酰亚胺酯(DSS)在冰上交联30分钟。用100 mM Tris淬灭交联反应后,通过10000 x g离心10分钟使线粒体沉淀,并通过SDS-PAGE和放射自显影进行分析。 耗氧量测定。[1] 如前所述,使用Clark型氧电极测量WT线粒体的耗氧量。简而言之,通过添加2 mM NADH,将状态II呼吸诱导到100µg/ml线粒体在0.23 M蔗糖、20 mM KCl、20 mM Tris-HCl、0.5 mM EDTA、4 mM KH2PO4和3 mM MgCl2(pH 7.2)中的悬浮液中。监测消耗速率约2分钟。将小分子或DMSO加入到最终载体浓度为1%的溶液中,并在另外约2分钟内测量呼吸。通过向腔室中加入20µM羰基氰化物3-氯苯腙(CCCP)实现了非耦合呼吸。 使用蛋白酶保护试验进行靶标鉴定。[1] 用含有20 mM Hepes pH 7.4、50 mM KCl和0.2%Triton X-100的缓冲液裂解40µg分离的酵母线粒体,然后在20000 X g下离心10分钟。裂解物在4°C下用1%DMSO或化合物处理15分钟,然后在25°C下与0.6µg/ml链霉蛋白酶孵育。在每个时间点去除四分之一的反应,通过加入Laemmli样品缓冲液立即淬灭链霉蛋白酶,然后在95°C下孵育15分钟。1µg重组Tim44在4°C下用1%DMSO或含20 mM Hepes KOH pH 7.4、50 mM KCl和0.01%BSA的缓冲液中的小分子处理15分钟。蛋白质在25°C下用链霉蛋白酶处理15分钟。 MB-10 抗性TIM44突变体的分离。[1] 将包含300 bp 5'和3'开放阅读框的TIM44基因克隆到pRS314中进行诱变。如前所述,使用易出错的PCR对TIM44进行诱变,缓冲液中含有Mg2+,腺嘌呤核苷酸的浓度降低了5倍。将突变片段与线性化载体pRS315共转化到Δtim44菌株中,该菌株从着丝粒URA3载体pRS316(称为改组菌株)表达tim44,并在缺乏色氨酸的培养基上选择转化子。随后将转化体转移到含有5-氟乳清酸(FOA)的平板上,以去除pRS316-TIM44质粒。选择携带tim44突变体的细胞是因为它们在15µM MB-10 存在下生长的能力。随后回收突变tim44质粒并测序和重新转化,以确认对MB-10 的抗性是质粒依赖性的。用单突变MB-10抗性突变(T290S和I297V)重建tim44突变体,并合成预测的MB-10 协调点突变(H292A、W316A、W417A、W316Y和W417Y)。 分离线粒体蛋白导入实验:分离酵母线粒体并重悬于导入缓冲液中,将放射性标记的前体蛋白(Su9-DHFR、pOTC)与MB-10(5-50 μM)在4°C预孵育15分钟后,与线粒体混合。25°C孵育30分钟后,通过蛋白酶处理和SDS-PAGE分离导入的蛋白与未导入的前体,放射自显影可视化放射性条带,密度分析法量化导入效率[1] - Tim44-Mge1结合实验:将重组酵母Tim44和Mge1蛋白与MB-10(0.1-50 μM)在结合缓冲液中混合,4°C孵育2小时。用特异性抗体免疫沉淀Tim44,Western blot检测共沉淀的Mge1,通过与溶媒对照组对比Mge1条带强度量化结合亲和力[1] |
| 细胞实验 |
细胞活力测定 [1]
细胞类型: 将表达 Su9-Ura3-myc 的质粒整合到 WT 和 tim23-2 菌株的 LEU2 基因座中。 测试浓度:100μM。 孵化持续时间:30 分钟。 实验结果:表达Su9-Ura3的WT菌株生长失败,而表达Su9-Ura3的tim23-2突变体生长更快。当培养基补充尿嘧啶时,菌株以相似的速率生长。 细胞活力测定 [1] 细胞类型: HeLa 细胞。 测试浓度:0-100 μM。 孵化持续时间:24 小时。 实验结果:抑制HeLa细胞活力,IC50为17.2 μM。 细胞活力测定。[1] 使用基于MTT的毒理学分析试剂盒测量细胞存活率。HeLa细胞在24孔培养皿中生长至80%融合。细胞用1%DMSO或不同浓度的MB-10 处理24小时。处理后,细胞用MTT溶液孵育4小时,如制造商方案所述。 免疫沉淀。[1] 将20μg分离的酵母线粒体用含有20 mM Hepes pH 7.4、80 mM KCl和0.2%Triton X-100的缓冲液裂解,然后在20000 X g下离心10分钟。裂解物在25°C下用1%DMSO或100µMMB-10 处理15分钟。小分子处理后,向裂解物中加入5 mM MgCl2和1 mM ATP,然后用抗mHsp70抗体和蛋白A琼脂糖珠进行免疫沉淀。免疫印迹分析检测Tim44。 下拉分析。[1] 线粒体(400μg)用1%DMSO或指定浓度的MB-10 预处理15分钟,随后在缓冲液A[1%洋地黄皂苷、20 mM K+HEPES(pH 7.4)、80 mM KCl、10%甘油和1mM PMSF]中裂解,然后在20000 x g下离心30分钟以去除不溶性物质。从上清液中去除50μg裂解物,用作总样品(T)的参考。将剩余的350μg稀释至0.4μg/μl缓冲液A。在4˚C下用30ul HisPur Ni2+珠旋转拔出2小时。结合后,去除50μg裂解物作为未结合材料的参考(表示为流通,FT)。用缓冲液洗涤珠粒4次。样品在添加了15%β-巯基乙醇和300mM咪唑的Laemmli样品缓冲液中洗脱。通过SDS-PAGE分离洗脱液(E)、总洗脱液和流动液,并通过免疫印迹进行分析。 细胞操作。[1] 对于显微镜实验,用DMSO、MB-10 或CCCP处理24小时的HeLa细胞用4%甲醛固定,并用冰冷的甲醇渗透。用兔抗细胞色素c抗体和Alexa fluor 488山羊抗兔IgG进行免疫染色。使用Plan Fluor 63x油物镜,用9Axiovert-200M显微镜观察细胞。图像是在室温下用Axiovision软件控制的电荷耦合器件相机采集的。 细胞内线粒体蛋白导入实验:HeLa细胞转染编码线粒体靶向序列(MTS)-GFP融合蛋白的质粒,24小时后用MB-10(10-50 μM)处理16小时。共聚焦显微镜分析GFP的线粒体定位,量化线粒体蛋白导入缺陷细胞(细胞质GFP累积)的比例[1] - 线粒体膜电位实验:HeLa细胞接种到96孔板,经MB-10(5-50 μM)处理24小时后,加入JC-1染料,酶标仪检测荧光强度(红/绿比值,反映膜电位),通过与溶媒对照组对比评估线粒体功能[1] - ATP生成实验:A549细胞经MB-10(10-50 μM)处理24小时后裂解,荧光素酶基ATP检测试剂盒检测ATP水平,发光强度归一化至蛋白浓度,以溶媒对照组的百分比表示ATP生成量[1] - 细胞活力实验:癌细胞(HeLa、A549)和正常人成纤维细胞以5×103个细胞/孔接种到96孔板,用MB-10(5-100 μM)处理72小时。MTT法评估细胞活力,从剂量-反应曲线计算EC50/CC50值[1] |
| 动物实验 |
斑马鱼操作。[1]
具有荧光心脏的斑马鱼源自转基因TL鱼,该转基因鱼表达由cmlc2(心肌细胞轻链-2)启动子调控的CoxIV靶向序列与DsRed融合蛋白。这些品系在14小时光照/10小时黑暗循环中饲养,并交配1小时以获得同步的胚胎发育。胚胎在E3缓冲液(5 mM NaCl、0.17 mM KCl、0.33 mM CaCl2、0.33 mM Mg2SO4)中培养3小时后,然后在添加了1% DMSO、MB-10、MB-10.2或Analog-4的E3缓冲液中于28.5°C孵育3天。处理后,使用Leica MZ16F荧光立体显微镜(TexasRed滤光片组)以5倍放大倍率对胚胎进行成像。或者,将 3 天大的胚胎用 10 µg/ml 吖啶橙染色,孵育 30 分钟。然后用 E3 缓冲液洗涤胚胎以去除残留染料,并使用 Leica MZ16F 荧光立体显微镜(FITC 滤光片组)对凋亡细胞进行成像。 |
| 参考文献 | |
| 其他信息 |
我们通过改进多年积累的遗传筛选方法,完成了对通用导入途径抑制剂的筛选。由于该筛选方法选择的是生长增强的化合物,因此通常会被排除在外的假阳性化合物(这些化合物通常是致死的)。评估和验证高通量筛选方法的指标包括:低命中率(通常低于0.14%)和筛选窗口系数(称为Z′因子)大于0.5。我们的筛选方法非常有效,具有较高的Z′因子(>0.8)和较低的命中率(0.02%)。该筛选方法的另一个优势是使用了野生型酵母菌株,而不是突变体。此外,正如之前的抑制剂MB-1和MB-6所示,MB-10能够抑制酵母和哺乳动物线粒体中的导入。蛋白质导入实验(图3)和斑马鱼实验(图9)的构效关系研究表明,MB-10似乎特异性地靶向Tim44。事实上,MB-10 和 MB-10.2 特异性地诱导了斑马鱼胚胎发育过程中的心脏缺陷,并抑制了其导入。相比之下,类似物 4 虽然与 MB-10 和 MB-10.2 具有相似的结构(图 9),但并未改变斑马鱼的发育。因此,这些探针在多种模型系统中具有重要的研究价值。[1]
多方面的策略表明,MB-10 可能靶向 Tim44,但也不能完全排除其与 PAM 和 TIM23 复合物其他组分界面相互作用的可能性。通过遗传学方法,tim23-2 突变体对 MB-10 的敏感性高于 tim10-1 突变体。使用每种转位子(TOM、TIM23 和 MIA(线粒体膜间隙组装))的底物进行的一系列导入实验,将候选因子缩小到 PAM 复合物的五到六个因子。后续的详细研究,包括与细胞色素b2(167)-DHFR的交联和蛋白酶保护实验,证实MB-10可能靶向Tim44。尽管将MB-10直接纳入晶体学研究的方法并不成功,但遗传学方法鉴定出了对MB-10不敏感的Tim44突变体。结合分子对接和分子动力学模拟,MB-10结合于Tim44 C端区域的一个口袋中,该口袋位于一个可能与细胞膜相互作用的大沟槽的对面。Tim44的N端区域与运动蛋白Hsp70、Mge1、Pam18和Pam16相互作用,但我们的研究表明,C端区域对于Tim44的功能也至关重要。事实上,C端区域高度保守,不变残基的突变会导致显性负性表型,而MB-10的加入则阻断了Tim44与导入的前体蛋白和Hsp70的相互作用。如图7D所示,我们推测MB-10阻断了Tim44 C端结构域与前体的结合,从而阻断了蛋白质转位。交联实验表明,前体蛋白与Hsp70的结合增加,但这种中间体不利于蛋白质导入。基于我们的下拉实验,MB-10并不破坏TIM23转位子和PAM复合物各组分之间的相互作用。因此,我们的研究结果与Mokranjac等人报道的C端结构域与转位蛋白相互作用的结果一致。因此,MB-10 是一种特异性探针,可阻断转位前体与 PAM 复合物的相互作用。[1] 在含有终止转移基序的底物导入研究中,100 μM 的 MB-10 抑制了分选至膜间隙的前体的导入(图 3)。这种导入抑制与先前报道的 tim44 温度敏感突变体的表型相似。最近,导入马达在侧向分选的前体(例如细胞色素 b2(167)-DHFR 和细胞色素 c1)转位中的作用一直存在争议。“模块化”模型提出 TIM23 复合物以两种形式存在:一种含有 Tim21,但缺乏导入马达,介导侧向插入;另一种含有导入马达,但缺乏 Tim21,介导转运至线粒体基质。 “单实体”模型提出,转位酶的所有必需亚基作为一个复合物发挥作用,该复合物可根据转位底物的靶向序列进行主动重塑。鉴于 MB-10 抑制细胞色素 b2(167)-DHFR 和细胞色素 c1 的导入,我们的研究倾向于支持“单实体”模型,因为马达蛋白 Tim44 是侧向分选前体蛋白导入所必需的。MB-10 将成为继续研究动态 TIM23 转位子如何介导蛋白质导入机制的有用工具。[1] 背景:MB-10 是一种通过改良的遗传筛选鉴定的小分子抑制剂,特异性靶向线粒体蛋白导入组分 Tim44[1] - 作用机制:与 Tim44 结合并破坏其与 Mge1 的相互作用,Mge1 是一种辅助伴侣蛋白,对于通过 TIM23 复合物将前体蛋白转运到线粒体至关重要。这会损害线粒体蛋白的输入,导致线粒体功能障碍,并降低依赖高效线粒体代谢的细胞的活力[1] - 研究意义:可作为研究Tim44和线粒体蛋白输入在细胞生理和疾病中作用的化学工具。对与线粒体蛋白输入失调相关的疾病(例如,某些癌症、神经退行性疾病)具有潜在的治疗价值[1] - 结构特征:该化合物的化学结构包含一个杂环核心和一个疏水侧链,这对于Tim44的结合至关重要。构效关系分析表明,侧链的修饰会降低抑制效力[1] |
| 分子式 |
C12H8FN3O3S
|
|---|---|
| 分子量 |
293.273624420166
|
| 精确质量 |
293.03
|
| 元素分析 |
C, 49.15; H, 2.75; F, 6.48; N, 14.33; O, 16.37; S, 10.93
|
| CAS号 |
394694-98-5
|
| 相关CAS号 |
394694-98-5
|
| PubChem CID |
6895129
|
| 外观&性状 |
Light yellow to yellow solid powder
|
| LogP |
3.1
|
| tPSA |
116
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
20
|
| 分子复杂度/Complexity |
402
|
| 定义原子立体中心数目 |
0
|
| SMILES |
C1=CC(=CC(=C1)F)C(=O)N/N=C/C2=CC=C(S2)[N+](=O)[O-]
|
| InChi Key |
QDYQZMWFIYLMNX-VGOFMYFVSA-N
|
| InChi Code |
InChI=1S/C12H8FN3O3S/c13-9-3-1-2-8(6-9)12(17)15-14-7-10-4-5-11(20-10)16(18)19/h1-7H,(H,15,17)/b14-7+
|
| 化学名 |
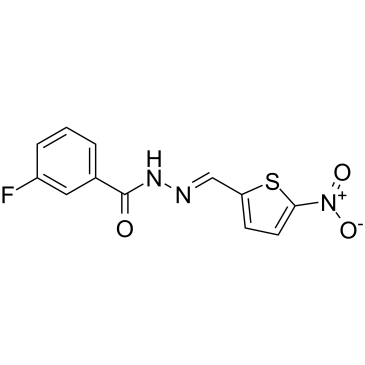
3-fluoro-N-[(E)-(5-nitrothiophen-2-yl)methylideneamino]benzamide
|
| 别名 |
MitoBloCK 10; MitoBloCK-10; MB10; MitoBloCK-10; 3-Fluoro-N'-((5-nitrothiophen-2-yl)methylene)benzohydrazide; 394694-98-5; 3-fluoro-N'-[(E)-(5-nitrothiophen-2-yl)methylidene]benzohydrazide; 3-fluoro-N-[(E)-(5-nitrothiophen-2-yl)methylideneamino]benzamide; MB-10; MB 10; MB-10
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~125 mg/mL (~426.2 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.08 mg/mL (7.09 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.4098 mL | 17.0491 mL | 34.0983 mL | |
| 5 mM | 0.6820 mL | 3.4098 mL | 6.8197 mL | |
| 10 mM | 0.3410 mL | 1.7049 mL | 3.4098 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|
|
|