| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| 5g |
|
||
| 10g |
|
||
| 25g |
|
||
| 50g |
|
||
| Other Sizes |
|
| 靶点 |
Phospholipase A2 (PLA2) (Ki: 0.12 ± 0.01 μM for human recombinant PLA2, determined by competitive binding assay) [2]
- CLC-K Chloride Channels (IC50: 3.5 ± 0.3 μM for rat CLC-K1 channel expressed in HEK293 cells; IC50: 4.2 ± 0.4 μM for rat CLC-K2 channel) [3] - Store-Operated Ca²⁺ Channels (SOC) (no IC50; 10 μM Niflumic acid inhibited SOC-mediated Ca²⁺ influx by 68 ± 5% in K562 cells) [4] - Ca²⁺-Dependent K⁺/Cl⁻ Channels (no IC50; 10 μM Niflumic acid reduced Ca²⁺-dependent K⁺ current by 72 ± 6% and Cl⁻ current by 65 ± 4% in K562 cells) [4] - Cyclooxygenase-2 (COX-2) (no IC50; 20 μM Niflumic acid inhibited COX-2-mediated PGE2 synthesis by 58 ± 4% in A549 lung cancer cells) [5] - Extracellular Signal-Regulated Kinase 1/2 (ERK1/2) (no IC50; 15 μM Niflumic acid reduced phosphorylated ERK1/2 (p-ERK1/2) by 48 ± 5% in CNE-2 nasopharyngeal carcinoma cells) [6] - Matrix Metalloproteinase 2/9 (MMP2/9) (no IC50; 15 μM Niflumic acid inhibited MMP2 activity by 52 ± 6% and MMP9 activity by 45 ± 5% in CNE-2 cells) [6] |
|---|---|
| 体外研究 (In Vitro) |
环格列酮与尼氟酸(100 和 200 μM;48 小时)的组合对 A549、H460 和 H1299 细胞有害 [5]。在 A549、H460 和 H1299 细胞中,尼富米酸(0-300 μM;36 小时)与环格列酮组合可引起细胞凋亡 [5]。在肺癌细胞中,尼富米酸(100 μM;30 小时)加西格列酮可激活 caspase-8/Bid/Bax 通路 [5]。
1. 抑制大鼠肠系膜血管床的升压反应:离体大鼠肠系膜血管床用Krebs-Henseleit溶液灌注,在给予去甲肾上腺素(NA,1 μM)或5-羟色胺(5-HT,1 μM)前10分钟,向灌注液中加入尼氟灭酸(Niflumic acid)(1 μM、10 μM、100 μM)。100 μM时,尼氟灭酸抑制NA诱导的升压反应达78±6%,抑制5-HT诱导的反应达72±5%;10 μM时,抑制率分别为45±4%(NA)和40±3%(5-HT)[1] 2. 抑制PLA2活性:人重组PLA2与尼氟灭酸(0.01-10 μM)和¹⁴C标记磷脂酰胆碱(底物)共孵育。0.1 μM时,尼氟灭酸抑制PLA2介导的脂肪酸释放达52±4%;1 μM时,抑制率达89±3%。X射线晶体学显示尼氟灭酸结合于PLA2活性位点,阻断底物结合[2] 3. 调节CLC-K氯通道:转染大鼠CLC-K1/K2质粒的HEK293细胞进行电压钳实验。尼氟灭酸(1-10 μM)在5 μM时使CLC-K1电流减少58±5%,CLC-K2电流减少52±4%,且抑制作用不依赖电压[3] 4. 调节K562细胞离子通道并诱导凋亡:K562细胞用尼氟灭酸(5-30 μM)处理48小时。20 μM时,抑制SOC Ca²⁺内流达68±5%,减少Ca²⁺依赖的K⁺/Cl⁻电流达72±6%/65±4%,凋亡率增加3.2±0.3倍(Annexin V-FITC/PI染色)。Western blot显示cleaved caspase-3上调2.8±0.2倍[4] 5. 诱导肺癌细胞凋亡:A549肺癌细胞用尼氟灭酸(10-40 μM)单药或与西格列酮(10 μM)联用处理。20 μM 尼氟灭酸+10 μM西格列酮使凋亡率增加4.5±0.4倍(尼氟灭酸单药为1.8±0.2倍),上调ER应激标志物(GRP78:2.1±0.2倍;CHOP:2.5±0.3倍)和cleaved caspase-8(3.1±0.3倍)[5] 6. 抑制鼻咽癌细胞增殖:CNE-2细胞用尼氟灭酸(5-25 μM)处理72小时,增殖抑制IC50为18.5±1.2 μM(MTT法)。15 μM时,减少p-ERK1/2达48±5%,抑制MMP2/9活性达52±6%/45±5%,克隆形成率降低62±5%[6] 7. 抑制杯状细胞脱颗粒:豚鼠气管上皮细胞用尼氟灭酸(1-20 μM)处理24小时。10 μM时,减少组胺诱导的MUC5AC分泌达48±5%,抑制杯状细胞脱颗粒达52±4%(阿尔新蓝染色)[8] |
| 体内研究 (In Vivo) |
在猪哮喘模型中,尼富米酸(30 mg/kg;10 分钟内呼吸两次)可抑制粘液颗粒分泌反应 [8]。
1. 调节小鼠免疫反应:6-8周龄雌性BALB/c小鼠每日口服尼氟灭酸(Niflumic acid)(5 mg/kg、20 mg/kg),连续7天。20 mg/kg时,血清IgG较对照组增加42±5%,IgM增加38±4%,伴刀豆蛋白A(ConA)诱导的脾细胞增殖增强52±6%;同时减少脾细胞培养中LPS诱导的TNF-α分泌35±4%[7] 2. 抑制豚鼠哮喘模型杯状细胞脱颗粒:300-350 g雄性豚鼠用卵清蛋白(OVA)致敏建立哮喘模型,每日口服尼氟灭酸(10 mg/kg、30 mg/kg),连续14天。30 mg/kg时,减少OVA诱导的气管杯状细胞脱颗粒达58±6%(组织学评分),降低支气管肺泡灌洗液(BALF)中MUC5AC浓度达45±5%,减少嗜酸性粒细胞浸润达42±4%[8] |
| 酶活实验 |
1. PLA2活性测定实验:
- 反应体系(200 μL):50 mM Tris-HCl(pH 8.0)、10 mM CaCl₂、0.1 mg/mL人重组PLA2、100 μM ¹⁴C标记磷脂酰胆碱(底物)以及系列稀释的尼氟灭酸(Niflumic acid)(0.01-10 μM)。 - 孵育:混合物在37°C孵育30分钟,加入50 μL 1 M HCl终止反应。 - 检测:用氯仿-甲醇(2:1,v/v)萃取脂肪酸产物,氮气吹干后重悬于闪烁液中,通过液体闪烁计数器测定放射性。抑制率=(1 - 样品放射性/对照放射性)×100%,采用Lineweaver-Burk双倒数作图法计算Ki[2] |
| 细胞实验 |
细胞活力测定[5]
细胞类型: A549、H460 和 H1299 细胞 测试浓度: 0 μM、100 μM、200 μM、300 μM 孵育时间: 48 小时 实验结果: 证明与环格列酮可显着协同降低细胞活力。 细胞凋亡分析[5] 细胞类型: A549、H460 和 H1299 细胞 测试浓度: 100 μM、200 μM 孵育时间:48小时 实验结果:证明与Ciglitazone具有显着的协同增加细胞凋亡的作用。 细胞活力测定[5] 细胞类型: A549、H460 和 H1299 细胞 测试浓度: 100 μM 孵育时间: 30 小时 实验结果: 证明 caspase-8、Bid 和 Bax 与 Ciglitazone 的蛋白质水平显着协同增加。 1. CLC-K通道电流测定实验(HEK293细胞): - 细胞转染:HEK293细胞以2×10⁵个细胞/皿接种于35 mm培养皿,用脂质体试剂转染大鼠CLC-K1/K2质粒+EGFP质粒(转染对照)。 - 电压钳实验:转染48小时后,细胞置于细胞外液(140 mM NaCl、5 mM KCl、2 mM CaCl₂、10 mM HEPES,pH 7.4)中,向液槽中加入尼氟灭酸(Niflumic acid)(1-10 μM),用膜片钳放大器记录全细胞电流,通过电压从-100 mV阶跃至+100 mV绘制电流-电压(I-V)曲线[3] 2. K562细胞凋亡与离子通道实验: - 细胞培养:K562细胞在含10%FBS的RPMI 1640中培养,以1×10⁵个细胞/mL的密度用尼氟灭酸(5-30 μM)处理48小时。 - 离子通道检测:用Fluo-4 AM(10 μM)和流式细胞术测定Ca²⁺内流;通过膜片钳记录K⁺/Cl⁻电流。 - 凋亡检测:细胞在避光条件下用Annexin V-FITC/PI染色15分钟,流式细胞术分析;Western blot检测cleaved caspase-3(一抗:抗cleaved caspase-3;二抗:HRP偶联IgG)[4] 3. A549肺癌细胞ER应激实验: - 细胞培养:A549细胞以2×10⁵个细胞/孔接种于6孔板,用尼氟灭酸(10-40 μM)±西格列酮(10 μM)处理48小时。 - ER应激检测:裂解细胞,Western blot检测GRP78、CHOP和cleaved caspase-8;RT-PCR检测GRP78/CHOP mRNA(引物:GRP78-F:5’-...-3’,GRP78-R:5’-...-3’;CHOP-F:5’-...-3’,CHOP-R:5’-...-3’)[5] 4. CNE-2细胞MMP活性实验: - 细胞培养:CNE-2细胞用尼氟灭酸(5-25 μM)处理72小时。 - MMP检测:收集培养上清液,通过明胶酶谱法(含0.1%明胶的10% SDS-PAGE)测定MMP2/9活性。凝胶用考马斯亮蓝染色,ImageJ定量溶解带强度[6] |
| 动物实验 |
动物/疾病模型:哮喘猪[8]
剂量:30 mg/kg 给药途径:吸入 实验结果:显著抑制黏液面积减少。 1.离体大鼠肠系膜血管床制备: -动物:雄性Wistar大鼠(250-300 g)用戊巴比妥钠(50 mg/kg,腹腔注射)麻醉。 -血管床分离:切除肠系膜动脉弓,清除脂肪组织,并在肠系膜上动脉处插管。用含氧(95% O₂/5% CO₂)的Krebs-Henseleit溶液(37°C,流速:5 mL/min)灌注。 - 给药:将尼氟酸溶于DMSO(终浓度≤0.1%),加入灌注液中。通过压力传感器记录NA(1 μM)或5-HT(1 μM)引起的升压反应[1] 2. 小鼠免疫调节模型: - 动物:雌性BALB/c小鼠(6-8周龄,18-22 g),n=18,随机分为对照组、尼氟酸5 mg/kg组和尼氟酸20 mg/kg组(每组n=6)。 - 给药:将尼氟酸溶于0.5% CMC-Na溶液中,每日一次口服给药(10 μL/g体重),连续7天;对照组给予0.5% CMC-Na溶液。 - 样本采集:第8天,通过眼眶静脉丛采集血液,用于血清IgG/IgM检测(ELISA)。切除脾脏,分离脾细胞进行增殖试验(MTT)和TNF-α检测(ELISA)[7] 3. 豚鼠哮喘模型: - 动物:雄性豚鼠(300-350 g),n=15,随机分为对照组、OVA组、OVA+尼氟酸10 mg/kg组、OVA+尼氟酸30 mg/kg组(每组n=3-4)。 - 模型建立:第0天和第7天,OVA组腹腔注射OVA(100 μg)+明矾(2 mg);对照组腹腔注射生理盐水+明矾。 - 给药:第14天至第27天,每日一次口服尼氟酸(溶于0.5% CMC-Na溶液,10 μL/g体重);OVA组口服0.5% CMC-Na溶液。 - 样本采集:第 28 天采集支气管肺泡灌洗液 (BALF) 用于 MUC5AC/嗜酸性粒细胞检测;切除气管进行组织学分析(杯状细胞评分)[8] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服后吸收良好。 代谢/代谢物 肝脏代谢。 生物半衰期 2.5 小时 |
| 毒性/毒理 (Toxicokinetics/TK) |
蛋白质结合
90%与血浆蛋白结合。 1.体外细胞毒性:尼氟酸对增殖抑制的IC50分别为18.5±1.2μM(CNE-2细胞)和22.3±1.5μM(A549细胞)(72小时,MTT法)。在浓度≤10 μM时,对正常人支气管上皮细胞(BEAS-2B,存活率≥85% vs. 对照组)无明显细胞毒性[5,6] 2. 体内毒性:在为期7天的小鼠研究中,尼氟酸(5-20 mg/kg,口服)对体重(最终体重:20.5 ± 1.2 g vs. 对照组 21.1 ± 1.3 g)或器官指数(肝脏/体重:3.2 ± 0.2% vs. 3.3 ± 0.2%;肾脏/体重:0.8 ± 0.1% vs. 0.8 ± 0.1%)均无影响。血清ALT(45 ± 5 U/L)和肌酐(0.5 ± 0.04 mg/dL)均在正常范围内[7] 3.豚鼠毒性:在为期14天的哮喘研究中,口服尼氟酸(10-30 mg/kg)未引起任何异常行为(例如嗜睡、腹泻)。血清AST(52 ± 6 U/L)和尿素氮(15.3 ± 1.2 mg/dL)均在正常范围内[8] |
| 参考文献 |
|
| 其他信息 |
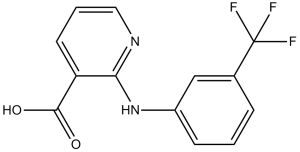
尼氟酸是一种芳香族羧酸,属于吡啶类化合物。
尼氟酸是一种镇痛抗炎药,用于治疗类风湿性关节炎。 一种用于治疗类风湿性关节炎的镇痛抗炎药。 药物适应症 用于治疗类风湿性关节炎。 作用机制 尼氟酸能够抑制磷脂酶A2和COX-2,从而发挥抗炎镇痛作用。 药效学 尼氟酸是一种非甾体抗炎药(NSAID),属于芬那酸类,是一种钙离子激活的氯离子通道阻滞剂。 1. 尼氟酸是一种具有多靶点活性的非甾体抗炎药(NSAID):它抑制…… 1. PLA2(减少脂质介质合成)、调节离子通道(调节细胞信号传导)以及靶向COX-2/MMPs(发挥抗炎/抗肿瘤作用)[2,5,6] 2. 其抗哮喘作用是通过抑制杯状细胞脱颗粒和MUC5AC分泌介导的,从而减少气道黏液阻塞——这与以支气管扩张为靶点的传统抗哮喘药物不同[8] 3. 在癌症治疗中,尼氟酸与PPARγ配体(例如西格列酮)具有协同作用,可通过增强内质网应激诱导的细胞凋亡发挥作用,提示其具有作为辅助抗肿瘤药物的潜力[5] 4. 在兽医学中,由于尼氟酸具有PLA2/COX抑制活性,且在治疗剂量下全身毒性较低,因此被用于治疗炎症性疾病(例如关节疼痛)[7] |
| 分子式 |
C13H9F3N2O2
|
|
|---|---|---|
| 分子量 |
282.22
|
|
| 精确质量 |
282.061
|
|
| CAS号 |
4394-00-7
|
|
| 相关CAS号 |
Niflumic Acid-d5;1794811-58-7;Niflumic acid-13C6;1325559-33-8
|
|
| PubChem CID |
4488
|
|
| 外观&性状 |
Light yellow to yellow solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 沸点 |
378.0±42.0 °C at 760 mmHg
|
|
| 熔点 |
203-204ºC
|
|
| 闪点 |
182.4±27.9 °C
|
|
| 蒸汽压 |
0.0±0.9 mmHg at 25°C
|
|
| 折射率 |
1.589
|
|
| LogP |
4.94
|
|
| tPSA |
62.22
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
7
|
|
| 可旋转键数目(RBC) |
3
|
|
| 重原子数目 |
20
|
|
| 分子复杂度/Complexity |
349
|
|
| 定义原子立体中心数目 |
0
|
|
| InChi Key |
JZFPYUNJRRFVQU-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C13H9F3N2O2/c14-13(15,16)8-3-1-4-9(7-8)18-11-10(12(19)20)5-2-6-17-11/h1-7H,(H,17,18)(H,19,20)
|
|
| 化学名 |
2-[3-(trifluoromethyl)anilino]pyridine-3-carboxylic acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (8.86 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (8.86 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.5433 mL | 17.7167 mL | 35.4333 mL | |
| 5 mM | 0.7087 mL | 3.5433 mL | 7.0867 mL | |
| 10 mM | 0.3543 mL | 1.7717 mL | 3.5433 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05761015 | Not yet recruiting | Drug: therapeutic program including intermittent drug intake and multimodal rehabilitation program |
Osteoarthritis, Knee Osteoarthritis, Hip Chronic Pain |
University Hospital, Clermont-Ferrand | December 1, 2023 | Phase 4 |