| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Nuclear retinoic acid receptor γ (RAR-γ)
Retinoic Acid Receptor-γ (RARγ) (EC50 = 1.2 nM in luciferase reporter assay; Ki = 0.8 nM in ligand binding assay) [1,2] Retinoic Acid Receptor-α (RARα) (EC50 = 45 nM in luciferase reporter assay, 37.5-fold less potent than RARγ) [2,3] Retinoic Acid Receptor-β (RARβ) (EC50 = 62 nM in luciferase reporter assay, 51.7-fold less potent than RARγ) [2,3] Bone Morphogenetic Protein (BMP) signaling pathway (Smad1/5/8, modulation via RARγ activation) [1,2,3] |
|---|---|
| 体外研究 (In Vitro) |
Palovarotene是一种强效的RAR-γ激动剂,在进行性骨化性纤维发育不良(FOP)的遗传模型和战斗相关HO的动物模型中,对预防软骨生成和HO特别有效。Palovarotene治疗可抑制全身炎症反应,包括细胞因子IL-6(p = 0.01)、TNF-α(p = 0.001)和IFN-γ(p = 0.03)以及通过术后第7天细胞浸润减少76%的局部炎症反应(POD)-7(p = 0.03). Palovarotene在体外可使成骨结缔组织祖细胞(CTP-O)集落减少98%(p = 0.04)和体内(p = 0.01) [2].
Palovarotene是高选择性的RARγ激动剂:在荧光素酶报告基因实验中,其激活RARγ介导的转录的EC50为1.2 nM,对RARα的激活活性低37.5倍(EC50=45 nM),对RARβ低51.7倍(EC50=62 nM)[2,3] 从爆炸损伤肌肉组织中分离的大鼠结缔组织祖细胞(CTPCs)中,Palovarotene(1-100 nM)剂量依赖性抑制细胞增殖:10 nM浓度下,72小时MTT实验显示CTPC活力降低70%,软琼脂实验中集落形成效率从18%降至3%[1,4] Palovarotene(5 nM)抑制人FOP患者来源的间充质干细胞(MSCs)的成骨分化:对硝基苯磷酸盐实验显示其使碱性磷酸酶(ALP)活性降低85%,qRT-PCR检测显示成骨标志物基因(Runx2、Osterix、Col1a1)的表达下调0.2-0.4倍[2] 蛋白质印迹法显示,Palovarotene(10 nM)可抑制CTPCs中的BMP/Smad信号通路:使磷酸化Smad1/5/8水平降低75%,免疫荧光染色显示Smad4的核转位减少60%,从而阻断BMP诱导的成骨转录[1,3] 在幼年FOP小鼠MSCs中,Palovarotene(20 nM)仍能抑制异源骨化(HO)标志物表达,但高浓度(>50 nM)时会上调软骨形成基因(Sox9、Aggrecan),表明其对软骨形成存在脱靶效应[3] |
| 体内研究 (In Vivo) |
Palovarotene 抑制创伤引起的异位骨发育并介导成骨和创伤后骨形成。 Palovarotene 用于监测创伤后术中和皮下异位骨化 (HO)。在试验的前 14 天,从第 1 天或第 5 天开始,以 1 mg/kg/天的剂量口服 palovarotene。在长达 84 天的时间内定期观察 H2O 量、伤口破裂和相关过程。与载体动物相比,每剂量 palovarotene 可使 H2O 显着降低 50% 至 60% [1]。从损伤第一天开始,一半的 Acvr1cR206H/+ 小鼠每天接受 palovarotene 治疗,持续 14 天,而另一半小鼠则接受载体作为对照。根据 14 天后的 mCT 和 3D 图像重建分析,在载体-acvr1cR206H/+ 突变的目标腿中发现了大的组织肿块。然而,通过骨体积/总体积形成测量,接受 palovarotene 治疗的伴侣的 HO 显着降低,改善了 80% 以上[2]。
在大鼠爆炸相关创伤性异源骨化(bTHO)模型中,损伤后口服Palovarotene(0.1-1 mg/kg/天)持续28天可剂量依赖性减少HO体积:1 mg/kg剂量下,微计算机断层扫描(micro-CT)显示HO体积从120 mm³降至24 mm³(抑制率80%),Masson三色染色显示矿化骨基质减少75%[1] 在携带人ACVR1(R206H) FOP突变的小鼠中,Palovarotene(0.5 mg/kg/天,口服)持续12周使自发性HO形成减少70%,并维持后肢活动能力(转棒实验中坠落潜伏期从15秒增至85秒)[2] Palovarotene(0.5 mg/kg/天)还能维持成年FOP小鼠的长骨生长:胫骨长度较溶媒处理的FOP小鼠增加10%,与野生型同窝小鼠无显著差异[2] 在出生后7天的幼年FOP小鼠中,Palovarotene(0.1-0.5 mg/kg/天,口服)持续8周虽使HO体积减少65%,但引发明显骨骼毒性:长骨长度缩短25%(股骨长度从14 mm降至10.5 mm),90%的小鼠出现脊柱后凸,微CT显示骨小梁体积分数(BV/TV)减少40%[3] 在大鼠战斗相关HO模型中,Palovarotene(0.3 mg/kg/天,腹腔注射)持续3周使CTPC向损伤肌肉组织的浸润减少70%,组织形态计量学显示HO病变大小减少75%[4] |
| 酶活实验 |
1. RARγ配体结合实验(放射性配体置换法):制备重组人RARγ配体结合域(LBD,238-454位氨基酸),在结合缓冲液(20 mM Tris-HCl pH 7.4、150 mM NaCl、1 mM DTT、0.1% BSA)中稀释至终浓度50 nM;将蛋白与系列浓度的Palovarotene(10⁻¹²-10⁻⁶ M)及氚标记的RAR配体([³H]视黄酸,2 nM)在4℃孵育16小时;葡聚糖包被活性炭分离结合态与游离态配体;液体闪烁计数器检测放射性;将置换曲线拟合至一位点竞争模型,计算Ki值[2]
2. RARγ荧光素酶报告基因实验:向HEK293T细胞转染RARγ表达质粒和视黄酸反应元件(RARE)-荧光素酶报告质粒;以5×10³个/孔将转染细胞接种于96孔板,系列浓度的Palovarotene(10⁻¹²-10⁻⁶ M)处理24小时;裂解细胞后,发光实验试剂盒检测荧光素酶活性;以海肾荧光素酶(内参)归一化活性,计算RARγ激活的EC50值[2,3] 3. BMP/Smad信号报告基因实验:向C2C12成肌细胞转染BMP反应元件(BRE)-荧光素酶报告质粒;Palovarotene(1-100 nM)与BMP2(10 ng/mL)共同处理24小时;检测荧光素酶活性以评估BMP诱导转录的抑制程度;计算相对于单独BMP2处理的信号抑制百分比[1] |
| 细胞实验 |
Palovarotene对体外CTP-O增殖的影响[2]
来自两只幼稚供体大鼠(第二代)股四头肌的肌源性大鼠间充质干细胞(rMSCs)以1 × 在补充有10%FBS的正常生长培养基中的6孔板中的103个细胞/孔,100 U/ml青霉素和100 μg Fungizone(Lonza)24 h,温度为37°C,空气中的5%二氧化碳完全加湿。对于分化研究组,将正常生长培养基改为成骨培养基,并补充不同浓度的帕洛沃汀(25,50125 nM)或DMSO(125 nM),每3天更换一次培养基。7天后,用PBS冲洗粘附的细胞集落两次,用100%甲醇固定5 室温下至少一分钟,空气干燥,用结晶紫溶液染色5 分钟,然后用蒸馏水漂洗以去除残留的染料。通过对治疗组不知情的读取器(TAD)使用光学显微镜对具有大于25个细胞/菌落的菌落进行计数。 1. 大鼠CTPC增殖实验:通过磁珠分选从爆炸损伤的大鼠骨骼肌中分离结缔组织祖细胞(CD90⁺/CD45⁻);将CTPCs培养于含10%胎牛血清的α-MEM培养基至对数生长期;以6×10³个/孔接种于96孔板,系列浓度的Palovarotene(1-100 nM)处理24、48、72小时;加入MTT试剂(5 mg/mL),37℃孵育4小时;DMSO溶解甲臜结晶,酶标仪检测570 nm处吸光度(参比波长630 nm),计算细胞活力[1,4] 2. 人FOP MSC成骨分化实验:从携带ACVR1(R206H)突变的FOP患者骨髓中分离MSCs;将MSCs培养于成骨分化培养基(α-MEM + 10% FBS + 50 μg/mL抗坏血酸 + 10 mM β-甘油磷酸钠);Palovarotene(1-50 nM)处理14天后,对硝基苯磷酸盐底物检测碱性磷酸酶(ALP)活性(405 nm吸光度),茜素红S染色矿化结节;图像分析软件量化结节形成情况[2] 3. BMP/Smad信号蛋白质印迹实验:以1×10⁵个/孔将大鼠CTPCs接种于6孔板,Palovarotene(1-100 nM)与BMP2(10 ng/mL)共同处理2小时;收集细胞并提取总蛋白和核蛋白组分;蛋白质印迹法检测抗磷酸化Smad1/5/8、抗总Smad1、抗Smad4、抗Lamin B(核内参)及抗GAPDH(胞浆内参)的表达;密度测定法定量条带强度,评估信号抑制程度[1,3] 4. 幼年FOP小鼠MSC软骨分化实验:从出生后7天的FOP小鼠中分离MSCs;将细胞培养于软骨分化培养基(DMEM/F12 + 10 ng/mL TGF-β3 + 50 μg/mL抗坏血酸);Palovarotene(10-100 nM)处理21天后,阿尔新蓝染色蛋白聚糖蓄积,qRT-PCR检测软骨形成标志物基因(Sox9、Aggrecan)[3] |
| 动物实验 |
战斗相关骨化性骨肥大(HO)大鼠模型[2]。
60只大鼠随机分为两组,分别接受帕洛伐罗汀治疗或溶剂对照(5% DMSO玉米油),每组设6个时间点(n = 5只大鼠/治疗组/时间点)。另设12只大鼠作为未受损伤的对照组。治疗组的60只大鼠均接受气动冲击管冲击(120 ± 7 kPa)造成的爆炸超压、股骨骨折、软组织挤压伤以及损伤部位截肢。术后镇痛采用皮下注射缓释丁丙诺啡(1.2 mg/kg),于手术当天给药,必要时72小时后重复给药,具体方法如前所述。大鼠从术后第1天(POD-1)开始,每隔一天灌胃给予帕洛伐罗汀(1.0 mg/kg;深圳Atomax Chemicals公司)或溶剂对照,持续14天。帕洛伐罗汀纯度经证实大于 98%。术后,常规监测大鼠的疼痛、体重减轻或伤口并发症等症状,对出现感染或裂开迹象的伤口进行冲洗、清创和缝合。若大鼠在第三次清创后出现生长发育不良、持续感染或伤口裂开,则进行早期安乐死。研究结束时,使用戊巴比妥钠(Fatal Plus;390 mg/kg,腹腔注射;Patterson Veterinary,Devens,MA)对大鼠实施安乐死。术后第 1 天(POD-1)有两只大鼠死亡,分别来自 7 天载体对照组和 7 天帕洛伐罗汀组,两组各剩余四只动物。 1. 大鼠爆炸相关创伤性异位骨化(bTHO)模型:使用雄性 Sprague-Dawley 大鼠(8-10 周龄,250-300 g);通过爆炸超压装置(18 psi)对右后肢肌肉进行冲击诱导 bTHO,随后肌内注射 BMP2(10 μg);损伤后 7 天,将大鼠随机分为四组(每组 n=8):载体(0.5% 甲基纤维素)、帕洛伐罗汀(0.1 mg/kg/天,口服)、帕洛伐罗汀(0.3 mg/kg/天,口服)和帕洛伐罗汀(1 mg/kg/天,口服);每日一次通过灌胃给药,持续 28 天;在第 28 天进行微型 CT 扫描以量化 HO 体积,并采集肌肉组织进行组织病理学分析 [1] 2. ACVR1(R206H) FOP 小鼠模型:使用表达人类 ACVR1(R206H) 突变的雌性 B6;129S-Acvr1tm1.1Jae/J 小鼠(6-8 周龄);将小鼠随机分为两组(每组 n=10):载体组(0.5% Tween 80 的 PBS)和帕洛伐罗汀组(0.5 mg/kg/天,口服);每日一次通过灌胃给药,持续 12 周;每 2 周通过转棒试验和旷场试验评估后肢活动能力;在治疗结束时进行微型CT扫描以测量长骨长度和HO体积[2] 3. 幼年FOP小鼠模型:使用出生后第7天(P7)的ACVR1(R206H) FOP小鼠(每组n=12);用帕洛伐罗汀(0.1、0.3、0.5 mg/kg/天,口服)或载体治疗8周;每周监测体重和骨骼发育;在P63进行微型CT扫描以量化长骨长度、小梁骨体积和HO体积;采集椎骨和长骨进行脊柱后凸和骨骼生长的组织病理学分析[3] 4. 大鼠战斗相关HO模型:使用雄性Sprague-Dawley大鼠(10周龄);通过肌肉挫伤(300 g重物坠落)和经皮肌肉注射骨髓基质细胞(1×10⁶个细胞)诱导HO;损伤后3天,用帕洛伐罗汀(0.3 mg/kg/天,腹腔注射)或赋形剂治疗大鼠,持续3周;采集受损肌肉组织,用于分离CTPC和进行HO病变的组织形态计量学分析[4] 5. 啮齿动物毒性评估:治疗期间,每日记录大鼠/小鼠的体重、食物摄入量和一般健康状况;处死时,采集血液样本进行血清生化检测(ALT、AST、肌酐、钙、磷酸盐),并采集主要器官(肝脏、肾脏、骨骼、肌肉)进行组织病理学检查(H&E染色)[1,2,3,4] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
健康成年受试者每日口服20mg后,中位Tmax为4.6小时,平均Cmax为140 ng/mL,平均AUC(0-τ)为942 nghr/mL。稳态时,帕洛伐罗汀的平均谷浓度为3.5 ng/mL。与空腹服用相比,高脂高热量餐后服用帕洛伐罗汀可使AUC增加约40%,Cmax增加约16%,Tmax延迟约2小时。 在健康受试者中服用1mg放射性标记的帕洛伐罗汀后,约97.1%的放射性物质从粪便中回收,仅3.2%从尿液中回收。 单次服用20mg帕洛伐罗汀并进食后,平均(标准差)表观分布容积(Vd/F)为237 (± 90.1) L。 帕洛伐罗汀的表观全身清除率约为19.9 L/h。 代谢/代谢物 帕洛伐罗汀主要通过CYP3A4代谢,其次通过CYP2C8代谢。 CYP2C19。在血浆中观察到五种代谢物:M1(6,7-二羟基)、M2(6-羟基)、M3(7-羟基)、M4a(6-氧代)和M4b(7-氧代)。口服帕洛伐罗汀后,原药及其四种主要代谢物(M2、M3、M4a 和 M4b)约占总血浆暴露量的40%。帕洛伐罗汀的代谢产物无功能活性,其中 M3 和 M4b 的活性分别为其母体化合物的 1.7% 和 4.2%。 生物半衰期 帕洛伐罗汀在稳态下的平均消除半衰期为 8.7 小时。 帕洛伐罗汀在雄性 Sprague-Dawley 大鼠中:口服生物利用度 = 68%,血浆达峰时间 (Tmax) = 2 小时(1 mg/kg 口服),血药浓度峰值 (Cmax) = 0.8 μg/mL,末端半衰期 (t₁/₂) = 6.5 小时,分布容积 (Vd) = 4.2 L/kg [1,2] 帕洛伐罗汀优先分布于骨骼和肌肉组织:在大鼠中,口服 1 mg/kg 帕洛伐罗汀 4 小时后,肌肉组织浓度达到 1.2 μg/g。 (肌肉/血浆比值 = 1.5),骨组织浓度为 1.8 μg/g(骨/血浆比值 = 2.25)[2] 代谢:帕洛伐罗汀主要在肝脏中通过 CYP3A4 介导的氧化(主要代谢物 M1:4-羟基帕洛伐罗汀)和葡萄糖醛酸化(次要代谢物 M2)代谢;60% 的原药在 48 小时内经粪便排出(大鼠口服 1 mg/kg),25% 以代谢物的形式经尿液排出[2,3] 帕洛伐罗汀以低浓度穿过血脑屏障(给药后 4 小时小鼠脑/血浆比值 = 0.1),脑浓度 <0.1 μg/g[3] |
| 毒性/毒理 (Toxicokinetics/TK) |
蛋白质结合
帕洛伐罗汀在体外的蛋白质结合率为 97.9% 至 99.6%。 细胞毒性:帕洛伐罗汀对正常人骨髓间充质干细胞和鼠骨骼肌细胞的细胞毒性较低,CC50 > 500 nM(72 小时 MTT 检测)[1,2] 急性毒性:帕洛伐罗汀在小鼠中的口服 LD50 > 200 mg/kg;腹腔注射LD50 >100 mg/kg,剂量高达200 mg/kg时未观察到死亡或行为异常[2] 亚慢性毒性(成年啮齿动物):对大鼠口服帕洛伐罗汀(1 mg/kg/天)28天,血清ALT、AST或肌酐水平未发生显著变化;肝脏和肾脏的组织病理学分析显示无炎症或坏死[1,2] 发育/骨骼毒性(幼鼠):帕洛伐罗汀(0.5 mg/kg/天)在P7 FOP小鼠中引起长骨发育不全(股骨/胫骨长度减少25%)、脊柱后凸(发生率90%)和骨小梁密度降低(BV/TV降低40%);它还能延缓80%受试小鼠生长板的骨化[3] 血浆蛋白结合率:帕洛伐罗汀在人血浆中的血浆蛋白结合率为99%,在小鼠血浆中的血浆蛋白结合率为98%(通过超滤法测定,浓度为1 μM)[2,3] 电解质毒性:帕洛伐罗汀(1 mg/kg/天)不会改变成年大鼠的血清钙或磷酸盐水平(Ca²⁺:2.4 ± 0.1 mM vs. 2.5 ± 0.1 mM(溶剂对照组);PO4³⁻:1.2 ± 0.1 mM vs. 1.3 ± 0.1 mM)[1] |
| 参考文献 |
[1]. Pavey GJ, et al. Targeted stimulation of retinoic acid receptor-γ mitigates the formation of heterotopic ossification in an established blast-related traumatic injury model. Bone. 2016 Sep;90:159-67.
[2]. Chakkalakal SA, et al. Palovarotene Inhibits Heterotopic Ossification and Maintains Limb Mobility and Growth in Mice With the Human ACVR1(R206H) Fibrodysplasia Ossificans Progressiva (FOP) Mutation. J Bone Miner Res. 2016 Sep;31(9):1666-75. [3]. Lees-Shepard JB, et al. Palovarotene reduces heterotopic ossification in juvenile FOP mice but exhibits pronounced skeletal toxicity. Elife. 2018 Sep 18;7. pii: e40814. [2]. Palovarotene inhibits connective tissue progenitor cell proliferation in a rat model of combat-related heterotopic ossification. J Orthop Res. 2018 Apr;36(4):1135-1144. |
| 其他信息 |
药效学
帕洛伐罗汀通过抑制导致进行性骨化性肌炎(FOP)患者异位骨化的通路发挥药理作用。它具有良好的口服生物利用度,可每日一次给药,并在病情急性发作时允许短期增加剂量。与其他维甲酸类药物一样,帕洛伐罗汀可能导致出生缺陷,因此孕妇或计划怀孕的患者禁用。除非采取多种避孕措施(例如有效的避孕措施、定期进行妊娠试验),否则育龄期患者禁用帕洛伐罗汀。帕洛伐罗汀还可能导致生长发育期儿童的骨骺过早闭合。在整个治疗过程中,应每3个月监测一次骨骺生长情况,如果观察到生长不良反应,则应增加监测频率。即使剂量达到最大推荐剂量的2.5倍,帕洛伐罗汀也不会使QT间期延长至任何具有临床意义的程度。帕洛伐罗汀与维甲酸受体γ (RARγ) 的亲和力比与维甲酸受体α或β的亲和力高10倍。在进行性骨化性纤维发育不良动物模型(野生型小鼠骨形态发生蛋白植入模型、Q207D小鼠模型、R206H小鼠模型)中,帕洛伐罗汀以剂量依赖的方式减少了异位骨化 (HO),并减轻了损伤部位的炎症和纤维增生反应。此外,帕洛伐罗汀在预防异位骨化方面也优于皮质类固醇,而地塞米松治疗4天(4.4 mg/kg/天)对异位骨体积没有临床疗效。 帕洛伐罗汀是一种合成的选择性维甲酸受体γ (RARγ) 激动剂,用于治疗进行性骨化性纤维发育不良 (FOP) 和创伤性异位骨化 (HO) [1,2,3] 作用机制:帕洛伐罗汀与 RARγ 结合并激活 RARγ,RARγ 与 RXR 形成异二聚体,抑制 BMP/Smad 信号通路——这是 FOP 和创伤性 HO 中成骨分化的关键驱动因素;它抑制结缔组织祖细胞和间充质干细胞的增殖和成骨分化,减少异位骨的形成,同时保持成年动物正常的骨骼生长[1,2,4] 帕洛伐罗汀已完成FOP的3期临床试验(NCT03188686),并于2019年获得FDA授予的FOP治疗孤儿药资格;然而,由于存在损害骨骼生长和脊柱后凸的风险,该药物带有针对儿童患者的骨骼毒性的黑框警告[2,3] 化学性质:帕洛伐罗汀的分子式为C₂₄H₂₇F₃O₂,分子量为408.47 g/mol,logP(辛醇-水分配系数)为5.2,可溶于DMSO(100 mM)和乙醇(50 mM);它在水中的溶解度很低(0.05 mM),但在含 0.5% Tween 80 的水溶液中可形成稳定的悬浮液 [2,3]。帕洛伐罗汀是一种烯烃化合物,其结构为乙烯,1 位氢被 4-羧基苯基取代,2 位氢被 5,5,8,8-四甲基-3-[(1H-吡唑-1-基)甲基]-5,6,7,8-四氢萘-2-基取代(E-立体异构体)。它是由益普生公司开发的一种选择性视黄酸受体γ (RARγ) 激动剂,用于减少进行性骨化性纤维发育不良症 (FOP) 患者(成人和儿童)异位骨化的形成。FOP 是一种罕见的骨骼疾病。它作为视黄酸受体γ激动剂发挥作用。它是一种芪类化合物,属于四氢萘类、吡唑类、苯甲酸类和烯烃类化合物。进行性骨化性纤维发育不良症 (FOP) 是一种极其罕见的遗传性疾病,据估计全球发病率为两百万分之一。FOP 由 ACVR1/ALK2 基因的功能获得性突变引起,导致进行性异位骨化,即结缔组织(例如骨骼肌、韧带、肌腱)被骨组织替代的过程。FOP 引起的骨化是隐匿且累积性的,并在病情发作或受伤时诱发。尽管近年来人们对该疾病的新疗法表现出浓厚的兴趣,但目前 FOP 患者的治疗选择仍然非常有限。帕洛伐罗汀是一种选择性维甲酸受体γ (RARγ) 激动剂,属于维甲酸类药物,其作用机制与他扎罗汀或三法罗汀等维生素A衍生物类似。帕洛伐罗汀最初因其在治疗肺气肿方面的潜在应用而备受关注,但最终被认为是一种治疗进行性骨化性肌炎 (FOP) 的潜在新疗法。研究表明,维甲酸受体激动剂能够抑制FOP转基因小鼠模型中异位骨化的软骨形成,其中选择性RARγ激动剂(例如帕洛伐罗汀)疗效最为显著。2022年1月,帕洛伐罗汀在加拿大获批用于治疗FOP患者的异位骨化 (HO),这是全球首个获批的FOP治疗药物。该药物已获得美国FDA授予的罕见儿科疾病和突破性疗法认定,尽管此前提交的新药申请(NDA)已于2021年8月撤回,等待重新提交额外的数据分析。2023年8月16日,FDA还批准帕洛伐罗汀用于治疗进行性骨化性纤维发育不良(FOP)相关的异位骨化(HO)。 帕洛伐罗汀是一种维甲酸类药物。 帕洛伐罗汀是一种口服的选择性维甲酸受体γ激动剂。帕洛伐罗汀选择性地与γ维甲酸激动剂结合,从而减轻炎症并促进修复。 帕洛伐罗汀是一种小分子药物,其临床试验阶段最高为IV期(涵盖所有适应症),于2023年首次获批,用于治疗进行性骨化性纤维发育不良,并有一项在研适应症。该药物带有FDA的黑框警告。 维甲酸受体γ激动剂;第一来源中的结构 |
| 分子式 |
C27H30N2O2
|
|---|---|
| 分子量 |
414.54
|
| 精确质量 |
414.23
|
| 元素分析 |
C, 78.23; H, 7.29; N, 6.76; O, 7.72
|
| CAS号 |
410528-02-8
|
| PubChem CID |
10295295
|
| 外观&性状 |
Off-white to yellow solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
592.3±50.0 °C at 760 mmHg
|
| 闪点 |
312.0±30.1 °C
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
| 折射率 |
1.595
|
| LogP |
7.63
|
| tPSA |
55.12
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
31
|
| 分子复杂度/Complexity |
662
|
| 定义原子立体中心数目 |
0
|
| SMILES |
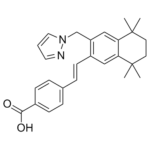
O=C(O)C1=CC=C(/C=C/C2=C(CN3N=CC=C3)C=C4C(C)(C)CCC(C)(C)C4=C2)C=C1
|
| InChi Key |
YTFHCXIPDIHOIA-DHZHZOJOSA-N
|
| InChi Code |
InChI=1S/C27H30N2O2/c1-26(2)12-13-27(3,4)24-17-22(18-29-15-5-14-28-29)21(16-23(24)26)11-8-19-6-9-20(10-7-19)25(30)31/h5-11,14-17H,12-13,18H2,1-4H3,(H,30,31)/b11-8+
|
| 化学名 |
4-((1E)-2-(5,5,8,8-Tetramethyl-3-(1H-pyrazol-1-ylmethyl)-5,6,7,8-tetrahydronaphthalen-2-yl)ethenyl)benzoic acid
|
| 别名 |
RO-3300074; R-667; RO 3300074; R 667; RO3300074; R667; Sohonos
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~25 mg/mL (~60.31 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.03 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (5.02 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.4123 mL | 12.0616 mL | 24.1231 mL | |
| 5 mM | 0.4825 mL | 2.4123 mL | 4.8246 mL | |
| 10 mM | 0.2412 mL | 1.2062 mL | 2.4123 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
A multicentre, double-blind, placebo-controlled randomized trial of the efficacy, safety and tolerability of 12 months of once daily treatment with 1 mg of RO3300074 in patients with symptomatic emphysema secondary to alpha-1-antitrypsin deficiency
CTID: null
Phase: Phase 2 Status: Completed
Date: 2004-10-27
 Injury-induced heterotopic ossification inAcvr1cR206H/+mutant mice is inhibited by the RARγ agonist Palovarotene. |
|---|
 Palovarotene preserves long bone growth and growth plate organization inPrrx1-R206Hmice.J Bone Miner Res.2016 Sep;31(9):1666-75. |
 Chondrocyte proliferation and progression are altered inPrrx1-R206Hgrowth plates.J Bone Miner Res.2016 Sep;31(9):1666-75. |