| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Sterol regulatory element-binding proteins (SREBPs)
|
|---|---|
| 体外研究 (In Vitro) |
Praeruptorin B 抑制 SREBP 活性并降低细胞内脂质水平。研究表明 Praeruptorin B 可以显着抑制 SRE 荧光素酶活性,并且这种影响具有剂量依赖性。即使浓度较高,Praeruptorin B 的细胞毒性也很低。 Praeruptorin B 还大幅下调 SREBP-1c 和 SREBP-2 的表达 [1]。 Praeruptorin B 还表现出对 UGT1A9 活性的显着抑制作用 [2]。
前胡素A(PA)和B(前胡素B/PB)是从白花前胡中分离得到的两个重要化合物,已被报道具有多种生化和药理活性。本研究旨在确定PA和PB对重要II期药物代谢酶尿苷5'-二磷酸葡萄糖醛酸基转移酶(UGTs)亚型活性的抑制作用。体外UGT孵育系统用于测定PA和PB对各种UGT亚型活性的抑制潜力。通过计算机模拟对接来解释PA和PB对UGT1A6活性的抑制差异。测定抑制行为,并使用体外抑制动力学参数(Ki)和PA体内暴露水平的组合进行体外-体内外推。前喷发素A(100μM)对UGT1A6和UGT2B7的活性抑制最强,100μM PA分别抑制了97.8%和90.1%的活性。计算机模拟对接研究表明,氢键相互作用对PA对UGT1A6的抑制作用比PB更强。前喷发素A非竞争性抑制UGT1A6的活性,竞争性抑制UGT2B7的活性。PA对UGT1A6和UGT2B7的抑制动力学参数(Ki)分别为1.2和3.3μM。PA对UGT1A6和UGT2B7的抑制[I]/Ki值分别为15.8和5.8,表明PA在体内对这两种UGT亚型具有很高的抑制潜力。因此,密切监测PA与主要经历UGT1A6或UGT2B7催化代谢的药物之间的相互作用是非常必要的。[2] 前喷发素A对UGT1A6和UGT2B7的活性抑制作用最强[2] 首先使用100微摩尔的PA和Praeruptorin B/PB来筛选对UGT亚型的抑制潜力(图1和图2)。在测试的UGT亚型中,PA和PB对UGT1A1、UGT1A3、UGT1A8和UGT1A10的活性没有或可以忽略不计的抑制潜力。100微摩尔的PA抑制了97.8%的活性(p < 0.001),但100 μM的PB没有抑制UGT1A6的活性。对于UGT1A7,其活性被抑制了68.3%(p < 0.001). PA和PB均对UGT1A9的活性表现出显著的抑制作用(p < 0.001). 100微摩尔的PA抑制了90.1%的UGT2B7活性(p < 0.001),100 μM的PB对UGT2B7的活性抑制了52.8%(p < 0.05). 在测试的UGT亚型中,PA对UGT1A6和UGT2B7的活性抑制作用最强。 氢键和疏水相互作用有助于前胡素A对UGT1A6的强烈抑制[2] 通过MODELLER程序构建了UGT1A6的三维结构,并在能量最小化后获得了最精细的模型。此外,配体PA和Praeruptorin B/PB被对接到UGT1A6的空腔中,活性空腔中的氨基酸残基如图3所示。配体PA和PB与UGT1A6的结合口袋由残基Gln34、Asp35、His38、Thr106、Ala107、Thr110、Glu111、Tyr112、Asn114、Asn115、Ala152、Arg172、Ile274、Gly275、Gly276、Met309、Ser311和Phe393组成。在结合袋中,抑制剂PA与Gly276的N原子形成一个氢键(图4)。此外,一些残基与PA形成疏水接触,包括疏水残基Ala152、Met309和Phe393;极性非带电残基Gln34、Tyr112、Asn114和Asn115;以及带极性电荷的残基Asp35、His38和Glu111,如图5A所示。前喷发蛋白B与UGT1A6没有形成氢键相互作用。前喷发蛋白B通过以下氨基酸残基与UGT1A6发生疏水相互作用:疏水残基Ala107、Ile274、Met309和Phe393;极性非带电残基Gln34、Thr106、Tyr112、Asn114、Asn115和Gly275;以及带极性电荷的残基Asp35、His38和Glu111(图5B)。 计算了抑制剂PA和PB对UGT1A6的结合自由能。前喷发素A以-5.52的结合自由能结合到UGT1A6的结合口袋中 kcal/mol,PB的结合自由能为-5.27 kcal/mol。因此,结合自由能的等级为PA < PB,表明PA对UGT1A6的抑制活性比PB更强,这与实验结果相当。 选择UGT1A8作为代表性的UGT亚型,以了解为什么PA没有特异性抑制某些UGT亚基。前爆发素A和B与UGT1A8的同一结合袋对接,结合袋中的残留物如支持信息中的图S1所示。UGT1A8的结合口袋由残基Ser36、His37、Phe39、Trp98、Phe109、Phe150、Arg170、Leu304、Gly305、Ser306、Met307、Arg333、Gln354、His369、Gly371、Ser372、His373、Gly374、Phe391、Asp393和Gln394组成。在PA和PB对UGT1A8的结合口袋中,这两种抑制剂与残基Gly374形成了相同的氢键(图S2)。此外,这两种抑制剂与UGT1A8形成疏水接触。前喷发蛋白A与残基Phe39、Phe109、Arg170、Ser306、Gln354、His369、Gly371、His373、Phe391和Asp393形成疏水接触。前喷发蛋白B与残基Ser36、His37、Phe39、Phe109、Phe150、Arg170、Leu304、Gly305、Ser306、Met307、Gly371、His369、His373、Phe391和Asp393形成疏水接触(图S3)。 前喷发蛋白A与UGT1A8相互作用,结合自由能为-7.64 kcal/mol。前喷发素B与PA的结合自由能与UGT1A8相似,结合自由能为-7.63 此外,PA和PB在结合袋中对UGT1A8产生了相似的相互作用。前喷发素A和B结合到UGT1A8的同一结合口袋中,并在结合口袋中与Gly374的N原子形成一个氢键。PA和PB都与非极性残基Phe39和Phe109形成疏水接触。所有这些结果都解释了为什么与PB相比,PA对UGT1A8没有表现出特异性抑制作用。 |
| 体内研究 (In Vivo) |
尽管它们仍然比饮食喂养的小鼠重,但用 Praeruptorin B (50 mg/kg) 治疗的小鼠明显比用载体治疗的小鼠轻,表明 Praeruptorin B 可能能够减轻饮食诱导的肥胖 (DIO)。更值得注意的是,用相同量的 Praeruptorin B 治疗的小鼠的脂肪/瘦肉和脂肪/体重比均显着降低。此外,研究表明,与高脂肪饮食的小鼠相比,用 prateruptorin B 治疗的动物血清 TC 和 TG 水平要低得多。与洛伐他汀类似,preruptorin B 会升高 HDL-c 并降低 LDL-c。此外,与给予赋形剂的小鼠相比,praeruptorin B 与洛伐他汀相当,它显着降低了肝脏中 TC 和 TG 的水平。根据染色结果,与用媒介物治疗的小鼠相比,用普拉普托林 B 治疗的小鼠显示出脂质积聚减少。在喂食高脂肪饮食的大鼠中,葡萄球菌前蛋白 B 显着降低升高的空腹血糖和胰岛素水平 [1]。
|
| 酶活实验 |
前胡素A和B对UGTs活性抑制潜力的测定[2]
根据之前的文献(Tang等人,2016;Liu等人,2016)对PA和Praeruptorin B/PB对UGTs活性的抑制作用进行了评估。体外培养混合物由以下成分组成 mM Tris-HCl缓冲液(pH = 7.4):MgCl2(5 mM)、II相辅因子UDPGA(5 mM”)、探针底物4-MU和重组UGT。PA和PB的储备溶液(20mM)通过使用二甲亚砜制备,并通过使用二甲基亚砜稀释制备各种浓度的工作溶液。预孵化5 min后,将UDPGA加入孵育混合物中以启动4-MU的葡糖醛酸化反应。反应温度、反应时间和分析条件已在之前描述过(Tang等人,2016;Liu等人,2016,Zhang等人,2017)。 |
| 动物实验 |
许多代谢性疾病是由脂质稳态紊乱引起的。甾醇调节元件结合蛋白(SREBPs)是一类与脂质从头合成相关的核转录因子,因此被认为是治疗代谢性疾病的潜在靶点。本研究鉴定出一种新型的SREBPs抑制剂——普拉普托林B。我们使用HepG2细胞验证了普拉普托林B的降脂作用。结果显示,SREBPs及其靶基因的表达均显著受到抑制。此外,我们发现普拉普托林B通过调控PI3K/Akt/mTOR通路抑制SREBP蛋白的表达。在高脂饮食(HFD)喂养的肥胖小鼠模型中,普拉普托林B显著改善了HFD诱导的脂质沉积、高脂血症和胰岛素抵抗,并且肝脏中SREBPs及其相关基因的表达也下调。这些研究结果表明,普拉普托林B通过调节SREBP发挥降脂作用,可能成为改善高脂血症及其并发症的潜在治疗选择。[1]
|
| 药代性质 (ADME/PK) |
既往文献已初步研究了PA和Praeruptorin B/PB的代谢消除途径。Song等人的实验表明,PA在人体内可快速代谢,氧化、水解、分子内酰基迁移和葡萄糖醛酸化是PA的主要代谢消除途径(Song等人,2014)。PB与人肝微粒体I相孵育混合物孵育后,生成了多种I相代谢物(Song等人,2011)。所有这些结果表明PA和PB可能与二甲氧基乙烷(DME)相互作用。本研究首次采用体外检测系统研究了PA和PB对各种UGT同工酶活性的抑制作用。结果显示,PA对UGT1A6和UGT2B7活性的抑制作用最强。采用计算机模拟分子对接方法解释了PA对代表性UGT同工酶UGT1A6活性的抑制作用强于PB的原因。PA和PB均可通过氢键和疏水相互作用对接至UGT1A6的活性腔。Praeruptorin A与UGT1A6形成一个氢键,而PB未与UGT1A6形成氢键。与PA相比,Praeruptorin B与UGT1A6形成更多的疏水相互作用。因此,氢键是PA对UGT1A6抑制作用较强的主要原因。
体内药物相互作用的强度可通过体外抑制动力学参数(Ki)和体内暴露浓度的结合进行预测。在肝硬化大鼠中,静脉注射5 mg/kg PA后,血浆浓度可达约7500 ng/mL(19 μM)。利用该值,计算得出PA对UGT1A6和UGT2B7抑制的[I]/Ki值分别为15.8和5.8。基于上述[I]/Ki标准,PA对UGT1A6和UGT2B7的体内抑制作用将非常强。 UGT1A6在异生物质和重要内源性物质的代谢中发挥着核心作用。例如,UGT1A6是催化神经递质血清素葡萄糖醛酸化代谢的关键酶(Sakakibara等,2015)。此外,UGT1A6还可以解毒致癌的芳胺和芳烃(Bock和Kohle,2005)。 UGT2B7 在催化多种临床药物(包括霉酚酸和 3′-叠氮-3′-脱氧胸苷(齐多夫定,AZT))的葡萄糖醛酸化代谢反应中发挥重要作用(Frymoyer 等,2013;Uchaipichat 等,2008)。UGT2B7 还可以结合一些内源性物质,包括胆汁酸、雄激素和雌激素(Gall 等,1999)。因此,PA 对这两种 UGT 同工酶的强抑制作用将显著干扰这些物质的代谢。 总之,本研究探讨了 PA 和Praeruptorin B/PB 对 UGT 同工酶的抑制作用,并证实了 PA 对 UGT1A6 和 UGT2B7 活性的强抑制作用。研究还预测了PA对UGT1A6和UGT2B7在体内可能具有高度抑制作用,这表明有必要监测PA与主要经UGT1A6或UGT2B7催化代谢的药物之间的相互作用。[1] |
| 参考文献 | |
| 其他信息 |
白花千屈菜(Peucedanum praeruptorum Dunn,伞形科)的干燥根是一种著名的传统中药,已被正式收录于《中国药典》。据报道,它具有多种生化和药理活性,包括解热和镇咳作用(Song et al., 2015; Xiong et al., 2012)。白花千屈菜素A(PA)和B(PB)是从白花千屈菜中分离得到的两种重要化合物,据报道它们具有多种治疗作用,包括心脏保护作用(Wang et al., 2004; Song et al., 2015)和抗炎作用(Yu et al., 2011; Xiong et al., 2012)。越来越多的研究发现PA和PB/白花千屈菜素B具有抗肿瘤的潜力。例如,PA及其衍生物已被证实能够逆转癌细胞中P-糖蛋白介导的多药耐药性(Shen et al., 2006; Shen et al., 2012; Fong et al., 2008)。据报道,Praeruptorin A和B对胃癌具有治疗作用(Liang et al., 2010)。因此,PA和PB是具有很高研发潜力的潜在候选药物。
新药候选药物的研发上市需要考虑诸多因素,药代动力学因素是其中最重要的因素之一。代谢行为仍然是药代动力学特性中最重要的因素,代谢评价包括代谢途径的鉴定和代谢酶抑制潜力的测定。药物代谢酶(DME)分为I期和II期DME。尿苷二磷酸葡萄糖醛酸转移酶(UGTs)是最重要的II期药物代谢酶,据报道参与多种外源性物质(例如药物、草药和污染物)(Atasilp等,2016)和内源性物质(例如雌激素、胆红素和胆汁酸)(Mu等,2016;Kallionpaa等,2015;Bock,2015)的代谢消除。UGTs活性的抑制会显著影响外源性物质和内源性物质的血浆暴露量。例如,茚地那韦和索拉非尼抑制UGT1A1催化的胆红素葡萄糖醛酸化,导致血浆胆红素浓度升高(Zucker等,2001;Peer等,2012)。双酚A和邻苯二甲酸酯对UGT同工酶活性的抑制作用已被用于解释双酚A和邻苯二甲酸酯的毒性机制(Jiang et al., 2013; Liu et al., 2016)。 本研究旨在确定PA和Praeruptorin B/PB对UGT同工酶活性的抑制作用。[2] |
| 分子式 |
C24H26O7
|
|---|---|
| 分子量 |
426.4590
|
| 精确质量 |
426.167
|
| 元素分析 |
C, 67.59; H, 6.15; O, 26.26
|
| CAS号 |
73069-28-0
|
| PubChem CID |
6450453
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.2±0.1 g/cm3
|
| 沸点 |
524.8±50.0 °C at 760 mmHg
|
| 熔点 |
175-176ºC
|
| 闪点 |
225.5±30.2 °C
|
| 蒸汽压 |
0.0±1.4 mmHg at 25°C
|
| 折射率 |
1.573
|
| LogP |
5.99
|
| tPSA |
92.04
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
31
|
| 分子复杂度/Complexity |
835
|
| 定义原子立体中心数目 |
0
|
| SMILES |
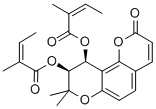
C/C=C(/C)\C(=O)OC1C(C(OC2=C1C3=C(C=C2)C=CC(=O)O3)(C)C)OC(=O)/C(=C\C)/C
|
| InChi Key |
PNTWXEIQXBRCPS-PVRNWPCDSA-N
|
| InChi Code |
InChI=1S/C24H26O7/c1-7-13(3)22(26)29-20-18-16(11-9-15-10-12-17(25)28-19(15)18)31-24(5,6)21(20)30-23(27)14(4)8-2/h7-12,20-21H,1-6H3/b13-7-,14-8-
|
| 化学名 |
[8,8-dimethyl-9-[(Z)-2-methylbut-2-enoyl]oxy-2-oxo-9,10-dihydropyrano[2,3-f]chromen-10-yl] (Z)-2-methylbut-2-enoate
|
| 别名 |
Praeruptorin B; Praeruptorin D; 73069-28-0; 73069-26-8; (9S,10S)-8,8-Dimethyl-2-oxo-9,10-dihydro-2H,8H-pyrano[2,3-f]chromene-9,10-diyl (2Z,2'Z)-bis(2-methylbut-2-enoate); (+/-)-Praeruptorin B; 4970-26-7; (+)-Praeruptorin B;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~25 mg/mL (~58.62 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (5.86 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.86 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液添加到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.3449 mL | 11.7244 mL | 23.4489 mL | |
| 5 mM | 0.4690 mL | 2.3449 mL | 4.6898 mL | |
| 10 mM | 0.2345 mL | 1.1724 mL | 2.3449 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。