| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Microbial Metabolite
|
|---|---|
| 药代性质 (ADME/PK) |
吸收、分布和排泄
本研究通过体外吸收实验探讨了二羟基丙酮 (DHA) 的代谢途径。在这些研究中,使用流通式扩散池测定了 24 小时或 72 小时内 DHA 在人体皮肤中的渗透和吸收情况。……对于 DHA,渗透研究发现,24 小时后,约 22% 的给药剂量残留在皮肤中(角质层和活性组织),形成药物储存库。渗透到皮肤中的 DHA 中,只有极少量能被全身吸收。 代谢/代谢产物 一些细菌利用甘油脱氢酶将甘油转化为二羟基丙酮 (DHA)。DHA 随后通过 ATP 或磷酸烯醇式丙酮酸 (PEP) 依赖性 DHA 激酶转化为磷酸二羟基丙酮 (DHA-P)。无害李斯特菌 (Listeria innocua) 含有两种潜在的 PEP 依赖性 DHA 激酶。其中一种由构成甘油(gol)操纵子的11个基因中的3个编码。该操纵子还包含golD(lin0362),它编码一种新型的DHA生成NAD+依赖性甘油脱氢酶。DHA的后续代谢需要通过PEP:糖磷酸转移酶系统组分酶I、HPr和EIIA(DHA)-2(Lin0369)进行磷酸化。P-EIIA(DHA)-2将其磷酸基团转移至DhaL-2,后者磷酸化与DhaK-2结合的DHA。生成的Dha-P可能主要通过磷酸戊糖途径代谢,因为gol操纵子中的两个基因编码类似于转酮醇酶和转醛醇酶的蛋白质。此外,纯化的Lin0363和Lin0364分别具有核糖-5-磷酸异构酶(RipB)和磷酸丙糖异构酶活性。后者将部分DHA-P转化为甘油醛-3-磷酸,后者与DHA-P一起通过糖异生途径代谢生成果糖-6-磷酸。转酮醇酶与另一个甘油醛-3-磷酸分子一起将果糖-6-磷酸转化为磷酸戊糖途径的中间体。gol操纵子前面是golR基因,该基因以相反的方向转录,编码一种DeoR型阻遏蛋白。golR基因的失活会导致整个gol操纵子(包括最后一个基因)组成型表达,但这种表达可被葡萄糖抑制。最后一个基因编码一种类乳酸菌素免疫(PedB样)蛋白。与野生型菌株或 pedB 样缺失突变体相比,golR 突变体中该物质合成水平升高,导致对乳酸菌素 PA-1 的免疫力略有增强。 |
| 毒性/毒理 (Toxicokinetics/TK) |
相互作用
……摄入二羟丙酮和丙酮酸 (DHP) 可增加正常男性肌肉对葡萄糖的提取。为了验证这些三碳化合物能否改善糖尿病患者的血糖控制,我们评估了 DHP 对 7 名非胰岛素依赖型糖尿病女性患者的血浆葡萄糖浓度、周转率、再利用率和耐受性的影响。受试者每日三次饮用含 1500 卡路里的膳食(55% 碳水化合物、30% 脂肪、15% 蛋白质),其中随机包含 13% 的卡路里来自 DHP (1/1) 或 Polycose(安慰剂;PL),持续 7 天。第 8 天,于早上 5:00 开始持续输注 [6-(3)H]-葡萄糖和 U-(14)C-葡萄糖,并在早上 9:00 进行 3 小时葡萄糖耐量试验(75 克葡萄糖)。两周后,受试者采用另一种饮食方案重复了该研究。空腹血糖水平在DHP组下降了14%(DHP = 8.0 ± 0.9 mmol/L;PL = 9.3 ± 1.0 mmol/L,p < 0.05),这解释了口服后血糖水平的降低(DHP = 13.1 ± 0.8 mmol/L,PL = 14.7 ± 0.8 mmol/L,p < 0.05)。 6-(3)H-葡萄糖周转率(DHP组为1.50 ± 0.19 mg/kg-L/min,PL组为1.77 ± 0.21 mg/kg-L/min,p < 0.05)和葡萄糖再循环率(6-(3)H-葡萄糖与U-(14)C-葡萄糖周转率之差)均随DHP的增加而降低(DHP组为0.25 ± 0.07 mg/kg-L/min,PL组为0.54 ± 0.10 mg/kg-L/min,p < 0.05)。空腹血糖、口服后血糖、血浆胰岛素、胰高血糖素和C肽水平不受DHP的影响。二羟基丙酮和丙酮酸的混合物。 二羟基丙酮 (DHA) 能有效拮抗氰化物对小鼠和兔的致死作用,尤其是在与硫代硫酸钠联合使用时。在小鼠腹腔注射氰化物前 10 分钟口服 DHA(2 和 4 g/kg),可使氰化物的 LD50 值分别从 5.7 mg/kg 增加到 12 和 17.6 mg/kg。在注射氰化物前 10-15 分钟口服 DHA 可最有效地预防氰化物引起的死亡。预先口服 DHA (4 g/kg) 并随后给予硫代硫酸钠 (1 g/kg) 可使氰化物的 LD50 值增加 9.9 倍。此外,在兔皮下注射氰化物5分钟后静脉注射DHA,氰化物的LD50从6 mg/kg增加到11 mg/kg以上;而静脉注射硫代硫酸钠(1 g/kg)后5分钟,氰化物的LD50仅增加到8.5 mg/kg。DHA还能预防氰化物中毒后发生的惊厥。 在小鼠中,二羟基丙酮(DHA)能有效拮抗氰化钾(CN)中毒,尤其是在与另一种CN解毒剂硫代硫酸钠联合使用时。DHA单独使用或与硫代硫酸钠联合使用也能预防氰化物引起的惊厥。在皮下注射CN后2分钟或前10分钟腹腔注射DHA(2 g/kg)分别使CN(8.7 mg/kg)的LD50值增加2.1倍和3.0倍。CN后联合使用DHA和硫代硫酸盐治疗使LD50值增加2.4倍。预先使用DHA和硫代硫酸盐(1 g/kg)治疗使CN的LD50值增加至83 mg/kg。CN后2分钟给予α-酮戊二酸(2.0 g/kg),而非丙酮酸,使CN的LD50值增加1.6倍。在体内给予CN治疗(有或无DHA)后,还测量了脑、心和肝脏的细胞色素氧化酶活性。预先使用DHA可阻止CN对细胞色素氧化酶活性的抑制,而CN后使用DHA治疗可加速细胞色素氧化酶活性的恢复,尤其是在脑和心匀浆中…… |
| 参考文献 |
|
| 其他信息 |
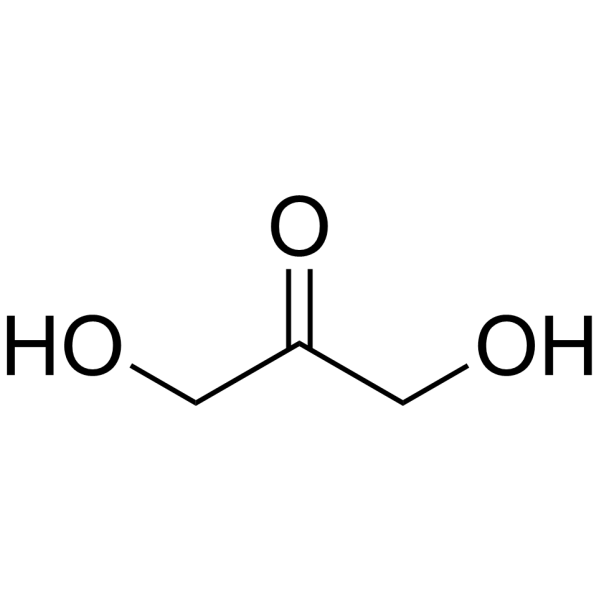
二羟基丙酮是一种酮三糖,由丙酮分子在1位和3位连接羟基构成。它是酮糖类中最简单的成员,也是甘油类化合物的母体。二羟基丙酮可作为代谢物、抗真菌剂、人体代谢物、酿酒酵母代谢物、大肠杆菌代谢物和小鼠代谢物。它是一种酮三糖,也是一种伯α-羟基酮。
二羟基丙酮是大肠杆菌(K12菌株、MG1655菌株)中发现或产生的代谢物。 拟南芥、人类和其他有相关数据的生物体中也报道过二羟基丙酮的存在。 二羟基丙酮是酿酒酵母中发现或产生的代谢物。 一种酮三糖化合物。在血液保存液中添加2,3-二磷酸甘油酸可更好地维持储存期间的2,3-二磷酸甘油酸水平。它易被红细胞中的三激酶磷酸化为磷酸二羟丙酮。与萘醌类化合物结合使用时,它可作为防晒剂。 作用机制 ……二羟丙酮的毒性似乎是由于其在细胞内转化为醛类化合物(推测为甲基乙二醛)所致,因为乙二醛酶突变体对二羟丙酮敏感。基于gldA基因位于ptsA同源基因和编码果糖-6-磷酸醛缩酶的talC基因所在的操纵子中这一信息,本研究提出gldA的主要功能是通过将有毒的二羟基丙酮转化为甘油来清除二羟基丙酮。 治疗用途 本研究的目的是评估一种新型二羟基丙酮(DHA)制剂在治疗暴露部位白癜风方面的特性。……十名面部和/或手部白癜风患者接受了一种新上市的、市售的含5% DHA的自晒黑霜的治疗。DHA每隔一天涂抹一次。治疗两周后,十名患者中有八名患者的特征性色素沉着显示出非常令人满意的美容效果。新型DHA配方是一种实用且广受认可的治疗方法。 /EXPL THER/ 二羟基丙酮 (DHA) 是一种三碳糖,是市售无日晒美黑产品中的褐变成分。……本研究测试了二羟基丙酮对皮肤真菌病致病菌(特别是皮肤癣菌和念珠菌属)的体外抗真菌活性。抗真菌活性采用肉汤微量稀释法测定,并参照美国临床和实验室标准协会 (CLSI) 针对酵母菌和丝状真菌的指南。所得数据显示,其杀菌活性浓度范围为1.6至50 mg/mL。DHA在与人工晒黑乳液相同的浓度下具有抗真菌特性,因此似乎是一种有前景的皮肤真菌病治疗物质。因此,由于其能渗透到皮肤角质层,它是一种潜在的低毒性抗真菌剂,可局部使用。 在为期七个月的春、夏、秋季临床试验中,30名UVA/B/Soret带光敏性患者依次局部涂抹二羟基丙酮(DHA),仅在睡前使用萘醌,获得了极佳的光保护效果,无一例治疗失败或患者失访。30名患者中有18名在七个月的时间里反复延长了光保护的耐受范围,能够在各种职业和休闲环境条件下耐受6至8小时的正午阳光照射而不被晒伤…… /实验治疗/……研究了局部应用二羟基丙酮(DHA)对浅色无毛hr/hr C3H/Tif小鼠预防太阳紫外线诱导的皮肤癌变的保护作用。三组小鼠每周接受四次紫外线照射,剂量相当于标准红斑剂量(SED)的四倍,其中一组小鼠每周两次涂抹5%或20%的DHA,另一组小鼠则不涂抹。同样,另三组小鼠接受DHA治疗后,再接受高剂量紫外线照射(8倍标准红斑剂量),模拟皮肤烧伤。两组小鼠(对照组)未接受照射,但未接受任何治疗,或仅接受20% DHA治疗。紫外线诱导的黑色素生成引起的皮肤色素沉着很容易与DHA诱导的皮肤褐变区分开来,并采用一种非侵入性的半定量方法进行测量。涂抹20% DHA可使4倍标准红斑剂量照射引起的色素沉着减少63%,但仅使8倍标准红斑剂量照射引起的色素沉着减少28%。此外,局部应用20% DHA显著延缓了接受4个标准红斑剂量照射的小鼠出现第一个≥1mm肿瘤的时间(P=0.0012)和第三个肿瘤出现的时间(P=2 x 10⁻⁶)。然而,20% DHA并未延缓接受8个标准红斑剂量照射的小鼠的肿瘤发展。5% DHA的应用对色素沉着或光致癌作用没有影响。 /实验治疗/……摄入二羟基丙酮和丙酮酸(DHP)可增加正常男性肌肉对葡萄糖的提取。为了验证这些三碳化合物能否改善糖尿病患者的血糖控制,我们评估了DHP对7名非胰岛素依赖型糖尿病女性患者的血浆葡萄糖浓度、周转率、再利用率和耐受性的影响。受试者连续7天每日三次饮用含1500卡路里的膳食(碳水化合物55%,脂肪30%,蛋白质15%),其中随机包含13%的卡路里以DHP(1/1)或聚葡萄糖(安慰剂;PL)的形式提供。第8天,于早上5:00开始持续输注[6-(3)H]-葡萄糖和[U-(14)C]-葡萄糖,并在早上9:00进行3小时葡萄糖耐量试验(75克葡萄糖)。两周后,受试者重复上述研究,但采用另一种膳食方案。 DHP 使空腹血糖水平降低了 14%(DHP = 8.0 + 或 - 0.9 mmol/L;PL = 9.3 + 或 - 1.0 mmol/L,p 小于 0.05),这解释了口服后血糖水平的降低(DHP = 13.1 + 或 - 0.8 mmol/L,PL = 14.7 + 或 - 0.8 mmol/L,p 小于 0.05)。 [6-(3)H]-葡萄糖周转率(DHP组为1.50 ± 0.19 mg/kg-L/min,PL组为1.77 ± 0.21 mg/kg-L/min,p < 0.05)和葡萄糖再循环率([6-(3)H]-葡萄糖和[U-(14)C]-葡萄糖周转率之差)均随DHP的增加而降低(DHP组为0.25 ± 0.07 mg/kg-L/min,PL组为0.54 ± 0.10 mg/kg-L/min,p < 0.05)。空腹血糖、口服后血糖、血浆胰岛素、胰高血糖素和C肽水平不受DHP的影响。/二羟丙酮和丙酮酸的混合物/。 |
| 分子式 |
C3H6O3
|
|---|---|
| 分子量 |
90.08
|
| 精确质量 |
90.031
|
| CAS号 |
96-26-4
|
| 相关CAS号 |
26776-70-5
|
| PubChem CID |
670
|
| 外观&性状 |
White to off-white solid
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
213.7±15.0 °C at 760 mmHg
|
| 熔点 |
75-80 °C
|
| 闪点 |
97.3±16.9 °C
|
| 蒸汽压 |
0.0±0.9 mmHg at 25°C
|
| 折射率 |
1.455
|
| LogP |
-0.78
|
| tPSA |
57.53
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
6
|
| 分子复杂度/Complexity |
44
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O=C(CO)CO
|
| InChi Key |
RXKJFZQQPQGTFL-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C3H6O3/c4-1-3(6)2-5/h4-5H,1-2H2
|
| 化学名 |
1,3-dihydroxypropan-2-one
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO :~100 mg/mL (~1110.12 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (27.75 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (27.75 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (27.75 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 11.1012 mL | 55.5062 mL | 111.0124 mL | |
| 5 mM | 2.2202 mL | 11.1012 mL | 22.2025 mL | |
| 10 mM | 1.1101 mL | 5.5506 mL | 11.1012 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。