| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
HDAC1 ( IC50 = 48 nM ); HDAC4 ( IC50 = 32 nM ); HDAC6 ( IC50 = 41 nM ); HIV-1
PTACH (compound 51) treatment increases p21WAF1/CIP1 and acetylated histone H4 levels in a dose-dependent manner[1]. PTACH (compound 51) exhibits robust activity in the assay for inhibiting the growth of cancer cells. At EC50 values of 2.3 μM, 9.1 μM, 3.0 μM, 2.6 μM, 1.1 μM, 4.5 μM, 2.4 μM, 5.0 μM, and 4.5 μM for MDA-MB-231, SNB-78, HCT116, NCI-H226, LOX-IMVI, SK-OV-3, RXF-631L, St-4, and DU-145 cells, respectively, PTACH inhibits a variety of cancer cells[1]. PTACH (NCH-51) increases the production of HIV-1 in latently infected OM10.1 cells. This reactivation is linked to a loss of HDAC1 occupancy and subsequent hyperacetylation of histones in nuc-1 at the HIV-1 promoter[2]. |
|---|---|
| 体外研究 (In Vitro) |
PTACH(化合物 51)治疗以剂量依赖性方式增加 p21WAF1/CIP1 和乙酰化组蛋白 H4 水平[1]。
PTACH(化合物 51)在抑制癌细胞的生长。 MDA-MB-231、SNB-78、HCT116、NCI-H226、LOX-的 EC50 值为 2.3 μM、9.1 μM、3.0 μM、2.6 μM、1.1 μM、4.5 μM、2.4 μM、5.0 μM 和 4.5 μM PTACH 分别在 IMVI、SK-OV-3、RXF-631L、St-4 和 DU-145 细胞中抑制多种癌细胞[1]。 PTACH (NCH-51) 可增加 HIV- 1 在潜伏感染的 OM10.1 细胞中。这种重新激活与 HDAC1 占据的丧失以及随后 HIV-1 启动子处 nuc-1 中组蛋白的过度乙酰化有关[2]。 用NCH-51单独处理潜伏感染HIV-1的OM10.1细胞(一种髓单核细胞白血病细胞系),能以剂量依赖方式(测试范围0-1.6 μM)诱导HIV-1 p24抗原的产生。与TNF-α (1 ng/ml)联合使用时,此效应进一步增强。 [1] 在经NCH-51处理的慢性感染HIV-1的ACH-2 T细胞中,也观察到类似的上调病毒产生的效果。 [1] 对OM10.1细胞全细胞裂解液的Western印迹分析显示,用NCH-51处理(0-1.6 μM,24小时)能以剂量依赖方式增加组蛋白H3在赖氨酸9或14位点的乙酰化。 [1] 在用1.6 μM NCH-51处理的OM10.1细胞中进行染色质免疫沉淀实验,结果显示HIV-1长末端重复序列的nuc-1区域组蛋白H3高度乙酰化,同时启动子处HDAC1的占据减少。该实验还显示HIV-1 LTR处正性转录因子(RNA聚合酶II、TBP)的富集以及负性调节因子AP-4的消失。 [1] 用拓扑异构酶II抑制剂新生霉素(100和200 μg/ml)处理OM10.1细胞,可抑制NCH-51介导的HIV-1 p24产生诱导,表明再激活涉及染色质结构的变化。 [1] 在293细胞和Jurkat T细胞中瞬时转染野生型和截短/突变型HIV-1 LTR驱动的荧光素酶报告质粒显示,NCH-51 (1.6 μM)能激活转录。突变所有三个Sp1结合位点(而非突变NF-κB位点)会严重减弱这种激活,表明Sp1位点对NCH-51的效应至关重要。 [1] 在TZM-bl细胞(含有稳定整合的HIV-1 LTR)中使用siRNA敲低Sp1,能显著抑制NCH-51诱导的LTR驱动的荧光素酶活性增加。 [1] 用Sp1抑制剂光神霉素A (50-100 nM)预处理OM10.1细胞,能以剂量依赖方式抑制NCH-51诱导的HIV-1 p24表达。 [1] |
| 细胞实验 |
细胞系:HCT 116 细胞
浓度:1 μM、5 μM、25 μM 孵育时间:8 小时 结果:乙酰化组蛋白 H4 和 p21 水平升高且呈剂量依赖性 WAF1/CIP1。 对于病毒复制实验,用或不用NCH-51处理潜伏感染的OM10.1细胞4小时,然后用或不用TNF-α (1 ng/ml)在37°C下刺激24小时。收集培养上清液,使用商业ELISA试剂盒检测HIV-1 p24抗原。使用WST-1方法平行测定化合物的细胞毒性,CC50定义为使细胞活力降低50%的浓度。 [1] 对于染色质免疫沉淀实验,OM10.1细胞用甲醛交联,裂解,染色质通过超声处理进行剪切。剪切后的染色质进行预清除,然后在4°C下与特异性抗体(如抗HDAC1、抗乙酰化H3、抗RNA Pol II)免疫沉淀过夜。使用磁珠收集免疫复合物,洗涤,洗脱,并进行反向交联。纯化DNA,并使用针对HIV-1 LTR nuc-1区域(-109至+79)的引物进行PCR分析。输入DNA(总染色质的10%)作为对照。 [1] 对于转染和荧光素酶实验,使用转染试剂将HIV-1 LTR-荧光素酶报告质粒转染到293细胞或Jurkat T细胞中。24小时后,用NCH-51 (1.6 μM)或TNF-α (5 ng/ml)作为阳性对照额外处理12或24小时。然后收获细胞,裂解,使用荧光素酶检测系统测量荧光素酶活性,并归一化至蛋白浓度。 [1] 对于siRNA敲低实验,TZM-bl细胞在培养板中培养,并根据制造商的说明使用脂质体转染试剂转染50 nM Sp1 siRNA或对照siRNA,孵育48小时。通过抗Sp1抗体的Western印迹确认敲低效率。然后将转染的细胞收获用于荧光素酶检测。 [1] |
| 药代性质 (ADME/PK) |
The article mentions that NCH-51 was designed based on the structure of SAHA (octanoylaniline hydroxamic acid), and that by replacing the hydroxamic acid group with an acylated thiol group, better pharmacokinetic properties and lower toxicity were obtained, and cites previous reports (reference 24). [1]
|
| 毒性/毒理 (Toxicokinetics/TK) |
After incubation for 48 hours in OM10.1 and ACH-2 cells, the cytotoxicity of NCH-51 was assessed using the WST-1 assay. The CC50 (50% cytotoxic concentration) of OM10.1 cells was estimated to be approximately 2.2 μM, and the CC50 of ACH-2 cells was estimated to be approximately 2.4 μM. [1]
|
| 参考文献 |
|
| 其他信息 |
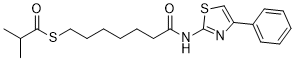
2-Methylpropionate S-[7-oxo-7-[(4-phenyl-2-thiazolyl)amino]heptyl] ester is an aromatic amide.
NCH-51 is a novel histone deacetylase inhibitor (HDACi). [1] It is designed based on the structure of the FDA-approved HDACi SAHA (vorinostat), replacing the hydroxamic acid group with an acylated thiol group in order to improve pharmacokinetics and reduce toxicity. [1] Studies have shown that NCH-51 can activate latent HIV-1 proviruses in latent cell line models (OM10.1, ACH-2). Its mechanism involves the inhibition of HDACs, leading to histone hyperacetylation, detachment of HDAC1 and the repressor AP-4 from the HIV-1 LTR, recruitment of positive transcription factors (RNA polymerase II, TBP), and subsequent activation of transcription. This transcriptional activation is highly dependent on the Sp1 binding site within the HIV-1 LTR promoter. [1] The combined use of NCH-51 and TNF-α can effectively activate HIV, suggesting its potential as a combination therapy against latent HIV infection. However, the study also points out that this type of approach needs careful evaluation. [1] |
| 分子式 |
C20H26N2O2S2
|
|---|---|
| 分子量 |
390.56264257431
|
| 精确质量 |
390.143
|
| 元素分析 |
C, 61.51; H, 6.71; N, 7.17; O, 8.19; S, 16.42
|
| CAS号 |
848354-66-5
|
| PubChem CID |
11395181
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.2±0.1 g/cm3
|
| 折射率 |
1.588
|
| LogP |
5.49
|
| tPSA |
112.6
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
11
|
| 重原子数目 |
26
|
| 分子复杂度/Complexity |
440
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O=C(C(C)C)SCCCCCCC(NC1SC=C(C2C=CC=CC=2)N=1)=O
|
| InChi Key |
MDYDGUOQFUQOGE-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C20H26N2O2S2/c1-15(2)19(24)25-13-9-4-3-8-12-18(23)22-20-21-17(14-26-20)16-10-6-5-7-11-16/h5-7,10-11,14-15H,3-4,8-9,12-13H2,1-2H3,(H,21,22,23)
|
| 化学名 |
S-[7-oxo-7-[(4-phenyl-1,3-thiazol-2-yl)amino]heptyl] 2-methylpropanethioate
|
| 别名 |
NCH-51; NCH 51; NCH51. PTACH
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~50 mg/mL (~128.0 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.40 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (6.40 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5604 mL | 12.8021 mL | 25.6043 mL | |
| 5 mM | 0.5121 mL | 2.5604 mL | 5.1209 mL | |
| 10 mM | 0.2560 mL | 1.2802 mL | 2.5604 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|
|