| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| Other Sizes |
|
| 靶点 |
Oxazolidinone antibacterial; MAO-A/B
|
||
|---|---|---|---|
| 体外研究 (In Vitro) |
体外活性:Tedizolid(以前称为 torezolid、TR-700 或 DA-7157,商品名 Sivextro)是一种针对革兰氏阳性菌的恶唑烷酮类抗生素。作用机制是通过与G+细菌的50S核糖体亚基结合来抑制蛋白质合成。磷酸泰地唑胺是活性化合物泰地唑胺的磷酸酯前药。它是由 Cubist Pharmaceuticals 收购 Trius Therapeutics(原韩国 Dong-A Pharmaceuticals)后开发的,并于 2014 年获得美国 FDA 批准,用于治疗急性细菌性皮肤和皮肤结构感染(也称为复杂性皮肤和皮肤感染)。皮肤结构感染(cSSSI))。激酶测定:泰地唑胺 (0.25 μg/mL) 抑制所有 28 种 PRSP 临床分离株,其抗 PRSP 效力是利奈唑胺的 4 倍 细胞测定:泰地唑胺 (0.25 μg/mL) 抑制所有 28 种 PRSP 临床分离株,且比利奈唑胺强 4 倍- 对抗 PRSP 的效力比利奈唑胺强一倍
|
||
| 体内研究 (In Vivo) |
雄性 ICR 小鼠(体重 18 至 20 g)腹膜内接种悬浮在 10% 粘蛋白中的 4 种 PRSP 分离株(DR9、DR10、DR11 或 DR14)中的 1 种,以诱导全身性肺炎链球菌感染。该悬浮液含有足够的细菌,足以杀死 100% 未经治疗的对照小鼠。感染后 1 小时,小鼠接受单剂量的磷酸泰地唑胺或利奈唑胺,并在感染后 7 天内每天评估存活情况。治疗以口服和静脉注射的方式进行,每种剂量有四种剂量(40毫克/千克体重、13.33毫克/千克、4.44毫克/千克和1.48毫克/千克),每组8只小鼠,根据剂量、递送方法、和感染菌株。使用概率分析计算每种递送途径的50%有效剂量(ED50),即允许50%受感染小鼠存活的剂量。
|
||
| 酶活实验 |
Tedizolid (0.25 μg/mL) 可抑制所有 28 种 PRSP 临床分离株,其抑制 PRSP 的效力是利奈唑胺的 4 倍。
敏感性测试。[1] PRSP(青霉素G MIC≥2μG/ml)临床分离株是在2002年至2004年间从韩国一家三级护理医院的患者身上收集的。该物种通过常规方法或使用ID 32 GN或ATB 32A系统进行鉴定。根据NCCLS指南,使用添加了5%羊血的Mueller Hinton琼脂,在琼脂稀释试验中测定了Tedizolid(活性形式)和利奈唑胺对28个PRSP分离株的MIC值。将噻二唑固体或利奈唑胺的储备溶液连续稀释2倍,得到10倍的溶液,在45至50°C下与9份Mueller Hinton琼脂混合,并补充5%的羊血。抗菌剂的最终浓度为128μg/ml至0.0313μg/ml。将琼脂倒入10cm的塑料培养皿中,深度为3-4mm,并在室温下固化。接种物由PRSP分离物过夜生长的单个菌落制备,方法是将其悬浮在肉汤中,调节浊度以匹配0.5 McFarland标准,并使用Steers复制器将104 CFU施加到制备的平板上,从无药物对照平板开始,以最高浓度的药物结束。在检查生长之前,将板在35°C下孵育16至20小时。肺炎链球菌ATCC 49619用作对照。每个分离物的MIC被确定为没有生长的最低浓度。 |
||
| 细胞实验 |
MIC测定[2]
根据CLSI指南,在阳离子调整的Mueller Hinton肉汤(CaMHB)中使用肉汤微量稀释法测定Tedizolid/TZD和LZD的MIC。简而言之,TZD以1.2mg/L的浓度溶解在二甲基亚砜(DMSO)中,随后在培养基中稀释。将细菌(约5×105 CFU/mL)接种到96孔微孔板中含有2倍稀释的抗生素(0.06-64μg/mL)的CaMHB中。将DMSO以与含TZD的孔中相同的浓度(最大浓度5%vol/vol)加入含LZD的孔。根据不含抗生素的对照孔的生长情况,在30°C下孵育3至5天后测定MIC,这在分离物之间有所不同。所有MIC均进行了三次,并报告了中值。使用参考菌株金黄色葡萄球菌CIP 4.83(ATCC 6538)作为对照。 时间杀伤试验[2] 如前所述(Lefebvre等人,2016),对Tedizolid/TZD进行了时间杀伤试验。脓肿分枝杆菌亚种的细菌悬浮液。将脓肿CIP 104536T在新鲜CaMHB中稀释1/1000,在30°C下在摇床培养箱(180 rpm)中培养2小时,使细菌密度达到105-106 CFU/mL。然后以相当于其MIC的4或8倍的浓度加入TZD,并将培养物在培养箱摇床(180 rpm。 协同研究[2] 如前所述(Bolhuis等人,2014),使用二维微稀释棋盘法进行协同测试。生长条件与MIC测定所用的条件相似,除了Tedizolid/TZD-克拉霉素组合,根据CLSI的建议,在第14天再次读取其结果,以监测耐药性的诱导。分数抑制浓度指数(FICI)计算如下:FICI=(MIC药物A联合/MIC药物A单独)+(MIC药物B联合/MIC药B单独),其中药物A为TZD,药物B为克拉霉素、替加环素、环丙沙星或阿米卡星。当FICI值≤0.5时,这两种化合物之间的相互作用被定义为协同作用,当FICI价值在0.5到4之间时,它们之间的作用是无关的,当FICI>4时,它们是拮抗的。 |
||
| 动物实验 |
|
||
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服替地唑胺后,血浆峰浓度在三小时内达到;静脉注射后,血浆峰浓度在一小时内达到;口服生物利用度约为91%。食物对吸收无影响。每日一次口服或静脉注射替地唑胺,约三天即可达到稳态血药浓度。口服单次给药后/稳态血药浓度峰值(Cmax)分别为2.0 ± 0.7/2.2 ± 0.6 mcg/mL,静脉注射分别为2.3 ± 0.6/3.0 ± 0.7 mcg/mL。同样,口服给药的Tmax中位数(范围)为2.5(1.0-8.0)/3.5(1.0-6.0)小时,静脉给药的Tmax中位数(范围)为1.1(0.9-1.5)/1.2(0.9-1.5)小时。口服给药的AUC为23.8±6.8/25.6±8.4 mcghr/mL,静脉给药的AUC为26.6±5.2/29.2±6.2 mcghr/mL。 单次口服给药后,约82%的替地唑利经粪便排泄,18%经尿液排泄。大部分以无活性的硫酸盐结合物形式存在,仅有3%以原形排出。超过 85% 的药物在 96 小时内消除。 单次静脉注射 200 mg 替地唑利后的分布容积为 67 至 80 L。在一项口服 200 mg 替地唑利至稳态的研究中,分布容积为 108 ± 21 L,而单次口服 600 mg 的表观分布容积为 113.3 ± 19.3 L。已观察到替地唑利可渗透至脂肪组织和骨骼肌组织的间质空间,也可在肺泡上皮衬液和肺泡巨噬细胞中发现。 单次口服替地唑利的表观清除率为 6.9 ± 1.7 L/hr,稳态清除率为 8.4 ± 2.1 L/hr。单次给药后,系统清除率为 6.4 ± 1.2 L/hr,稳态清除率为 5.9 ± 1.4 L/hr。 代谢/代谢物 替地唑胺以磷酸盐前药的形式给药,并在体内转化为替地唑胺(循环中的活性成分)。在排泄前,大部分替地唑胺在肝脏中转化为无活性的硫酸盐结合物,但这一过程不太可能涉及细胞色素 P450 家族酶的作用。 生物半衰期 替地唑胺的半衰期约为 12 小时。 |
||
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
替地唑利治疗与1%至4%的患者出现轻度、短暂的血清转氨酶和碱性磷酸酶水平升高有关,尽管使用包括利奈唑胺在内的类似药物治疗感染的患者也会出现类似的升高率。所有病例中,这些升高均无症状或黄疸,并在停药后恢复正常。 虽然替地唑利尚未与临床上明显的肝病伴黄疸病例相关,但利奈唑胺(一种类似的噁唑烷酮类抗生素)与乳酸性酸中毒和全身性损伤病例相关。这种综合征通常在治疗1至8周后出现,有时伴有肝损伤和黄疸的证据。乳酸性酸中毒通常是由于肝线粒体功能障碍或丢失所致,导致微泡性脂肪变性和肝功能紊乱(不一定伴有黄疸,甚至ALT或碱性磷酸酶升高)。其他与线粒体损伤相关的严重副作用包括周围神经病变和视神经病变、胰腺炎、5-羟色胺综合征和肾损伤。线粒体损伤被认为是由线粒体核糖体功能抑制所致,这与恶唑烷酮类药物对细菌核糖体功能的已知作用相符。乳酸性酸中毒通常在治疗1至8周后出现,病情可能较重,但停药后可迅速缓解。相比之下,此类抗生素引起的视神经病变和周围神经病变消退较慢,且可能为永久性。乳酸性酸中毒可能致命,在利奈唑胺引起的严重病例中,曾有肝功能障碍和黄疸的报道。尚未明确证实该综合征与替地唑利治疗有关。 可能性评分:E(未经证实但怀疑是肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于哺乳期使用替地唑利的信息。替地唑利在母体血浆中的结合率为70%至90%,因此预计不会有大量药物进入母乳。如果母亲需要服用替地唑利,这并非停止母乳喂养的理由,但由于目前尚无关于母乳喂养期间服用替地唑利的已发表经验,因此可能更倾向于选择其他药物,尤其是在哺乳新生儿或早产儿时。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 约70%至90%的替地唑利与人血浆蛋白结合。 |
||
| 参考文献 |
|
||
| 其他信息 |
药效学
替地唑胺是一种噁唑烷酮类抗生素,其作用机制是通过抑制细菌核糖体的蛋白质合成。然而,噁唑烷酮类抗生素也能与人线粒体核糖体结合,但不能与细胞质核糖体结合。线粒体蛋白质合成抑制与神经系统、血液系统和胃肠道毒性等不良反应相关,尽管替地唑胺的耐受性优于相关药物利奈唑胺。在治疗伴有急性细菌性皮肤及皮肤结构感染(ABSSSI)的中性粒细胞减少症患者时,应考虑其他治疗方案。已有报道,接受替地唑胺治疗的患者出现艰难梭菌相关性腹泻。 磷酸替地唑胺是一种磷酸单酯,由等摩尔量的磷酸与替地唑胺的羟基缩合而成。它是替地唑利的前药,用于治疗由某些敏感细菌引起的急性细菌性皮肤感染,包括金黄色葡萄球菌(包括耐甲氧西林菌株 (MRSA) 和甲氧西林敏感菌株)、多种链球菌属和粪肠球菌。它具有抗菌剂、蛋白质合成抑制剂和前药的双重作用。它是一种氨基甲酸酯、有机氟化合物、噁唑烷酮、吡啶类化合物、四唑类化合物和磷酸单酯。耐药菌,例如耐甲氧西林金黄色葡萄球菌、耐万古霉素粪肠球菌和耐青霉素肺炎链球菌,对公共卫生构成巨大威胁。替地唑胺属于噁唑烷酮类抗生素,该类抗生素还包括此前已获批准的利奈唑胺,通常对多重耐药革兰氏阳性菌有效。替地唑胺适用于治疗急性细菌性皮肤及皮肤软组织感染(ABSSSI),其疗效和耐受性通常优于利奈唑胺。2014年6月20日,美国食品药品监督管理局(FDA)批准替地唑胺上市,由Cubist Pharmaceuticals公司生产,商品名为磷酸替地唑胺(SIVEXTRO®)。该产品目前有口服片剂和静脉注射用粉剂两种剂型。 磷酸替地唑胺是替地唑胺的磷酸盐形式,替地唑胺是一种噁唑烷酮类抗菌药物,用于治疗由某些革兰氏阳性菌引起的急性细菌性皮肤及皮肤软组织感染。静脉注射后,替地唑利靶向并结合细菌核糖体的50S亚基,从而抑制细菌蛋白质合成。 磷酸替地唑利是一种小分子药物,其临床试验阶段最高为IV期(涵盖所有适应症),于2014年首次获批,用于治疗细菌感染引起的皮肤病,并有7个在研适应症。 作用机制 尽管人们加大了对抗抗菌素耐药性传播的努力,但包括耐甲氧西林金黄色葡萄球菌等革兰氏阳性菌在内的多重耐药菌仍然构成威胁。噁唑烷酮类药物是一类相对较新的抗菌药物,通过抑制蛋白质合成发挥作用,通常能够克服细菌对其他蛋白质合成抑制剂的耐药性。蛋白质合成涉及核糖体的作用,核糖体是由蛋白质和核糖体RNA(rRNA)取代基组成的多亚基复合物。信使RNA的转位以及伴随的蛋白质合成需要肽基转移酶中心(PTC)的A、P和E位点的作用,这些位点接受带电荷的氨酰tRNA并催化它们之间形成肽键。细菌70S核糖体由一个小的(30S)亚基和一个大的(50S)亚基组成。早期对恶唑烷酮类抗生素作用机制的研究表明,它们抑制蛋白质合成起始步骤。然而,这种机制与已定位的耐药突变不符。后续的交联和结合位点直接结构测定研究表明,包括利奈唑胺和替地唑胺在内的噁唑烷酮类药物通过与23S rRNA组分相互作用而结合于肽基转移酶中心(PTC)的A位点。结构研究还发现,噁唑烷酮类药物的结合会改变23S rRNA中一个保守核苷酸(大肠杆菌中的U2585)的构象,从而使PTC无法进行肽键形成。因此,替地唑胺通过抑制细菌蛋白质合成发挥作用。 药物适应症 替地唑胺适用于治疗皮肤及皮肤软组织急性细菌感染(ABSSSI)。为防止耐药性,替地唑利仅应用于由敏感细菌引起的感染。 Sivextro适用于治疗12岁及以上成人和青少年的急性细菌性皮肤及皮肤结构感染(ABSSSI)。 总之,本研究表明,替地唑利在体外对耐药肺炎链球菌(PRSP)分离株的效力是利奈唑胺的4倍,并且口服或静脉注射替地唑利磷酸盐可有效治疗小鼠体内PRSP分离株引起的全身感染。口服替地唑利磷酸盐也可有效治疗PSSP菌株引起的肺炎。这些结果表明,有必要进一步研究替地唑利磷酸盐在呼吸道中的药效学,以及对替地唑利磷酸盐治疗肺炎球菌感染进行临床评估。[1] 本研究表明,替地唑利类药物(TZD)在体外对脓肿分枝杆菌的活性优于利奈唑胺(LZD)。细胞内噻唑烷二酮类药物(TZD)的蓄积及其与克拉霉素对某些分离株的协同作用值得进一步研究。然而,推荐剂量200 mg后血浆药物浓度不足(Cmax ≈ 2 μg/mL)(Flanagan等人,2014),与该药物的最低抑菌浓度(MIC)相比,这使得人们对TZD治疗脓肿分枝杆菌感染的疗效产生怀疑,尽管更高的剂量可能克服这一问题。需要进一步研究以探索更高剂量TZD的疗效和毒性。[2] |
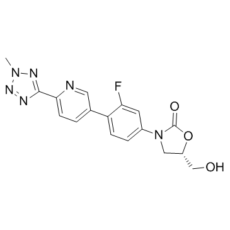
| 分子式 |
C17H15FN6O3
|
|---|---|
| 分子量 |
370.34
|
| 精确质量 |
370.118
|
| 元素分析 |
C, 55.13; H, 4.08; F, 5.13; N, 22.69; O, 12.96
|
| CAS号 |
1431699-67-0
|
| 相关CAS号 |
Tedizolid;856866-72-3;Tedizolid phosphate;856867-55-5; (S)-Tedizolid;1431699-67-0;Tedizolid-13C,d3; 856867-39-5 (disodium);
|
| PubChem CID |
71576658
|
| 外观&性状 |
Typically exists as White to off-white solid at room temperature
|
| 密度 |
1.6±0.1 g/cm3
|
| 沸点 |
614.5±65.0 °C at 760 mmHg
|
| 闪点 |
325.4±34.3 °C
|
| 蒸汽压 |
0.0±1.9 mmHg at 25°C
|
| 折射率 |
1.725
|
| LogP |
1.56
|
| tPSA |
106
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
8
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
27
|
| 分子复杂度/Complexity |
543
|
| 定义原子立体中心数目 |
1
|
| SMILES |
O=C1O[C@H](CO)CN1C2=CC=C(C3=CC=C(C4=NN(C)N=N4)N=C3)C(F)=C2
|
| InChi Key |
XFALPSLJIHVRKE-LBPRGKRZSA-N
|
| InChi Code |
InChI=1S/C17H15FN6O3/c1-23-21-16(20-22-23)15-5-2-10(7-19-15)13-4-3-11(6-14(13)18)24-8-12(9-25)27-17(24)26/h2-7,12,25H,8-9H2,1H3/t12-/m0/s1
|
| 化学名 |
(5S)-3-[3-fluoro-4-[6-(2-methyltetrazol-5-yl)pyridin-3-yl]phenyl]-5-(hydroxymethyl)-1,3-oxazolidin-2-one
|
| 别名 |
C17H15FN6O3; AMY30662; (S)-Tedizolid; 1431699-67-0; ent-Tedizolid; (5S)-3-[3-fluoro-4-[6-(2-methyltetrazol-5-yl)pyridin-3-yl]phenyl]-5-(hydroxymethyl)-1,3-oxazolidin-2-one; Tedizolid, (S)-; TYR9KD6MVB; C17H15FN6O3; (5S)-3-{3-fluoro-4-[6-(2-methyl-2H-1,2,3,4-tetrazol-5-yl)pyridin-3-yl]phenyl}-5-(hydroxymethyl)-1,3-oxazolidin-2-one;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ≥ 100 mg/mL (~270.02 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 3.75 mg/mL (10.13 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 37.5 mg/mL 澄清的 DMSO 储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL 生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 3.75 mg/mL (10.13 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 37.5 mg/mL 澄清 DMSO 储备液加入 900 μL 20% SBE-β-CD 生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More配方 3 中的溶解度: font color= ‘FF0000’>10% DMSO+40% PEG300+5% Tween-80+45% Saline: ≥ 3.75 mg/mL (10.13 mM) 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.7002 mL | 13.5011 mL | 27.0022 mL | |
| 5 mM | 0.5400 mL | 2.7002 mL | 5.4004 mL | |
| 10 mM | 0.2700 mL | 1.3501 mL | 2.7002 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。