| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
MIP-1α-CCR5 ( IC50 = 1 nM ); MIP-1β-CCR5 ( IC50 = 1 nM ); RANTES-CCR5 ( IC50 = 1.4 nM ); MCP-1-CCR2b ( IC50 = 27 nM ); R5 HIV-1 (Ba-L) ( EC50 = 1.2 nM ); R5 HIV-1 (Ba-L) ( EC90 = 5.7 nM ); R5 HIV-1 (Ba-L) ( EC50 = 3.7 nM ); R5 HIV-1 (Ba-L) ( EC90 = 12.8 nM ); R5 HIV-1 (KK) ( EC50 = 1.6 nM ); R5 HIV-1 (KK) ( EC90 = 20.8 nM ); R5 HIV-1 (HHA) ( EC50 = 3.2 nM ); R5 HIV-1 (HHA) ( EC90 = 7.5 nM ); R5 HIV-1 (CTV) ( EC50 = 3.5 nM ); R5 HIV-1 (CTV) ( EC90 = 27 nM ); mCXCR3( IC50 = 369 nM )
TAK-779 deters R5 HIV-1 in MAGI-CCR5 cells. It is a strong and selective nonpeptide antagonist of CCR5, with a Ki of 1.1 nM, with an effective and selective EC50 and EC90 of 1.2 nM and 5.7 nM, respectively. In CHO/CCR2b cells, TAK-779 less effectively inhibits the binding of [125I]-monocyte chemotactic protein 1 to CCR2b, with an IC50 of 27 nM for CCR2b. With an IC50 of 1.4 nM, TAK-779 also totally prevents [125I]-RANTES from binding to CHO/CCR5 cells. CCR5-mediated Ca2+-signaling is specifically inhibited by TAK-779 (20 nM). Furthermore, on X4 HIV-1 strains, TAK-779 exhibits no inhibition[1]. As an antagonist of CXCR3, TAK-779 prevents T cell migration but not proliferation[2]. |
|---|---|
| 体外研究 (In Vitro) |
TAK-779 (TAK779) 是一种有效的、选择性的 CCR5 非肽拮抗剂,Ki 为 1.1 nM,可有效、选择性地抑制 R5 HIV-1,在 MAGI-CCR5 中,EC50 和 EC90 分别为 1.2 nM 和 5.7 nM细胞。 TAK-779 不太有效地阻断 CHO/CCR2b 细胞中 [125I]-单核细胞趋化蛋白 1 与 CCR2b 的结合,CCR2b 的 IC50 为 27 nM。 TAK-779 还完全抑制 [125I]-RANTES 与 CHO/CCR5 细胞的结合,IC50 为 1.4 nM。 TAK-779 (20 nM) 选择性抑制 CCR5 介导的 Ca2+ 信号传导。此外,TAK-779 对 X4 HIV-1 毒株没有抑制作用[1]。 TAK-779 是 CXCR3 的拮抗剂,抑制 T 细胞的迁移,但不抑制 T 细胞增殖[2]。
TAK-779 处理并未降低抗 MOG T 细胞对 MOG 35-55 肽刺激的增殖反应。有趣的是,来自 TAK-779 处理小鼠的 T 细胞显示出更强的增殖反应。[3] 当与抗原呈递细胞 (APC) 在 MOG 存在下共培养时,TAK-779 不影响 MOG 特异性 T 细胞产生 IFN-γ。[3] TAK-779 处理不影响来自免疫小鼠的 APC 在与 MOG 特异性 T 细胞共培养时产生 IL-12 的能力。[3] TAK-779 处理对免疫小鼠脾细胞或淋巴结细胞在 MOG 刺激下产生 IL-17 没有显著影响。[3] TAK-779 处理不影响免疫小鼠纯化 T 细胞中 CXCR3 和 CCR5 的 mRNA 表达。[3] |
| 体内研究 (In Vivo) |
TAK-779 (TAK779)(每天 10 mg/kg,皮下注射)可显着延长大鼠肠移植模型的同种异体移植物存活时间。 TAK-779 还可以减少脾脏、血液和受体肠系膜淋巴结 (MLN) 中 CD4+ 和 CD8+ T 细胞的数量[2]。 TAK-779(每只小鼠 150 µg,皮下注射)可抑制髓磷脂少突胶质细胞糖蛋白 (MOG) 免疫的 C57BL/6 小鼠实验性自身免疫性脑脊髓炎 (EAE) 的发展。 TAK-779 减少携带 CXCR3 和 CCR5 的白细胞向脊髓的浸润。 TAK-779 不会改变髓磷脂少突胶质细胞糖蛋白 (MOG) 特异性免疫反应,也不影响 MOG 特异性 T 细胞转移实验性自身免疫性脑脊髓炎 (EAE) 的潜力[3]。
皮下注射 TAK-779(每日每只小鼠 150 μg)能显著降低 C57BL/6 小鼠中 MOG 诱导的实验性自身免疫性脑脊髓炎 (EAE) 的发病率和严重程度。它延迟了疾病发作并降低了最高平均临床评分。[3] TAK-779 处理防止了 EAE 小鼠的体重减轻。[3] TAK-779 处理不影响 MOG 特异性 T 细胞过继转移 EAE 至受体小鼠的能力。无论受体接受来自溶剂对照组还是 TAK-779 处理组供体的 T 细胞,其疾病的发作、严重程度和持续时间均相似。[3] 组织病理学、流式细胞术和实时荧光定量 PCR 分析表明,TAK-779 处理显著抑制了表达 CXCR3/CCR5 的 CD4⁺、CD8⁺ T 细胞和 CD11b⁺ 白细胞向脊髓的迁移。[3] TAK-779 处理显著降低了 EAE 小鼠脊髓中几种趋化因子 (CCL2, CCL3, CCL4, CXCL9, CXCL10) 和细胞因子 (IFN-γ, IL-17) 的 mRNA 表达,但未改变 CCL5 的表达。它还降低了 CCR2 mRNA 的表达。[3] |
| 酶活实验 |
β趋化因子受体CCR5被认为是抑制嗜巨噬细胞(CCR5使用或R5)HIV-1复制的有吸引力的靶点,因为具有非功能受体(CCR5编码区中的纯合32bp缺失)的个体显然是正常的,但对R5 HIV-1的感染有抵抗力。在这项研究中,我们发现TAK-79-一种小分子量的非肽类化合物(Mr531.13)拮抗RANTES(受激活调节,正常T细胞表达和分泌)与表达CCR5的中国仓鼠卵巢细胞的结合,并在纳摩尔浓度下阻断CCR5介导的Ca2+信号传导。TAK--779对β趋化因子受体的抑制似乎对CCR5是特异性的,因为该化合物在较小程度上拮抗CCR2b,但不影响CCR1、CCR3或CCR4。因此,TAK--779显示出对R5 HIV-1复制的高效和选择性抑制,而对宿主细胞没有显示出任何细胞毒性。该化合物以1.6-3.7nM的浓度抑制R5 HIV-1临床分离株以及实验室菌株在外周血单核细胞中的复制,尽管它对使用或X4的嗜T细胞系(CXCR4)HIV-1完全没有活性[1]
Binding分析[1] 在微量滴定盘中培养CHO-K1和表达CCR5的CHO(CHO/CR5)细胞(每100μl 5×104个细胞)。在37°C下孵育24小时后,用结合缓冲液[Ham's F-12培养基含有20mM Hepes和0.5%BSA(pH 7.2)]代替培养基。在[125I]-RANTES(比活性:2000 Ci/mmol;Amersham Pharmacia)和各种浓度的测试化合物存在下,在室温下进行40分钟的结合反应。通过用冷PBS冲洗掉游离配体来终止结合反应,并通过Top计数闪烁计数器计数细胞相关的放射性。以类似的方式进行其他受体CCR1、CCR2b、CCR3、CCR4和CXCR4的结合测定 Ca2+ Mobilization测定。[1] 将CHO/CR5细胞(5×106个细胞/ml)悬浮在测定缓冲液(5mM KCl/147mM NaCl/0.22mM KH2PO4/1.1mM Na2HPO4/5.5mM葡萄糖/0.3mM MgSO4/1mM MgCl2/10mM Hepes,pH 7.4)中。将细胞在37°C下用5μM Fura-PE3AM加载30分钟,用含有1mM CaCl2的测定缓冲液洗涤两次,并以1×107个细胞/ml的速度重悬于同一缓冲液中。在暴露于TAK-79150秒后,加入20nM RANTES,并通过F-2000荧光光谱仪监测细胞质Ca2+水平的相对增加。用50μM离子霉素对总Ca2+释放进行校准,用5mM EGTA对Ca2+螯合进行校准。 To evaluate receptor binding, Chinese hamster ovary (CHO) cells stably expressing human CCR5 (CHO/CCR5) were used. Cells were cultured in microtiter trays. After incubation, the medium was replaced with a binding buffer. Binding reactions were performed at room temperature for 40 minutes in the presence of a radiolabeled chemokine ligand (e.g., [¹²⁵I]-RANTES) and various concentrations of TAK-779. The reaction was terminated by washing with cold PBS, and cell-associated radioactivity was measured using a scintillation counter. Specific binding was calculated by subtracting nonspecific binding (to parental CHO-K1 cells). Inhibition constants (Ki) were calculated using the Cheng-Prusoff derivation from competitive binding experiments.[1] |
| 细胞实验 |
测试化合物(TAK-779等)的抗HIV-1活性基于对MAGI-CCR5细胞中病毒诱导的感染灶形成的抑制以及PBMC中p24抗原产生的减少。简而言之,MAGI-CCR5 细胞(每孔 1 × 104 个细胞)在微量滴定盘中培养。 37℃孵育24小时后,用含有病毒(每孔约300焦点形成单位)和各种浓度的测试化合物(TAK-779等)的新鲜培养基替换培养物上清液。孵育 2 天后,固定细胞并用 5-溴-4-氯-3-吲哚基-β-d-半乳糖苷酶染色。通过显微镜计数受感染(蓝色)细胞的数量。对于 PBMC 测定,植物血凝素刺激的 PBMC(每 500 μl 2.5 × 105 个细胞)在不同浓度的测试化合物(TAK-779 等)存在下感染 HIV-1。用于感染的病毒量取决于每种毒株的可复制性,通常为每 2.5 × 105 细胞 1-10 ng p24。在 37°C 过夜孵育后,对细胞进行彻底清洗,以去除未吸附的病毒颗粒,并用含有与病毒吸附期间所用化合物浓度相同的化合物的培养基进一步孵育。病毒感染后第 6 天,收集培养物上清液并使用夹心 ELISA 试剂盒测定其 p24 抗原水平。化合物的细胞毒性与其抗病毒活性并行评估。它们基于模拟感染细胞的活力和增殖[1]。
淋巴细胞增殖实验: 取免疫小鼠的引流淋巴结细胞(每孔 2 × 10⁵ 个),在 96 孔板中与不同浓度的 MOG 35-55 肽或单纯培养基一起培养。60 小时后,每孔加入 0.5 μCi 的 [³H]-胸腺嘧啶,继续培养 12 小时。将细胞收集到滤膜上,使用液体闪烁计数器测量掺入的放射性。[3] ELISA 检测细胞因子 (IFN-γ, IL-12p70, IL-17): 对于 IFN-γ,将来自免疫小鼠的纯化 T 细胞(每孔 4 × 10⁵ 个)与来自正常小鼠的 APC 富集群(每孔 1 × 10⁵ 个)在有无 MOG (10 μg·mL⁻¹) 的条件下共培养。48 小时后收集上清。对于 IL-12p70,将来自免疫小鼠的 APC 富集群(每孔 1 × 10⁵ 个)与来自免疫小鼠的纯化 T 细胞(每孔 4 × 10⁵ 个)在有无 MOG (10 μg·mL⁻¹) 的条件下共培养。24 小时后收集上清。对于 IL-17,将来自免疫小鼠的脾细胞或淋巴结细胞(每孔 4 × 10⁵ 个)在有无 MOG (10 μg·mL⁻¹) 的条件下培养。72 小时后收集上清。所有上清中的细胞因子水平均使用特异性 ELISA 试剂盒进行测量。[3] RNA 提取与 PCR 分析: 裂解细胞或组织,提取总 RNA。将 RNA 反转录为 cDNA。对于标准 RT-PCR,用特异性引物扩增 cDNA,产物在琼脂糖凝胶上分离并显影。对于定量实时荧光 PCR,使用基于 SYBR Green 的系统进行反应,mRNA 水平均以 β-肌动蛋白为内参进行标准化。使用的特异性引物针对的基因包括 CD4、CD8、CD11b、CCR2、CCR5、CXCR3、CCL2、CCL3、CCL4、CCL5、CXCL9、CXCL10、IFN-γ 和 IL-17 等。[3] CNS 浸润细胞的流式细胞术分析: 通过酶消化和 Percoll 梯度离心从脊髓中分离单核细胞。封闭细胞,用针对表面标记物(如 CD4、CD8、CD11b、CXCR3、CCR5)的荧光标记抗体染色,洗涤后通过流式细胞仪分析。特定白细胞亚群的绝对数量通过其百分比乘以浸润白细胞的总数来计算。[3] |
| 动物实验 |
小鼠:除MOG免疫外,小鼠还接受TAK-779或载体注射。MOG免疫后,小鼠(N = 10)每天皮下注射150 µg TAK-779(溶于5%甘露醇溶液),注射体积为100 µL。从免疫后的第一天开始,每天注射一次TAK-779,持续22天。基于既往研究结果,即每只小鼠需要超过100 µg的剂量才能产生显著的抑制作用,因此选择150 µg的剂量。50 µg/只的剂量无效。除了用于哮喘和同种异体移植排斥模型外,150 µg/只的剂量也已用于其他小鼠实验模型。对照组小鼠(N = 10)每日注射等体积的含5%甘露醇的PBS作为对照[3]。
C57BL/6小鼠的EAE诱导和TAK-779治疗:雌性C57BL/6小鼠(6-8周龄)在三个部位皮下注射含有200 μg MOG 35-55肽和400 μg结核分枝杆菌H37Ra的乳剂,该乳剂溶于弗氏完全佐剂中。此外,每只小鼠在免疫当天和72小时后腹腔注射400 ng百日咳毒素。从免疫后第0天开始,小鼠每天皮下注射150 μg TAK-779(溶于5%甘露醇溶液)或等体积的载体对照(5%甘露醇PBS溶液),持续22天。每日对EAE的临床症状进行评分。[3] 过继转移EAE实验:供体C57BL/6小鼠用MOG 35-55免疫,并用TAK-779或载体进行治疗。10天后,收集引流淋巴结细胞,并将淋巴细胞与MOG 35-55(50 μg·mL⁻¹)和鼠重组IL-12(20 ng·mL⁻¹)共同培养4天。受体C57BL/6小鼠每只静脉注射1 × 10⁷个活化细胞,并在移植后立即和48小时后腹腔注射两次百日咳毒素(每次200 ng)。对受体小鼠进行长达24天的EAE临床症状监测。[3] 组织病理学评估:在疾病高峰期(免疫后第17天),用固定液灌注小鼠。收集脊髓,切片,并用苏木精-伊红(H&E)染色。根据单核细胞浸润情况,在显微镜下对脊髓象限的炎症进行评分。[3] 中枢神经系统浸润细胞的分离分析:用冰冷的PBS灌注小鼠。挤出脊髓,用胶原酶消化,并通过细胞筛过滤。通过 Percoll 梯度离心分离单核细胞,用于后续的流式细胞术或其他分析。[3] |
| 参考文献 |
|
| 其他信息 |
β-趋化因子受体CCR5被认为是抑制巨噬细胞嗜性(CCR5型或R5型)HIV-1复制的理想靶点,因为携带非功能性受体(CCR5编码区32 bp纯合缺失)的个体虽然表型正常,但却对R5型HIV-1感染具有抵抗力。本研究发现,小分子量(Mr 531.13)的非肽类化合物TAK-779能够拮抗RANTES(活化调节,正常T细胞表达和分泌)与表达CCR5的中国仓鼠卵巢细胞的结合,并在纳摩尔浓度下阻断CCR5介导的Ca2+信号传导。TAK-779对β-趋化因子受体的抑制作用似乎具有CCR5特异性,因为该化合物对CCR2b的拮抗作用较弱,但对CCR1、CCR3或CCR4没有影响。因此,TAK-779 对 R5 HIV-1 复制表现出高效且选择性的抑制作用,且对宿主细胞无细胞毒性。该化合物在浓度为 1.6-3.7 nM 时可抑制外周血单核细胞中 R5 HIV-1 临床分离株和实验室毒株的复制,但对 T 细胞嗜性(CXCR4 受体或 X4 受体)HIV-1 完全无效。[1]
本研究采用大鼠肠移植模型,探讨了 CCR5 和 CXCR3 拮抗剂 FK506 和 TAK-779 的作用。将 DA 大鼠的小肠异位移植到 LEW 大鼠体内。受体大鼠分别接受 FK506(1 mg/kg/天,第 0-5 天)和 TAK-779(10 mg/kg/天,第 0-10 天)治疗。通过混合淋巴细胞反应和IFN-γ产生来评估移植存活率和对这些材料的免疫反应。同时检测了淋巴细胞上趋化因子受体的表达。同种异体组、FK506组、TAK-779组和双药联合组的平均存活时间分别为7.0±0.3天、12.0±1.0天、9.8±0.5天和18.0±1.5天。与TAK-779组相比,FK506组的细胞增殖反应和IFN-γ产生均显著受到抑制。此外,双药联合治疗组的抑制作用强于FK506单药治疗组,这与体内实验和组织病理学数据相符。 FACS分析显示,FK506组和TAK-779组受体血液中CD4(+)和CD8(+)细胞数量均显著降低,TAK-779组移植肠系膜淋巴结中CD4(+)和CD8(+)细胞数量也显著降低,而FK506组则未见此现象。此外,移植肠系膜浸润淋巴细胞的双重染色显示,与同种异体组相比,TAK-779组表达CCR5和CXCR3的淋巴细胞数量显著减少,而FK506组则未见此现象。FK506虽然抑制细胞增殖和效应功能,但对淋巴细胞中CCR5和CXCR3的表达影响较小。进一步探索FK506联合TAK-779治疗的效果,有望为肠移植提供一种新的治疗方法。 [2] 背景与目的:CC趋化因子受体CCR5和CXC趋化因子受体CXCR3参与T细胞介导的免疫反应的调节,以及这些细胞的迁移和活化。为了确定阻断这些趋化因子受体是否能调节中枢神经系统(CNS)的炎症反应,我们研究了非肽类趋化因子受体拮抗剂TAK-779对实验性自身免疫性脑脊髓炎(EAE)小鼠的影响。实验方法:通过用髓鞘少突胶质细胞糖蛋白(MOG)35-55免疫C57BL/6小鼠诱导EAE。免疫后,每天皮下注射一次TAK-779。通过组织病理学评估和流式细胞术(FACS)检测浸润脊髓的炎症细胞、聚合酶链式反应(PCR)定量检测mRNA表达、通过[3H]-胸苷掺入法检测T细胞增殖以及通过酶联免疫吸附试验(ELISA)检测细胞因子生成,监测疾病发生率和严重程度(持续3周)。主要结果:TAK-779治疗降低了实验性自身免疫性脑脊髓炎(EAE)的发生率和严重程度。它显著抑制了表达CXCR3/CCR5的CD4+、CD8+和CD11b+白细胞向中枢神经系统(CNS)的迁移。TAK-779不降低抗髓鞘少突胶质细胞糖蛋白(MOG)T细胞的增殖、T细胞产生干扰素-γ(IFN-γ)或T细胞上CXCR3的表达。此外,TAK-779 不影响抗原呈递细胞产生 IL-12、T 细胞上 CCR5 的诱导以及 MOG 特异性 T 细胞转移 EAE 的能力。结论和意义:TAK-779 抑制了 MOG 诱导的 EAE 的发展。这种作用涉及减少炎症细胞向中枢神经系统的迁移,而不影响抗 MOG T 细胞的反应或 MOG 特异性 T 细胞转移 EAE 的能力。[3] TAK-779 是一种合成的非肽类趋化因子受体拮抗剂,最初因其 CCR5 拮抗活性而被开发用于 HIV 治疗。 [3] 在实验性自身免疫性脑脊髓炎 (EAE) 的背景下,TAK-779 通过抑制表达 CXCR3 和/或 CCR5 的炎症细胞(T 细胞和单核细胞/巨噬细胞)向中枢神经系统的迁移来缓解疾病,而不会损害致脑炎性 T 细胞本身的活化或效应功能。[3] 该研究表明,趋化因子受体(例如 CCR5、CXCR3 和 CCR2)在自身免疫性神经炎症期间白细胞向中枢神经系统的迁移中起着关键作用,阻断这些受体代表了一种潜在的治疗策略,可用于治疗多发性硬化症等组织特异性自身免疫性疾病。[3] |
| 分子式 |
C33H39CLN2O2
|
|---|---|
| 分子量 |
531.127968072891
|
| 精确质量 |
530.27
|
| 元素分析 |
C, 74.63; H, 7.40; Cl, 6.67; N, 5.27; O, 6.02
|
| CAS号 |
229005-80-5
|
| 相关CAS号 |
229005-80-5 (Cl); 263765-56-6 (cation)
|
| PubChem CID |
183789
|
| 外观&性状 |
White to beige solid powder
|
| LogP |
8.171
|
| tPSA |
26.3
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
38
|
| 分子复杂度/Complexity |
769
|
| 定义原子立体中心数目 |
0
|
| SMILES |
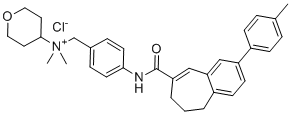
C[N+](C1CCOCC1)(CC1C=CC(NC(=O)C2CCCC3=CC=C(C4C=CC(C)=CC=4)C=C3C=2)=CC=1)C.[Cl-]
|
| InChi Key |
VDALIBWXVQVFGZ-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C33H38N2O2.ClH/c1-24-7-11-27(12-8-24)28-14-13-26-5-4-6-29(22-30(26)21-28)33(36)34-31-15-9-25(10-16-31)23-35(2,3)32-17-19-37-20-18-32;/h7-16,21-22,32H,4-6,17-20,23H2,1-3H3;1H
|
| 化学名 |
dimethyl-[[4-[[3-(4-methylphenyl)-8,9-dihydro-7H-benzo[7]annulene-6-carbonyl]amino]phenyl]methyl]-(oxan-4-yl)azanium;chloride
|
| 别名 |
TAK-779 Chloride; TAK779; TAK 779
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ≥ 25 mg/mL (~47.1 mM)
H2O: ~16.7 mg/mL (~31.4 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.58 mg/mL (4.86 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.58 mg/mL (4.86 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.8mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.58 mg/mL (4.86 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 50 mg/mL (94.14 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8828 mL | 9.4139 mL | 18.8278 mL | |
| 5 mM | 0.3766 mL | 1.8828 mL | 3.7656 mL | |
| 10 mM | 0.1883 mL | 0.9414 mL | 1.8828 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|
|
|
|