| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
Heavy metal chelator
TPEN is a cell-permeable heavy metal chelator that targets divalent heavy metal cations (cadmium, mercury, methylmercury, zinc, copper) [1] TPEN targets intracellular copper to induce ROS-dependent DNA damage in colon cancer cells [2] TPEN chelates intracellular zinc released by thiol oxidation, inhibiting zinc-mediated neuronal apoptosis [3] |
||
|---|---|---|---|
| 体外研究 (In Vitro) |
镉、汞和甲基汞都会引起 fura-2 荧光的改变,这种改变会被重金属螯合剂 TPEN 减弱。 TPEN 是一种细胞渗透性低亲和力的重金属 Ca2+ 阳离子螯合剂。当向细胞中添加10或30μM氯化镉时,升高的fura-2荧光比率在10分钟内显着降低至基础水平(10或30μM氯化镉诱导的ΔRatio降低119.6±2.4%或109±1.5%(F340/F380))分别为 30 μM 氯化镉)。这表明氯化镉引起的fura-2荧光比率的增加依赖于细胞内重金属阳离子而不是细胞内Ca2+[1]。 TPEN 是一种金属螯合剂,利用铜氧化还原循环来靶向结肠癌细胞。 TPEN 降低细胞活力的方式取决于剂量和时间。铜氧化还原循环对于 TPEN 诱导的细胞死亡也是必要的,因为铜螯合剂新铜脯氨酸可防止 DNA 损伤并降低 ATM、γ-H2AX、pChk1 和其他蛋白质的表达。所有三种细胞系均表现出响应低 TPEN 浓度的 ATM/ATR 信号传导;然而,与某些 ATM 和 DNA-PK 抑制剂预孵育可防止细胞中发生 TPEN 诱导的 DNA 损伤 [2]。
TPEN(20 µM)可将人SH-SY5Y神经母细胞瘤细胞中由10或30 µM氯化镉诱导升高的fura-2荧光比率降至基础水平[1] TPEN(20 µM)可显著降低10 µM氯化汞或甲基汞(MeHg)在SH-SY5Y细胞中诱导的fura-2荧光比率,但对30 µM氯化汞或甲基汞诱导的荧光比率无显著影响[1] TPEN以剂量和时间依赖的方式降低人结肠癌细胞系(HCT116、SW480、HT29)的细胞活力;24小时时,随着TPEN浓度升高,细胞毒性显现,5 µM TPEN可显著诱导DNA损伤(通过彗星实验检测)[2] TPEN(5 µM)在HCT116细胞中诱导ROS生成,预先使用抗氧化剂(NAC 5 mM、CAT 500 IU)可逆转TPEN诱导的ROS产生和DNA损伤,并降低γ-H2AX和p-Chk1蛋白的表达[2] 预先使用铜螯合剂新铜试剂(25 µM)可抑制TPEN诱导的DNA损伤,并降低HCT116细胞中pChk1、γ-H2AX和ATM蛋白的表达[2] TPEN可阻断2,2'-二硫二吡啶(DTDP)诱导的培养神经元凋亡,表现为DNA梯状条带和染色质不对称形成的消失;同时可逆转DTDP介导的细胞内游离锌浓度升高(通过Newport Green、fura-2和magfura-2荧光检测)[3] 通过siRNA沉默Chk1、DNA-PK或ATM可消除γ-H2AX的表达,并逆转TPEN在HCT116、SW480和HT29细胞中诱导的细胞死亡[2] |
||
| 细胞实验 |
已知重金属刺激可诱导许多细胞类型中的钙(Ca(2+))动员。负载钙指示剂fura-2的细胞中的重金属对细胞内钙浓度测量的干扰是一个持续存在的问题。在这项研究中,我们使用TPEN(一种特定的细胞渗透性重金属螯合剂)分析了重金属对人SH-SY5Y神经母细胞瘤细胞中fura-2荧光比的影响。氯化锰(30-300µM)不会引起fura-2荧光比的显著变化。高浓度(300µM)的醋酸铅导致fura-2荧光比略有升高。相比之下,氯化镉、氯化汞或甲基汞(3-30µM)的刺激以剂量依赖的方式引起fura-2荧光比的明显升高。在用10或30µM氯化镉刺激的细胞中,添加TPEN会将升高的fura-2荧光比降低到基础水平。在用汞或甲基汞刺激的细胞中,添加TPEN显著降低了较低浓度(10µM)汞或甲基汞诱导的fura-2荧光比的升高,但不降低较高浓度(30µM)诱导的fura-2荧光比的提高。用钙通道阻断剂(如维拉帕米、2-APB或氯化镧)预处理对fura-2荧光比有不同的影响。我们的研究描述了几种重金属对二价阳离子动员的影响以及重金属对神经元细胞的毒性。[1]
最近,我们发现金属螯合剂TPEN通过铜的氧化还原循环靶向癌症结肠癌细胞。在此,我们研究了TPEN的DNA损伤潜力,并阐明了Chk1、ATM和DNA-PK在3种人结肠癌癌症细胞系HCT116、SW480和HT29中TPEN诱导的毒性中的作用。我们还研究了活性氧(ROS)在TPEN诱导的DNA损伤中的作用。TPEN以剂量和时间依赖的方式降低细胞存活率。细胞毒性与显著的DNA损伤、γ-H2AX蛋白的高表达和ATM/ATR信号通路的激活有关。TPEN导致的细胞死亡取决于ROS的产生,这可以从细胞存活率的逆转、DNA损伤和抗氧化剂存在下γ-H2AX水平的消除中得到证明。然而,在高TPEN浓度(10µM)下,抗氧化剂治疗未能逆转细胞毒性。TPEN诱导的细胞死亡也依赖于铜的氧化还原循环,因为铜螯合剂新亚铜灵抑制了DNA损伤,降低了pChk1、γ-H2AX和ATM蛋白的表达。低TPEN浓度导致的细胞死亡涉及所有3种细胞系中的ATM/ATR信号传导,因为与ATM和DNA-PK的特异性抑制剂预孵育导致细胞从TPEN诱导的DNA损伤中恢复。此外,Chk1、DNA-PK和ATM的siRNA沉默消除了γ-H2AX的表达并逆转了细胞死亡,表明Chk1和DNA-PK介导了TPEN-诱导的结肠癌癌症细胞的细胞毒性。本研究首次表明Chk1、DNA-PK和ATM参与了TPEN诱导的DNA损伤,并证实了我们之前的发现,即ROS的产生和铜对TPEN的氧化还原循环是该化合物诱导人类结肠癌癌症细胞死亡的主要机制。抑制ATM或DNA-PK并不能逆转高TPEN浓度下的细胞毒性,TPEN浓度会导致ROS水平过高和不可逆的细胞损伤[2]。 将人SH-SY5Y神经母细胞瘤细胞负载fura-2后,用氯化镉(3–30 µM)、氯化汞(3–30 µM)或甲基汞(3–30 µM)刺激;刺激3小时后加入TPEN(20 µM),检测加入TPEN前后的fura-2荧光比率(F340/F380),评估重金属诱导的荧光变化[1] SH-SY5Y细胞预先用钙通道阻滞剂(维拉帕米10 µM、2-APB 10 µM、氯化镧100 µM)处理30分钟,再用30 µM氯化镉、氯化汞或甲基汞刺激;检测fura-2荧光比率,评估阻滞剂对重金属诱导荧光的影响[1] 将人结肠癌细胞系(HCT116、SW480、HT29)用不同浓度的TPEN处理24或48小时,通过MTT实验检测细胞活力,并用彗星实验(40倍荧光显微镜观察)检测DNA损伤[2] HCT116细胞预先用抗氧化剂(NAC 5 mM、CAT 500 IU)或铜螯合剂新铜试剂(25 µM)处理2小时,再用TPEN(5 µM)处理;通过DCFDH实验检测ROS生成,并用蛋白质印迹和流式细胞术分析γ-H2AX、p-Chk1、ATM等蛋白的表达[2] 用脂质体将Chk1、DNA-PK或ATM的siRNA转染结肠癌细胞;转染24小时后,用3 µM TPEN处理细胞72小时,通过MTT实验和膜联蛋白染色检测细胞死亡情况[2] 将培养的神经元暴露于2,2'-二硫二吡啶(DTDP)以诱导硫醇氧化和锌释放,加入TPEN螯合细胞内锌离子;通过DNA梯状条带和染色质染色检测神经元凋亡,同时通过Newport Green、fura-2和magfura-2荧光检测锌离子水平[3] |
||
| 动物实验 |
|
||
| 参考文献 |
|
||
| 其他信息 |
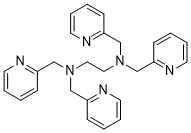
N,N,N',N'-四(2-吡啶甲基)乙二胺是一种N-取代的二胺,其结构为乙二胺,其中四个氨基氢被2-吡啶甲基取代。它具有螯合剂、细胞凋亡诱导剂和铜螯合剂的作用。它属于吡啶类化合物,是一种叔胺化合物,也是一种N-取代的二胺。它在功能上与乙二胺相关。
TPEN(N,N,N',N'-四(2-吡啶甲基)乙二胺)是一种高选择性、细胞渗透性二价重金属阳离子螯合剂,广泛用于研究重金属毒性和细胞内金属稳态[1] TPEN通过ROS生成和铜氧化还原循环诱导结肠癌细胞DNA损伤,Chk1和DNA-PK介导其细胞毒性作用;高浓度TPEN(10 µM)会导致不可逆的细胞损伤,这种损伤无法被抗氧化剂逆转[2] TPEN通过螯合硫醇氧化过程中释放的细胞内锌来抑制DTDP诱导的神经元凋亡,这表明锌在氧化应激介导的神经元死亡中发挥作用[3] |
| 分子式 |
C26H28N6
|
|
|---|---|---|
| 分子量 |
424.55
|
|
| 精确质量 |
424.237
|
|
| 元素分析 |
C, 73.56; H, 6.65; N, 19.80
|
|
| CAS号 |
16858-02-9
|
|
| 相关CAS号 |
|
|
| PubChem CID |
5519
|
|
| 外观&性状 |
Typically exists as Light yellow to brown solids at room temperature
|
|
| 密度 |
1.2±0.1 g/cm3
|
|
| 沸点 |
542.1±45.0 °C at 760 mmHg
|
|
| 熔点 |
110-112 °C
|
|
| 闪点 |
281.7±28.7 °C
|
|
| 蒸汽压 |
0.0±1.4 mmHg at 25°C
|
|
| 折射率 |
1.632
|
|
| LogP |
2.68
|
|
| tPSA |
58.04
|
|
| 氢键供体(HBD)数目 |
0
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
11
|
|
| 重原子数目 |
32
|
|
| 分子复杂度/Complexity |
419
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
N(C([H])([H])C1=C([H])C([H])=C([H])C([H])=N1)(C([H])([H])C1=C([H])C([H])=C([H])C([H])=N1)C([H])([H])C([H])([H])N(C([H])([H])C1=C([H])C([H])=C([H])C([H])=N1)C([H])([H])C1=C([H])C([H])=C([H])C([H])=N1
|
|
| InChi Key |
CVRXLMUYFMERMJ-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C26H28N6/c1-5-13-27-23(9-1)19-31(20-24-10-2-6-14-28-24)17-18-32(21-25-11-3-7-15-29-25)22-26-12-4-8-16-30-26/h1-16H,17-22H2
|
|
| 化学名 |
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2 mg/mL (4.71 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2 mg/mL (4.71 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.0mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2 mg/mL (4.71 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.3554 mL | 11.7772 mL | 23.5544 mL | |
| 5 mM | 0.4711 mL | 2.3554 mL | 4.7109 mL | |
| 10 mM | 0.2355 mL | 1.1777 mL | 2.3554 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
TPEN decreases the viability and induces DNA damage in human colon cancer cell lines.Cancer Biol Ther.2016 Nov;17(11):1139-1148. |
|---|
 DNA damage by TPEN is dependent on ROS.Cancer Biol Ther.2016 Nov;17(11):1139-1148. |
 DNA damage by TPEN is dependent on redox cycling of copper.Cancer Biol Ther.2016 Nov;17(11):1139-1148. |
 TPEN-induced cell death involves Chk1, DNA-PK and ATM.Cancer Biol Ther.2016 Nov;17(11):1139-1148. |
|---|
Silencing Chk1 and DNA-PK inhibits TPEN-induced apoptosis.Cancer Biol Ther.2016 Nov;17(11):1139-1148. |
 Effect of TPEN on fura-2 fluorescence changes induced by stimulation with cadmium chloride, mercury chloride or MeHg.J Vet Med Sci.2016 Jun 1;78(5):761-7. |