| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Dipeptidyl peptidase II (DPPII) inhibitor (IC50 = 0.48 ± 0.04 nM).
The compound shows high selectivity for DPPII over DPPIV (IC50 = 165 ± 9 µM) and over DPP activity not caused by DPPII or DPPIV (DPP activity in cell homogenates after removal of DPPII and DPPIV by affinity chromatography).[1] |
|---|---|
| 体外研究 (In Vitro) |
DPP 活性不是由 DPPIV 或 DPPII 产生的,因为与 DPPIV (IC50=165±9 µM) 相比,UAMC00039 对 DPPII (IC50=0.48±0.04 nM) 具有极高的选择性。为了阐明 DPPII 的作用并确认其作为治疗靶点的潜力,UAMC00039 似乎是一种有前途的工具 [1]。 DPPII 抑制剂对抗酶的强度,以及它们穿透细胞并在培养基中保持稳定的能力,决定了它们在细胞培养中的有效性。在 37°C 下至少 48 小时,UAMC00039 在培养基和 DPPII 测试缓冲液中保持稳定。一分钟内,该化学物质可以渗透 PBMC 并以浓度依赖性方式阻断细胞内 DPPII 活性,同时使“非 DPPII”DPP 活性不受影响。 PBMC 和 U937 细胞中超过 90% 的 DPPII 活性被 1 和 100 μM UAMC00039 抑制[2]。
|
| 体内研究 (In Vivo) |
在大鼠、小鼠和兔子的外周器官中,口服给药后(静脉注射后)观察到 DPPII 的剂量依赖性抑制,但 DPPIV 未见。 UAMC00039 当以2 mg/kg的剂量口服时,评估以下参数:一般行为、体温、呼吸、出血时间、血压、尿量、肝功能、空腹血糖和胃功能。此外,任何肠道参数都没有显着变化,例如酸度、蠕动和刺激性[1]。
给家兔单次静脉推注UAMC-00039 dihydrochloride(1 µmol/kg)后,血清DPPII活性在15分钟内降至初始值的5%以下,并在2天后恢复正常。较低剂量(0.2 µmol/kg)的抑制效果略弱,表明存在剂量依赖性。在第5天和第40天重复注射后,观察到同样显著的抑制作用和类似的恢复动力学。血清DPPIV活性未受抑制。[1] 给大鼠口服(1 µmol/kg)后,血清DPPII活性在1小时内降至初始值的30%以下。[1] 给小鼠和大鼠口服(最高分别达5 µmol/kg和1 µmol/kg)或给家兔静脉注射(1 µmol/kg)后,在外周器官(肾脏、肝脏、脾脏、肺、心脏、大脑)中观察到DPPII活性的剂量依赖性抑制,但DPPIV活性不受影响。[1] |
| 酶活实验 |
DPPII酶活性通过动力学方法测定,在37°C下监测405 nm处对硝基苯胺释放的初始速度,持续10分钟。测定使用Lys-Ala-对硝基苯胺(1 mM)作为底物,反应体系为0.1 M二甲胂酸-NaOH缓冲液(pH 5.5),含有10 mM EDTA和抑肽酶(14 µg/mL)。[1]
DPPIV酶活性使用类似方法测定,底物为Gly-Pro-对硝基苯胺(0.5 mM),反应体系为0.05 M Tris缓冲液(pH 8.3)。[1] 一个酶活力单位定义为在测定条件下,每分钟催化释放1 µmol对硝基苯胺的酶量。[1] |
| 动物实验 |
功效和口服生物利用度试验:
本研究使用了雄性瑞士小鼠(~0.023 kg)、雄性Wistar大鼠(~0.46 kg)和雄性新西兰白兔(~4.00 kg)。[1] 对于兔子的静脉注射(IV)给药,抑制剂以2 mM的浓度溶于50 mM磷酸钠缓冲液(pH 7.4)中,给药剂量为0.5 mL/kg。[1] 对于大鼠的口服给药,采用灌胃法给予相同的2 mM磷酸钠缓冲液溶液,剂量为0.5 mL/kg。[1] 对于小鼠的口服给药,化合物以2% Tween 80混悬液的形式灌胃给药,剂量为10 mL/kg。小鼠在给药前禁食 24 小时。[1] 在给药后不同时间点,从耳动脉(兔子)、尾静脉(大鼠)或腹腔静脉(小鼠,麻醉后)采集血样。[1] 在最后一次给药后 3-5 小时(兔子、大鼠)或 2 小时(小鼠)处死动物,以采集组织(肾脏、肝脏、脾脏、肺、心脏、脑)。将组织在含有抑蛋白酶 (1%) 和辛基葡糖苷 (1%) 的 PBS 缓冲液中匀浆,取上清液进行酶活性测定。[1] 药理学和毒理学分析: 本研究使用了雄性或雌性 ICR 小鼠、Wistar 和 Long Evans 大鼠以及 Duncan Hartley 豚鼠。[1] 在所有体内试验中,均采用盲法,以 2 mg/kg(约 5 µmol/kg)的剂量,用 2% Tween 80 (10 mL/kg) 的溶剂进行口服给药。[1] 对于体外组织试验(例如,心肌、平滑肌),将抑制剂溶解于 DMSO 中,并在浴槽中稀释至最终浓度为 30 µM(0.1% DMSO)。[1] |
| 药代性质 (ADME/PK) |
该研究证实了UAMC-00039二盐酸盐的体内疗效和口服生物利用度。[1]
对兔进行静脉注射(1 µmol/kg)后,血清DPPII活性迅速下降(15分钟内降至初始值的5%以下)。[1] 对大鼠进行口服(1 µmol/kg)后,血清DPPII活性下降(1小时内降至初始值的30%以下)。[1] 静脉注射(兔)和口服(小鼠、大鼠)后,该化合物均表现出对血清和外周器官中DPPII的剂量依赖性抑制作用。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
在功效和口服生物利用度试验中,对兔进行静脉注射以及对小鼠和大鼠进行口服给药,剂量高达 5 µmol/kg,均未观察到任何急性毒性。[1]
在一项广泛的药理学和毒理学筛选中,口服 2 mg/kg 的 UAMC-00039 二盐酸盐未引起急性毒性迹象或多种评估功能的显著变化。这些功能包括一般行为、体温、呼吸、出血时间、血压、尿量、肝功能、空腹血糖、胃肠道参数、镇痛作用、胆碱能、多巴胺能、血清素能、肾上腺素能和其他神经递质系统功能,以及在 30 µM 浓度下体外对心脏、平滑肌和其他各种组织的影响。[1] |
| 参考文献 | |
| 其他信息 |
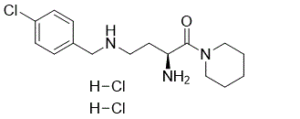
UAMC-00039 二盐酸盐(N-(4-氯苄基)-4-氧代-4-(1-哌啶基)-1,3-(S)-丁二胺二盐酸盐)是一种强效且高选择性的 DPPII 抑制剂,被开发为一种工具化合物,用于阐明 DPPII 的生理功能并验证其作为治疗靶点的潜力。[1]
该化合物是 1-[(S)-2,4-二氨基丁酰基]哌啶的 γ-氨基取代类似物。[1] 其对 DPPII 相对于相关酶(如 DPPIV 和 DPP8/9)的高选择性,对于预测其良好的副作用特征具有潜在重要意义,因为其他研究表明抑制 DPP8/9 与毒性相关。[1] 在广泛的筛选实验中未观察到显著的药理作用,表明预计不会出现严重的副作用(例如心血管副作用),这支持了其作为工具化合物的用途。用于进一步的体内研究。[1] |
| 分子式 |
C16H26CL3N3O
|
|---|---|
| 分子量 |
382.7561
|
| 精确质量 |
381.114
|
| CAS号 |
697797-51-6
|
| PubChem CID |
24757888
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
58.4
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
23
|
| 分子复杂度/Complexity |
313
|
| 定义原子立体中心数目 |
1
|
| SMILES |
C1CCN(CC1)C(=O)[C@H](CCNCC2=CC=C(C=C2)Cl)N.Cl.Cl
|
| InChi Key |
IWXMOQGMIWZNPR-CKUXDGONSA-N
|
| InChi Code |
InChI=1S/C16H24ClN3O.2ClH/c17-14-6-4-13(5-7-14)12-19-9-8-15(18)16(21)20-10-2-1-3-11-20;;/h4-7,15,19H,1-3,8-12,18H2;2*1H/t15-;;/m0../s1
|
| 化学名 |
(2S)-2-Amino-4-[[(4-chlorophenyl)methyl]amino]-1-(1-piperidinyl)-1-butanone dihydrochloride
|
| 别名 |
UAMC00039 2HCl, UAMC 00039, UAMC-00039, UAMC 00039 dihydrochloride, UAMC 00039 2HCl
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ≥ 150 mg/mL (~391.89 mM)
H2O : ~100 mg/mL (~261.26 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (261.26 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6126 mL | 13.0630 mL | 26.1260 mL | |
| 5 mM | 0.5225 mL | 2.6126 mL | 5.2252 mL | |
| 10 mM | 0.2613 mL | 1.3063 mL | 2.6126 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。