| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| Other Sizes |
|
| 靶点 |
Hepatitis C virus (HCV) nonstructural protein (NS) 3/4A protease
|
|---|---|
| 体外研究 (In Vitro) |
为了使 HCV 编码的多蛋白(NS3、NS4A、NS4B、NS5A 和 NS5B 蛋白的未成熟形式)被蛋白酶切割并随后进行病毒复制,需要 NS3/4A 蛋白酶[1]。在酶测定中利用反式和重组 NS3 蛋白酶结构域中提供的同基因 NS4A 肽辅因子。在表达编码海肾荧光素酶的 HCV 复制子的稳定细胞系(Huh-7-Lunet 或 Huh7-1C 细胞)中,Voxilaprevir 对 HCV 基因型 1b 和 3a[1] 的 NS3 蛋白酶的 Ki 值分别为 0.038 nM 和 0.066 nM )。在基因型 1 至 6 中,vitilaprevir 表现出强大的全基因型抗病毒活性,EC50 范围为 0.33 至 6.6 nM。 Voxilaprevir 对 HCV 复制子株 DQ314805、H77、Con1、JFH-1、J6、J8(全长)的 IC50 值分别为 0.33 nM、3.9 nM、3.3 nM、3.7 nM、4.5 nM、1.8 nM 和 6.6 nM、1.9 nM 、HM568433、SA13(NS3嵌合体)[1]。
|
| 体内研究 (In Vivo) |
在这项研究中,对慢性HCV基因型1-4感染患者进行了Voxilaprevir/GS-9857的安全性、耐受性、抗病毒活性和药代动力学(PK)评估。基因型1-4感染的患者在禁食条件下接受安慰剂或每日一次GS-9857,剂量范围为50至300mg,持续3天。GS-9857耐受良好;所有报告的不良事件(AE)严重程度均为轻度或中度。腹泻和头痛是最常见的不良事件。17%接受GS-9857治疗的患者观察到3级或4级实验室异常;丙氨酸氨基转移酶、天冬氨酸氨基转移酶或碱性磷酸酶水平没有3级或4级异常。GS-9857在慢性HCV感染患者中显示出强大的抗病毒活性,在HCV基因型1a、1b、2、3或4感染患者服用100mg剂量后,HCV RNA的平均和中位最大减少量≥3 log10IU/mL。GS-9857的抗病毒活性不受预处理NS3 RAV存在的影响。在基因型1-4感染的患者中,GS-9857表现出线性PK,中位半衰期为29-42小时,支持每日一次给药。因此,GS-9857的耐受性、疗效和药代动力学特征支持其对慢性HCV感染患者治疗的进一步评估。[2]
在没有肝硬化的初次治疗患者中,接受6周治疗的患者SVR12的发生率为71%(24/34;95%CI,53-85),接受8周治疗的病人为100%(36/36;95%CI90-100)(表2)。在初次接受治疗的肝硬化患者中,接受8周sofosbuvir-velatasvir联合Voxilaprevir/GS-9857治疗的患者SVR12的发生率为94%(31/33;95%CI,80-99),接受8周sofosbuvi-velatasVir联合GS-9857加利巴韦林治疗的患者为81%(25/31;95%CI63-93)(表2)。在之前接受过含DAA方案治疗的患者中,接受12周治疗的非肝硬化患者SVR12的发生率为100%(31/31;95%CI,89-100),接受12周治疗的肝硬化患者为100%(32/32;95%CI,89-100%)。根据基线差异,各组的SVR12率没有显著差异(附录)。18名病毒学失败的患者在治疗结束后复发;在治疗过程中,没有患者出现病毒学突破(附录)。 表3显示了无RAS和具有1%测序截止水平的单类和多类NS3、NS5A和NS5B RAS的患者的SVR率。在未接受治疗的患者中,使用索非布韦-维帕他韦加<强>伏西拉匹韦/GS-9857治疗8周,不使用利巴韦林,分别导致96%(24人中的23人)和98%(45人中的44人)的无基线RAS患者和有基线RAS的患者出现SVR12。使用15%的测序截止水平也得到了类似的结果(补充材料)。所有有DAA经验的患者,无论是否存在单类或多类RAS,在接受索非布韦-维帕他韦联合GS-9857治疗12周后均达到SVR12。有12名DAA患者在基线时患有NS5A RAS Y93H/N,所有患者均达到SVR12。 在一项2期开放标签试验中,我们发现索非布韦-维拉帕斯韦联合伏西拉匹韦/GS-9857治疗8周对未接受治疗的患者是安全有效的;对于之前接受DAAs治疗的患者,12周是安全有效的。该组合对有或没有代偿性肝硬化的患者都是安全有效的。Clinicaltrials.gov编号:NCT02378935[3]。 |
| 动物实验 |
这是一项双盲、多中心、随机、安慰剂对照研究,旨在评估Voxilaprevir/GS-9857在慢性丙型肝炎病毒(HCV)感染患者中的安全性、耐受性、抗病毒活性和药代动力学(NCT02185794)(图1)。获批的研究方案允许最多设置10个不同的给药组,其中前三个组为安慰剂对照组,并在空腹状态下给药;其余适应性组不设安慰剂对照,可在空腹或餐后状态下给药。最终纳入7个组;本文报告了空腹状态下接受GS-9857治疗的5个组的结果,而餐后状态下接受GS-9857治疗的2个组的结果将另行报告。 [2]
\n\n患者在首次服用研究药物前 30 天内接受筛查。符合研究标准的患者被随机分组,并于第-1天入院,开始在基线/第1天接受给药。患者每日一次接受研究药物治疗3天(第1、2和3天)后,于第4天出院。短期随访在第5、6、7、8和10天进行,长期随访安排在第12、24和48周进行。[2] \n\nHCV基因1a型、HCV基因2型和HCV基因3型患者在空腹状态下每日一次接受双盲Voxilaprevir/GS-9857(HCV基因1a型和3型患者剂量为50、100或300 mg,HCV基因2型患者剂量为100 mg)或安慰剂治疗,持续3天。 (图 1)。在空腹条件下,对 HCV 基因 1b 型和 HCV 基因 4 型患者每日一次给予 100 mg GS-9857,连续 3 天。[2] \n\n为了评估 Voxilaprevir/GS-9857 对 HCV 基因 1-4 型感染患者的抗病毒活性,确定了主要疗效终点,即 HCV RNA 从基线到每次给药后评估的变化。在筛选时;第 1 天给药前;以及首次给药后 2、4、6、8、12、16、24(第 2 天给药前)、36、48(第 3 天给药前)、54、60、72 和 96 小时采集血浆样本;在随访期的第6、7、8和10天早晨,以及第12、24和48周,分别进行检测。采用COBAS TaqMan HCV Test v2.0(Roche Molecular Diagnostics,美国加利福尼亚州普莱森顿)检测HCV RNA病毒载量,该试剂盒与High Pure系统配合使用。该检测的定量下限(LLOQ)为15 IU/mL。采用VERSANT HCV Genotype INNO-line probe assay (LiPA) 2.0(Siemens Medical Solutions USA, Inc.,美国宾夕法尼亚州马尔文)确定筛选时的病毒基因型和亚型。次要疗效终点包括每次评估时HCV RNA水平的绝对值;根据治疗方案和队列,对HCV RNA从基线到每次给药后评估(直至第10天)期间下降<1、≥1且<2、≥2且<3或≥3 log10 IU/mL的患者进行分类下降;并汇总每次给药后评估时HCV RNA \n\n计算的药代动力学参数包括:血浆浓度-时间曲线下面积(AUClast,从零到最后一次可定量浓度)、血浆浓度-时间曲线下面积(外推至无穷大)(AUCinf)、血浆浓度-时间曲线下面积(至24小时)(AUC0–24)、最大血浆浓度(Cmax)、给药后24小时的血浆浓度(C24)、最后一次可定量血浆药物浓度(Clast)、达到最大血浆浓度的时间(Tmax)、最后一次可定量血浆药物浓度的时间(Tlast)、消除半衰期(t1/2)、末端消除速率常数(λz)以及给药后表观口服清除率(CL/F)。采用幂函数模型和方差分析法,基于第1天和第3天的AUC0–24、C24和Cmax评估剂量比例性。通过比较第 3 天和第 1 天的 AUC0–24、C24 和 Cmax 值,总结了 Voxilaprevir/GS-9857 的累积指数。[2] \n\n \n\n队列 1 [3] \n研究开始时,队列 1 纳入了两组初治患者:一组为无肝硬化患者,接受索非布韦-维帕他韦联合 Voxilaprevir/GS-9857 治疗 6 周;另一组为肝硬化患者,接受索非布韦-维帕他韦联合 GS-9857 治疗 8 周。方案规定,如果接受 8 周治疗的肝硬化患者的复发率低于 10%,则可以考虑再纳入一组患者接受 6 周的治疗。我们没有采用这个方案。相反,前两组的初步结果促使我们修改方案,在该队列中增加两组患者:一组是无肝硬化患者,接受为期 8 周的索非布韦-维帕他韦联合 GS-9857 治疗;另一组是肝硬化患者,接受为期 8 周的索非布韦-维帕他韦联合 GS-9857 和利巴韦林治疗。 \n队列 2 [3] \n队列 2 纳入了两组既往接受过 DAA 治疗的患者——一组有肝硬化,另一组无肝硬化。两组患者均接受了为期 12 周的索非布韦-维帕他韦联合 Voxilaprevir/GS-9857 治疗。方案规定,如果其中任何一组的复发率低于 10%,则可以选择再招募一组患者接受为期 8 周的治疗。未采用此选项。\n \n所有患者均每日一次服用索非布韦400 mg和维帕他韦100 mg的固定剂量复方片剂,以及每日一次服用100 mg的伏西瑞韦/GS-9857片剂,均需与食物同服。利巴韦林每日分次服用,剂量为1000-1200 mg(体重<75 kg的患者每日1000 mg,体重≥75 kg的患者每日1200 mg)。这是一项开放标签研究,患者由研究中心的研究人员招募。研究期间,所有参与者和研究人员均未对治疗分配情况进行盲法处理。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
当以固定剂量复方制剂 Vosevi 与 [DB08934] 和 [DB11613] 联合使用时,伏西瑞韦在给药后 4 小时达到最大血药浓度 (Cmax) 为 192 ng/mL。 伏西瑞韦主要通过胆汁排泄。 代谢/代谢物 伏西瑞韦主要由细胞色素 P450 3A4 (CYP3A4) 代谢,少量由 CYP2C8 和 CYP1A2 代谢。 生物半衰期 33 小时 伏西瑞韦[1] 伏西瑞韦(VOX) 迅速被吸收进入体循环,并在给药后 4 小时达到最大血药浓度。给药后 2-5 小时。在测试的多个剂量中,VOX 的中位稳态半衰期为 28-41 小时。该药物的血浆蛋白结合率 >99%,并由 CYP3A4 代谢。因此,与 CYP3A4 抑制剂/诱导剂合用时,药物浓度可能会发生变化。该药物经胆汁途径消除,末端消除半衰期为 33 小时。约 95% 的药物(其中 40% 为原药)经粪便排出 [1]。 索非布韦/维帕他韦/伏西瑞韦 [1] 健康成人和活动性 HCV 患者的 SOF 的 AUC0-24 和 Cmax 相似。与健康受试者 (N = 137) 相比,HCV 感染者的 VEL 的 AUC0-24 和 Cmax 分别降低了 41% 和 39%。在丙型肝炎病毒感染患者中,VOX 的 AUC0–24 和 Cmax 均比健康受试者(N = 63)高 260% 安全性 [1] 在 POLARIS-2 和 POLARIS-3 研究中,SOF/VOX/VEL 组均无患者因严重不良事件而停止治疗。在 POLARIS-2 研究中,SOF/VOX/VEL 组 72% 的患者出现不良事件,3% 的患者出现严重不良事件。仅有一例患者出现过一次严重不良事件。在 POLARIS-2 研究中,肾盂肾炎是两个治疗组中观察到的唯一严重不良事件。 SOF/VOX/VEL治疗组观察到的其他不良事件包括头痛(27%)、疲乏(20%)、腹泻(18%)和恶心(16%),而SOF/VEL治疗组的相应不良事件发生率分别为头痛(23%)、疲乏(21%)、腹泻(7%)和恶心(9%)。在POLARIS-3研究中,75%的SOF/VOX/VEL治疗患者出现不良事件。在110例患者中,有2例患者发生了4例严重不良事件。SOF/VOX/VEL治疗组的不良事件发生率与SOF/VEL 12周治疗组相当,但SOF/VOX/VEL治疗组出现轻度恶心和腹泻的情况与既往NS3/4A蛋白酶抑制剂的不良事件发生率相似。 据报道,在接受或已完成丙型肝炎病毒(HCV)直接抗病毒药物(DAA)治疗的HCV和乙型肝炎病毒(HBV)合并感染患者中,HBV可能发生再激活。已有暴发性肝炎、肝功能衰竭和死亡等病例报告。接受HCV直接抗病毒药物(DAA)治疗的患者,若同时服用某些免疫抑制剂或化疗药物,或乙肝表面抗原(HBsAg)阳性,或血清学证据表明乙肝病毒(HBV)已清除,则HCV再激活的风险可能增加。 药代动力学结果[2] 除一名接受100 mg伏西瑞韦/GS-9857治疗的患者外,所有患者在单次或多次给药后,均可在给药后24小时内检测到血浆药物浓度。无论HCV基因型如何,给药1天或3天后,GS-9857的血浆浓度-时间曲线相似。给予50-300 mg GS-9857可使Cmax和AUC0-24呈剂量比例增加。首次给药后,中位Tmax范围为1.3至4.0小时;三次给药后为1.8至5.0小时(表S2)。第3天的中位t1/2在各队列中约为29至42小时。与GS-9857的半衰期一致,在所评估的剂量水平下均观察到显著的药物蓄积。 暴露-反应关系[2] 在基因型1a、1b、2或4感染的患者中,抗HCV活性与50、100或300 mg的Voxilaprevir/GS-9857剂量无关;而在基因型3感染的患者中,中位抗病毒反应与GS-9857剂量相关。使用治疗第3天的AUC0-24,可以采用简单的最大抗HCV活性(Emax)模型充分描述这种暴露-反应关系。使用GS-9857 Cmax或C24的类似模型也提供了类似的暴露-反应关系。 |
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期影响
◉ 哺乳期用药概述 尚未对正在接受丙型肝炎治疗的哺乳期妇女进行伏西瑞韦的研究。由于其与母体血浆蛋白的结合率超过99%,因此母乳中的含量可能非常低。一些资料建议,当伏西瑞韦与利巴韦林联合使用时,应避免母乳喂养。 丙型肝炎不会通过母乳传播,并且母乳已被证明可以灭活丙型肝炎病毒(HCV)。然而,美国疾病控制与预防中心建议,如果HCV感染的母亲乳头皲裂或出血,则应考虑停止母乳喂养。目前尚不清楚此警告是否适用于正在接受丙型肝炎治疗的母亲。 HCV感染母亲所生的婴儿应接受HCV感染检测;由于母体抗体在婴儿出生后的前18个月以及婴儿产生免疫反应之前一直存在,因此建议进行核酸检测。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 伏西瑞韦与人血浆蛋白的结合率超过99%。 耐受性[1] 在POLARIS-2和POLARIS-3研究中,接受SOF/VOX/VEL治疗8周的患者中,无一例因严重不良事件而停止治疗;相比之下,POLARIS-2研究中接受SOF/VEL治疗12周的患者中,有0.5%的患者因严重不良事件而停止治疗。在POLARIS-4研究中,SOF/VOX/VEL治疗组12周内无患者因治疗中断而停止治疗,而SOF/VEL治疗组12周内有1例患者因治疗中断而停止治疗。对于轻度或中度肾功能不全患者,SOF/VOX/VEL无需调整剂量。因此,该疗法在患者中耐受性良好。 安全性[2] 表2列出了各治疗组患者在治疗期间出现的不良事件。总体而言,11例患者(16.4%)出现不良事件,其中9例接受了Voxilaprevir/GS-9857治疗(9/59;15.3%),2例接受了安慰剂治疗(2/8;25.0%)。接受GS-9857治疗的患者中,治疗相关不良事件的发生率为6.8%(4/59),接受安慰剂治疗的患者中,治疗相关不良事件的发生率为12.5%(1/8)。研究期间未发生严重不良事件、导致研究药物停用的不良事件或死亡。所有不良事件均为轻度或中度。最常见的不良事件是腹泻,GS-9857 组发生率为 5.1% (3/59),安慰剂组为 12.5% (1/8);最常见的不良事件是头痛,GS-9857 组发生率为 1.7% (1/59),安慰剂组为 25.0% (2/8)。不良事件的发生率与研究药物剂量无关。接受 Voxilaprevir/GS-9857 治疗的患者中,15.3% (9/59) 出现 3 级实验室异常,1.7% (1/59) 出现 4 级实验室异常(表 S1)。安慰剂组患者在实验室检查中均未出现3级或4级异常。3级和4级实验室异常的发生率与GS-9857剂量无关,剂量与不良事件也无关。按治疗组分析生命体征测量值和体格检查结果,或按个体患者分析心电图测量值,均未发现研究期间相对于基线有临床意义的改变。 |
| 参考文献 | |
| 其他信息 |
药效学
Voxilaprevir 是一种直接抗病毒药物,靶向病毒 NS3/4A 蛋白,可降低血清 HCV RNA 水平。它通过特异性抑制 NS3/4A 蛋白在复制复合物中的关键功能来阻断 HCV 复制。即使剂量达到最大推荐剂量的 9 倍,它似乎也不会延长 QT 间期。 Voxilaprevir 是一种直接抗病毒药物 (DAA),用于联合治疗慢性丙型肝炎。慢性丙型肝炎是由丙型肝炎病毒 (HCV) 感染引起的传染性肝病。HCV 是一种单链 RNA 病毒,分为九种不同的基因型,其中 1 型基因型在美国最为常见,影响 72% 的慢性 HCV 患者。伏西瑞韦通过可逆性结合并抑制丙型肝炎病毒 (HCV) 的 NS3/4A 丝氨酸蛋白酶发挥抗病毒作用。HCV 病毒复制遗传物质并翻译成单条多肽链后,非结构蛋白 3 (NS3) 及其激活辅助因子非结构蛋白 4A (NS4A) 负责将遗传物质切割成以下结构蛋白和非结构蛋白,这些蛋白是成熟病毒组装所必需的:NS3、NS4A、NS4B、NS5A 和 NS5B。伏西瑞韦通过抑制病毒蛋白酶 NS3/4A,从而阻止病毒复制和功能。自 2011 年以来,随着伏西瑞韦等直接抗病毒药物 (DAA) 的研发,慢性丙型肝炎的治疗选择取得了显著进展。自 2017 年 7 月起,伏西瑞韦 (Voxilaprevir) 与索非布韦 (sofosbuvir) 和维帕他韦 (velpatasvir) 以固定剂量复方制剂的形式上市,商品名为 Vosevi。Vosevi 获批用于治疗基因型为 1、2、3、4、5 或 6 的慢性丙型肝炎病毒 (HCV) 感染成人患者。值得注意的是,Vosevi 获批用于既往接受过 NS5A 抑制剂治疗的基因型为 1-6 的患者,或既往接受过不含 NS5A 抑制剂的索非布韦 HCV 治疗方案的基因型为 1a 或 3 的患者。在 Vosevi 上市之前,对于既往接受过含 NS5A 抑制剂的治疗方案但治疗失败的慢性 HCV 感染患者,尚无获批的再治疗方案。 伏西瑞韦是一种丙型肝炎病毒 NS3/4A 蛋白酶抑制剂。沃西拉普韦的作用机制是作为丙型肝炎病毒 (HCV) NS3/4A 蛋白酶抑制剂、P-糖蛋白抑制剂、乳腺癌耐药蛋白抑制剂、有机阴离子转运多肽 1B1 抑制剂和有机阴离子转运多肽 1B3 抑制剂。 沃西拉普韦是一种口服生物利用度高的丙型肝炎病毒 (HCV) 非结构蛋白 3/非结构蛋白 4A (NS3/NS4A) 丝氨酸蛋白酶抑制剂,具有抗病毒活性。给药后,沃西拉普韦与 HCV NS3/NS4A 丝氨酸蛋白酶结合,阻止 NS3/NS4A 蛋白酶介导的多聚蛋白成熟。这会破坏病毒蛋白的加工和病毒复制复合物的形成,从而抑制病毒复制和功能。 NS3 是一种丝氨酸蛋白酶,对 HCV 多聚蛋白内多个位点的蛋白水解切割至关重要,并在 HCV 核糖核酸 (RNA) 复制过程中发挥关键作用。NS4A 是 NS3 的激活因子。HCV 是一种小型、有包膜的单链 RNA 病毒,属于黄病毒科;HCV 感染与肝细胞癌 (HCC) 的发生密切相关。丙型肝炎是一种影响全球的重大疾病。近年来,该病的治疗发生了革命性的变化。随着第二代直接抗病毒药物的获批,丙型肝炎的治疗发生了根本性的转变,目前用于治疗丙型肝炎的药物比以往获批的药物疗效显著提高,安全性也更高。对于直接抗病毒药物治疗失败的患者,治疗方案一直以来都十分复杂且难以实施,但索非布韦/维帕他韦/伏西瑞韦的获批为这些患者带来了新的治疗选择。本文将介绍索非布韦/维帕他韦/伏西瑞韦,这是一种近期获批用于治疗丙型肝炎的联合疗法。本文回顾了该联合疗法获批的相关研究,并分析了其疗效和安全性。专家观点:索非布韦/维帕他韦/伏西瑞韦填补了丙型肝炎治疗领域此前的一个空白,即针对耐药病毒感染导致治疗失败的患者。随着这一空白的填补,新疗法的研发速度似乎普遍放缓。尽管可以理解,但从长远来看,丙型肝炎新药研发的减少会带来相当大的风险。[1] 结论 SOF/VOX/VEL联合疗法对其他丙型肝炎药物治疗无效的患者来说是一种耐受性良好且有效的治疗方案。此外,它对所有主要丙型肝炎病毒基因型均有效。虽然该药物存在一些副作用,但总体耐受性良好,在III期临床试验中仅有一例患者因不良反应而停止使用SOF/VOX/VEL。尤其与前几代丙型肝炎治疗药物相比,观察到的副作用在很多情况下都较轻微。即使是其他治疗方案失败的患者,接受 SOF/VOX/VEL 治疗的患者也具有很高的 SVR 率,这确保了 SOF/VOX/VEL 在未来几年内仍将是 HCV 治疗的重要补充。 专家意见 过去 7 年,HCV 药物审批和治疗领域的革命性变革彻底改变了抗 HCV 药物的格局,以至于 2011 年获批的药物在很多情况下现在已经过时。随着这些显著变化,抗 HCV 新药的审批和研发速度有所放缓。事实上,针对所有主要 HCV 基因型,许多 HCV 治疗领域似乎已被有效且耐受性良好的治疗方案所占据。虽然对DAA方案治疗失败的患者可以使用已获批准的药物进行治疗,但在SOF/VOX/VEL获批之前,对于对新型DAA治疗失败的患者,治疗选择并不充分。 在这一领域,SOF/VOX/VEL有望成为HCV治疗的重要药物,并代表了一种治疗耐药HCV的重要新疗法组合。全面评估SOF/VOX/VEL对对包括SOF/VEL和glecaprevir/pibrentasvir在内的新型方案治疗失败的患者的疗效也至关重要。尽管由于POLARIS-2试验的结果,该药物尚未在美国获批用于初治患者,但对于一线治疗失败的患者而言,迫切需要有效的治疗方法。即使在对已获批准的直接抗病毒药物(DAA)产生耐药性的丙型肝炎病毒(HCV)感染者中,SOF/VOX/VEL方案仍能保持较高的持续病毒学应答率(SVR),这很可能确保SOF/VOX/VEL方案在未来HCV治疗中占据关键地位。由于SOF/VOX/VEL方案包含三大类DAA药物,即使对其中一种药物存在部分耐药性,仍可能获得治疗成功。我们认为,鉴于绝大多数已获批准用于初治患者的治疗方案,尤其是疗程仅需8周的方案,其SVR率都很高,因此,治疗费用和医保覆盖范围的差异可能是决定治疗方案选择的主要因素之一。格卡瑞韦/哌仑他韦方案近期获批,该方案同样适用于初治患者,疗程仅需8周,且SVR率高,价格也相对较低。如果SOF/VOX/VEL方案最终在美国获批用于初治患者,那么格卡瑞韦/哌仑他韦方案可能会限制SOF/VOX/VEL方案在该适应症中的应用。丙型肝炎治疗领域一个值得关注的进展是,随着时间的推移,疗程和副作用情况都得到了显著改善。即使是新型直接抗病毒药物(DAA),许多方案的疗程也从12周缩短至8周。然而,更短的疗程是否有效仍是一个悬而未决的问题。2016年的一项研究调查了使用ledipasvir/SOF治疗1型基因感染的6周疗程,结果显示持续病毒学应答率(SVR)较高。这与之前其他DAA试验的结果形成鲜明对比,那些试验表明6周疗程的疗效较低。这种疗效是否能推广到其他基因型或其他治疗方案,仍然是一个重要的问题。新型DAA的研发速度也反映了抗丙型肝炎药物的市场需求是如何被填补的。许多制药公司已将其研发重点从丙型肝炎转向乙型肝炎病毒(HBV)以及其他疾病。目前看来,抗击丙型肝炎病毒 (HCV) 的下一步主要措施将是疫苗研发,而非其他药物干预。 从经济角度来看,将研发重心从新型抗 HCV 药物转向其他疾病是可以理解的,但这并非没有风险。虽然目前使用的药物疗效显著,耐药风险相对较低,但大多数直接抗病毒药物 (DAA) 仍可能出现耐药性,据报道某些药物的耐药率在 10% 至 15% 之间。正如抗菌药物的情况一样,随着时间的推移,即使是这些较新的药物也可能出现耐药性。由于新型 DAA 的研发速度较慢,这些药物产生耐药性的风险也随之增加。[1] 在这项随机 1b 期研究中,研究人员评估了 Voxilaprevir/GS-9857 在 50 至 300 mg 剂量范围内对慢性基因 1-4 型 HCV 感染患者的安全性、抗病毒疗效和药代动力学。 GS-9857每日一次,连续给药3天,慢性丙型肝炎病毒(HCV)感染患者总体耐受性良好。所有不良事件(AE)均为轻度或中度,其中腹泻和头痛最为常见。尽管既往报道某些基于蛋白酶抑制剂的治疗方案会增加皮疹、瘙痒、恶心和贫血的发生率7-10,但本研究中未观察到此类事件。接受GS-9857治疗的患者中有16.9%出现3级或4级实验室异常,且与GS-9857剂量或不良事件无关。值得注意的是,ALT、AST和碱性磷酸酶水平的评估未发现任何3级或4级异常,表明GS-9857给药不会引起肝功能的显著变化。体格检查和心电图评估未发现具有临床意义的发现。 使用 100 mg 或 300 mg 剂量的 GS-9857 治疗后,所有基因型(包括基因型 3)的病毒载量较基线均降低了 >3 log10 IU/mL,表明 GS-9857 在 HCV 感染患者中表现出强大的抗病毒活性。这一观察结果与体外数据一致,体外数据显示GS-9857对1至6型基因型复制子具有泛基因型活性,半数最大有效浓度范围为1.5至6.6 nM5。除接受剂量<100 mg GS-9857治疗的3a型基因型感染患者外,所有患者的HCV RNA水平均快速且持续下降,并维持至第10天。对于接受50 mg GS-9857治疗的3a型基因型感染患者,HCV RNA水平下降速度较慢。 本研究对36、41、43、54、55、80、122、155、156、168和170位点的氨基酸替换进行了表征,据报道这些替换与NS3/4A蛋白酶抑制剂的耐药性相关11-17。在开始GS-9857治疗前,22.4%接受测序的患者携带NS3耐药相关变异(RAV)。GS-9857治疗后,无论患者是否携带NS3 RAV,其平均最大病毒载量下降幅度均相似,表明GS-9857的抗病毒疗效在存在通常与耐药性相关的突变的情况下仍然得以维持。在接受GS-9857治疗3天后进行测序的患者中,大多数(73.6%)未出现新的NS3 RAV,且在基因型2或4感染的患者中也未出现新的NS3 RAV。A156V或A156T是基因型1a或1b感染患者中最常见的突变。体外数据表明,GS-9857对除A156T外的最常见的基因型1 RAV具有强效活性。这种替换与高水平的耐药性(>100倍)相关,但病毒适应性较低(与野生型1a基因型复制子相比仅为1.5%)12。NS3耐药相关变异(RAV)的总体低发生率表明,与其他第一代蛋白酶抑制剂相比,GS-9857具有相对较高的耐药屏障,这对于既往接受过DAA方案治疗失败的患者进行再治疗而言可能具有显著优势。 在空腹条件下,给予50至300 mg剂量的GS-9857,其暴露量呈剂量比例增加。各队列的中位半衰期约为29-42小时,支持每日一次给药。与其较长的中位半衰期一致,观察到GS-9857暴露量的显著累积。 GS-9857 的血浆药代动力学在基因型为 1a、1b、2、3 或 4 的 HCV 感染患者中相似。 本初步研究排除了肝硬化或慢性肝病患者。因此,未观察到显著的安全性问题可能是由于研究人群不易发生不良事件所致。需要对病情更严重或伴有其他并发症的患者进行 GS-9857 的进一步评估,以证实本研究的结果。 总之,多次给予 GS-9857 耐受性良好,并可显著降低基因型为 1-4 的 HCV 感染患者的 HCV RNA 水平。值得注意的是,即使存在与蛋白酶抑制剂耐药性相关的常见 NS3 突变,GS-9857 仍保持其强大的抗病毒活性。在空腹条件下,GS-9857 以 50 至 300 mg 的剂量给药时,表现出线性药代动力学特征。GS-9857 的中位半衰期为 29 至 42 小时,适合每日一次给药。此外,体外研究表明,GS-9857 与索非布韦或维帕他韦联合用药具有叠加的抗病毒活性。综上所述,这些数据支持进一步开发每日一次的 GS-9857 与其他直接抗病毒药物 (DAA) 联合用于治疗慢性丙型肝炎病毒 (HCV) 感染患者。[2] 我们试验中一个意想不到的结果是,对于初治肝硬化患者,在索非布韦-维帕他韦联合伏西瑞韦/GS-9857 的基础上加用利巴韦林似乎没有获益。尽管接受利巴韦林治疗的该组患者的SVR12率在数值上低于未接受治疗的肝硬化患者接受索非布韦-维帕他韦联合GS-9857治疗(不含利巴韦林)的治疗组(81% vs 94%),但置信区间存在重叠,这可能反映了样本量较小。 限制本试验结果解释的因素包括样本量小以及非对照、开放标签设计。尽管该试验仅纳入了基因型 1 的 HCV 患者,但另一项设计类似的试验已开展,以评估该联合方案在非基因型 1 的 HCV 患者中的疗效。 总之,索非布韦-维帕他韦联合 GS-9857 治疗 12 周,在目前无其他治疗选择的患者群体中(包括既往接受过含 NS5A 抑制剂方案治疗但未达到 SVR 的代偿性肝硬化患者和非代偿性肝硬化患者),SVR12 率高达 100%,且耐受性良好。在初治患者中,索非布韦-维帕他韦联合GS-9857的安全性良好,且能有效将疗程缩短至8周,同时保持较高的SVR12率。这3种强效泛基因型DAA已被共同配制成固定剂量复方片剂。3期临床试验将评估该固定剂量复方制剂在初治患者中的疗效,疗程为8周;在既往接受过DAA治疗的患者(包括既往接受过NS5A抑制剂治疗的患者)中的疗效,疗程为12周。[3] |
| 分子式 |
C40H52F4N6O9S
|
|
|---|---|---|
| 分子量 |
868.94
|
|
| 精确质量 |
868.345
|
|
| 元素分析 |
C, 55.29; H, 6.03; F, 8.75; N, 9.67; O, 16.57; S, 3.69
|
|
| CAS号 |
1535212-07-7
|
|
| 相关CAS号 |
|
|
| PubChem CID |
89921642
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 折射率 |
1.596
|
|
| LogP |
3.83
|
|
| tPSA |
203.6
|
|
| 氢键供体(HBD)数目 |
3
|
|
| 氢键受体(HBA)数目 |
15
|
|
| 可旋转键数目(RBC) |
9
|
|
| 重原子数目 |
60
|
|
| 分子复杂度/Complexity |
1780
|
|
| 定义原子立体中心数目 |
8
|
|
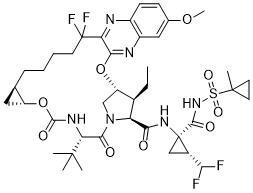
| SMILES |
S(C1(C)CC1)(NC([C@]1(C[C@H]1C(F)F)NC([C@@H]1[C@H](CC)[C@@H]2CN1C([C@H](C(C)(C)C)NC(=O)O[C@@H]1C[C@H]1CCCCC(C1C(=NC3C=C(C=CC=3N=1)OC)O2)(F)F)=O)=O)=O)(=O)=O
|
|
| InChi Key |
MZBLZLWXUBZHSL-FZNJKFJKSA-N
|
|
| InChi Code |
InChI=1S/C40H52F4N6O9S/c1-7-22-27-19-50(28(22)32(51)48-39(18-23(39)31(41)42)35(53)49-60(55,56)38(5)14-15-38)34(52)30(37(2,3)4)47-36(54)59-26-16-20(26)10-8-9-13-40(43,44)29-33(58-27)46-25-17-21(57-6)11-12-24(25)45-29/h11-12,17,20,22-23,26-28,30-31H,7-10,13-16,18-19H2,1-6H3,(H,47,54)(H,48,51)(H,49,53)/t20-,22-,23+,26-,27+,28+,30-,39-/m1/s1
|
|
| 化学名 |
(33R,34S,35S,91R,92R,5S)-5-(tert-butyl)-N-((1R,2R)-2-(difluoromethyl)-1-(((1-methylcyclopropyl) sulfonyl)carbamoyl)cyclopropyl)-34-ethyl-14,14-difluoro-17-methoxy-4,7-dioxo-2,8-dioxa-6-aza-1(2,3)-quinoxalina-3(3,1)-pyrrolidina-9(1,2)-cyclopropanacyclotetradecaphane-35-carboxamide
|
|
| 别名 |
GS-9857; GS 9857; Voxilaprevir; 1535212-07-7; Voxilaprevir [INN]; Voxilaprevir [USAN:INN]; VOXILAPREVIR [MI]; (1R,18R,20R,24S,27S,28S)-24-tert-butyl-N-[(1R,2R)-2-(difluoromethyl)-1-[(1-methylcyclopropyl)sulfonylcarbamoyl]cyclopropyl]-28-ethyl-13,13-difluoro-7-methoxy-22,25-dioxo-2,21-dioxa-4,11,23,26-tetrazapentacyclo[24.2.1.03,12.05,10.018,20]nonacosa-3,5(10),6,8,11-pentaene-27-carboxamide; GS9857; trade name: Vosevi
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ≥ 100 mg/mL (~115.08 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (2.88 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.1508 mL | 5.7541 mL | 11.5083 mL | |
| 5 mM | 0.2302 mL | 1.1508 mL | 2.3017 mL | |
| 10 mM | 0.1151 mL | 0.5754 mL | 1.1508 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT02402452 | COMPLETED | Drug: Voxilaprevir | HCV Infection | Gilead Sciences | 2015-05-05 | Phase 1 |
| NCT06180590 | RECRUITING | Drug: Sofosbuvir / Velpatasvir / Voxilaprevir Oral Tablet [Vosevi] |
Chronic Hepatitis C Medication Reaction |
The Third Affiliated Hospital of Guangzhou Medical University |
2023-02-28 | |
| NCT05717400 | RECRUITING | Drug:Bevacizumab Drug:Atezolizumab Drug:Sofosbuvir |
Liver Cancer | M.D. Anderson Cancer Center |
2023-02-07 | Phase 4 |
| NCT02397707 | COMPLETED | Drug: Voxilaprevir | HCV Infection | Gilead Sciences | 2015-03-24 | Phase 1 |
| NCT02185794 | COMPLETED | Drug:Voxilaprevir Drug:Placebo to match voxilaprevir Drug:SOF/VEL |
Hepatitis C Virus Infection | Gilead Sciences | 2014-06-13 | Phase 1 |
|