| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
P2X7 receptor – IC50 = 20 nM (human P2X7, calcium influx); IC50 = 42 nM (rat P2X7, calcium influx); IC50 = 150 nM (mouse P2X7, calcium influx); IC50 = 37 nM (BzATP-stimulated IL-1β release in differentiated human THP-1 cells); IC50 = 7 nM (BzATP-stimulated YO-PRO uptake in differentiated human THP-1 cells); pIC50 = 7.67 ± 0.04 (human), 7.36 ± 0.02 (rat), 6.83 ± 0.03 (mouse) [1]; pA2 = 8.1 (competitive antagonist) [1]
|
|---|---|
| 体外研究 (In Vitro) |
体外活性: A-839977在稳定表达人(IC50 = 20 nM)、大鼠(IC50 = 42 nM)或小鼠(IC50 = 150 nM)P2X7受体的1321N1细胞中强效阻断BzATP诱发的细胞内钙浓度变化。[1]
A-839977在分化的人THP-1细胞中强效阻断BzATP刺激的IL-1β释放(IC50 = 37 nM)和YO-PRO摄取(IC50 = 7 nM)。[1] A-839977使BzATP浓度-效应钙内流曲线产生平行右移,pA2值为8.1,表明其为竞争性拮抗剂。[1] 在培养的大鼠视神经头星形胶质细胞中,A-839977(50 nM)阻止了肿胀诱导的IL-1β mRNA上调。[2] 在培养的小鼠视神经头星形胶质细胞中,A-839977(100 nM)减少了肿胀触发的IκBα降低,表明抑制了NFκB活化。[2] A839977 通过抑制 BzATP 诱导的钙流入哺乳动物 P2X7 受体,特异性阻止分化的人 THP-1 细胞中激动剂诱导的 YO-PRO 摄取和 IL-1beta 释放 (IC50=20-150 nM)。在动物研究中,它已被证明可以减轻神经性疼痛和炎症[1]。在视星形胶质细胞中,839977(50 nM,1 小时预处理)可有效抑制应激引起的 IL-1β 起始的增加 [2]。 |
| 体内研究 (In Vivo) |
体内活性: 在大鼠骨癌痛模型(胫骨内MRMT-1癌细胞)中,脊髓应用A-839977(0.4和1.2 mg/kg)以剂量依赖性方式显著降低背角神经元对高强度机械刺激(26g和60g)和高强度热刺激(48°C)的反应。对低强度刺激的反应或假手术/未处理动物无影响。[3]
在同一模型中,全身给予A-839977(40 mg/kg,腹腔注射)显著增加荷癌动物的机械撤足阈值(von Frey试验),对假手术动物或溶媒处理无影响。更高剂量(120 mg/kg)显示毒性效应。[3] A-839977(40 mg/kg,腹腔注射)在疾病晚期显著增加荷癌动物的负重比率(失能测试仪)和肢体使用评分,溶媒处理无影响。[3] A-839977(40 mg/kg,腹腔注射)在未处理大鼠的转棒测试中不影响运动协调。[3] 在CFA诱导的炎症性疼痛小鼠模型中,A-839977剂量依赖性地减轻热痛觉过敏(小鼠ED50 = 40 μmol/kg,腹腔注射;大鼠ED50 = 100 μmol/kg,腹腔注射)。在IL-1αβ敲除小鼠中未观察到抗痛觉过敏作用。[1] 在大鼠中,A-839977(30 mg/kg,腹腔注射)在测试前30分钟给药可减轻CFA诱导的热痛觉过敏。[1] 在小鼠视网膜机械应变模型(控制性眼压升高)中,A-839977(体外50 nM,或通过P2X7敲除)阻止了IL-1β mRNA和蛋白的上调。[2] 在大鼠中,足底注射完全弗氏佐剂 (CFA) 时,A839977(30 μmol/kg、100 μmol/kg、300 μmol/kg;预注射 30 分钟)以剂量依赖性方式降低热痛觉过敏 [1]。 A839977(10μmol/kg、30μmol/kg和100μmol/kg;预注射30分钟)对野生型小鼠的CFA炎症疼痛模型有显着影响,而IL-1alphabeta敲除小鼠则不显着。做作的。大鼠无效[1]。在患有癌症的动物中,A839977 会降低背角神经元的反应 [3]。 |
| 酶活实验 |
酶/受体实验: 钙内流FLIPR实验:将稳定表达P2X7受体的1321N1细胞接种于多聚-D-赖氨酸包被的黑色96孔板中,加载Fluo-4染料。洗涤后,细胞与A-839977预孵育3分钟,然后加入激动剂。使用EC70浓度的BzATP(小鼠:150 μM,大鼠:10 μM,人:5 μM)作为激动剂。测量荧光3分钟。计算IC50值。[1]
YO-PRO摄取实验:将分化的人THP-1细胞铺板,与A-839977预孵育30分钟。加入BzATP(90 mM)并测量YO-PRO摄取1小时。[1] IL-1β释放实验:分化的人THP-1细胞用LPS(25 ng/ml)和IFNγ(10 ng/ml)引发3小时。在BzATP(1 mM)刺激前30分钟加入A-839977。通过ELISA测量上清液中的IL-1β水平。[1] |
| 细胞实验 |
细胞实验: 稳定表达小鼠、大鼠或人P2X7受体的1321N1人星形细胞瘤细胞维持在含1% L-丙氨酰-L-谷氨酰胺、1%抗生素/抗真菌剂、10% FBS和300 μg/ml Geneticin的DMEM中。对于钙内流实验,细胞以每板5 × 10⁶个细胞的密度接种。[1]
THP-1人单核细胞用LPS(25 ng/ml)和IFNγ(10 ng/ml)分化成巨噬细胞表型,分化时间分别为3小时(IL-1β释放)或过夜(孔形成)。细胞维持在含10%胎牛血清的RPMI中。[1] 大鼠视神经头星形胶质细胞:从新生大鼠幼崽(PD3-5)分离原代星形胶质细胞,在含10% FBS、1%青霉素/链霉素和25 ng/ml EGF的DMEM/F12中培养。通过GFAP染色确定细胞>99%为星形胶质细胞。对于肿胀实验,细胞在30%低渗溶液中孵育4小时。在肿胀前1小时加入A-839977(50 nM)。[2] 小鼠视神经头星形胶质细胞:从3月龄C57BL/6J和P2X7-/-小鼠分离。培养方法与大鼠星形胶质细胞类似。使用A-839977(100 nM)。[2] RT-PCR[2] 细胞类型:视星形胶质细胞 测试浓度: 50 nM 孵育时间: 1小时(治疗前) 实验结果:防止星形胶质细胞中 IL-1β 的启动 |
| 动物实验 |
动物/疾病模型:雄性SD(SD(Sprague-Dawley))、balb/c(Bagg ALBino)小鼠和IL-1(−/−)小鼠,用于CFA诱导的慢性炎症。剂量:30 μmol/kg、100 μmol/kg、300 μmol/kg(大鼠);10 μmol/kg、30 μmol/kg、100 μmol/kg(小鼠)
给药途径:注射;注射前30分钟 实验结果:在大鼠和小鼠中以剂量依赖的方式减轻CFA诱导的热痛觉过敏,但对IL-1(−/−)小鼠无影响。 |
| 药代性质 (ADME/PK) |
A-839977具有中枢神经系统穿透性,脑/脊髓与血浆比值为0.15-0.25。[1][3]
对于体内电生理,A-839977每日溶解于10% DMSO、10% ChromEL和无菌生理盐水中。[3] 对于行为学研究,A-839977溶解于30% NMP、30% PEG400和40%羟丙基-β-环糊精中。[3] |
| 毒性/毒理 (Toxicokinetics/TK) |
在骨癌痛模型中,120 mg/kg剂量的A-839977(腹腔注射)显示出明显的毒性效应,未进一步测试。40 mg/kg剂量耐受良好,未观察到运动协调缺陷。[3]
在CFA炎症性疼痛模型中,A-839977在有效剂量下未产生任何明显的行为紊乱迹象。[1] |
| 参考文献 |
|
| 其他信息 |
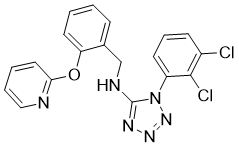
A-839977(1-(2,3-二氯苯基)-N-(2-(吡啶-2-基氧基)苄基)-1H-四唑-5-胺)是一种强效、选择性、竞争性的P2X7受体拮抗剂,源自一系列基于四唑的化合物。它具有中枢神经系统穿透性,已被用于证明P2X7受体拮抗剂在炎症性和骨癌痛模型中产生抗伤害作用。A-839977的抗痛觉过敏作用通过阻断IL-1β释放介导,因为在IL-1αβ敲除小鼠中该作用消失。A-839977还用于研究机械应变后星形胶质细胞中P2X7受体在炎症小体启动中的作用。[1][2][3]
|
| 分子式 |
C19H14CL2N6O
|
|---|---|
| 分子量 |
413.260060787201
|
| 精确质量 |
412.061
|
| 元素分析 |
C, 55.22; H, 3.41; Cl, 17.16; N, 20.34; O, 3.87
|
| CAS号 |
870061-27-1
|
| PubChem CID |
53325875
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
4.19
|
| tPSA |
80.98
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
28
|
| 分子复杂度/Complexity |
489
|
| 定义原子立体中心数目 |
0
|
| SMILES |
ClC1C(Cl)=C(N2C(NCC3C(OC4C=CC=CN=4)=CC=CC=3)=NN=N2)C=CC=1
|
| InChi Key |
GMVNBKZQJFRFAR-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C19H14Cl2N6O/c20-14-7-5-8-15(18(14)21)27-19(24-25-26-27)23-12-13-6-1-2-9-16(13)28-17-10-3-4-11-22-17/h1-11H,12H2,(H,23,24,26)
|
| 化学名 |
1-(2,3-dichlorophenyl)-N-{[2-(pyridin-2-yloxy)phenyl]methyl}-1H-1,2,3,4-tetrazol-5-amine
|
| 别名 |
A839977; A-839977; A-839,977; A839,977; 1-(2,3-dichlorophenyl)-N-{[2-(pyridin-2-yloxy)phenyl]methyl}-1H-1,2,3,4-tetrazol-5-amine; 1-(2,3-dichlorophenyl)-N-((2-(pyridin-2-yloxy)phenyl)methyl)-1H-1,2,3,4-tetrazol-5-amine; 870061-27-1; A 839977
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~241.98 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.05 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (6.05 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.05 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.4198 mL | 12.0989 mL | 24.1978 mL | |
| 5 mM | 0.4840 mL | 2.4198 mL | 4.8396 mL | |
| 10 mM | 0.2420 mL | 1.2099 mL | 2.4198 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|