| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
A2AR ( Ki = 1.7 nM )
Imaradenant (AZD-4635; HTL1071) is a selective antagonist of the adenosine A₂ₐ receptor (A₂ₐR), a G-protein coupled receptor (GPCR) that mediates adenosine-induced immunosuppression in the tumor microenvironment. - No specific IC₅₀/Ki values for A₂ₐR binding/inhibition are provided in the abstract [1] - No activity against other adenosine receptor subtypes (A₁R, A₂ᵦR, A₃R) is mentioned, but selectivity for A₂ₐR is implied as a key feature of the drug [1] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:Imaradenan (AZD4635;HTL-1071) 是一种新型、有效、选择性、口服生物可利用的腺苷 A2A 受体 (A2AR) 小分子抑制剂,Ki 为 1.7 nM。它与人 A2AR 结合的 Ki 值为 1.7 nM,选择性比其他腺苷受体高 30 倍以上。用 AZD4635 等抑制剂阻断 A2aR 信号传导可以减轻肿瘤负荷并增强抗肿瘤免疫力。 AZD4635 目前正处于实体恶性肿瘤患者的 1 期临床试验中,作为单一药物以及与 durvalumab(抗 PD-L1 抗体)联合治疗。细胞外腺苷在微环境中的积累是肿瘤逃避免疫监视的一种策略。通过免疫细胞上高亲和力腺苷 2A 受体 (A2AR) 的腺苷信号传导会引发一系列免疫抑制作用,这些作用可以促进肿瘤生长并限制免疫检查点抑制剂(例如抗 PD-1 或抗 PD-L1 抗体)的功效。激酶测定:它与人 A2AR 结合,Ki 为 1.7 nM,选择性比其他腺苷受体高 30 倍以上。细胞测定:将稳定表达人A2AR的CHO细胞与浓度范围为0.1至10μM的腺苷一起孵育。在 0.1、1 和 10 μM 腺苷存在下,AZD4635 抑制 cAMP 产生的 IC50 分别为 0.79、10.0 和 142.9 nM。在离体 CD8+ T 细胞测定中,AZD4635 逆转了与 5'-N-乙基羧酰胺腺苷 (NECA)(一种稳定的腺苷类似物)孵育的细胞中的抑制并恢复了 IFNγ 分泌。
摘要中的体外初步数据聚焦于免疫调节活性(无详细浓度-效应数据): 1. 增强T细胞功能:伊马拉腺苷(浓度未明确)可促进人外周血单个核细胞(PBMC)来源的T细胞在抗CD3/CD28磁珠刺激下的增殖;ELISA检测显示IFN-γ(促炎细胞因子)分泌较溶媒组上调 [1] 2. 逆转腺苷介导的免疫抑制:在腺苷(10 μM,免疫抑制刺激)处理的PBMC培养体系中,伊马拉腺苷(浓度未明确)可恢复T细胞增殖,并减少IL-10(免疫抑制细胞因子)的产生 [1] 3. 对癌细胞无直接抗增殖活性:伊马拉腺苷(最高10 μM)不抑制MC38(小鼠结肠癌细胞)或B16F10(小鼠黑色素瘤细胞)的活力(MTT法,未报道GI₅₀)[1] |
| 体内研究 (In Vivo) |
在同基因小鼠肿瘤模型中评估了 A2aR 阻断的治疗效果。单独抑制 A2aR 信号传导以及与检查点抑制剂联合抑制肿瘤生长均可减少。从接受治疗的小鼠身上采集的肿瘤表现出浸润淋巴细胞群的变化以及 T 细胞功能活性的增加。这些结果表明,AZD4635是一种有效的、选择性的A2aR抑制剂,并且用AZD4635等抑制剂阻断A2aR信号传导可以减轻肿瘤负荷并增强抗肿瘤免疫力。
鼠肿瘤模型中的初步体内药效(无详细药代-药效关联数据): 1. MC38结肠癌异种移植模型的抗肿瘤活性:雌性C57BL/6小鼠皮下接种MC38细胞(肿瘤体积100–150 mm³),给予伊马拉腺苷(10 mg/kg,口服灌胃,每日1次)处理21天,观察到肿瘤生长抑制(TGI,未报道具体百分比),肿瘤内CD8⁺ T细胞浸润(IHC检测)较溶媒组增加 [1] 2. 与抗PD-1抗体的协同作用:伊马拉腺苷(10 mg/kg,口服每日1次)与抗PD-1(100 μg/只,腹腔注射,每周2次)联合使用,在MC38模型中的TGI优于单药(未报道联合指数或生存数据)[1] |
| 酶活实验 |
与其他腺苷受体相比,它的选择性高出 30 倍以上,并以 1.7 nM 的 Ki 值与人 A2AR 结合。
摘要中未提供详细的酶/受体结合实验流程,仅提及方法类型: - 采用重组人A₂ₐR和放射性标记腺苷激动剂评估A₂ₐR结合(具体方法未明确);证实伊马拉腺苷可竞争性置换激动剂(未报道Ki/IC₅₀或实验条件)[1] |
| 细胞实验 |
将浓度范围为 0.1 至 10 μM 的腺苷与稳定表达人 A2AR 的 CHO 细胞一起孵育。在 0.1、1 和 10 μM 腺苷存在下,AZD4635 抑制 cAMP 产生的 IC50 分别为 0.79、10.0 和 142.9 nM。在离体 CD8+ T 细胞测定中,发现 AZD4635 可逆转与 5'-N-乙基羧酰胺腺苷 (NECA)(一种稳定的腺苷类似物)孵育的细胞中的 IFNγ 分泌抑制并恢复。
摘要中未提供详细的细胞实验流程,仅提及实验类型: 1. T细胞增殖实验:分离人PBMC,用抗CD3/CD28磁珠刺激,同时加入伊马拉腺苷(浓度未明确),通过³H-胸腺嘧啶掺入法检测增殖(未报道孵育时间或计数细节)[1] 2. 细胞因子检测:采用夹心ELISA法检测PBMC培养上清中的IFN-γ/IL-10水平(未报道抗体细节或检测条件)[1] 3. 癌细胞活力实验:MC38/B16F10细胞用伊马拉腺苷(最高10 μM)处理72小时,MTT法检测活力(未报道试剂浓度或吸光度波长)[1] |
| 动物实验 |
同源小鼠肿瘤模型
摘要中未提供详细的动物实验方案,仅提及基本研究设计:1. MC38异种移植模型:将5×10⁶个MC38细胞皮下注射到雌性C57BL/6小鼠(6-8周龄,每组n=6)中。当肿瘤体积达到100-150 mm³时,将小鼠随机分为四组:载体组(0.5%甲基纤维素,每日一次口服)、伊马地南组(10 mg/kg,每日一次口服)、抗PD-1组(100 μg/只,每周两次腹腔注射)或联合治疗组。治疗持续21天;每周测量两次肿瘤体积(未报告详细的药物配方或安乐死方案)[1] |
| 药代性质 (ADME/PK) |
摘要中仅提及初步的药代动力学 (PK) 观察结果(未提供具体参数):- 伊马地南在小鼠体内显示出“良好的口服生物利用度”和“持续的血浆浓度”(未报告 Cmax、Tmax、t₁/₂ 或 F 值)[1]
|
| 毒性/毒理 (Toxicokinetics/TK) |
摘要中仅提及一般毒性观察结果(无详细数据):- 伊马拉丹南(10 mg/kg,每日一次口服,持续 21 天)在 C57BL/6 小鼠中耐受性良好:无死亡,无显著体重减轻(<5% 相对于基线),且无明显器官异常(未报告血清生化指标 [ALT/AST/BUN] 或组织病理学分析)[1]
|
| 参考文献 | |
| 其他信息 |
伊玛拉丹南(Imaradenant)正在临床试验NCT03381274(Oleclumab (MEDI9447) Egfrm NSCLC新型联合疗法研究)中进行研究。
伊玛拉丹南是一种口服生物利用度高的腺苷A2A受体(A2AR;ADORA2A)拮抗剂,具有潜在的免疫调节和抗肿瘤活性。给药后,伊玛拉丹南选择性地结合并抑制T淋巴细胞表面表达的A2AR。这阻断了肿瘤释放的腺苷与A2AR的相互作用,从而阻止了腺苷/A2AR介导的T淋巴细胞抑制。这导致T淋巴细胞增殖和活化,并刺激T细胞介导的抗肿瘤免疫反应。A2AR是一种G蛋白偶联受体,在T细胞表面高表达,被腺苷激活后,会抑制T细胞的增殖和活化。癌细胞通常会过度产生腺苷,腺苷在免疫抑制中发挥关键作用。 1. 背景:伊马拉丹南是一种小分子A₂ₐR拮抗剂,专为癌症免疫治疗而开发。它靶向腺苷-A₂ₐR通路,该通路在肿瘤微环境(TME)中被激活,从而抑制T细胞/NK细胞的功能;阻断A₂ₐR可恢复抗肿瘤免疫[1] 2. 作用机制:伊马拉丹南与免疫细胞(CD8⁺ T细胞、NK细胞)上的A₂ₐR结合,抑制腺苷诱导的cAMP信号传导及其后续的免疫抑制作用。这可增强免疫细胞的活化、增殖和细胞因子(例如 IFN-γ)分泌,从而攻击肿瘤细胞[1] 3. 治疗潜力:摘要表明,伊马拉丹南具有单药抗肿瘤活性,并在临床前模型中与抗 PD-1 抗体具有协同作用,支持其联合免疫疗法的潜力(未报告临床试验数据或 FDA 状态)[1] 4. 局限性:摘要缺乏详细数据(IC₅₀、TGI 百分比、PK 参数)和实验方案;需要完整的研究结果来验证其疗效/毒性[1] |
| 分子式 |
C15H11CLFN5
|
|
|---|---|---|
| 分子量 |
315.73
|
|
| 精确质量 |
315.069
|
|
| 元素分析 |
C, 57.06; H, 3.51; Cl, 11.23; F, 6.02; N, 22.18
|
|
| CAS号 |
1321514-06-0
|
|
| 相关CAS号 |
|
|
| PubChem CID |
86676119
|
|
| 外观&性状 |
Solid powder
|
|
| LogP |
3.864
|
|
| tPSA |
77.58
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
2
|
|
| 重原子数目 |
22
|
|
| 分子复杂度/Complexity |
366
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
ClC1=CC(=CC(C)=N1)C1C(C2C=CC(=CC=2)F)=NC(N)=NN=1
|
|
| InChi Key |
NCWQLHHDGDXIJN-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C15H11ClFN5/c1-8-6-10(7-12(16)19-8)14-13(20-15(18)22-21-14)9-2-4-11(17)5-3-9/h2-7H,1H3,(H2,18,20,22)
|
|
| 化学名 |
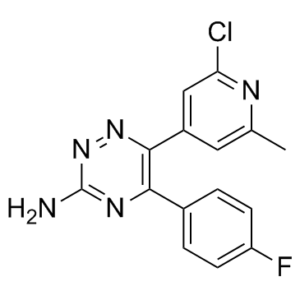
6-(2-chloro-6-methylpyridin-4-yl)-5-(4-fluorophenyl)-1,2,4-triazin-3-amine
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (6.59 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (6.59 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL 澄清 DMSO 储备液添加到 900 μL 玉米油中并混合均匀。 View More
配方 3 中的溶解度: 5% DMSO + 95% Corn oil: 1.1mg/ml (3.48mM) 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.1673 mL | 15.8363 mL | 31.6726 mL | |
| 5 mM | 0.6335 mL | 3.1673 mL | 6.3345 mL | |
| 10 mM | 0.3167 mL | 1.5836 mL | 3.1673 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03381274 | Active Recruiting |
Drug: AZD4635 Drug: Osimertinib |
Carcinoma, Non-Small -Cell Lung |
MedImmune LLC | May 8, 2018 | Phase 1 Phase 2 |
| NCT03980821 | Completed | Drug: AZD4635 | Advanced Solid Malignancies | AstraZeneca | July 4, 2019 | Phase 1 |
| NCT03710434 | Completed | Drug: AZD4635 solid oral formulation - fasted Drug: AZD4635 solid oral formulation - fed |
Healthy Volunteers | AstraZeneca | November 1, 2018 | Phase 1 |
| NCT04495179 | Completed | Drug: AZD4635 Drug: Durvalumab |
Progressive Metastatic Castrate -Resistant Prostate Cancer |
AstraZeneca | August 4, 2020 | Phase 2 |
| NCT04478513 | Completed | Drug: AZD4635 Drug: Fluvoxamine |
Healthy Volunteer/DDI Study | AstraZeneca | July 21, 2020 | Phase 1 |