| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 500μg |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Influenza virus[1] Cap-dependent endonuclease (CEN)[1][2]
Influenza virus RNA polymerase PA subunit endonuclease: - For influenza A virus (H1N1, H3N2) PA endonuclease: The half-maximal inhibitory concentration (IC₅₀) was 0.3-0.8 μM [2] - For influenza B virus PA endonuclease: The IC₅₀ was 0.9-1.2 μM [2] - Recombinant influenza A virus (H5N1) PA endonuclease: The dissociation constant (Ki) was 0.15 μM [5] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:Baloxavir(商品名 Xofluza;Baloxavir 酸或 BXA)是一种口服小分子帽依赖性核酸内切酶抑制剂,由 Roche 和 Shionogi 开发。它有效且选择性地抑制甲型和乙型流感病毒聚合酶 PA 亚基内的帽子依赖性核酸内切酶。 2018年2月,巴洛沙韦在日本获得全球首个批准,用于治疗甲型或乙型流感病毒感染。美国、欧盟和其他国家正在进行该适应症的 III 期开发。该药物通过抑制 mRNA 合成的起始来阻止流感病毒的增殖。 PA I38T 取代是降低 BXA 敏感性的主要途径,A 型病毒和 B 型病毒的 EC50 变化分别为 30 至 50 倍和 7 倍。带有 I38T 取代的病毒在细胞中表现出严重受损的复制适应性,并相应地降低了体外核酸内切酶活性。激酶测定:奥司他韦酸在 MES 测定缓冲液中连续稀释 [32.5 mmol/L MES 和 4 mmol/L CaCl2,溶于 DW(用 4 N NaOH 调节 pH 6.5)]。为了制备 NA 酶溶液,用 0.1% NP-40 灭活病毒原液,并用 MES 测定缓冲液稀释。 10 μL 奥司他韦酸溶液和 10 μL NA 酶溶液混合,37℃孵育 30 分钟,然后加入 30 μL 100 μmol/L 2'-(4-甲基伞形基)-α-DN -乙酰神经氨酸钠盐水合物(MUNANA;Sigma-Aldrich Co., Ltd.)。反应混合物在37℃下孵育60分钟,加入150μL终止液[0.1mol/L甘氨酸和25%乙醇(用4N NaOH调节pH 10.7)]终止反应。使用酶标仪EnVision 2103 (PerkinElmer Inc.)在激发波长355 nm和发射波长460 nm下测量荧光强度,然后使用XLfit软件计算IC50值。 FC是通过将每种测试病毒的IC50除以同源野生型病毒的IC50来计算的。细胞测定:犬肾MDCK细胞获自欧洲细胞培养物保藏中心。人准二倍体肿瘤RPMI2650和人胚胎肾293 T细胞由美国典型培养物保藏中心提供。 MDCK 和 RPMI2650 细胞维持在补充有 10% 胎牛血清 (FBS) 和 100 µg/mL 卡那霉素 (Thermo Fisher Scientific, Inc.) 的基本必需培养基 (MEM) 中。 293 T 细胞在含有 10% FBS 和 100 µg/mL 卡那霉素的 Dulbecco 改良 Eagle 培养基中培养。采用基于八个质粒的反向遗传学技术来产生所描述的重组病毒。 rgA/WSN/33 (H1N1) 质粒组和空载体 pHW2000 由 St. Jude 儿童研究医院的 Robert Webster 博士提供。用于生成 rgA/Victoria/3/75 和 rgB/Maryland 病毒的质粒是通过标准分子生物学技术用 pHW2000 构建的。所使用的引物序列可根据要求提供。 MDCK 和 293 T 细胞的共培养物用八种质粒转染并孵育 48 至 72 小时,然后在 MDCK 细胞中繁殖病毒。重组病毒的PA序列通过Sanger测序进行验证。通过MDCK细胞中的标准组织培养感染剂量(TCID)50测定或空斑形成单位(PFU)测定来测定病毒滴度。
抗甲型和乙型流感病毒活性: - 在感染甲型流感病毒(H1N1 pdm09株)的MDCK细胞中:Baloxavir(0.001-0.1 μM)呈剂量依赖性降低病毒产量,EC₅₀为0.008 μM;0.1 μM时,病毒产量较溶剂对照组降低约99% [2] - 在感染甲型流感病毒(H3N2株)的MDCK细胞中:EC₅₀为0.012 μM;0.1 μM Baloxavir抑制病毒复制约98% [2] - 在感染乙型流感病毒(山形系)的MDCK细胞中:EC₅₀为0.015 μM;0.1 μM Baloxavir降低病毒产量约97% [2] - 对奥司他韦耐药流感毒株的活性:在感染奥司他韦耐药甲型流感(H1N1)毒株(H275Y突变)的MDCK细胞中,Baloxavir仍表现出强效抗病毒活性,EC₅₀为0.009 μM,与对野生型毒株的活性相当 [6] - 抑制病毒mRNA合成:在感染甲型流感(H1N1)病毒的A549细胞中,Baloxavir(0.1 μM)在感染后8小时显著降低病毒M1和NP mRNA水平(qPCR检测),分别降低约85%和80%,证实其抑制病毒转录 [6] - 低细胞毒性:在MDCK、A549和HepG2细胞中,Baloxavir的半数细胞毒性浓度(CC₅₀)>10 μM,对所有测试流感毒株的选择指数(SI = CC₅₀/EC₅₀)>1000 [2] |
| 体内研究 (In Vivo) |
病毒神经氨酸酶抑制剂对感染人分离的H7N9甲型流感病毒的小鼠疗效有限。尽管巴洛沙韦可保护小鼠免受从人身上分离的低致病性H7N9禽流感病毒的致命攻击感染,但其对最近感染高致病性H7N9人分离株的小鼠的功效尚不清楚。本实验研究了巴洛沙韦对感染高致病性人H7N9病毒a /Guangdong/17SF003/2016的小鼠的疗效。用单次1.5 mg/kg剂量的巴洛沙韦治疗感染小鼠,保护小鼠免受高致病性人H7N9病毒感染的效果与奥司他韦50 mg/kg剂量的治疗相同,每天两次,连续5天。以15或50 mg/kg的剂量每日治疗5天,显示出卓越的治疗效果,在很大程度上阻止了病毒在呼吸器官中的复制。这些结果表明,巴洛沙韦是人类高致病性H7N9病毒感染患者有价值的候选治疗药物。[6]
在临床试验中,单剂量的巴洛沙韦可显着降低病毒滴度并减轻流感症状。 甲型流感(H1N1 pdm09株)感染小鼠模型的疗效: - 6-8周龄雄性ICR小鼠经鼻感染甲型流感病毒(100× LD₅₀)。Baloxavir以0.1、0.3、1 mg/kg剂量口服给药,每日1次,连续3天,从感染后1天开始。1 mg/kg剂量时,Baloxavir显著阻止体重下降(感染后7天体重变化:-5% vs 溶剂对照组-25%),并将存活率提高至100%(溶剂对照组存活率20%)[1][3] - 小鼠肺部病毒载量:感染后4天,1 mg/kg Baloxavir使肺部病毒滴度(空斑实验检测)从溶剂对照组的10⁶.⁵ PFU/g降至10².³ PFU/g [1][3] - 甲型流感(H1N1 pdm09株)感染雪貂模型的疗效: - 6-8月龄雌性雪貂经鼻感染甲型流感病毒。Baloxavir在感染后1天单次口服给药1 mg/kg。感染后3天,鼻洗液病毒滴度较溶剂对照组降低约10⁴倍;Baloxavir处理组雪貂无发热(体温<39.5°C),鼻分泌物减少 [6] - 降低雪貂体内流感病毒传播:在雪貂间传播模型中,对感染雪貂给予Baloxavir(1 mg/kg,口服,感染后1天)可减少病毒排出,使病毒向未感染接触雪貂的传播率降低50%(溶剂对照组传播率100%)[6] |
| 酶活实验 |
奥司他韦酸在 MES 测定缓冲液中连续稀释 [32.5 mmol/L MES 和 4 mmol/L CaCl2,溶于 DW(用 4 N NaOH 调节 pH 6.5)]。为了制备 NA 酶溶液,用 0.1% NP-40 灭活病毒原液,并用 MES 测定缓冲液稀释。 10 μL 奥司他韦酸溶液和 10 μL NA 酶溶液混合,37℃孵育 30 分钟,然后加入 30 μL 100 μmol/L 2'-(4-甲基伞形基)-α-DN -乙酰神经氨酸钠盐水合物(MUNANA;Sigma-Aldrich Co., Ltd.)。反应混合物在37℃下孵育60分钟,加入150μL终止液[0.1mol/L甘氨酸和25%乙醇(用4N NaOH调节pH 10.7)]终止反应。使用酶标仪EnVision 2103 (PerkinElmer Inc.)在激发波长355 nm和发射波长460 nm下测量荧光强度,然后使用XLfit软件计算IC50值。 FC是通过将每种测试病毒的IC50除以同源野生型病毒的IC50来计算的。
重组流感PA核酸内切酶活性测定(荧光底物法): - 反应体系为50 μL,含20 mM Tris-HCl(pH 7.5)、5 mM MgCl₂、1 mM DTT、0.1 mg/mL BSA、50 nM重组PA核酸内切酶及1 μM荧光标记DNA底物(模拟宿主mRNA的5'-帽结构)。Baloxavir浓度为0.01-10 μM。混合物37°C孵育60分钟后,检测荧光强度(激发485 nm,发射520 nm)以评估底物切割情况。通过绘制Baloxavir浓度与酶活性百分比(相对于溶剂对照组)的剂量-效应曲线,计算IC₅₀ [2] - PA核酸内切酶Ki值测定: - 采用上述相同反应体系,调整荧光底物浓度(0.25-2 μM)和Baloxavir浓度(0.05-0.5 μM),测定初始反应速率并绘制Lineweaver-Burk双倒数图。根据图中直线交点计算Ki值,证实Baloxavir对PA核酸内切酶的竞争性抑制作用 [5] |
| 细胞实验 |
犬肾 MDCK 细胞获自欧洲细胞培养物保藏中心。人准二倍体肿瘤RPMI2650和人胚胎肾293 T细胞由美国典型培养物保藏中心提供。 MDCK 和 RPMI2650 细胞维持在补充有 10% 胎牛血清 (FBS) 和 100 µg/mL 卡那霉素 (Thermo Fisher Scientific, Inc.) 的基本必需培养基 (MEM) 中。 293 T 细胞在含有 10% FBS 和 100 µg/mL 卡那霉素的 Dulbecco 改良 Eagle 培养基中培养。采用基于八个质粒的反向遗传学技术来产生所描述的重组病毒。 rgA/WSN/33 (H1N1) 质粒组和空载体 pHW2000 由 St. Jude 儿童研究医院的 Robert Webster 博士提供。用于生成 rgA/Victoria/3/75 和 rgB/Maryland 病毒的质粒是通过标准分子生物学技术用 pHW2000 构建的。所使用的引物序列可根据要求提供。 MDCK 和 293 T 细胞的共培养物用八种质粒转染并孵育 48 至 72 小时,然后在 MDCK 细胞中繁殖病毒。重组病毒的PA序列通过Sanger测序进行验证。通过MDCK细胞中的标准组织培养感染剂量(TCID)50测定或空斑形成单位(PFU)测定来测定病毒滴度。
MDCK细胞流感病毒感染及病毒产量测定: - MDCK细胞以5×10⁴个/孔接种于24孔板,过夜培养。细胞感染流感病毒(感染复数MOI=0.01),37°C孵育1小时。移除病毒接种液后,加入含Baloxavir(0.0001-10 μM)的培养基,37°C(5% CO₂)孵育48小时。收集上清液,通过MDCK细胞空斑实验测定病毒滴度。EC₅₀定义为使病毒滴度较溶剂对照组降低50%的Baloxavir浓度 [2] - A549细胞病毒mRNA qPCR检测: - A549细胞以2×10⁵个/孔接种于6孔板,感染甲型流感(H1N1)病毒(MOI=1),孵育1小时。细胞用Baloxavir(0.1 μM)或溶剂处理后,37°C继续孵育。感染后4、8、12小时提取总RNA,逆转录合成cDNA。采用病毒M1和NP基因特异性引物进行qPCR,以GAPDH为内参基因,通过2⁻ΔΔCt法计算相对病毒mRNA水平 [6] - 细胞毒性实验(MTT法): - MDCK、A549或HepG2细胞以1×10⁴个/孔接种于96孔板,过夜培养。细胞用Baloxavir(0.1-100 μM)或溶剂处理72小时。每孔加入10 μL MTT试剂(5 mg/mL),37°C孵育4小时。DMSO溶解甲臜结晶后,检测570 nm处吸光度。CC₅₀定义为使细胞活力降低50%的Baloxavir浓度 [2] |
| 动物实验 |
为了评估巴洛沙韦酯在体内感染H7N9病毒后的疗效,研究人员以5和50 mg/kg的剂量,每天两次,连续五天,对小鼠进行口服巴洛沙韦酯治疗。结果表明,巴洛沙韦酯能够完全保护小鼠免受低致病性禽源H7N9人源分离株A/Anhui/1/2013的致死性攻击感染。高致病性病毒A/Guangdong/17SF003/2016由于PB2-482R、PB2-588V和PA-497R突变,在哺乳动物体内具有增强的聚合酶活性,其致病性高于A/Anhui/1/2013,因为它能够引起小鼠、雪貂和猕猴的全身性感染;这种更高的致病性可能会影响巴洛沙韦酯的疗效。尽管A/Guangdong/17SF003/2016在人支气管上皮细胞中的生长受到抑制,但该病毒的PA基因存在A100V、R262K、V387I、N394D、I465V和K497R突变,这些突变可能影响其对巴洛沙韦酯的敏感性,与A/Anhui/1/2013相比。因此,我们在此评估了巴洛沙韦酯对这种高致病性人H7N9病毒的体外和体内疗效。[6]接下来,我们评估了巴洛沙韦酯对感染高致病性人H7N9病毒的小鼠的疗效。六周龄雌性小鼠(BALB/c,日本SLC公司)用异氟烷麻醉后,经鼻内感染10个小鼠致死剂量50(MLD50;104.3 PFU)的高致病性A/Guangdong/17SF003/2016 (H7N9)病毒株,该病毒株携带NA-294R突变(NA第294位精氨酸残基表示对NA抑制剂敏感)。每组5只感染小鼠分别口服奥司他韦磷酸酯(5或50 mg/kg,每日两次,连续5天)或巴洛沙韦酯(1.5、15或50 mg/kg,每日一次或两次,连续5天)。阴性对照组小鼠灌胃0.5%甲基纤维素溶液,因为该试剂用作溶剂。对这些小鼠的体重变化进行了14天的监测,体重下降25%或以上的小鼠被判定为死亡,并根据机构指南实施安乐死。所有动物实验均按照东京大学的《动物护理和使用条例》进行,该条例已获得东京大学医科学研究所动物实验委员会的批准(批准号:PA15-12)。注射甲基纤维素的小鼠出现体重立即下降,并在感染后8天内死亡。连续5天给予5 mg/kg磷酸奥司他韦治疗,可略微延长感染小鼠的存活时间(p = 0.009,log-rank检验),但未能保护它们免受致死性攻击感染。连续5天给予50 mg/kg磷酸奥司他韦治疗,可保护80%的小鼠免受感染,但会导致严重的体重下降。相比之下,单次注射1.5 mg/kg巴洛沙韦酯的小鼠中有60%存活了14天,而其他巴洛沙韦治疗组的所有小鼠均存活且体重无明显下降(p = 0.0016,log-rank检验)。这些结果表明,单次注射15 mg/kg巴洛沙韦酯足以保护小鼠免受高致病性人H7N9病毒感染[6]。
小鼠流感感染模型: - 将雄性ICR小鼠(20-25 g,6-8周龄)随机分为4组(每组n=10):载体对照组和巴洛沙韦组(0.1、0.3、1 mg/kg)。巴洛沙韦溶于含0.5%甲基纤维素和0.1%吐温80的蒸馏水溶液中。小鼠用异氟烷麻醉后,经鼻内感染甲型流感病毒(H1N1 pdm09)(100 μL,100× LD₅₀)。感染后24小时开始,每天灌胃一次巴洛沙韦,连续3天(对照组灌胃相同体积的溶剂)。连续14天监测小鼠的体重和存活情况。感染后第4天,每组处死3只小鼠,取出肺组织,通过噬斑试验测定病毒滴度[1][3]。 - 雪貂流感感染和传播模型:- 实验前,雌性雪貂(1-1.5 kg,6-8月龄)适应环境1周。雪貂用氯胺酮/赛拉嗪麻醉后,经鼻内感染甲型流感病毒(H1N1 pdm09)(1 mL,10⁶ PFU)。巴洛沙韦溶于0.5%甲基纤维素/0.1%吐温80溶液中,于感染后第1天以1 mg/kg的剂量口服给药(对照组给予溶剂)。连续7天每日收集鼻腔冲洗液,通过噬斑试验测定病毒滴度。记录体温和临床症状(鼻腔分泌物、打喷嚏)。在传播实验中,将感染的雪貂(分别用巴洛沙韦或溶剂处理)与未感染的雪貂(1:1比例)共同饲养7天;检测未感染雪貂的鼻腔冲洗液中的病毒,以确定传播率[6] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
在12岁及以上青少年和成人中口服40 mg巴洛沙韦酯后,AUC为5520 ng·hr/mL,Cmax为68.9 ng/mL。服用80 mg后,AUC为6930 ng·hr/mL,Cmax为82.5 ng/mL。Tmax约为4小时。食物使Cmax降低48%,AUC0-inf降低36%。在5至12岁、体重小于20 kg的儿童患者中,服用2 mg/kg剂量后,AUCinf为5830 ng·hr/mL,Cmax为148 ng/mL。在体重≥20 kg的儿科患者中,服用40 mg剂量后,AUCinf为4360 ng·hr/mL,Cmax为81.1 ng/mL。Tmax范围为3.5至4.5小时。 巴洛沙韦主要通过胆汁排泄。约80.1%的总剂量经粪便排出。约14.7%的剂量经尿液排出,其中3.3%的回收剂量为原药。 分布容积为1180 L。 巴洛沙韦的清除率为10.3 L/h。 代谢/代谢物巴洛沙韦主要通过UGT1A3介导的代谢生成葡萄糖醛酸结合物。随后经 CYP3A4 代谢生成亚砜。 生物半衰期 巴洛沙韦的表观末端消除半衰期为 79.1 小时。 口服生物利用度:在小鼠中,口服巴洛沙韦 (1 mg/kg) 的口服生物利用度约为 70% [5] - 小鼠血浆药代动力学:口服巴洛沙韦 (1 mg/kg) 后,最大血浆浓度 (Cmax) 为 1.2 μM,血浆浓度-时间曲线下面积 (AUC₀₋₂₄h) 为 8.5 μM·h;消除半衰期 (t₁/₂) 约为 6 小时 [5] - 组织分布:在口服巴洛沙韦 (1 mg/kg) 的小鼠中,给药后 2 小时,肺部和鼻黏膜(流感病毒感染靶部位)的药物浓度分别为 2.5 μM 和 3.1 μM,均高于血浆浓度 (1.2 μM) [1][3] - 代谢:在人肝微粒体中,巴洛沙韦的代谢极少;孵育 2 小时后,母体药物转化为代谢物的不到 10%,表明其对肝细胞色素 P450 酶的依赖性较低 [4] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在临床试验中,几乎没有证据表明巴洛沙韦会导致肝损伤,无论是血清酶升高还是临床上明显的肝病。部分急性甲型流感患者在急性期可能出现轻微的血清酶升高,但这与治疗无关,且似乎不会因巴洛沙韦而加重。 可能性评分:E(不太可能是临床上明显的肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于哺乳期使用巴洛沙韦酯的信息。由于巴洛沙韦与血浆蛋白的结合率为93%,因此其在乳汁中的含量可能很低。如果母亲需要服用巴洛沙韦,这并非停止母乳喂养的理由,但可能更倾向于选择其他药物,尤其是在哺乳新生儿或早产儿时。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 急性毒性:在小鼠中,口服剂量高达 200 mg/kg 的巴洛沙韦,14 天内未引起死亡或明显的临床症状(例如,嗜睡、体重减轻)[5]。 - 亚急性毒性:在大鼠中,口服巴洛沙韦(10、30、100 mg/kg/天)28 天,未观察到体重、食物消耗量或血清生化指标(ALT、AST、与对照组相比,BUN(血尿素氮)、肌酐)[5] - 血浆蛋白结合率:在人血浆中,巴洛沙韦的血浆蛋白结合率约为90%[4] - 药物相互作用:在小鼠中,巴洛沙韦与奥司他韦(另一种抗流感药物)联合用药,未影响两种药物的血浆浓度,也未观察到协同或拮抗毒性[6] |
| 参考文献 | |
| 其他信息 |
巴洛沙韦正在临床试验 NCT04327791(巴洛沙韦和奥司他韦联合疗法治疗住院流感患者(COMBO 试验 1))中进行研究。
巴洛沙韦是一种聚合酶酸性核酸内切酶抑制剂。巴洛沙韦的作用机制是作为聚合酶酸性内切酶抑制剂和螯合剂。 巴洛沙韦是流感病毒帽依赖性内切酶的抑制剂,用于治疗甲型和乙型流感。巴洛沙韦单次给药,未发现与血清酶升高或临床上明显的肝损伤相关。 另见:巴洛沙韦酯(活性成分)。 巴洛沙韦酸 (BXA) 由前药巴洛沙韦酯 (BXM) 衍生而来,可强效且选择性地抑制甲型和乙型流感病毒聚合酶 PA 亚基内的帽依赖性内切酶。临床试验表明,单次服用 BXM 可显著降低病毒滴度并缓解流感症状。本文旨在阐明临床研究治疗后监测中检测到的变异病毒对BXA敏感性和复制能力的影响。我们发现PA I38T突变是降低病毒对BXA敏感性的主要途径,A型和B型病毒的EC50值分别降低了30至50倍和7倍。携带I38T突变的病毒在细胞内复制能力显著受损,体外内切酶活性也相应降低。野生型和I38T突变型甲型和乙型流感内切酶与BXA结合的共晶体结构显示,该突变降低了与抑制剂的范德华接触。BXA结合的内切酶稳定性降低也支持了I38T突变体亲和力降低的观点。这些机制方面的见解为未来对接受治疗人群的监测提供了标志物。[1] 帽依赖性核酸内切酶 (CEN) 位于流感病毒的 PA 亚基中,介导病毒 RNA 转录的关键“帽捕获”步骤,被认为是一种很有前景的抗流感靶点。本文描述了一种新型 CEN 抑制剂——巴洛沙韦酸 (BXA) 的体外特性,BXA 是巴洛沙韦酯 (BXM) 的活性形式。酶活性测定表明,BXA 通过选择性抑制 CEN 活性来抑制病毒 RNA 转录;细胞病变效应测定表明,BXA 可在不产生细胞毒性的情况下抑制感染细胞中的病毒复制。此外,在季节性甲型和乙型流感病毒(包括神经氨酸酶抑制剂耐药毒株)的减毒实验中也证实了 BXA 的抗病毒活性。此外,BXA 对多种甲型流感病毒亚型(H1N2、H5N1、H5N2、H5N6、H7N9 和 H9N2)均表现出广泛的抗菌活性。此外,在 BXA 存在下对病毒进行连续传代培养,可分离出对 BXA 敏感性降低的 PA/I38T 变异株。反向遗传学的表型和基因型分析表明,BXA 的作用机制是通过抑制感染细胞中的 CEN 酶。这些结果揭示了 BXA 的体外特性,并支持 BXM 用于治疗流感的临床应用。[2] 巴洛沙韦酯(Xofluza™;巴洛沙韦)是一种口服的帽依赖性核酸内切酶抑制剂,由罗氏和盐野义制药联合开发。该药物通过抑制 mRNA 合成的起始来阻断流感病毒的增殖。 2018年2月,巴洛沙韦在日本获得全球首个批准,用于治疗甲型或乙型流感病毒感染。目前,该药物已在美国、欧盟和其他国家开展III期临床试验。本文总结了巴洛沙韦研发历程中的重要里程碑,最终促成了其首次获得全球批准用于治疗甲型或乙型流感病毒感染。[4] 巴洛沙韦(Xofluza;BXA;S033447)是一种新型的帽依赖性核酸内切酶抑制剂,靶向流感病毒RNA聚合酶的PA亚基,用于治疗甲型和乙型流感病毒感染。[4][5] - 作用机制:巴洛沙韦抑制流感病毒的PA核酸内切酶活性,该酶对病毒mRNA的合成至关重要(该酶切割宿主mRNA的5'端帽结构,启动病毒mRNA的合成)。通过阻断这一步骤,巴洛沙韦可抑制病毒转录和复制[2][6] - 临床意义:巴洛沙韦半衰期长,在呼吸道组织中组织穿透性高,可单次口服给药。它对奥司他韦耐药的流感病毒株有效,有助于应对流感药物耐药性挑战[4][6] - 监管状态:截至2018年,巴洛沙韦已在包括美国和日本在内的多个国家获批用于治疗成人和儿童(≥12岁)的非复杂性甲型和乙型流感病毒感染[4] |
| 分子式 |
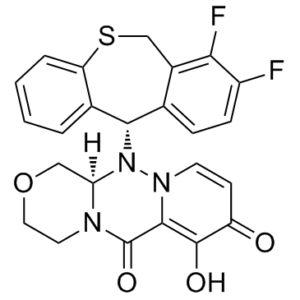
C₂₄H₁₉F₂N₃O₄S
|
|---|---|
| 分子量 |
483.49
|
| 精确质量 |
483.106
|
| 元素分析 |
C, 59.62; H, 3.96; F, 7.86; N, 8.69; O, 13.24; S, 6.63
|
| CAS号 |
1985605-59-1
|
| 相关CAS号 |
Baloxavir marboxil;1985606-14-1;Baloxavir-d5;Baloxavir-d4;2415027-80-2
|
| PubChem CID |
124081876
|
| 外观&性状 |
White to yellow solid powder
|
| 密度 |
1.6±0.1 g/cm3
|
| 沸点 |
644.7±65.0 °C at 760 mmHg
|
| 闪点 |
343.7±34.3 °C
|
| 蒸汽压 |
0.0±2.0 mmHg at 25°C
|
| 折射率 |
1.757
|
| LogP |
1.51
|
| tPSA |
98.6Ų
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
9
|
| 可旋转键数目(RBC) |
1
|
| 重原子数目 |
34
|
| 分子复杂度/Complexity |
932
|
| 定义原子立体中心数目 |
2
|
| SMILES |
S1CC2C(=C(C=CC=2[C@@H](C2C=CC=CC1=2)N1[C@@H]2COCCN2C(C2=C(C(C=CN12)=O)O)=O)F)F
|
| InChi Key |
FIDLLEYNNRGVFR-CTNGQTDRSA-N
|
| InChi Code |
InChI=1S/C24H19F2N3O4S/c25-16-6-5-13-15(20(16)26)12-34-18-4-2-1-3-14(18)21(13)29-19-11-33-10-9-27(19)24(32)22-23(31)17(30)7-8-28(22)29/h1-8,19,21,31H,9-12H2/t19-,21+/m1/s1
|
| 化学名 |
({(12aR)-12-[(11S)-7,8-difluoro-6,11-dihydrodibenzo[b,e]thiepin-11-yl]-6,8-dioxo-3,4,6,8,12,12ahexahydro-1H-[1,4]oxazino[3,4-c]pyrido[2,1-f][1,2,4]triazin-7-yl}oxy)
|
| 别名 |
Trade name Xofluza; Baloxavir acid; BXA; Baloxavir acid; 4G86Y4JT3F; S-033447; UNII-4G86Y4JT3F; (3R)-2-[(11S)-7,8-difluoro-6,11-dihydrobenzo[c][1]benzothiepin-11-yl]-11-hydroxy-5-oxa-1,2,8-triazatricyclo[8.4.0.03,8]tetradeca-10,13-diene-9,12-dione; Baloxavir (USAN); Baloxavir marboxil; S-033447; S 033447; S033447; Baloxavir;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : 25~41.67 mg/mL ( 51.7~86.19 mM )
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.30 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (4.30 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 View More
配方 3 中的溶解度: 10% DMSO+40% PEG300+5% Tween-80+45% Saline : ≥ 2.08 mg/mL (4.30 mM) 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0683 mL | 10.3415 mL | 20.6830 mL | |
| 5 mM | 0.4137 mL | 2.0683 mL | 4.1366 mL | |
| 10 mM | 0.2068 mL | 1.0341 mL | 2.0683 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05012189 | Active, not recruiting | Drug: Oseltamivir Drug: Baloxavir |
Influenza Influenza, Human | Insight Therapeutics, LLC | August 6, 2021 | Phase 4 |
| NCT06094010 | Recruiting | Drug: Baloxavir Marboxil | Influenza | Hoffmann-La Roche | November 22, 2023 | Phase 3 |
| NCT03969212 | Recruiting | Drug: Baloxavir Marboxil Drug: Placebo |
Influenza | Hoffmann-La Roche | October 10, 2019 | Phase 3 |
| NCT04327791 | Recruiting | Drug: Baloxavir Drug: Placebos |
Influenza | Bassett Healthcare | April 3, 2020 | Phase 2 Phase 3 |
 In vitroendonuclease activity and inhibition of PA variants and thermal stabilization induced by the binding of BXA.Sci Rep.2018 Jun 25;8(1):9633. |
|---|
 BXA binding to influenza A/H1N1 PA endonuclease. BXA interacts with (A) PA-A WT and (B) PA-A I38T by chelating the two manganese ions in the active site.Sci Rep.2018 Jun 25;8(1):9633. |
 Comparison of PA endonuclease from Flu A and Flu B bound to BXA in either WT or I38T form. Superposition of PA-BXA complexes: (A) PA-A WT and PA-A I38T, (B) PA-B WT and PA-B I38T, (C) PA-A WT and PA-B WT, (D) PA-A I38T and PA-B I38T.Sci Rep.2018 Jun 25;8(1):9633. |
 Local interactions of residue 38 in apo- and BXA-bound FluB PA (A) Superposition of ligand-free PA-B WT (PDB:5FML, in hotpink) and bound to BXA (green sticks for BXA, teal sticks/cartoon for PA). (B) Superposition of ligand-free (forest green) and BXA-bound PA-B I38T (light magenta sticks for BXA, orange sticks/cartoon for PA).Sci Rep.2018 Jun 25;8(1):9633. |
 Replicative capacity of variant viruses with indicated AA substitutions in PA protein. Canine MDCK cells (A–C) or human RPMI2650 cells (D,E) were infected with WT or I38x viruses based on rgA/WSN/33 (H1N1) (A,D), rgA/Victoria/3/75 (H3N2) (B,E), or B/Maryland/1/5 |