| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| 5g |
|
||
| 10g |
|
||
| Other Sizes |
|
| 靶点 |
mFAAH (IC50 = 1.8 μM); rFAAH (IC50 = 1.4 μM); hFAAH (IC50 = 2.4 μM)
Fatty acid amide hydrolase (FAAH) (Ki = 3.7 μM; IC50 = 4.2 μM) [1] - Cyclooxygenase-1 (COX-1) (IC50 > 100 μM) [1] - Cyclooxygenase-2 (COX-2) (IC50 > 100 μM) [1] - Monoamine oxidase A (MAO-A) (IC50 > 100 μM) [1] - Monoamine oxidase B (MAO-B) (IC50 > 100 μM) [1] |
|---|---|
| 体外研究 (In Vitro) |
Biochanin A对FAAH-2活性的影响[1]
FAAH-2是第二种N-酰基乙醇胺水解酶,与FAAH具有约20%的序列同一性,存在于灵长类动物中,但不存在于大鼠或小鼠中(Wei等人,2006)。以16nM[3H]油酰乙醇胺为底物,研究了Biochanin A对FAAH-2活性的影响。还对FAAH转染的膜进行了比较测试(图3)。正如预期的那样,FAAH被Biochanin A抑制,pI50值为6.21±0.02,对应的IC50值为0.62µM。在这些实验中,细胞本身(即模拟转染子)对总活性的贡献非常低。然而,FAAH-2转染细胞的膜的催化活性也很低。因此,在所需的较高蛋白质浓度下(与FAAH的情况相比),模拟转染的细胞膜中[3H]OEA发生了显著水解。这种基础水解对生物蛋白A敏感,因此可能代表了细胞天然FAAH的低水平。模拟转染和FAAH转染的细胞之间的差异,用作FAAH-2活性的估计,不受Biochanin A抑制。因此,该化合物对FAAH和FAAH-2具有选择性。 Biochanin A、大豆苷元、芒柄花素和染料木素与CB受体的相互作用[1] 图5显示了四种异黄酮抑制CB受体激动剂配体[3H]CP 55940与脑CB1受体和重组CB2受体结合的能力。尽管这些化合物可以显著降低[3H]CP 55940与两种受体的特异性结合,但这些影响是适度的。因此,发现脑CB1受体和重组CB2受体的最大抑制率分别为27±7%和33±5%,这两种情况下都用30µM的生物铜蛋白A产生。 Biochanin A抑制小鼠、大鼠和人 FAAH 对 0.5 μM AEA 的水解,IC50 值分别为 1.8、1.4 和 2.4 μM。 Biochanin A 抑制 FAAH,pIC50 为 6.21±0.02,IC50 为 0.62 μM。 Biochanin A 在高纳摩尔至低微摩尔浓度下抑制 URB597 敏感的氚保留。使用人 FAAH 和 0.5 μM [3H]AEA 进行实验,测定条件提高了利用率。 Biochanin A、Genistein、芒柄花素和大豆苷元在低微摩尔范围内抑制活性,IC50 值分别为 6.0、8.4、12 和 30 μM [1]。 Biochanin A 对FAAH表现出强效且选择性的抑制活性,Ki值为3.7 μM,IC50值为4.2 μM。在浓度高达100 μM时,它对COX-1、COX-2、MAO-A或MAO-B无显著抑制作用[1] - 在C6胶质瘤细胞中,用Biochanin A(10 μM)处理30分钟后,细胞内花生四烯酸乙醇胺(AEA)水平较对照组显著升高2.3倍,证实其在细胞环境中能抑制FAAH介导的AEA水解[1] - Biochanin A 对FAAH的抑制作用具有可逆性,将化合物从酶反应体系中洗脱后,FAAH活性可恢复至接近对照组水平[1] |
| 体内研究 (In Vivo) |
单独或与AEA联合静脉注射Biochanin A的行为影响[1]
这些化合物要么与不同剂量的AEA一起服用。正如预期的那样,AEA对四分体测试的所有四个组成部分(运动、伤害感受、体温和环不动)都产生了剂量依赖性影响。Biochanin A(15 mg·kg-1静脉注射)本身没有影响,但显著增强了AEA(10 mg·kg−1静脉注射)的影响(图7)。经Biochanin A处理的动物大脑中的AEA水平不受影响(图8)。未测量其他N-酰基乙醇胺的水平。还测试了大豆苷元(10 mg·kg−1 i.p.)。然而,在这种情况下,单独使用AEA的行为反应水平更高,没有明显的增强作用,尽管AEA+大豆苷元的组合产生的结果与Biochanin A+AEA的结果相似(数据未显示)。实验在不同的场合进行(按时间顺序,大豆苷元是第一个,这种化合物的结果导致选择了不同的给药途径)。 静脉注射URB597和Biochanin A对福尔马林诱导的脊髓ERK磷酸化的影响[1] 将福尔马林静脉注射到戊巴比妥麻醉小鼠的后爪中,在L4-S1腰脊髓同侧产生了ERK的快速磷酸化,但注射对侧没有(图6A-C),这与清醒动物的数据一致(Karim等人,2001)。通过静脉注射100µg选择性FAAH抑制剂URB597,而不是30或10µg,可以减少这种磷酸化。同时服用CB1受体拮抗剂/反向激动剂AM251(30µg)可显著抑制100µg URB597的作用。 在30、100和300µg的剂量下测试了Biochanin A。最高剂量也以AM251拮抗的方式降低了福尔马林诱导的ERK磷酸化(图6E)。因此,对爪子局部给药后,biocanin A的行为类似于URB597。 Biochanin A 的测试剂量为 30、100 和 300 μg。 AM251 抑制的方式是,最大剂量也降低了福尔马林诱导的 ERK 磷酸化。因此,局部涂抹于爪子后,Biochanin A表现出与 URB597 类似的行为。 URB597(30 μg i.pl.)和 Biochanin A(100 μg i.pl.)均可防止细胞外信号调节激酶的脊髓磷酸化,该激酶是通过将福尔马林注射到麻醉下的小鼠足底区域而产生的。 AM251,30 μg i.pl。 CB1 受体拮抗剂/反向激动剂,大大减轻了两种物质的作用。虽然Biochanin A (15 mg/k iv) 不会提高大脑 AEA 浓度,但它确实略微改善了 10 mg/kg iv AEA 的四分体测试效果。虽然 AEA (10 mg/kg iv) 本身影响不大,但Biochanin A (15 mg/kg iv) 大大增强了其效果 [1]。 在ICR小鼠中,口服给予Biochanin A(10、30、100 mg/kg)在甩尾实验中产生剂量依赖性镇痛作用。100 mg/kg剂量下,甩尾潜伏期较溶媒对照组显著延长42%,作用在给药后1小时达到峰值[1] - Biochanin A(30、100 mg/kg,口服)显著抑制角叉菜胶诱导的小鼠足肿胀,在角叉菜胶注射后3小时,抑制率分别为28%和45%[1] - 小鼠口服Biochanin A(100 mg/kg)后,脑内AEA水平较溶媒处理组升高1.8倍,脊髓内AEA水平升高1.6倍,与其实验室FAAH抑制活性一致[1] - 用CB1受体拮抗剂利莫那班(3 mg/kg,腹腔注射)预处理后,Biochanin A(100 mg/kg,口服)的镇痛作用被拮抗,表明该镇痛活性通过内源性大麻素系统介导[1] |
| 酶活实验 |
FAAH活性测量[1]
对于FAAH的实验,使用了大鼠肝匀浆、小鼠脑匀浆和转染有人酶的COS7细胞的膜。将成年C57BL/6小鼠的冷冻(-80°C)肝脏和成年Wistar或Sprague-Dawley大鼠的冷冻大脑(减去小脑)在20 mM HEPES、1 mM MgCl2、pH 7中解冻并均质化。匀浆在4°C下以35000×g的速度离心20分钟。在缓冲液中重新悬浮后,进行再离心和第二次缓冲液中再悬浮,将颗粒在37°C下孵育15分钟。进行孵育是为了水解所有内源性FAAH底物。然后如上所述离心匀浆,重新离心并重新悬浮在pH 7.4的50 mM Tris-HCl缓冲液中,该缓冲液含有1 mM EDTA和3 mM MgCl2。然后将匀浆在-80°C下等分冷冻,直至用于分析。采用Boldrup等人(2004)的方法,使用分子乙醇胺部分标记的0.5µM[3H]AEA(除非另有说明)在匀浆和COS7细胞膜中测定FAAH。空白值是通过使用缓冲液而不是匀浆获得的。在比较生物素A对FAAH和FAAH-2的影响的实验中,使用了相同的测定方法,但使用16 nM[3H]油酰乙醇酰胺([3H]OEA)作为底物,并在室温下进行孵育阶段。FAAH-2选择OEA而非AEA是出于相对水解速率的考虑:FAAH-2代谢OEA的速度是AEA的四倍,而FAAH的OEA水解速率约为AEA的三分之一(Wei等人,2006)。当使用0.5µM[3H]AEA作为底物时,选择大鼠脑和小鼠肝脏的测定条件,使添加的底物代谢率<10%。对于人类FAAH样本,在所有情况下,<5%的[3H]AEA被代谢。对于16 nM[3H]OEA,昂贵配体的有限供应意味着无法进行优化,并且使用的底物量更高(FAAH及其相应的模拟转染分别为34±1%和0.5±0.1%;FAAH-2及其相应的模型转染分别为40±2和21±0.4)。然而,当我们用人FAAH和0.5µM[3H]AEA进行实验,并在具有这些较高利用率的测定条件下进行时,在低微摩尔范围内,活性仍然受到生物素A、染料木素、芒柄花素和大豆苷元的抑制(IC50值分别为6.0、8.4、12和30µM;数据未显示)。 福尔马林诱导细胞外信号调节激酶(ERK)磷酸化 该方法基于Karim等人(2001)的方法。雄性成年C57BL/6小鼠(体重约22g)通过腹腔注射0.075mL av 100mg·mL-1戊巴比妥进行麻醉。麻醉后,将受试化合物(URB597,生物素A±AM251)或赋形剂(生理盐水中的3%吐温-80)注射到右后爪中(注射体积20µL)。之所以选择这种载体,是因为它已被其他研究i.pl.URB597在疼痛模型中的作用的人使用(Jhaveri等人,2006;Sagar等人,2008),从而可以比较有效剂量。10分钟后,将福尔马林(10µL 3%溶液溶于生理盐水)注射到动物的同一只爪子中。福尔马林注射后五分钟(除非另有说明),用温盐水(37°C,0.9%NaCl)经心灌注小鼠,然后用300 mL冰冷的4%多聚甲醛溶液灌注。使用5分钟的时间,因为此时pERK对福尔马林的反应已经完全发展(见结果)。解剖脊髓并将其放入含有冰冷的4%多聚甲醛溶液的Falcon管中。在4°C下4小时后,将样品转移到含有30%蔗糖的0.1 M磷酸盐缓冲液的Falcon管中,并保持在4°℃,更换冷冻保护溶液,直到脊髓样品饱和。对腰椎增大进行定位和解剖,并在对侧做一个切口,以便在显微镜下进行识别。将样品放入低温模具中,并使用OCT化合物固定在干冰上。使用冷冻滑动低温恒温器切割冠状切片(30µM),并将切片转移到含有0.1 M磷酸盐缓冲液的24孔培养板上。在室温下用磷酸盐缓冲液(两次)和PBS(一次)洗涤后,将切片在室温下与过氧化物酶抑制溶液(10%MeOH,0.3%H2O2在0.1M PBS中)孵育30分钟。在室温下用PBS洗涤三次后,加入含有0.02%(v/v,终浓度)Triton X-100(1%NGST)的0.1M PBS中的1%正常山羊血清。加入初级pERK R6多克隆抗体(1:500,在NGST中),将切片在4°C下孵育72小时,然后在室温下用1%NGST洗涤三次。将第二抗体(生物素化抗兔IgG,BA-1000,在1%NGST中以1:100稀释)与切片在室温下孵育2小时,用铝箔覆盖平板。在加入1%NGST中的ExtrAvidin过氧化物(1:1000)并在室温下孵育1小时之前,用1%NGST洗涤样品三次。在室温下用PBS洗涤两次和用磷酸盐缓冲液洗涤一次后,使用DAB试剂盒对样品进行染色。将切片放在载玻片上,脱水,干燥过夜,在显微镜下观察。一名对所讨论动物的治疗一无所知的研究人员在显微镜下分析了每只动物的四个切片,并计算了四个切片的平均得分。 FAAH活性测定:从大鼠脑膜中纯化FAAH,反应体系包含纯化的FAAH、[3H]-AEA(底物)和不同浓度的Biochanin A。在37°C下孵育15分钟后,加入冰浴的氯仿/甲醇(2:1,体积比)终止反应。分离水相,通过液体闪烁计数法测定水解产物的放射性,计算抑制率,并通过非线性回归分析确定Ki/IC50值[1] - COX-1/COX-2活性测定:COX-1来源于绵羊精囊,COX-2为人类重组酶。反应体系包含酶、花生四烯酸(底物)和Biochanin A(0.1–100 μM),37°C孵育10分钟后,采用酶联免疫试剂盒检测前列腺素E2(PGE2)的生成量,评估抑制活性[1] - MAO-A/MAO-B活性测定:酶来源于大鼠肝线粒体,反应体系包含酶、相应底物(MAO-A底物为酪胺,MAO-B底物为β-苯乙胺)和Biochanin A(0.1–100 μM)。37°C孵育20分钟后,通过分光光度法检测脱氨基产物,判断抑制效果[1] |
| 细胞实验 |
用[3H]AEA[1]孵育悬浮细胞后,RBL2H3细胞膜中氚的URB597敏感积聚
RBL2H3细胞在含有Earl盐、15%胎牛血清和100 U·mL-1青霉素+100µg·mL-1链霉素(“培养基”)的最低必需培养基中培养。离心并重新悬浮在Eppendorf管中的培养基中(每管2×105个细胞;5×105细胞·mL−1)后,将细胞与受试化合物或URB597在37°C下预孵育10分钟。加入培养基中的[3H]AEA(测定浓度100 nM;分子花生四烯酸部分标记的底物),并将细胞再孵育10分钟(最终测定体积200µL)。孵育后,使用微量离心机(1分钟,1000×g)沉淀细胞,然后用冰冷的介质洗涤两次,通过快速过滤和用去离子水洗涤来测定细胞膜保留的氚,如Thors等人(2008)所述。URB597对氚的敏感累积被定义为测试化合物或载体对照的放射性减去用100 nM URB597处理的细胞的相应放射性。
放射性配体结合实验[1] 异黄酮与CB1和CB2受体相互作用的能力是使用小鼠脑膜作为前者的来源,以及用人CB2受体转染的CHO细胞的膜作为后者的来源来评估的。使用标准过滤测定法(详见Ross等人,1999;Thomas等人,2005),放射性配体([3H]CP 55940)的浓度为0.7 nM。在1µM未标记的CP 55940存在下测定非特异性结合。 C6胶质瘤细胞在适宜培养基中培养,以每孔5×105个细胞的密度接种到6孔板中。过夜孵育后,用Biochanin A(1、10、30 μM)或溶媒处理细胞30分钟。收集细胞后,用氯仿/甲醇(2:1,体积比)提取AEA,采用液相色谱-串联质谱法(LC-MS/MS)结合稳定同位素内标进行定量分析[1] |
| 动物实验 |
10 mg·kg-1 iv AEA。
小鼠行为学效应 染料木素 A [1] 使用 ICR 小鼠(Harlan Laboratories,印第安纳州印第安纳波利斯,美国)进行行为学测试,测量自发活动(10 分钟测试期)、直肠温度、环形不动时间(5 分钟测试期)和伤害性阈值(甩尾测试)(详情参见 Pertwee,1972;Martin 等,1991;Burston 等,2008)。AEA 和 染料木素 A 溶解于由乙醇、Emulphor-620 和生理盐水按 1:1:18 (v/v) 比例混合的溶剂中,并通过尾静脉注射给动物(注射量为 10 µL·g-1 体重)。镇痛程度以最大可能效应百分比 (%MPE) 表示,定义为 [(测试时间 – 对照时间)/(10 – 对照时间)]× 100。 脑内 AEA 水平的定量分析 [1] 上述用载体而非 AEA 处理的小鼠在注射异黄酮 1 小时后断头处死。收集脑组织并浸入液氮中以确保快速冷却。用甲醇/氯仿提取脂质后(Hardison 等,2006),采用液相色谱/质谱分析法测定 AEA 水平(Kingsley 和 Marnett,2003)。 镇痛活性测试:将雄性 ICR 小鼠(20–25 g)随机分为载体对照组和 染料木素 A 处理组(10、30、100 mg/kg)。将该化合物悬浮于 0.5% 羧甲基纤维素钠 (CMC-Na) 溶液中,并进行口服给药。使用甩尾镇痛仪 [1] 测量给药前及给药后 0.5、1、2 和 4 小时的甩尾潜伏期。 - 抗炎活性测试:将小鼠按上述分组,并在皮下注射 0.1 mL 角叉菜胶(1% 生理盐水)至右后爪前 1 小时口服给予 Biochanin A。使用体积描记器测量注射角叉菜胶前及注射后 1、2、3 和 4 小时的爪体积 [1]。 - 脑/脊髓 AEA 水平测定:小鼠分别口服给予 Biochanin A(100 mg/kg)或溶剂对照。1 小时后,处死小鼠,并解剖脑和脊髓。将组织匀浆,提取AEA,并用LC-MS/MS进行定量分析[1] - 拮抗作用研究:小鼠在口服给予Biochanin A(100 mg/kg)前30分钟,预先腹腔注射利莫那班(3 mg/kg)。在给予Biochanin A后1小时测量甩尾潜伏期[1] |
| 药代性质 (ADME/PK) |
代谢/代谢物
生物素A已知的代谢物包括染料木素。 小鼠口服生物素A(30 mg/kg)后,血浆最大浓度(Cmax)为1.2 μM,达峰时间(Tmax)为1小时。血浆半衰期(t1/2)为2.3小时[1] - 生物素A能够穿过血脑屏障,口服给药(30 mg/kg)1小时后,脑组织浓度为0.8 μM[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
生物素驱避性 鸟类 红翅黑鹂 口服 R50(驱避率 50)> 1%
生物素毒性 鸟类 红翅黑鹂 口服 LD50(半数致死量)> 100 mg/kg 小鼠口服生物素 A 剂量高达 300 mg/kg 后,未观察到急性毒性症状(例如,死亡、行为异常、体重减轻)[1] - 生物素 A 在小鼠血浆中的血浆蛋白结合率为 89% [1] |
| 参考文献 | |
| 其他信息 |
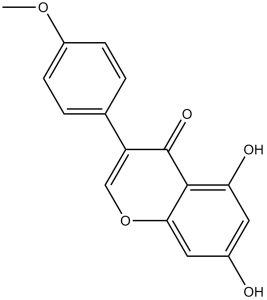
生物素A属于7-羟基异黄酮类化合物,它是在7-羟基异黄酮的5位引入一个羟基,在4'位引入一个甲氧基后形成的。它是一种植物雌激素,可能具有膳食预防癌症的功效。它具有多种功能,包括作为植物雌激素、植物代谢产物、EC 3.5.1.99(脂肪酸酰胺水解酶)抑制剂、酪氨酸激酶抑制剂和抗肿瘤药物。它既属于7-羟基异黄酮类化合物,也属于4'-甲氧基异黄酮类化合物。它是生物素A(1-)的共轭酸。
生物素A正在临床试验NCT02174666(异黄酮治疗绝经后骨质疏松症)中进行研究。 据报道,生物素A存在于黑黄檀(Dalbergia nigrescens)、台湾紫锥菊(Euchresta formosana)和其他一些有相关数据的生物体中。 植物雌激素生物素A是从红三叶草(Trifolium pratense)中分离得到的异黄酮衍生物,具有抗癌特性。单独用生物素A处理MCF-7人乳腺癌细胞,可导致CYP1A1 mRNA的积累,并以剂量依赖的方式增加CYP1A1特异性7-乙氧基试卤灵O-脱乙基酶(EROD)的活性。生物素A可能是一种天然配体,可与芳烃受体结合,并作为该通路的拮抗剂/激动剂发挥作用。(A7920)染料木素A抑制核因子κB驱动的白细胞介素-6 (IL-6) 表达。IL-6除了作为急性应激细胞因子发挥生理免疫功能外,其持续高表达还会促进慢性炎症性疾病、衰老虚弱和肿瘤发生。(A7921) 染料木素A以剂量依赖的方式降低U87MG细胞的侵袭活性。(A7922) 染料木素A激活过氧化物酶体增殖物激活受体(PPAR) PPARα和PPARγ,并促进3T3-L1前脂肪细胞的体外分化,提示异黄酮,尤其是染料木素A及其母体植物提取物,具有作为抗糖尿病药物和调节脂质代谢的潜在价值。(A7923) 背景与目的:脂肪酸酰胺水解酶 (FAAH) 是负责代谢内源性大麻素 (CB) 受体配体花生四烯酸乙醇胺 (AEA) 的酶,其抑制剂在多种动物疼痛模型中均显示出疗效。本研究旨在探讨一系列异黄酮抑制 FAAH 的能力。 实验方法:采用体外 FAAH 活性和 CB 受体亲和力测定来筛选关键化合物。体内实验包括麻醉小鼠对福尔马林的生化反应测定以及中枢 CB 受体激活的“四联体”试验。 主要结果:在所测试的化合物中,染料木素 A 被认为是最有前景的化合物。染料木素 A 可抑制小鼠、大鼠和人 FAAH 对 0.5 μM AEA 的水解,IC50 值分别为 1.8、1.4 和 2.4 μM。该化合物与 CB(1) 或 CB(2) 受体以及 FAAH-2 均无显著相互作用。在麻醉小鼠中,URB597(30 μg,足底注射)和染料木素 A(100 μg,足底注射)均能抑制足底注射福尔马林引起的脊髓细胞外信号调节激酶 (ERK) 磷酸化。CB(1) 受体拮抗剂/反向激动剂 AM251(30 μg,足底注射)显著降低了这两种化合物的作用。染料木素 A(15 mg·kg⁻¹,静脉注射)不增加脑内 AEA 浓度,但在四联体试验中,它能轻微增强 10 mg·kg⁻¹ 静脉注射 AEA 的作用。 结论和意义:结论是,染料木素 A 除了具有其他生化特性外,还能在体外和体内外周抑制 FAAH。[1] 本研究探讨了一系列与染料木素和黄豆苷元相关的异黄酮对脂肪酸酰胺水解酶 (FAAH) 的影响。在所测试的化合物中,我们选择了异黄酮化合物染料木素A进行深入研究。染料木素A是一种混合型大鼠FAAH抑制剂,对大鼠、小鼠和重组人FAAH均表现出相似的低微摩尔级抑制活性。在完整的RBL2H3细胞中,1 µM染料木素A可显著降低URB597敏感的氚标记积累(降低约75%),这与染料木素A抑制这些细胞中的FAAH活性相符。相比之下,染料木素A对[3H]CP 55940与CB1和CB2受体的结合影响较小。在福尔马林诱导的持续性疼痛模型中,对足底筋膜下注射福尔马林的行为反应(如畏缩、舔舐和啃咬爪子)相对迅速,并分为两个阶段:注射后数秒内出现的初始阶段,是由于伤害感受器受到直接刺激;短暂延迟后,出现第二阶段,这是中枢伤害感受器敏化的结果。福尔马林试验的第二阶段对FAAH抑制剂(Lichtman等人,2004a;Maione等人,2007;Sit等人,2007)以及该酶的基因敲除(Lichtman等人,2004b)均敏感。有充分证据表明,L4-S1腰椎脊髓中pERK的表达是中枢伤害性感受敏化激活的有效标志物,例如在后爪注射福尔马林后观察到的情况(综述见Gao和Ji,2009)。因此,麻醉大鼠后爪受到有害刺激(而非无害刺激)可诱导pERK表达(Ji等,1999),并且在福尔马林处理的小鼠和大鼠中,其表达模式与伤害性防御行为的第二阶段的时间进程一致(Ji等,1999;Karim等,2001)。重要的是,PD98059(一种MEK激酶抑制剂,可阻止ERK磷酸化)能够阻断两种物种的第二阶段伤害性防御行为(Ji et al., 1999; Karim et al., 2001)。在脊髓切片中,CB1受体激动剂花生四烯酸-2′-氯乙酰胺可降低辣椒素诱导的pERK表达(Kawasaki et al., 2006)。后者的发现提示,该通路可能对FAAH抑制引起的CB1受体间接激活有反应。我们发现,在所用的C57BL/6小鼠品系(Karim et al., 2001所用品系)中,URB597确实抑制了注射同侧(而非对侧)脊髓ERK的福尔马林诱导磷酸化。 URB597 的有效剂量与先前在其他疼痛模型中观察到的剂量范围相同,尽管这些模型是大鼠而非小鼠(Jhaveri 等,2006;Desroches 等,2008;Sagar 等,2008)。同时给予 AM251 可显著降低 URB597 的作用,表明 URB597 的作用至少部分是由 CB1 受体介导的。生物素 A 对脊髓 ERK 磷酸化的抑制作用与 URB597 观察到的 AM251 敏感性抑制作用模式相同,这与体内局部 FAAH 抑制作用一致。生物素A和URB597相对效力的微小差异(与体外实验中URB597在低纳摩尔浓度范围内抑制FAAH的显著差异相比;Kathuria等人,2003)可能反映了炎症组织局部pH值的降低(Häbler,1929),因为URB597以pH敏感的方式抑制完整细胞中的FAAH(Paylor等人,2006)。 虽然目前的数据表明,在麻醉的C57BL/6小鼠中,生物素A和URB597对福尔马林诱导的脊髓ERK磷酸化产生相同的影响,并且两者均可被CB1受体反向激动剂AM251拮抗,但这些数据并不能排除其他通路参与的可能性。尽管详细的分析超出了本研究的范围,但考虑到AEA能够与其他受体(例如CB2、PPARγ和TRPV1)相互作用,以及FAAH的抑制会导致其他内源性底物(例如棕榈酰乙醇胺)水平的变化,而这些底物本身也具有细胞靶点(例如PPARα)(综述见Ross,2003;O'Sullivan,2007),因此可以考虑几种潜在的通路。使用PPARγ拮抗剂GW9662的初步数据表明,该PPAR亚型在生物素A对pERK模型的影响中没有明显的贡献(L. Thors,未发表数据),但仍需进一步研究以确定这些其他通路在多大程度上参与了生物素A对甲醛诱导的ERK磷酸化的影响。 当以15 mg·kg−1的剂量静脉注射生物素A给ICR小鼠时,生物素A对脑内AEA水平没有影响,但增强了AEA在四联体测试中的行为效应。考虑到静脉注射的AEA会受到FAAH在外周和中枢的代谢,这些数据与以下假设相符:ICR小鼠的行为效应是由于外周FAAH活性降低所致。当然,与此处观察到的生物素A较为温和的作用相比,中枢通透性(尽管非选择性)的FAAH抑制剂苯甲基磺酰氟在ICR小鼠的四联体测试中产生了非常显著的AEA增强作用(Compton和Martin,1997)。关于异黄酮的药代动力学研究,染料木素A在体内转化为染料木素,随后发生结合反应(Setchell等,2001;Moon等,2006)。虽然静脉注射30 mg·kg⁻¹染料木素后可在大鼠脑内检测到染料木素(但静脉注射10 mg·kg⁻¹后则检测不到),但其脑血分布比非常低(0.04 ± 0.01)(Tsai,2005)。Yueh和Chu(1977)报道,大鼠静脉注射40 mg·kg⁻¹大豆苷元15分钟后,血浆浓度约为30 µg·mL⁻¹(相当于约120 µM)。肝脏、肺脏和肾脏中大豆苷元的浓度约为0.1 µmol·(mg湿重)−1,而脑组织中的浓度则低约五倍(Yueh和Chu,1977)。鉴于染料木素A是一种天然化合物,膳食异黄酮的摄入量显然是一个需要考虑的问题。虽然本研究的主要目的并非探讨正常摄入异黄酮对脂肪酸酰胺水解酶(FAAH)活性的影响,但考虑到膳食异黄酮在动脉粥样硬化、乳腺癌和前列腺癌方面的健康益处(尽管存在争议)(Sirtori等,2005;Messina和Wood,2008),对此的讨论是不可避免的。就染料木素和黄豆苷元而言,至少在大豆摄入量高的人群中,抑制脂肪酸酰胺水解酶(FAAH)被认为是可能的(Morton等人,2002),这是基于它们对啮齿动物酶的抑制效力(Thors等人,2007a,b)。黄豆苷元对重组人FAAH的抑制效力较低(表1),但上述推测仍然适用于染料木素。生物素A和芒柄花素不存在于大豆制品中,但存在于红三叶草提取物中,这些提取物因其据称对更年期女性有益而在保健食品商店有售(综述见Booth等人,2006)。在一项研究中,志愿者连续两周每日服用80毫克红三叶草异黄酮提取物(双倍剂量片剂),结果显示,生物素A和芒柄花素的血浆峰浓度分别为48(范围18-80)和11(范围<5-35)ng·mL⁻¹,分别相当于约170 nM和约40 nM(Howes等,2002)。染料木素和黄豆苷元的血浆峰浓度分别为114和63 ng·mL⁻¹,分别相当于约420 nM和约250 nM(Howes等,2002)。因此,与大豆摄入量高的人群不同,服用红三叶草提取物后,不太可能达到足以抑制脂肪酸酰胺水解酶(FAAH)的异黄酮浓度。总之,本研究表明,生物素A(一种天然存在但中枢渗透性有限的化合物)以混合型方式抑制FAAH,不影响FAAH-2活性,且对CB受体的影响也较弱。在体内,该化合物能够抑制外周疼痛敏化的生化相关指标——麻醉小鼠脊髓内注射福尔马林后脊髓ERK的磷酸化。FAAH抑制剂目前正作为潜在的镇痛药(和抗抑郁药)进行药物开发,其中领先的化合物已进入早期临床开发阶段(综述见Seierstad和Breitenbucher,2008)。尽管这些化合物在体内不会产生“类似大麻素”的行为,但中枢FAAH抑制的其他行为效应可能被忽视,并且有证据表明FAAH的多态性与某些特征相关,例如觅药行为(Flanagan等,2006)。在这方面,FAAH基因敲除和URB597给药均会影响乙醇偏好和摄入量(Basavarajappa等人,2006;Blednov等人,2007)。与野生型动物相比,FAAH−/−小鼠对化学诱发的癫痫发作也表现出更高的易感性(Clement等人,2003)。鉴于i.pl. AEA 和 URB597 的给药在多种疼痛模型中均产生了效果(Calignano 等,2001;Sokal 等,2003;Guindon 等,2006;Jhaveri 等,2006;Desroches 等,2008;Khasabova 等,2008;Sagar 等,2008),这表明外周限制性 FAAH 抑制剂有望成为新型镇痛剂。本文数据结合先前发表的药代动力学研究表明,染料木素 A 主要作为外周 FAAH 抑制剂发挥作用。这提示该化合物可能作为模板,用于设计更有效的外周限制性化合物。当然,异黄酮类化合物本身就具有多种生化和药理作用。这些特性包括对雌激素受体、酪氨酸激酶、过氧化物酶体增殖激活受体亚型、DNA拓扑异构酶II、NFκB激活和转化生长因子β1信号传导等的作用(综述见Kurzer和Xu,1997;Kim等人,1998;Banerjee等人,2008;另见Lam等人,2004;Shen等人,2006),因此,异黄酮离成为FAAH选择性化合物还很远。然而,筛选方案可以纳入一些筛选措施,以减少不良反应(例如对雌激素受体的影响),从而定制更具选择性的FAAH抑制剂,或设计能够作用于该酶和其他潜在有用靶点(例如环氧合酶-2)的化合物[1]。 染料木素A是一种天然存在的异黄酮,存在于红三叶草(Trifolium pratense)和鹰嘴豆(Cicer arietinum)等植物中[1]。 - 其作用机制涉及对FAAH的可逆性抑制,导致内源性大麻素(例如AEA)水平升高,从而激活CB1受体,进而发挥镇痛和抗炎作用[1]。 - 与合成抑制剂URB597(Ki = 0.5 nM)相比,染料木素A对FAAH的抑制效力较低,但对FAAH的选择性高于其他受试酶[1]。 |
| 分子式 |
C16H12O5
|
|
|---|---|---|
| 分子量 |
284.26
|
|
| 精确质量 |
284.068
|
|
| 元素分析 |
C, 67.60; H, 4.26; O, 28.14
|
|
| CAS号 |
491-80-5
|
|
| 相关CAS号 |
|
|
| PubChem CID |
5280373
|
|
| 外观&性状 |
White to light yellow solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 沸点 |
518.6±50.0 °C at 760 mmHg
|
|
| 熔点 |
210-213 °C(lit.)
|
|
| 闪点 |
198.3±23.6 °C
|
|
| 蒸汽压 |
0.0±1.4 mmHg at 25°C
|
|
| 折射率 |
1.669
|
|
| LogP |
3.14
|
|
| tPSA |
79.9
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
5
|
|
| 可旋转键数目(RBC) |
2
|
|
| 重原子数目 |
21
|
|
| 分子复杂度/Complexity |
424
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
COC1=CC=C(C=C1)C2=COC3=CC(=CC(=C3C2=O)O)O
|
|
| InChi Key |
WUADCCWRTIWANL-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C16H12O5/c1-20-11-4-2-9(3-5-11)12-8-21-14-7-10(17)6-13(18)15(14)16(12)19/h2-8,17-18H,1H3
|
|
| 化学名 |
5,7-dihydroxy-3-(4-methoxyphenyl)-4H-chromen-4-one
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (8.79 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (8.79 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.5179 mL | 17.5895 mL | 35.1791 mL | |
| 5 mM | 0.7036 mL | 3.5179 mL | 7.0358 mL | |
| 10 mM | 0.3518 mL | 1.7590 mL | 3.5179 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05013593 | Completed | Dietary Supplement: Red Clover Extract (RCE) |
Urge Incontinence Overactive Bladder |
Vendsyssel Hospital | July 15, 2019 | Not Applicable |
| NCT06209697 | Completed | Dietary Supplement: red clover | Menopause | Medipol University | March 20, 2022 | Not Applicable |
| NCT02174666 | Completed | Dietary Supplement: Red clover extract | Osteopenia Osteoporosis |
University of Aarhus | June 2014 | Not Applicable |