| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| Other Sizes |
|
| 靶点 |
CGP-42112 (≥1 nM) significantly reduces the basal value of cGMP production. From the basal value, CGP-42112 (≥1 nM) significantly inhibits TH-enzyme activity. PD123319 (an AT(2)-R antagonist) completely eliminates the inhibitory effects of CGP-42112 on TH-enzyme activity and cGMP production, whereas CV-11974 (an AT(1)-R antagonist) has no effect[1]. [1255I] CGP-42112 selectively binds to the subtype of angiotensin II receptor known as AT2. [1255I] Compared to the adrenal, the brain is where CGP-42112 binds more strongly. Although it does not change its binding in the adrenal gland, beta-Mercaptoethanol increased the binding of [1255I]CGP-42112 in the brain[2]. High affinity binding is observed for [1255I]CGP-42112 (Kd = 0.07-0.3 nM, depending on the region studied). [1255I]CGP-42112 binding is selective for AT2 receptors, as shown by the non-selective peptides Ang II and angiotensin III (Ang III) as well as competition from the AT2 ligands PD 123177, unlabeled CGP-42112, and losartan, the AT1 ligand[4].
|
|---|---|
| 体外研究 (In Vitro) |
CGP-42112 (≥1 nM) 显着抑制基础值的 cGMP 产生。 CGP-42112 (≥1 nM) 显着抑制基础值的 TH 酶活性。 CGP-42112 对 TH 酶活性和 cGMP 产生的这些抑制作用被 PD123319(AT(2)-R 拮抗剂)消除,而 CV-11974(AT(1)-R 拮抗剂)则无效[1]。 [125I]CGP-42112 选择性结合 AT2 血管紧张素 II 受体亚型。 [125I]CGP-42112 在大脑中的结合亲和力高于在肾上腺中的结合力。 β-巯基乙醇增强 [125I]CGP-42112 在大脑中的结合,但不会改变其在肾上腺中的结合[2]。 [125I]CGP-42112 以高亲和力结合(Kd = 0.07-0.3 nM,取决于研究领域)。 [125I]CGP-42112 结合对 AT2 受体具有选择性,这是通过缺乏与 AT1 配体氯沙坦的竞争以及 AT2 配体 PD 123177 和未标记的 CGP-42112 以及非选择性肽 Ang II 和血管紧张素 III 的竞争来确定的。昂三世)[4]。
在培养的猪肾上腺髓质嗜铬细胞中,CGP-42112 (浓度≥1 nM) 以浓度依赖性方式显著抑制细胞内cGMP的产生 (例如,1 nM抑制18%,100 nM抑制41%,1 μM抑制52%)。该抑制作用可被AT₂-R拮抗剂PD123319 (100 nM) 消除,但不能被AT₁-R拮抗剂CV-11974 (100 nM) 消除 [1] 。 CGP-42112 (浓度≥1 nM) 以浓度依赖性方式显著抑制酪氨酸羟化酶 (TH) 的酶活性 (例如,1 nM抑制14%,100 nM抑制35%,1 μM抑制52%)。该抑制作用可被PD123319 (100 nM) 阻断,但不能被CV-11974 (100 nM) 阻断 [1] 。 用1 mM 8-Br-cGMP (一种膜通透性cGMP类似物) 预处理细胞,可防止CGP-42112 (100 nM) 对TH酶活性的抑制作用,而用1 mM 8-Br-cAMP预处理则不能 [1] 。 CGP-42112 (浓度≥1 nM) 在孵育8小时后,以浓度依赖性方式显著降低酪氨酸羟化酶 (TH) mRNA水平 (例如,1 nM抑制18%,100 nM抑制54%,1 μM抑制65%)。该效应可被PD123319 (100 nM) 消除,但不能被CV-11974 (100 nM) 消除 [1] 。 CGP-42112 (浓度≥1 nM) 在孵育24小时后,以浓度依赖性方式显著降低酪氨酸羟化酶 (TH) 蛋白水平 (例如,1 nM抑制12%,100 nM抑制48%,1 μM抑制74%)。该效应可被PD123319 (100 nM) 消除,但不能被CV-11974 (100 nM) 消除 [1] 。 使用[¹²⁵I]-Ang II作为示踪剂的放射配体结合竞争实验表明,CGP-42112和AT₂-R拮抗剂PD123319都能强烈竞争猪肾上腺髓质细胞上的结合位点,而AT₁-R拮抗剂CV-11974竞争能力较弱,表明这些细胞中主要表达AT₂-R [1] 。 |
| 体内研究 (In Vivo) |
静脉输注 CGP-42112(0.1 和 1 mg kg-1 min-1)和 PD 123319(0.36 和 1 mg kg-1 min-1)将 CBF 自动调节的上限转向更高的血压,而不影响基线 CBF[3 ]。
|
| 酶活实验 |
酪氨酸羟化酶 (TH) 酶活性测定: 将细胞与测试物质在HEPES缓冲的Krebs缓冲液中于37°C孵育10分钟。孵育后,细胞在蔗糖溶液中匀浆。酶反应混合物包含组织匀浆、乙酸钠缓冲液 (pH 6.0)、L-酪氨酸、辅因子溶液 (6-甲基-5,6,7,8-四氢蝶呤溶于2-巯基乙醇) 和过氧化氢酶。混合物于37°C孵育30分钟,反应用含有内标的高氯酸终止。产物DOPA采用氧化铝方法进行提取。提取的DOPA随后通过高效液相色谱结合电化学检测进行分离,TH活性以每分钟每毫克蛋白质生成的DOPA量来计算 [1]
|
| 细胞实验 |
细胞培养: 从猪肾上腺髓质中制备原代分散的嗜铬细胞,并通过差异贴壁法进行纯化。将细胞铺板并在补充有胎牛血清、青霉素、链霉素和抗真菌剂的DMEM中作为单层培养物维持。培养物在5% CO₂/95% O₂的湿润气氛中于37°C下培养2-3天后用于实验 [1]
。 cGMP产生测量: 洗涤细胞,并在含有0.2 mmol/L 3-异丁基-1-甲基黄嘌呤 (IBMX) 的Eagle极限必需培养基中预孵育5分钟。然后用含有测试物质和0.2 mmol/L IBMX的HEPES缓冲Krebs缓冲液替换培养基,细胞在37°C孵育30分钟。通过添加HCl终止反应。酸提取物用于使用商业cGMP检测试剂盒测量cGMP水平 [1] 。 TH mRNA的Northern印迹分析: 从细胞中提取总RNA。RNA样品在甲醛-琼脂糖凝胶上电泳,转移至硝酸纤维素膜,并与³²P标记的人酪氨酸羟化酶 (TH) cDNA探针杂交。大鼠G3PDH cDNA用作内参。使用图像分析仪对杂交信号进行定量 [1] 。 TH蛋白的Western印迹分析: 细胞在含有SDS、Triton X-100、脱氧胆酸钠和Tris-HCl的缓冲液中溶解。蛋白质通过SDS-PAGE分离,转移至硝酸纤维素膜,并进行封闭。膜与抗酪氨酸羟化酶单克隆抗体孵育,然后与辣根过氧化物酶标记的Protein A孵育。使用增强化学发光 (ECL) 试剂检测信号,并通过光密度分析进行定量 [1] 。 受体结合研究: 将细胞与固定浓度的[¹²⁵I]-Ang II示踪剂以及递增浓度的未标记竞争剂 (CGP42112、PD123319或CV-11974) 在结合缓冲液中于20°C孵育90分钟。然后洗涤细胞,裂解,并用γ计数器测量细胞结合的放射性,以确定结合竞争情况 [1] |
| 参考文献 |
|
| 其他信息 |
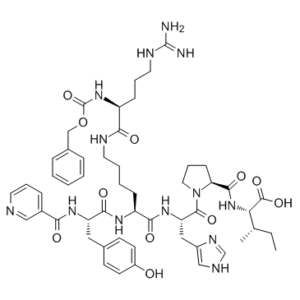
CGP-42112A 是一种六肽,由 L-酪氨酸、L-赖氨酸、L-组氨酸、L-脯氨酸和 L-异亮氨酸氨基酸残基按顺序连接而成。其中,L-酪氨酸残基的氨基被 (吡啶-3-基羰基)腈基取代,L-赖氨酸残基的侧链氨基被 {N(2)-[(苄氧基)羰基]-L-精氨酰基}腈基取代。它是一种强效的血管紧张素 II 受体 2 型 (AT2 受体) 激动剂。它具有血管紧张素受体激动剂、血管扩张剂、抗肿瘤剂、抗炎剂和神经保护剂等多种作用。它是一种寡肽、苄酯和吡啶甲酰胺。
研究表明,CGP-42112 对 AT₂ 受体的刺激可抑制肾上腺嗜铬细胞中儿茶酚胺的生物合成。其机制涉及细胞内 cGMP 水平的降低,从而导致限速酶酪氨酸羟化酶 (TH) 的活性和合成减少,无论是在酶活性还是基因/蛋白质表达水平上 [1] 。 在多个系统中,CGP-42112 被描述为完全的 AT₂ 受体激动剂 [1] 。 |
| 分子式 |
C52H69N13O11
|
|
|---|---|---|
| 分子量 |
1052.19
|
|
| 精确质量 |
1051.523
|
|
| 元素分析 |
C, 59.36; H, 6.61; N, 17.31; O, 16.73
|
|
| CAS号 |
127060-75-7
|
|
| 相关CAS号 |
|
|
| PubChem CID |
123794
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 折射率 |
1.659
|
|
| LogP |
2.38
|
|
| tPSA |
365.14
|
|
| 氢键供体(HBD)数目 |
11
|
|
| 氢键受体(HBA)数目 |
14
|
|
| 可旋转键数目(RBC) |
30
|
|
| 重原子数目 |
76
|
|
| 分子复杂度/Complexity |
1930
|
|
| 定义原子立体中心数目 |
7
|
|
| SMILES |
CC[C@H](C)[C@@H](C(O)=O)NC([C@H]1N(C([C@H](CC2=CNC=N2)NC([C@H](CCCCNC([C@H](CCCNC(N)=N)NC(OCC3=CC=CC=C3)=O)=O)NC([C@H](CC4=CC=C(C=C4)O)NC(C5=CC=CN=C5)=O)=O)=O)=O)CCC1)=O
|
|
| InChi Key |
UXGNARZDONUMMK-LRMQDCNJSA-N
|
|
| InChi Code |
InChI=1S/C52H69N13O11/c1-3-32(2)43(50(73)74)64-48(71)42-17-11-25-65(42)49(72)41(27-36-29-56-31-59-36)62-46(69)39(60-47(70)40(26-33-18-20-37(66)21-19-33)61-44(67)35-14-9-22-55-28-35)15-7-8-23-57-45(68)38(16-10-24-58-51(53)54)63-52(75)76-30-34-12-5-4-6-13-34/h4-6,9,12-14,18-22,28-29,31-32,38-43,66H,3,7-8,10-11,15-17,23-27,30H2,1-2H3,(H,56,59)(H,57,68)(H,60,70)(H,61,67)(H,62,69)(H,63,75)(H,64,71)(H,73,74)(H4,53,54,58)/t32-,38-,39-,40-,41-,42-,43-/m0/s1
|
|
| 化学名 |
(2S,3S)-2-[[(2S)-1-[(2S)-2-[[(2S)-6-[[(2S)-5-(diaminomethylideneamino)-2-(phenylmethoxycarbonylamino)pentanoyl]amino]-2-[[(2S)-3-(4-hydroxyphenyl)-2-(pyridine-3-carbonylamino)propanoyl]amino]hexanoyl]amino]-3-(1H-imidazol-5-yl)propanoyl]pyrrolidine-2-carbonyl]amino]-3-methylpentanoic acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.03.00
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (2.38 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (2.38 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: 2.5 mg/mL (2.38 mM) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.9504 mL | 4.7520 mL | 9.5040 mL | |
| 5 mM | 0.1901 mL | 0.9504 mL | 1.9008 mL | |
| 10 mM | 0.0950 mL | 0.4752 mL | 0.9504 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。