| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
G9a (IC50 = 8 nM); EHMT1/GLP/KMT1D (IC50 = 2 nM); DNMT1 (IC50 = 382 nM); DNMT3A (IC50 = 85 nM); DNMT3B (IC50 = 1200 nM)
CM-272 targets G9a (EHMT2, Histone-Lysine N-Methyltransferase) and DNMT1 (DNA Modification Methylase) ; it is a reversible dual inhibitor of G9a and DNMTs (DNMT1) [1] |
|---|---|
| 体外研究 (In Vitro) |
用 CM-272(100-1000 nM;12-72 小时;CEMO-1、MV4-11 和 OCI-Ly10 细胞系)处理以时间和剂量依赖性方式抑制细胞生长 [1]。 CM-272 处理(100-1000 nM;24 小时;CEMO-1、MV4-11 和 OCI-Ly10 细胞系)可阻断细胞周期进程[1]。在 ALL、AML 和 DLBCL 细胞系中,CM-272(100–1000 nM;12-72 小时;CEMO-1、MV4-11 和 OCI-Ly10 细胞系)治疗会导致时间和剂量依赖性细胞凋亡方式[1]。 CEMO-1 急性淋巴细胞白血病 (ALL)、MV4-11 急性髓细胞白血病 (AML) 和 OCI-Ly10 细胞系治疗 48 小时后,CM-272 弥漫性大 B 细胞淋巴瘤 (DLBCL) 细胞系表现出减少H3K9me2 和 5mC 的总体水平(GI50 值分别为 218 nM、269 nM 和 455 nM [1]。CM-272 的加工活性依赖于肿瘤细胞中 I 型干扰素反应的早期产生,这可能会导致细胞发生细胞自主免疫原性死亡[1]。
1. 抗增殖活性:CM-272 可抑制血液系统恶性肿瘤细胞系的增殖,对CEMO-1(ALL)、MV4-11(AML)、OCI-Ly10(DLBCL)细胞系的GI₅₀值(具体数值未在可用内容中明确,仅雷达图中包含pGI₅₀值);以GI₂₅、GI₅₀、GI₇₅浓度的CM-272 处理CEMO-1、MV4-11、OCI-Ly10细胞12、24、48、72小时,可剂量依赖性降低细胞增殖能力 [1] 2. 表观遗传调控:不同剂量CM-272 处理CEMO-1(ALL)细胞48小时,可降低H3K9me2(组蛋白H3赖氨酸9二甲基化)和5mC(5-甲基胞嘧啶)水平(以总H3为内参);不同剂量CM-272 处理MV4-11(AML)细胞48小时,同样降低H3K9me2和5mC水平(以总H3为内参);不同剂量CM-272 处理OCI-Ly10(DLBCL)细胞48小时,可降低H3K9me2水平(以总H3为内参) [1] 3. 细胞周期与凋亡影响:以GI₂₅、GI₅₀、GI₇₅浓度的CM-272 处理CEMO-1、MV4-11、OCI-Ly10细胞24小时,可改变细胞周期分布(展示三次实验的代表性数据);相同浓度CM-272 处理上述三种细胞12、24、48、72小时,可剂量依赖性、时间依赖性诱导细胞凋亡 [1] 4. 免疫相关效应:CM-272 处理48小时可诱导CEMO-1、MV4-11、OCI-Ly10细胞中干扰素刺激基因(ISGs)富集(经GSEA验证);qRT-PCR证实CEMO-1和MV4-11细胞经CM-272 处理48小时后ISGs表达上调;qChIP-PCR分析显示,CEMO-1细胞(250 nM CM-272)和MV4-11细胞(270 nM CM-272)经48小时处理后,ISGs的表观遗传调控发生改变;以GI₂₅、GI₅₀浓度的CM-272 处理48小时,可诱导CEMO-1、MV4-11、OCI-Ly10细胞钙网蛋白暴露(FACS检测)和HMGB1分泌(ELISA检测),提示诱导免疫原性细胞死亡 [1] 5. 酶选择性:10 μM CM-272 对37种不同家族的表观遗传酶靶点面板具有高选择性,主要作用于G9a和DNMT1 [1] |
| 体内研究 (In Vivo) |
CM-272 治疗(2.5 mg/kg;静脉注射;每天;持续 28 天;雌性 Rag2/γc/小鼠)显着扩展了 CEMO-1 细胞异种模型 [1]。
CM-272在体内具有抗白血病作用。[1] br> 将all来源的CEMO细胞(10 × 106)静脉注射于免疫缺陷的Rag2−/−γ - c−/−小鼠,每天给予2.5 mg kg−1 CM-272,注射后3天开始,持续28天。对照动物按相同方案给予生理盐水。与对照动物相比,CM-272治疗诱导小鼠的总生存期(OS)有统计学意义的增加(中位OS;92±5.7天vs 55±10.5天;P=0.0009)(图4a)。测定全肝提取物中H3K9me2和5mC的水平。通过流式细胞术(FACS)分析肝脏匀浆中的肿瘤浸润情况,发现60-80%的人细胞(hCD45+)浸润。治疗1周后,从动物身上获得的白血病细胞中,这两种标记都降低了(补充图10f)。治疗后的动物没有明显的体重减轻(补充图10g)。我们在como -1细胞的第二次体内复制中获得了类似的结果(补充图11a)。为了分析CM-272在体内的剂量依赖性功效,我们重复了同样的研究,给药1 mg kg - 1 CM-272(补充图12)。我们没有观察到动物体重的差异(补充图12a),也没有观察到1 mg kg - 1或2.5 mg kg - 1 CM-272与对照组之间的血液学参数的显著变化(补充图12b)。正如预期的那样,在2.5 mg kg - 1 CM-272处理的小鼠组中,CM-272血浆浓度更高(补充图12c)。然而,与2.5 mg kg - 1 CM-272不同,1 mg kg - 1 CM-272不能延长小鼠的存活时间(补充图12d)。这些结果表明CM-272的有效性是剂量依赖性的,2.5 mg kg - 1剂量的CM-272足以显示出积极的抗肿瘤功效。在第二种异种模型中,将10 × 106个aml来源的MV4-11细胞静脉注射Rag2 - / - γ - c - / -小鼠,14天后的动物用2.5 mg kg -1 CM-272治疗28天。与ALL细胞一样,CM-272治疗延长了小鼠的生存期(治疗组和未治疗组的中位生存期分别为78±12天和57±0.9天;P=0.0005)(图4b)。我们在MV4-11细胞的第二次体内复制中获得了类似的结果(补充图11b),没有任何毒性迹象(补充图10h)。最后,将OCI-Ly10活化的b细胞DLBCL细胞系2.5 × 106个细胞同样静脉注射到Rag2−/−γc−/−小鼠体内。与对照组相比,在8周内用相同剂量的CM-272治疗也延长了治疗小鼠的生存期(中位生存期;59±8天vs 49±6天;P=0.010)(图4c)。我们在OCI-Ly10细胞的第二次体内复制中获得了类似的结果(补充图11c),没有任何毒性迹象(补充图10i)。虽然对淋巴瘤细胞的影响在统计学上是显著的,但其效果不如AML和ALL细胞那么强。这些结果表明,CM-272通过抑制G9a/GLP和dnmt的甲基转移酶活性,在体内对不同类型的血液系统恶性肿瘤具有有效的抗肿瘤活性。除了上述信息外,与其他sam依赖的表观遗传酶相比,最小的混杂性(补充表4a和4b),进一步对癌症中其他药物靶点的脱靶选择性分析(一组97种激酶,补充表12-14)证实了G9a(和GLP)和dnmt是CM-272的主要靶点。 1. 异种移植模型中的抗肿瘤疗效:CM-272 处理可显著延长移植ALL来源CEMO-1细胞、AML来源MV4-11细胞、DLBCL来源OCI-Ly10细胞的小鼠生存期(Kaplan–Meier生存曲线显示与对照组相比有统计学差异,P值采用log-rank检验);CM-272 可降低异种移植小鼠肝脏、脾脏、骨髓中的肿瘤细胞浸润水平 [1] |
| 酶活实验 |
G9a和DNMT1酶活性测定[1]
采用时间分辨荧光能量转移法(TR-FRET)测定G9a和DNMT1活性。对于G9a,在G9a酶促反应后,将生物素化组蛋白单甲基H3K9肽与crypate标记的抗二甲基组蛋白H3K9抗体和链亲和素XL665孵育,观察TR-FRET。对于DNMT1,将Lumi4-Tb(供体)标记的s -腺苷型同型半胱氨酸特异性抗体与d2标记的s -腺苷型同型半胱氨酸(受体)一起孵育,使用EPIgeneous methyltransferase assay,观察到TR-FRET。详情请参阅补充资料。 针对G9a、DNMT1和GLP的放射性配体结合试验由Reaction Biology Corporation (http://www.reactionbiology.com)进行。 表观遗传选择性面板[1] 选择性的CM-272 和cm - 579对37表观遗传酶目标包括Bromodomain-containing酶(ATAD2A、ATAD2B BAZ2B, BRD1, BRD2(1型+ BD2), BRD4(1型+ BD2), BRDT(1型),CREBBP, TRIM24, TAF1),组蛋白甲基转移酶(EZH1, EZH2, GLP、PRMT1 PRMT3, PRMT4, PRMT5, PRMT6, PRMT8, SETD2, SET7/9, SUV39H1, SUV39H2和MLL-WARD), DNA甲基转移酶(种能阻碍DNMT3B DNMT3A和)和组蛋白demethylase (JMJD2A、JMJD2B JMJD2C, JMJD2D, JMJD2E, JMJD3, JMJD1A, LSD1, Jarid1A,Jarid1B和Jarid1C)由BPS Bioscience (http://www.bpsbioscience.com/index.ph)进行。 HDAC1和HDAC6酶活性测定[1] HDAC1和HDAC6酶的活性是用特定的荧光标记的底物来测定的,底物含有乙酰化的赖氨酸侧链,经过hdac去乙酰化。详情请参阅补充资料。 激酶选择性分析[1] 在DiscoverRx (http://www.discoverx.com/home)上使用KINOMEscan筛选平台,在10 μM的测试浓度下,对分布在kinome中的97个选定的激酶(其中90个是非突变激酶)进行CM-272 的选择性分析。 直接结合分析[1] 采用微尺度热泳术(MST)定量CM-579与DNMT1(全长)之间的生物分子相互作用。MST分析使用Monolith NT.115仪器进行。 ADME分析[1]< br > 以下ADME研究:CYP对人肝微粒体5种细胞色素p450 (1A2, 2C9, 2C19, 2D6和3A4, 10 μM)的抑制作用,血浆蛋白结合,动力学溶解度,Pampa渗透性和人和小鼠肝微粒体稳定性的研究由无锡公司(http://www.wuxi.com/)完成。 hERG阻断试验[1] 使用PredictorTM hERG荧光偏振商业检测试剂盒测定化合物对hERG钾通道的影响。 1. G9a酶活性实验:将重组G9a蛋白与SAM辅因子、组蛋白肽底物(PepMe1)及系列浓度的CM-272 共孵育;通过检测甲基化组蛋白产物评估酶活性;通过改变SAM辅因子浓度(评估与SAM结合口袋的竞争性)和组蛋白肽(PepMe1)浓度(评估与组蛋白结合槽的竞争性)开展竞争实验;采用分子对接模拟预测CM-272 与G9a组蛋白结合槽的结合模式(其7-(3-吡咯烷-1-基)丙氧基侧链与赖氨酸结合通道相互作用,且CM-272 不结合SAM结合口袋) [1] 2. DNMT1酶活性实验:将重组DNMT1蛋白与SAM辅因子、DNA底物及系列浓度的CM-272 共孵育;通过检测甲基化DNA产物评估酶活性;通过改变SAM辅因子浓度(评估与SAM结合口袋的竞争性)和DNA底物浓度(评估与DNA结合槽的竞争性)开展竞争实验;采用分子对接模拟预测CM-272 与DNMT1 DNA结合槽的结合模式(其7-(3-吡咯烷-1-基)丙氧基侧链与DNA胞嘧啶重叠,占据催化口袋并与小鼠DNMT1的催化性谷氨酸E1269相互作用,且CM-272 不结合SAM结合口袋) [1] 3. 表观遗传酶选择性实验:将10 μM CM-272 与37种不同的表观遗传酶靶点(覆盖多个家族)共孵育;采用靶点特异性底物和检测方法测定各靶点的酶活性;通过对比存在/不存在CM-272 时的相对酶活性,绘制选择性图谱 [1] |
| 细胞实验 |
细胞增殖测定[1]
细胞类型: CEMO-1、MV4-11 和 OCI-Ly10 细胞系 测试浓度: 125 nM、250 nM , 500 nM(CEMO-1 细胞); 135 nM、270 nM、540 nM(MV4-11 细胞); 100 nM、400 nM、1000 nM(OCI-Ly10 细胞) 孵育时间:12 小时、24 小时、48 小时和 72 小时 实验结果:以剂量和时间依赖性方式抑制细胞增殖。 细胞周期分析 [1] 细胞类型: CEMO-1、MV4-11 和 OCI-Ly10 细胞系 测试浓度: > 125 nM、250 nM、500 nM(CEMO-1 细胞); 135 nM、270 nM、540 nM(MV4-11 细胞); 100 nM、400 nM、1000 nM(OCI-Ly10 细胞) 孵育时间: 24 小时 实验结果: 阻断细胞周期进程。 细胞凋亡分析[1] 细胞类型: CEMO-1、MV4-11 和 OCI-Ly10 细胞系 测试浓度: 125 nM、250 nM、500 nM(CEMO-1 细胞); 135 nM、270 nM、540 nM(MV4-11 细胞); 100 nM、400 nM、1000 nM(OCI-Ly10 细胞) 孵育时间:12 小时、24 小时、48 小时和 72 小时 实验结果:以剂量和时间依赖性方式诱导 ALL、AML 和 DLBCL 细胞系凋亡。 1. 细胞增殖实验:将CEMO-1(ALL)、MV4-11(AML)、OCI-Ly10(DLBCL)细胞以适宜密度接种于96孔板;加入系列浓度的CM-272,孵育12、24、48、72小时;采用标准细胞活力实验(方法未明确)定量细胞增殖;从剂量-反应曲线计算GI₂₅、GI₅₀、GI₇₅值(n=3次重复) [1] 2. 表观遗传标志物Western blot实验:以不同剂量CM-272 处理CEMO-1、MV4-11、OCI-Ly10细胞48小时;裂解细胞,将蛋白提取物进行SDS-PAGE分离;将蛋白转移至膜上,用抗H3K9me2、5mC和总H3(内参)抗体进行孵育;采用标准化学发光方法检测免疫反应条带(n=3次重复) [1] 3. 细胞周期分析实验:以GI₂₅、GI₅₀、GI₇₅浓度的CM-272 处理CEMO-1、MV4-11、OCI-Ly10细胞24小时;收集细胞,固定后用DNA结合荧光染料(未明确)染色,通过流式细胞术分析细胞周期分布(展示三次独立实验的代表性数据) [1] 4. 凋亡实验:以GI₂₅、GI₅₀、GI₇₅浓度的CM-272 处理CEMO-1、MV4-11、OCI-Ly10细胞12、24、48、72小时;收集细胞,用凋亡检测试剂(未明确)染色,通过流式细胞术定量凋亡细胞(n=3次重复,误差线表示标准差) [1] 5. GSEA和基因表达分析实验:以CM-272 处理CEMO-1、MV4-11、OCI-Ly10细胞48小时;提取总RNA,绘制基因表达谱;采用GSEA分析ISG基因集(Schoggins等人和Sistigu等人发表)的富集情况;采用qRT-PCR验证CEMO-1和MV4-11细胞中选定ISGs的表达(引物未明确)(n=3次重复,误差线表示标准差) [1] 6. qChIP-PCR实验:以250 nM CM-272 处理CEMO-1细胞、270 nM CM-272 处理MV4-11细胞,持续48小时;将染色质交联、剪切后,用抗表观遗传标志物抗体(未明确)进行免疫沉淀;纯化DNA片段,采用针对ISG启动子的引物(未明确)进行qPCR(n=3次重复) [1] 7. 免疫原性细胞死亡实验:以GI₂₅、GI₅₀浓度的CM-272 处理CEMO-1、MV4-11、OCI-Ly10细胞48小时;采用特异性抗体通过FACS检测细胞表面钙网蛋白暴露(n=3次重复);采用ELISA定量细胞上清中HMGB1的分泌(n=3次重复,误差线表示标准差) [1] |
| 动物实验 |
动物/疾病模型:雌性BALB/Ca-Rag2−/−γc−/−小鼠(6-8周龄),接种CEMO-1细胞[1]
剂量:2.5 mg/kg 给药途径:静脉注射(iv);每日一次;持续28天 实验结果:可显著提高小鼠的总生存期(OS)。 血浆样本中CM-272和CM-579的药代动力学研究[1] 使用配备电喷雾电离(ESI)源的Xevo-TQ MS三重四极杆质谱仪和Acquity UPLC测定血浆样本中的CM-272和CM-579。将固体CM-272和CM-579溶于生理盐水中制备溶液。单次静脉注射给药,药物剂量分别为1 mg kg⁻¹或2.5 mg kg⁻¹(CM-272)或1 mg kg⁻¹(CM-579)。在注射后24小时内,于预定时间点采集血液样本(CM-272:0.25、2、4、6、8和24小时;CM-579:0.25、1、2、4和8小时)。采用Acquity UPLC BEH C18色谱柱(50 × 2.1 mm,1.7 μm粒径),以0.6 ml min⁻¹的流速进行梯度洗脱,实现色谱分离。使用WinNonlin软件,将血药浓度-时间数据拟合到非房室模型,获得药代动力学参数。详细信息见补充信息。 体内实验[1] 人急性淋巴细胞白血病(ALL)CEMO-1(生理盐水对照组,n=6;CM-272治疗组,n=6)、急性髓系白血病(AML)MV4-11(生理盐水对照组,n=8;CM-272治疗组,n=8)和弥漫性大B细胞淋巴瘤(DLBCL)OCI-Ly10(生理盐水对照组,n=6;CM-272治疗组,n=6)异种移植小鼠模型的构建方法如下:将细胞稀释于100 μl生理盐水中,经尾静脉注射至6-8周龄雌性BALB/cA−Rag2−/−γc−/−小鼠体内,具体方法见补充信息。CM-272的给药方法详见补充信息。统计结果采用统计软件medcalc进行计算。 CM-272毒性试验:血液学和肝脏参数[1] 将Rag2−/−γc−/−小鼠每日静脉注射2.5 mg kg−1的CM-272,持续4周,随后进行7天的洗脱期,并按照补充信息中所述方法测量血液学和肝脏参数。 1. 异种移植模型建立和治疗:将CEMO-1(ALL)、MV4-11(AML)或OCI-Ly10(DLBCL)肿瘤细胞(移植方法未具体说明)移植到BALB/c雌性小鼠(品系指定为近交系BALB C)体内;肿瘤移植后,将小鼠随机分为对照组和治疗组;对照组接受生理盐水(CM-272 的稀释液),治疗组接受 CM-272(剂量、给药途径和频率未指定);监测小鼠的生存时间,并绘制 Kaplan-Meier 生存曲线(采用对数秩检验计算 P 值);实验结束时,处死小鼠,并收集肝脏、脾脏和骨髓组织,以评估肿瘤细胞浸润水平 [1] |
| 药代性质 (ADME/PK) |
在进行药代动力学研究之前,研究人员确定了CM-272的最大耐受剂量(MTD),为2.5 mg kg−1(静脉注射,iv);然而,对于CM-579,我们无法给予高于1 mg kg−1(iv)的剂量。研究人员使用MTD剂量进行的药代动力学研究(补充表9-11)显示,CM-579的清除率为5.7 l h−1 kg−1,CM-272的清除率为0.91 l h−1 kg−1。
|
| 毒性/毒理 (Toxicokinetics/TK) |
在评估我们双重抑制剂的体内疗效之前,研究人员考察了这两种分子的治疗窗口及其药代动力学 (PK) 参数。因此,我们使用非肿瘤性肝细胞系 THLE-2(LC50 分别为 1.78 和 1.30 μM)以及来自健康供体的外周血单核细胞 (PBMC)(LC50 分别为 1.90 和 7.39 μM)(补充表 2)研究了 CM-272 和 CM-579 的毒性,并将其与体外抗肿瘤细胞系的活性进行了比较(补充表 3)。研究人员发现,CM-272 和 CM-579 具有可接受的治疗窗口(约 1 个对数单位)。在进行药代动力学研究之前,我们确定了CM-272的最大耐受剂量(MTD),为2.5 mg kg−1(静脉注射,iv);然而,对于CM-579,研究人员无法给予超过1 mg kg−1(iv)的剂量。我们使用MTD剂量进行的药代动力学研究(补充表9-11)显示,CM-579的清除率为5.7 l h−1 kg−1,CM-272的清除率为0.91 l h−1 kg−1。[1]接下来,研究人员检测了CM-272在Rag2−/−γc−/−小鼠中的潜在毒性。连续4周每日静脉注射2.5 mg kg−1剂量的CM-272,随后进行7天的洗脱期,结果显示小鼠体重未减轻(补充图10b),其他疾病体征也未出现异常,血液学参数也未发生显著变化(补充图10c)。此外,与对照组小鼠相比,CM-272治疗组小鼠的肝组织学检查和肝脏参数也未见异常(补充图10d,e)。综上所述,这些结果表明CM-272是一种对小鼠安全的分子。[1]
|
| 参考文献 | |
| 其他信息 |
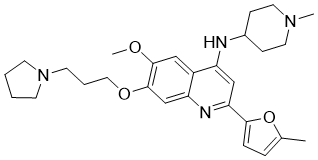
CM-272 属于氨基喹啉类化合物,其喹啉衍生物的 2、4、6 和 7 位分别被 5-甲基呋喃-2-基、(1-甲基哌啶-4-基)氨基、甲氧基和 3-(吡咯烷-1-基)丙氧基取代。它是一种具有抗肿瘤活性的双重 G9a/DNA 甲基转移酶抑制剂。它能抑制 G9a、DNMT1、DNMT3A、DNMT3B 和 GLP(IC50 值分别为 8 nM、382 nM、85 nM、1200 nM 和 2 nM)。它具有诱导细胞凋亡、诱导铁死亡、抗肿瘤、抑制EC 2.1.1.43(增强子Zeste同源物2)和抑制EC 2.1.1.37(DNA(胞嘧啶-5-)甲基转移酶)等活性。它是一种N-烷基吡咯烷类化合物,属于呋喃类、氨基喹啉类、芳香醚类、哌啶类、叔胺类、仲胺类和二醚类化合物。
表观遗传学在癌症中发挥着不可否认的作用,且表观遗传改变具有可逆性,这促进了表观遗传药物的研发。本研究设计并合成了高效、新型、选择性强且可逆的化学探针,可同时抑制G9a和DNMTs甲基转移酶的活性。体外实验表明,先导化合物CM-272可抑制血液肿瘤(急性髓系白血病-AML、急性淋巴细胞白血病-ALL和弥漫性大B细胞淋巴瘤-DLBCL)细胞增殖并促进细胞凋亡,诱导干扰素刺激基因表达和免疫原性细胞死亡。CM-272显著延长了AML、ALL和DLBCL异种移植模型的生存期。我们的研究结果首次发现了G9a/DNMTs双重抑制剂,并证实该系列化合物有望成为血液肿瘤治疗领域未满足需求的有效工具。[1] CM-272治疗后的转录组分析结果一致表明,AML、ALL和DLBCL细胞均出现肿瘤I型干扰素反应,伴有ISG表达和免疫原性细胞死亡(ICD)的诱导,提示其具有共同的抗肿瘤作用机制。尽管免疫原性细胞死亡(ICD)尚未被描述为表观遗传药物的作用机制,但这些结果或许至少部分可以预测,因为近期研究表明,干扰素刺激基因(ISG)的表达受H3K9me2的表观遗传调控(参考文献30),这支持了G9a抑制在激活I型干扰素反应和ICD中的作用。因此,我们推测,使用无法产生抗肿瘤免疫反应的免疫缺陷小鼠可能低估了CM-272对肿瘤细胞的疗效,因此需要评估免疫功能正常的模型,以探索我们化合物的全部潜在治疗效果33。基于近期研究表明I型干扰素反应有助于提高化疗药物的疗效32,CM-272与此类药物和/或免疫调节剂(例如检查点抑制剂)联合使用可能是一种有吸引力的治疗策略。 总之,CM-272是一种强效的新型首创双重可逆抑制剂,可抑制G9a (GLP)和DNMTs,它至少部分通过诱导免疫原性细胞死亡来延长血液系统恶性肿瘤体内模型的生存期。这些化合物代表了一种安全有效地靶向癌症的新方法,为治疗多种预后不良的人类肿瘤铺平了道路。[1] 1. CM-272是一种首创的可逆双重小分子抑制剂,可抑制G9a和DNMTs (DNMT1),其设计和合成旨在作为血液系统恶性肿瘤的表观遗传药物候选物。[1] 2. CM-272 与 G9a 和 DNMT1 的结合模式与 SAM 辅因子呈非竞争性结合(不与 SAM 结合口袋结合),但与组蛋白肽 (G9a) 和 DNA 底物 (DNMT1) 呈竞争性结合 [1] 3. CM-272 通过多种机制在血液系统恶性肿瘤(AML、ALL、DLBCL)中发挥抗肿瘤作用:抑制细胞增殖、诱导细胞凋亡、表观遗传调控基因表达、诱导干扰素刺激基因表达以及免疫原性细胞死亡 [1] 4. CM-272 在血液系统肿瘤的未满足医疗需求方面显示出良好的治疗潜力,这已在 AML、ALL 和 DLBCL 的异种移植模型中得到证实,其可显著延长生存期 [1] |
| 分子式 |
C28H38N4O3
|
|
|---|---|---|
| 分子量 |
478.64
|
|
| 精确质量 |
478.294
|
|
| 元素分析 |
C, 70.26; H, 8.00; N, 11.71; O, 10.03
|
|
| CAS号 |
1846570-31-7
|
|
| 相关CAS号 |
1846570-31-7;1846570-32-8 (TFA);
|
|
| PubChem CID |
118607432
|
|
| 外观&性状 |
Light brown to brown solid powder
|
|
| 密度 |
1.2±0.1 g/cm3
|
|
| 沸点 |
631.9±55.0 °C at 760 mmHg
|
|
| 闪点 |
336.0±31.5 °C
|
|
| 蒸汽压 |
0.0±1.9 mmHg at 25°C
|
|
| 折射率 |
1.601
|
|
| LogP |
5.41
|
|
| tPSA |
63
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
7
|
|
| 可旋转键数目(RBC) |
9
|
|
| 重原子数目 |
35
|
|
| 分子复杂度/Complexity |
640
|
|
| 定义原子立体中心数目 |
0
|
|
| InChi Key |
RLQLKZTYUYIWDB-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C28H38N4O3/c1-20-7-8-26(35-20)25-18-23(29-21-9-14-31(2)15-10-21)22-17-27(33-3)28(19-24(22)30-25)34-16-6-13-32-11-4-5-12-32/h7-8,17-19,21H,4-6,9-16H2,1-3H3,(H,29,30)
|
|
| 化学名 |
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.35 mM) (饱和度未知) in 10% DMSO + 40% PEG300 +5% Tween-80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80+,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0893 mL | 10.4463 mL | 20.8925 mL | |
| 5 mM | 0.4179 mL | 2.0893 mL | 4.1785 mL | |
| 10 mM | 0.2089 mL | 1.0446 mL | 2.0893 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Small molecules with a dual inhibitory activity against G9a and DNMT.Nat Commun.2017 May 26;8:15424. |
|---|
CM-272inhibits cell proliferation and induces apoptosis.Nat Commun.2017 May 26;8:15424. |
CM-272induces type I IFN response and immunogenic cell death.Nat Commun.2017 May 26;8:15424. |
CM-272shows anti-leukaemic effectsin vivo.Nat Commun.2017 May 26;8:15424. |
|---|