| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 500mg |
|
||
| 1g |
|
||
| 5g |
|
||
| 10g |
|
||
| 25g |
|
||
| Other Sizes |
|
| 靶点 |
Fungal cytochrome P450 51 (CYP51, 14α-demethylase, key enzyme in ergosterol synthesis):
- Inhibition of Candida albicans CYP51: MIC (Minimum Inhibitory Concentration) ≈ 0.125–0.5 μg/mL [1]; - Inhibition of Trichophyton rubrum CYP51: MIC ≈ 0.06–0.25 μg/mL [1]; - Inhibition of Microsporum canis CYP51: MIC ≈ 0.25–1 μg/mL [3] |
|---|---|
| 体外研究 (In Vitro) |
益康唑硝酸盐是细胞系 V79、XEM2 和 XEMd-MZ(表达 CYP1A2)中窄剂量范围内微核的有效诱导剂。 MTT法和集落形成实验表明,硝酸益康唑对MCF-7细胞增殖的抑制作用呈时间和剂量依赖性。硝酸益康唑导致 MCF-7 细胞凋亡的典型特征,包括形态变化和 DNA 片段化。硝酸益康唑导致 procaspase-3、procaspase-9 和 bcl-2 的表达减少。益康唑抑制表达重组人 TRPM2 (hTRPM2) 的 HEK-293 细胞中的 ADP-核糖激活电流。益康唑对 TRPM2 介导的电流产生基本上完全的抑制。 Econodium (25-50 mM) 部分抑制由另一种内质网 Ca2+ 泵抑制剂 cyclopiazonic Acid 诱导的电容性 Ca2+ 进入。益康唑通过两种不同的途径诱导 Ca2+ 流入:一种对 La3+ 敏感,另一种则不敏感。益康唑以剂量和时间依赖性方式可逆抑制 MA-10 细胞中 (Bu)(2)cAMP 刺激的孕酮产生,而不影响总蛋白合成或 P450(scc) 和 3β-羟基类固醇脱氢酶 (3β-HSD) 酶表达或活动。益康唑是一种钙池操纵的 Ca2+ 通道拮抗剂,可诱导白血病的细胞毒性细胞死亡。益康唑 (5-20 mM) 将人类结肠癌细胞阻滞在细胞周期的 G0/G1 期。益康唑诱导 COLO 205 细胞凋亡,这一点通过 DNA 片段化分析中梯子的形成和亚 G1 峰得到证实。
抗真菌活性(文献[1]、[2]、[3]): 1. 酵母类真菌(念珠菌属): - 硝酸益康唑(0.03–8 μg/mL,肉汤微量稀释法)抑制白色念珠菌(MIC₈₀≈0.125 μg/mL)、光滑念珠菌(MIC₈₀≈0.5 μg/mL)、热带念珠菌(MIC₈₀≈0.25 μg/mL)。1 μg/mL浓度下,白色念珠菌生长较对照组降低~90%[1] 2. 皮肤癣菌(丝状真菌): - 红色毛癣菌(体癣致病菌):MIC₈₀≈0.06 μg/mL(琼脂扩散法);0.5 μg/mL浓度抑制孢子萌发~95%[1]; - 须癣毛癣菌(足癣致病菌):MIC₈₀≈0.125 μg/mL [3]; - 犬小孢子菌(头癣致病菌):MIC₈₀≈0.25 μg/mL [3] 3. 其他致病真菌: - 糠秕马拉色菌(花斑癣致病菌):MIC₈₀≈0.5 μg/mL(肉汤稀释法)[2] - 真菌细胞膜破坏作用: 1. 0.5 μg/mL 硝酸益康唑处理白色念珠菌24小时:麦角固醇含量降低~70%(HPLC分析);细胞膜通透性增加~40%(荧光素二乙酸酯染色,流式细胞术)。光镜下可见细胞肿胀、形态不规则[1] |
| 体内研究 (In Vivo) |
豚鼠须癣毛癣菌感染模型(体癣模型,文献[3]):
1. 分组:豚鼠(n=6/组)随机分为3组:(1)未处理对照组;(2)基质对照组(外用乳膏基质);(3)硝酸益康唑1%外用乳膏组[3] 2. 给药方案:背部脱毛后,接种1×10⁶ CFU/mL须癣毛癣菌孢子悬液。接种24小时后开始外用给药,每日1次,持续14天(感染区域涂抹0.1 g/cm²乳膏)[3] 3. 疗效: - 皮损评分(红斑、脱屑、瘙痒):给药14天时,药物组较基质对照组降低~80%; - 真菌清除:药物处理组100%动物皮肤刮取物真菌培养阴性(沙氏琼脂培养),对照组均为阳性[3] - 小鼠白色念珠菌皮肤感染模型: 1. 给药方案:感染背部皮肤外用硝酸益康唑0.5%溶液,每次0.05 mL/cm²,每日1次,持续7天[1] 2. 疗效:7天时皮肤真菌载量(CFU/g组织)较基质对照组降低~99%;病理切片未见残留真菌菌丝[1] |
| 酶活实验 |
真菌CYP51活性抑制实验:
1. 蛋白制备:酿酒酵母中表达重组白色念珠菌CYP51,镍螯合层析纯化,重悬于实验缓冲液(50 mM Tris-HCl,pH7.4,1 mM EDTA,0.1 mM DTT)[1] 2. 反应体系:200 μL混合物含纯化CYP51(0.5 μg)、底物羊毛固醇(10 μM)、NADPH(1 mM)及硝酸益康唑(0.01–10 μg/mL),溶剂(DMSO)作为对照[1] 3. 孵育与检测:37℃孵育60分钟,加入50 μL甲醇终止反应。HPLC(280 nm紫外检测)定量产物(14α-去甲基羊毛固醇)。抑制率=(1–药物组产物量/对照组产物量)×100%[1] 4. 数据分析:四参数逻辑斯蒂拟合计算CYP51抑制IC₅₀≈0.08 μg/mL[1] |
| 细胞实验 |
真菌肉汤微量稀释药敏实验(文献[1]、[2]):
1. 真菌制备:白色念珠菌/红色毛癣菌在沙氏葡萄糖肉汤(SDB)中培养至对数期,调整浓度为1×10⁴ CFU/mL(酵母)或1×10³ CFU/mL(皮肤癣菌)[1][2] 2. 药物处理:96孔板中对硝酸益康唑进行梯度稀释(0.03–8 μg/mL),与真菌悬液等体积混合。35℃孵育48小时(酵母)或72小时(皮肤癣菌)[1][2] 3. 生长检测:酵母生长通过600 nm吸光度测定;皮肤癣菌生长通过肉眼观察。MIC₈₀定义为抑制80%生长的最低浓度[1][2] - 真菌细胞膜通透性实验: 1. 细胞处理:白色念珠菌(1×10⁶个细胞/mL)用硝酸益康唑(0.125–2 μg/mL)处理24小时[1] 2. 染色:加入荧光素二乙酸酯(FDA,5 μg/mL)37℃染色30分钟。FDA可进入完整细胞并转化为荧光素,细胞膜损伤会降低荧光强度[1] 3. 分析:流式细胞术测定荧光强度,通透性增加率=(1–药物组荧光强度/对照组荧光强度)×100%[1] |
| 动物实验 |
豚鼠须癣毛癣菌感染方案:
1. 动物饲养:雌性豚鼠(250–300 g)饲养于标准设施中(22–24°C,12 小时光照/黑暗循环),自由摄食饮水[3] 2. 感染诱导:用脱毛膏去除背部皮肤(2×2 cm 区域)的毛发。接种 100 μL 浓度为 1×10⁶ CFU/mL 的须癣毛癣菌孢子悬液(溶于 0.9% 生理盐水),用无菌纱布覆盖 24 小时以保持湿润[3] 3. 分组和治疗:接种 24 小时后,将动物随机分为 3 组。使用 1% 硝酸益康唑乳膏(油包水基质),每日一次局部涂抹(0.1 g/cm²),持续 14 天。赋形剂组仅使用乳膏基质;未治疗组不进行任何干预[3] 4. 监测和分析:每3天记录一次皮损评分(0-4分制:0=正常,4=严重红斑/脱屑)。第14天,收集皮肤刮片,接种于沙氏琼脂培养基(35℃,7天)进行真菌培养。将皮肤组织固定于10%福尔马林溶液中进行组织病理学检查(PAS染色以检测真菌菌丝)[3] |
| 药代性质 (ADME/PK) |
局部皮肤吸收(文献[3]、[4]):
1. 人体皮肤吸收:健康志愿者(n=5)在前臂涂抹1%硝酸益康唑乳膏(10 cm²面积,0.1 g/cm²)。涂抹后24小时: - 角质层浓度:~5–10 μg/g; - 真皮层浓度:~0.1–0.3 μg/g; - 血浆浓度:<0.01 μg/mL(HPLC检测不到)[4] 2. 豚鼠皮肤吸收:与人体相似;局部涂抹1%乳膏24小时后,血浆浓度<0.005 μg/mL [3] - 口服药代动力学: 1. 口服生物利用度:<5%(大鼠,10 mg/kg口服剂量与静脉注射剂量比较);大部分药物在胃肠道内不被吸收[1] 2. 半衰期:局部用药:局部皮肤半衰期约为 8–12 小时(豚鼠)[3];口服:终末半衰期约为 2.5 小时(大鼠)[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
体外毒性:
1. 人角质形成细胞(HaCaT 细胞):硝酸益康唑(0.1–20 μg/mL,24 小时处理)未显示明显的细胞毒性;10 μg/mL 时细胞活力 >90%(MTT 法)[4] 2. 人成纤维细胞:20 μg/mL 硝酸益康唑 使细胞活力降低 <10%(LDH 释放试验)[4] - 体内毒性(文献 [3]、[4]): 1. 急性口服毒性: - 小鼠单次口服 LD₅₀ ≈ 1600 mg/kg; - 大鼠单次口服 LD₅₀ ≈ 2000 mg/kg; - 过量症状:短暂性腹泻和嗜睡,48 小时内缓解 [3] 2. 局部皮肤毒性: - 豚鼠封闭式斑贴试验(1% 乳膏,24 小时):无红斑或水肿;原发性刺激指数 (PII) <0.5(归类为“无刺激性”)[4]; - 兔眼刺激试验:无角膜混浊或结膜充血(1% 溶液,单次滴眼)[3] - 血浆蛋白结合率:~95%(人血浆,37°C 平衡透析)[1] |
| 参考文献 | |
| 其他信息 |
硝酸益康唑是一种白色结晶性粉末。(NTP, 1992)
硝酸益康唑是一种咪唑衍生物,具有抑菌作用,是一种广谱抗真菌剂。硝酸益康唑抑制麦角甾醇的生物合成,从而破坏真菌细胞壁膜并改变其通透性,导致细胞内必需成分的丢失。此外,硝酸益康唑抑制甘油三酯和磷脂的生物合成,并抑制氧化酶和过氧化酶的活性,这可能导致细胞坏死和细胞死亡。硝酸益康唑对某些革兰氏阳性菌也有效。这种抗真菌剂用于治疗各种皮肤真菌病。 一种常用的局部抗真菌剂。 另见:益康唑(含有活性成分);硝酸益康唑;烟酰胺(成分)……查看更多…… 背景:硝酸益康唑是一种咪唑类抗真菌药物,用于局部治疗浅表真菌感染。它靶向真菌CYP51,CYP51是麦角甾醇(真菌细胞膜必需成分)合成的关键酶[1][3] -作用机制:抑制真菌CYP51,阻断羊毛甾醇(麦角甾醇的前体)的14α-去甲基化。这会导致真菌细胞膜中麦角甾醇减少,有毒的甲基化甾醇积累,破坏细胞膜的结构/功能,最终导致真菌细胞死亡[1][3] - 治疗适应症:局部治疗皮肤癣菌病(体癣、股癣、足癣、头癣)、念珠菌病(皮肤念珠菌病、外阴阴道念珠菌病、包皮念珠菌病)和花斑癣[4] - FDA 状态:已获准作为局部抗真菌药物(例如,Spectazole® 1% 乳膏)用于人体;适用于浅表真菌感染[4] - 注意事项:避免接触眼睛和黏膜;如果出现过敏反应(皮疹、瘙痒),请停止使用;不可全身使用[4] |
| 分子式 |
C18H15CL3N2O.HNO3
|
|---|---|
| 分子量 |
444.7
|
| 精确质量 |
443.02
|
| 元素分析 |
C, 48.62; H, 3.63; Cl, 23.92; N, 9.45; O, 14.39
|
| CAS号 |
24169-02-6
|
| 相关CAS号 |
Econazole;27220-47-9
|
| PubChem CID |
68589
|
| 外观&性状 |
White to off-white solid powder.
|
| 熔点 |
162°C
|
| LogP |
5.976
|
| tPSA |
93.1
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
28
|
| 分子复杂度/Complexity |
404
|
| 定义原子立体中心数目 |
0
|
| SMILES |
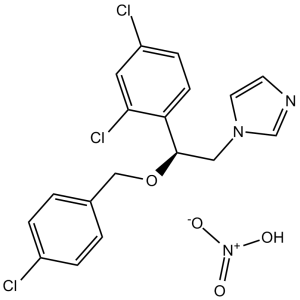
ClC1C([H])=C(C([H])=C([H])C=1C([H])(C([H])([H])N1C([H])=NC([H])=C1[H])OC([H])([H])C1C([H])=C([H])C(=C([H])C=1[H])Cl)Cl.O([H])[N+](=O)[O-]
|
| InChi Key |
DDXORDQKGIZAME-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C18H15Cl3N2O.HNO3/c19-14-3-1-13(2-4-14)11-24-18(10-23-8-7-22-12-23)16-6-5-15(20)9-17(16)21;2-1(3)4/h1-9,12,18H,10-11H2;(H,2,3,4)
|
| 化学名 |
1-[2-[(4-chlorophenyl)methoxy]-2-(2,4-dichlorophenyl)ethyl]imidazole;nitric acid
|
| 别名 |
Econazole Nitrate; R 14,827; R 14827; Spectazole; SQ 13050; SQ13050; SQ-13050; Ecoza; epi-Pevaryl; Gyno-pevaryl; Ifenec.
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : 50~89 mg/mL ( 112.44~200.13 mM )
H2O : 0.67 mg/mL (1.51 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.62 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.62 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (5.62 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 10% DMSO+40% PEG300+5% Tween-80+45% Saline: ≥ 2.5 mg/mL (5.62 mM) 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2487 mL | 11.2435 mL | 22.4871 mL | |
| 5 mM | 0.4497 mL | 2.2487 mL | 4.4974 mL | |
| 10 mM | 0.2249 mL | 1.1244 mL | 2.2487 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT01358240 | Completed | Drug: Econazole Nitrate Foam 1% Drug: Vehicle Foam |
Tinea Pedis Athlete's Foot |
AmDerma | June 2011 | Phase 3 |
| NCT01353976 | Completed Has Results | Drug: Econazole Nitrate Foam 1% Other: Vehicle Foam |
Tinea Pedis Athlete's Foot |
AmDerma | May 2011 | Phase 3 |
| NCT01696799 | Completed | Drug: Econazole Nitrate Drug: placebo |
Interdigital Tinea Pedis | AmDerma | September 2011 | Phase 2 |
| NCT03129321 | Completed Has Results | Drug: Econazole Nitrate Cream, 1% Drug: Placebo |
Tinea Pedis | Mylan Inc. | March 15, 2016 | Phase 3 |
|
|---|
|