| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Cyclooctadepsipeptide; anthelmintic
The semisynthetic derivative emodepside of PF1022A has a para-positional morpholine attached to each of the two D-phenyllactic acids. Emodepside works well against a range of nematodes that invade the gastrointestinal tract. In nematodes, emodepside binds to a presynaptic latrophilin receptor[1]. Emodepside causes a slow, concentration-dependent, time-dependent (20 min) hyperpolarization and increase in voltage-activated K currents. It is also sensitive to 4-aminopyridine.Emodepside inhibits the process of spiking. The ryanodine spike frequency increase between 20 and 35 minutes is significantly inhibited by emodepside, with a reduction of 9.8 spikes/min[2]. When emodepside is present, significantly elevated currents are detected without depolarization up to a 0 mV threshold and without the need for extra stimuli to fictitiously raise [Ca 2+]i levels. These new discoveries verify that emodepside directly targets Slo-1[3]. |
|---|---|
| 体外研究 (In Vitro) |
PF1022A 的半合成衍生物艾默德苷在两个 D-苯基乳酸上分别连接有一个对位吗啉。 Emodepside 对一系列侵入胃肠道的线虫有很好的作用。在线虫中,艾莫德苷与突触前卵白蛋白受体结合[1]。 Emodepside 会引起缓慢的、浓度依赖性、时间依赖性(20 分钟)超极化,并增加电压激活的 K 电流。它对 4-氨基吡啶也敏感。Emodepside 抑制加标过程。兰尼定尖峰频率在 20 至 35 分钟之间的增加受到艾默德赛的显着抑制,减少了 9.8 个尖峰/分钟[2]。当 emodepside 存在时,检测到显着升高的电流,而无需去极化高达 0 mV 阈值,并且不需要额外的刺激来虚构地提高 [Ca 2+]i 水平。这些新发现证实 emodepside 直接靶向 Slo-1[3]。
Emodepside (1 µM 和 10 µM) 可引起猪蛔虫肌肉膜电位缓慢起效、浓度依赖性的超极化,1 µM 作用 10 分钟平均超极化幅度为 -5.2 mV,10 µM 作用更强。该效应可被钾通道阻断剂 4-氨基吡啶抑制。[2] Emodepside (1 µM) 以时间依赖性方式增加电压激活的钾电流,对晚期钾电流的增强在 0 mV 时最为明显。给药 10、20、30 分钟后,电流分别增至对照组的约 130%、146% 和 167%。洗脱后效应仍持续增强。[2] 在较高浓度下 (10 µM),emodepside 使钾通道激活的电压依赖性曲线左移约 -2.9 mV,表明通道对电压的敏感性增加,但最大电导未变。[2] Emodepside 对钾电流的效应依赖于细胞外钙,因为在无钙溶液中其效应显著减弱。[2] 一氧化氮供体硝普钠和 PKC 激活剂佛波酯可增强 emodepside 的效应。相反,NOS 抑制剂 N-硝基-L-精氨酸和广谱激酶抑制剂星形孢菌素可抑制其效应。[2] Emodepside (1 µM) 可抑制兰尼碱诱导的肌肉锋电位发放,使锋电位频率的增加减少 9.8 次/分钟。此抑制作用的起效速度慢于神经肽 PF1。[2] Emodepside 激活的钾电流可被大电导钙激活钾通道选择性阻断剂 Iberiotoxin 部分抑制。[2] Emodepside (1 µM) 对猪蛔虫肌肉的电压激活钙电流无显著影响。[2] |
| 体内研究 (In Vivo) |
艾莫德赛抑制三个重要的生理过程:进食、繁殖和运动。它通过干扰咽部神经肌肉接头、体壁肌肉和产卵肌肉的信号传导来实现这一点[4]。
本研究提及伊码菌素在体内具有广谱杀线虫活性,包括在小鼠模型中对鼠鞭虫的效力。 [3] 据报道,与对喉瘤盘尾丝虫等其他丝虫物种的活性相反,伊码菌素在体内和体外对马来丝虫和彭亨丝虫的疗效较差。 [3] |
| 酶活实验 |
环十八肽类的研究始于20世纪90年代初。PF1022A是emodepside的起始原料,是日本山茶属植物Mycelia steria真菌的天然次生代谢产物。PF1022A由四种N-甲基-L-亮氨酸、两种D-乳酸和两种D-苯基乳酸组成,它们形成了一种具有交替L-D-L-构型的环状十八肽。Emodepside是PF1022A的半合成衍生物,其中吗啉连接在两种D-苯基乳酸的对位。Emodepside对多种胃肠道线虫有效。大黄素与线虫的突触前latrophilin受体结合。以下突触前信号转导是通过Gqalpha蛋白和磷脂酶Cβ的激活发生的,这导致二酰基甘油(DAG)的动员。然后,DAG激活UNC-13和突触结合蛋白,这两种蛋白质在突触前囊泡功能中起着重要作用。这最终导致了一个目前身份不明的发射器的释放。发射器(或调制器)在突触后膜上发挥作用,并诱导线虫咽部和躯体肌肉组织的弛缓性麻痹[1]
环十八肽emodepside及其母体化合物PF1022A是广谱杀线虫药物,能够消除对其他驱虫剂有抗药性的线虫。环十八肽的作用方式仅部分了解,但涉及latrophilin Lat-1受体和电压和钙激活的钾通道Slo-1。遗传证据表明,emodepside主要通过Slo-1发挥其驱虫活性。事实上,slo-1缺陷型秀丽隐杆线虫菌株完全对emodepside耐药。然而,emodepside对Slo-1的直接作用尚未有报道,这些通道仅对秀丽隐杆线虫和相关的Strongylida进行了表征。分子和生物信息学分析鉴定了猪蛔虫、雌马寄生虫、犬弓首线虫、短尾丝虫、马来丝虫、点滴红尾蛇和鼠强线虫的全长Slo-1 cDNA。在鼠鞭毛虫、猪鞭毛虫和旋毛虫中发现了两个副目。在鞭虫属中鉴定出几个编码截短通道的剪接变体。毛头类的Slo-1通道形成一个单系群,表明在Enoquase和Chromadorea分化后发生了重复。为了探索代表性蛋白质的功能,秀丽隐杆线虫Slo-1a在非洲爪蟾卵母细胞中表达,并在电生理(电压钳)实验中进行了研究。在没有实验性增加的细胞内Ca2+的情况下,用1-10µM emodepside孵育卵母细胞会在宽范围的阶跃电位上显著增加电流,这表明emodepside直接打开秀丽隐杆线虫Slo-1a。Emodepside洗除并不能逆转效果,Slo-1抑制剂疣原仅在Emodepside之前使用时有效,而在emodepide之后无效。在一些寄生线虫中鉴定出几种剪接变体和同源物表明,物种之间的通道特性存在很大差异。最重要的是,这项研究首次表明emodepside直接打开Slo-1通道,显著提高了对这类药物作用方式的理解[3]。 采用 RT-PCR 检测猪蛔虫肌肉瓣中 slo-1 和 lat-1 基因的表达。提取总 RNA,经 DNase 处理后,使用 oligo(dT) 引物和逆转录酶进行逆转录。使用根据 Asu-slo-1 和 Asu-lat-1 cDNA 序列设计的基因特异性引物进行巢式 PCR。扩增产物经克隆和测序以确认其身份,为这些基因在肌肉组织中的表达提供了证据。[2] |
| 细胞实验 |
采用RT-PCR技术研究slo-1和lat-1在A.suum肌瓣中的表达,并采用两种微量移液器电流钳和电压钳技术记录emodepside的电生理效应。
主要结果:检测到slo-1和lat-1的表达。Emodepside产生缓慢的时间依赖性(20分钟)、4-氨基吡啶敏感的浓度依赖性超极化和电压激活K电流的增加。硝普钠增加了超极化和K电流。N-硝基-L-精氨酸抑制超极化和K电流。佛波醇-12-肉豆蔻酸酯-13乙酸酯增加了K电流,而星孢菌素抑制了超极化和K电流。伊维菌素减少了这些emodepside K电流。emodepside在无钙溶液中的作用减弱。Emodepside对电压激活的钙电流没有影响。
结论和意义:Asus-lo-1和Asus-lat-1在成人A.suum肌瓣中表达,emodepside缓慢激活电压激活的钙依赖性slo-1样K通道。emodepside的作用通过刺激蛋白激酶C和NO通路而增强。这些数据与一个模型一致,在该模型中,NO、PKC和emodepside信号通路是分开的,并会聚在K通道上,或者emodepside激活NO和PKC信号通路以增加K通道的开放[2]。
从成年猪蛔虫前部制备体壁肌肉瓣。沿侧线切开约 1 cm 长的虫段,去除肠道,将肌肉瓣固定在涂有 Sylgard 的培养皿中。制备好的样本在 34°C 下用低钾猪蛔虫围食膜液灌流。[2] 采用双微电极电压钳和电流钳技术记录肌肉袋细胞。微电极内充灌 3 M 醋酸钾。电压钳记录时,将细胞钳制在 -35 mV,并阶跃至不同测试电位以激活钾电流或钙电流。电流经漏减后进行分析。[2] 电流钳模式下,监测膜电位和输入电导。药物(包括 emodepside)通过灌流施加。通常,调节剂(如 SNP、PMA、NNLA、星形孢菌素)先灌流 10 分钟,然后与 emodepside 共同灌流 10 分钟。在不同时间点测量效应,并在无药液中冲洗 20 分钟后评估洗脱效应。[2] |
| 动物实验 |
环辛肽类化合物依莫地平是一种广谱驱虫药,此前研究表明其能麻痹模式线虫秀丽隐杆线虫的体壁肌和咽肌。我们通过两项独立的运动行为实验证明,野生型秀丽隐杆线虫L4期幼虫对依莫地平的敏感性低于成虫:琼脂平板上的体弯试验(成虫IC50为3.7 nM,L4期幼虫IC50为13.4 nM)和液体中的摆动行为试验(10 μM依莫地平处理1小时后,成虫摆动行为占对照组的百分比为16%,L4期幼虫为48%)。我们还发现,从卵开始,野生型秀丽隐杆线虫在整个生命周期中持续暴露于依莫地平会减缓其发育,且这种效应与依莫地平的浓度呈正相关。在含有依莫地平的琼脂平板上,虫卵孵化率与对照组无显著差异,表明该药物影响的是孵化后的发育,而非孵化本身。依莫地平还能抑制野生型秀丽隐杆线虫的产卵,500 nM 的急性药物暴露可在 1 小时内几乎完全抑制产卵。然而,产卵速率并未受到抑制,因此经依莫地平处理的线虫体内充满虫卵,最终破裂。这表明依莫地平对繁殖的影响并非由于抑制产卵,而是由于其对产卵肌肉的麻痹作用。这些结果结合之前的研究表明,依莫地普西会干扰体壁肌肉(Willson等,2003)、咽部(Willson等,2004)和产卵肌肉的神经肌肉接头处的信号传导,从而抑制三种重要的生理功能:运动、摄食和繁殖[4]。
每周从猪肉加工厂收集猪蛔虫成虫。它们被保存在32℃的洛克氏溶液(155 mM NaCl、5 mM KCl、2 mM CaCl₂、1.5 mM NaHCO₃、5 mM葡萄糖)中。溶液每天更换两次,蛔虫在收集后4天内用于实验。[2] |
| 参考文献 | |
| 其他信息 |
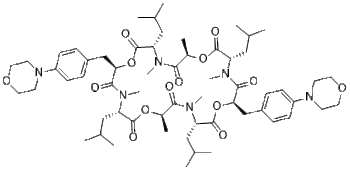
依莫地平是一种环辛肽,由D-乳酰基、N-甲基-L-亮氨酰、3-[4-(4-吗啉基)苯基]-D-乳酰基、N-甲基-L-亮氨酰、D-乳酰基、N-甲基-L-亮氨酰、3-[4-(4-吗啉基)苯基]-D-乳酰基和N-甲基-L-亮氨酰残基按顺序连接而成,形成一个24元大环。它是一种驱虫药,常与吡喹酮联合用于治疗和控制猫的钩虫、蛔虫和绦虫感染。它具有抗线虫药的作用。它是一种半合成衍生物,属于环辛肽类药物。
依莫德普西是一种驱虫药,对多种胃肠道线虫有效,已获准用于猫,属于辛肽类药物,这是一类相对较新的驱虫药。 另见:依莫德普西;吡喹酮(成分)。 依莫德普西是一种环辛肽类驱虫药,是PF1022A的半合成类似物。它对其他主要驱虫药(如苯并咪唑类、左旋咪唑和伊维菌素)耐药的寄生线虫有效。 [2] 依莫德普西的作用机制涉及缓慢激活SLO-1样钾离子通道,从而导致膜超极化和肌肉松弛/抑制。这种作用受NO和PKC信号通路调节,可能通过与latrophilin样受体相互作用而启动。[2] 该研究得出结论,数据与以下模型相符:依莫德普西、NO和PKC信号通路汇聚于钾离子通道,或者依莫德普西激活NO和PKC通路以增加通道开放。[2] |
| 分子式 |
C60H90N6O14
|
|---|---|
| 分子量 |
1119.3884
|
| 精确质量 |
1118.65
|
| 元素分析 |
C, 64.38; H, 8.10; N, 7.51; O, 20.01
|
| CAS号 |
155030-63-0
|
| 相关CAS号 |
1610546-58-1 (with toltrazuril);155030-63-0;
|
| PubChem CID |
6918632
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
5.219
|
| tPSA |
211.38
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
16
|
| 可旋转键数目(RBC) |
14
|
| 重原子数目 |
80
|
| 分子复杂度/Complexity |
1900
|
| 定义原子立体中心数目 |
8
|
| SMILES |
O1C([C@]([H])(C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H])N(C([H])([H])[H])C([C@@]([H])(C([H])([H])[H])OC([C@]([H])(C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H])N(C([H])([H])[H])C([C@@]([H])(C([H])([H])C2C([H])=C([H])C(=C([H])C=2[H])N2C([H])([H])C([H])([H])OC([H])([H])C2([H])[H])OC([C@]([H])(C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H])N(C([H])([H])[H])C([C@@]([H])(C([H])([H])[H])OC([C@]([H])(C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H])N(C([H])([H])[H])C([C@@]1([H])C([H])([H])C1C([H])=C([H])C(=C([H])C=1[H])N1C([H])([H])C([H])([H])OC([H])([H])C1([H])[H])=O)=O)=O)=O)=O)=O)=O)=O
|
| InChi Key |
ZMQMTKVVAMWKNY-YSXLEBCMSA-N
|
| InChi Code |
InChI=1S/C60H90N6O14/c1-37(2)31-47-57(71)77-41(9)53(67)61(11)50(34-40(7)8)60(74)80-52(36-44-17-21-46(22-18-44)66-25-29-76-30-26-66)56(70)64(14)48(32-38(3)4)58(72)78-42(10)54(68)62(12)49(33-39(5)6)59(73)79-51(55(69)63(47)13)35-43-15-19-45(20-16-43)65-23-27-75-28-24-65/h15-22,37-42,47-52H,23-36H2,1-14H3/t41-,42-,47+,48+,49+,50+,51-,52-/m1/s1
|
| 化学名 |
(3S,6R,9S,12R,15S,18R,21S,24R)-3,9,15,21-tetraisobutyl-4,6,10,16,18,22-hexamethyl-12,24-bis(4-morpholinobenzyl)-1,7,13,19-tetraoxa-4,10,16,22-tetraazacyclotetracosan-2,5,8,11,14,17,20,23-octaone
|
| 别名 |
PF 1022-221; PF-1022 221; PF-1022-221; Emodepside; 155030-63-0; Emodepside [INN]; UNII-YZ647Y5GC9; emodepsida; emodepsidum; BAY 444400; BAY444400; BAY-444400; BAY 44-4400; BAY44-4400; BAY-44-4400;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : 100~120 mg/mL ( 89.33~107.20 mM )
Ethanol : ~20 mg/mL H2O :< 0.1 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 3 mg/mL (2.68 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 30.0 mg/mL 澄清的 DMSO 储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL 生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 3 mg/mL (2.68 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 30.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 3 mg/mL (2.68 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 10% DMSO+40% PEG300+5% Tween-80+45% Saline: 3 mg/mL (2.68 mM) 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.8933 mL | 4.4667 mL | 8.9334 mL | |
| 5 mM | 0.1787 mL | 0.8933 mL | 1.7867 mL | |
| 10 mM | 0.0893 mL | 0.4467 mL | 0.8933 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|
|
|
|
|