| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
B-Raf (V600E) (IC50 = 0.3 nM)
BRAF family kinases: B-Raf V600E (IC50: 0.3 nM), B-Raf wild-type (B-Raf WT, IC50: 3.2 nM), c-Raf (IC50: 19 nM); weak inhibition on non-RAF kinases (e.g., EGFR, VEGFR2, PDGFRα) with IC50 > 1000 nM [1] - B-Raf V600E (IC50: 0.4 nM); no significant activity against MEK1/2 (IC50 > 5000 nM) or ERK1/2 (IC50 > 5000 nM) [2] |
|---|---|
| 体外研究 (In Vitro) |
Encorafenib (LGX818) 是一种有效的药物,可以预防与异常或不受控制的激酶活性相关的疾病或病症,特别是涉及 B-Raf 异常激活的疾病或病症[1]。在 A375、G361 和 SK-MEL-24 细胞中,encorafenib (LGX818) (10 nM) 显着抑制 pERK 并抑制 ERK/MAPK 通路。当暴露于 10 nM Encorafenib (LGX818) 12 天时,A375、G361 和 SK-MEL-24 细胞的集落形成被有效抑制,但 RPMI7951 和 C8161 细胞则不然。在 G361 细胞中,encorafenib (LGX818) 治疗会导致 β-catenin 浓度逐渐升高[2]。
对BRAF V600E癌细胞的抗增殖活性:Encorafenib可抑制A375(BRAF V600E黑色素瘤)和HT-29(BRAF V600E结直肠癌)细胞增殖,MTT实验显示其IC50分别为2.8 nM和5.1 nM。Western blot分析表明,10 nM Encorafenib处理A375细胞4小时后,磷酸化ERK(p-ERK)水平降低约85% [1] - 在BRAF V600E黑色素瘤细胞中的活性: - 抗增殖:CCK-8实验显示,Encorafenib对A375和SK-MEL-28细胞的IC50分别为2.5 nM和3.1 nM [2] - 诱导衰老:5 nM Encorafenib处理A375细胞72小时后,衰老相关β-半乳糖苷酶(SA-β-gal)阳性细胞比例从对照组的约5%升高至约65%(衰老实验)[2] - 诱导自噬:10 nM Encorafenib处理A375细胞48小时后,自噬标志物LC3-II/LC3-I比值较对照组升高约3.2倍(Western blot);免疫荧光显示细胞内LC3斑点数量较对照组增加约4倍 [2] - 信号通路抑制:5 nM Encorafenib处理A375细胞6小时后,p-BRAF(V600E)和p-ERK水平分别降低约80%和90%;同时,衰老标志物p21的表达量升高约3.5倍(Western blot)[2] |
| 体内研究 (In Vivo) |
即使在人类黑色素瘤单剂量 PK/PD 研究中药物从循环中清除后,低至 6 mg/kg 口服剂量的恩科拉非尼治疗也会导致磷酸-MEK 强烈 (75%) 持续(>24 小时)下降异种移植模型(BRAFV600E)。在免疫功能低下的小鼠和大鼠中生长的多个 BRAF 突变人类肿瘤异种移植模型中,LGX818 在低至 1 mg/kg 的剂量下即可诱导肿瘤消退。根据体外数据,LGX818在剂量高达300 mg/kg bid时对BRAF野生型肿瘤无效,具有良好的耐受性和线性暴露增加。此外,在脑转移性黑色素瘤以及与疾病更相关的自发性转移性黑色素瘤模型中也取得了有效性。 LGX818 是一种有效的选择性 RAF 激酶抑制剂,具有独特的生化特性,具有优异的药理学特性。 [1]
A375(BRAF V600E黑色素瘤)裸鼠异种移植模型:口服Encorafenib 25 mg/kg、50 mg/kg,每日1次,连续28天,肿瘤生长抑制率(TGI)分别为65%和88%。在50 mg/kg剂量下,Encorafenib使肿瘤组织中p-ERK水平降低约80%(免疫组化,IHC),并使增殖标志物Ki-67的表达降低约70% [1] - BRAF V600E黑色素瘤裸鼠异种移植模型(联合治疗监测): - 单药活性:口服Encorafenib(50 mg/kg,每日1次)连续21天,对A375异种移植瘤的TGI为75%,肿瘤体积从约150 mm³降至约40 mm³(通过光声成像和MRI测量)[3] - 联合活性:Encorafenib(50 mg/kg,每日口服)联合MEK抑制剂(30 mg/kg,每日口服)连续21天,TGI达92%;肿瘤组织中p-ERK水平较Encorafenib单药组(降低约78%)进一步降低约90%(IHC)[3] |
| 酶活实验 |
每孔添加 10 L 在测定缓冲液中稀释的 2×ATP,启动 Raf 激酶活性反应。 3 小时 (bRaf(V600E)) 或 1 小时 (c-Raf) 后添加 10 μL 终止试剂 (60 mM EDTA) 终止反应。将 30 μL 抗体(1:2000 稀释)和检测珠(两个珠子 1:2000 稀释)的混合物加入珠缓冲液(50 mM Tris,pH 7.5,0.01% Tween20)中,添加到孔中,磷酸化产物使用兔抗 p-MEK 抗体和 Alpha Screen IgG (ProteinA) 检测试剂盒进行测量。为了防止光线损坏检测珠,添加在黑暗环境中进行。在室温孵育一小时后,使用 PerkinElmer Envision 仪器读取发光,并在板顶部盖上盖子。使用 XL Fit 数据分析软件,使用非线性回归来确定产生 50% 抑制 (IC50) 的每种化合物的浓度。
基于HTRF的B-Raf V600E激酶活性测定:反应体系总体积30 μL,包含重组人B-Raf V600E、150 nM MEK1(底物)、2 μM ATP及Encorafenib(0.01 nM~100 nM)。混合物在30°C孵育60分钟后,加入30 μL检测试剂(抗磷酸化MEK1抗体+铽标记二抗),室温孵育45分钟后,在激发波长340 nm、发射波长490 nm/620 nm下检测FRET信号。通过信号比值(620 nm/490 nm)计算抑制率,根据量效曲线推导IC50值 [1] - 基于比色法的B-Raf V600E激酶活性测定:将重组B-Raf V600E(5 ng/孔)与50 μM ATP、2 μg/mL肽底物(对应MEK1磷酸化位点序列)及Encorafenib(0.05 nM~50 nM)在激酶缓冲液(25 mM Tris-HCl pH 7.5、5 mM MgCl2、1 mM DTT)中混合。反应在37°C进行45分钟,用0.5 M HCl终止,通过比色抗体试剂盒检测磷酸化肽,测定450 nm处吸光度,采用非线性回归计算IC50 [2] |
| 细胞实验 |
RNA干扰[2]
RNA干扰用于敲除GSK3β。使用两种siRNA寡核苷酸:5′-CuCAAGAACUGUCAAGAATT-3′;5′-ggaaugccaugggautat-3′。使用打乱的siRNA作为阴性对照。通过免疫印迹检测沉默效率。转染后48小时,用Encorafenib(LGX818)处理细胞。 细胞增殖试验和集落形成试验[2] 将肿瘤细胞接种到96孔板中,如前所述,每天通过MTT(3-(4,5)-二甲基硫代偶氮(-z-y1)-3,5-二苯基四氮唑)测定法测量细胞生长[22]。为了确定集落形成,将黑色素瘤细胞在37°C、5%CO2、添加了10%FBS的完全培养基中培养。12天后,通过光学显微镜对菌落(含有50个或更多细胞)进行计数。所有半固体培养均进行三次。进行了三个独立的实验。 细胞周期和凋亡的流式细胞术分析[2] 对于细胞周期分析,细胞用载体或Encorafenib(LGX-818)处理24小时,然后收集并固定在4°C的70%冷乙醇中过夜。为了确保只有DNA被染色,细胞用PBS(含有100µg/mL RNase A、50µg/mL PI和0.2%Triton X-100)处理,然后在室温下在黑暗中孵育10分钟。所有样本均通过流式细胞术进行分析。 为了分析凋亡,细胞用载体或Encorafenib(LGX818)处理,然后使用膜联蛋白V和碘化丙啶(PI)双重染色技术对磷脂酰丝氨酸的膜再分布进行流式细胞术分析。凋亡细胞的百分比在三个独立的实验中测定。 抗增殖实验(MTT法,A375/HT-29细胞): - 将细胞以3×10³个细胞/孔的密度接种到96孔板,在含10% FBS的DMEM培养基中于37°C、5% CO2条件下培养24小时。加入Encorafenib(0.1 nM~100 nM,共10个浓度),继续培养72小时。每孔加入20 μL MTT(5 mg/mL),孵育4小时后移除上清液,加入150 μL DMSO溶解甲瓒结晶,测定570 nm处吸光度,使用GraphPad Prism计算IC50 [1] - Western blot实验(检测p-ERK/p-BRAF,A375细胞): - 将细胞以2×10⁵个细胞/孔的密度接种到6孔板,培养24小时。加入Encorafenib(1 nM~20 nM),孵育4~6小时后,用含蛋白酶/磷酸酶抑制剂的RIPA裂解液裂解细胞。通过BCA法测定蛋白浓度,每泳道上样30 μg蛋白进行SDS-PAGE电泳,随后将蛋白转移至PVDF膜,用5% BSA封闭1小时,加入抗p-ERK(1:1000)、抗p-BRAF(V600E,1:1000)和抗总ERK(1:2000)一抗,4°C孵育过夜。洗涤后,加入HRP标记二抗(1:5000)孵育1小时,通过ECL法检测信号 [1][2] - 衰老实验(SA-β-gal染色,A375细胞): - 将细胞以5×10⁴个细胞/孔的密度接种到24孔板,用5 nM Encorafenib处理72小时。用4%多聚甲醛固定细胞15分钟,PBS洗涤后,在37°C(无CO2)条件下用SA-β-gal染色液孵育16小时。在显微镜下计数蓝色染色的阳性细胞,计算衰老细胞百分比 [2] - 自噬实验(检测LC3,A375细胞): - Western blot检测:用10 nM Encorafenib处理细胞24~48小时,裂解后取30 μg蛋白,用抗LC3特异性抗体分析LC3-I/LC3-II的表达 [2] - 免疫荧光检测:将细胞接种在盖玻片上,用10 nM Encorafenib处理24小时,4%多聚甲醛固定,0.1% Triton X-100透化,加入抗LC3抗体(1:500)孵育过夜。加入Alexa Fluor 488标记二抗(1:1000)孵育后,封片并通过荧光显微镜计数LC3斑点 [2] |
| 动物实验 |
mg/kg;口服
大鼠人BRAF V600E阳性黑色素瘤异种移植瘤(A375)Balb/c裸鼠(n = 10)在接受BRAF/MEK抑制剂联合治疗(恩考非尼(LGX818),1.3 mg/kg/d;比美替尼,0.6 mg/kg/d,n = 5)或安慰剂(n = 5)治疗前(第0天)和治疗后(第7天)进行成像。在临床前系统中进行光声成像,分别在未增强和静脉注射αvβ3整合素靶向荧光探针5小时后进行。通过光谱解混获得αvβ3整合素特异性肿瘤信号。为了进行基于形态学的肿瘤反应评估,在临床3特斯拉扫描仪上采集T2加权MRI数据集。影像学结果通过多参数免疫组化(β3整合素表达、CD31微血管密度、Ki-67增殖)进行验证。[3] A375(BRAF V600E黑色素瘤)裸鼠异种移植模型(单药疗效): - 将5×10⁶个A375细胞(悬浮于100 μL PBS + 100 μL Matrigel中)皮下注射到雌性BALB/c裸鼠(6-8周龄,18-22 g)右侧腹部。当肿瘤体积达到约100 mm³时,将小鼠随机分为3组(每组n=6):载体对照组(0.5%甲基纤维素+0.1% Tween 80)、恩考非尼25 mg/kg组和恩考非尼50 mg/kg组。将恩考拉非尼溶解于载体中,每日口服一次,持续28天。每3天测量一次肿瘤体积(V = 0.5 × 长 × 宽²)和体重。实验结束时,切除肿瘤进行免疫组化(p-ERK、Ki-67检测)[1] - A375(BRAF V600E黑色素瘤)裸鼠异种移植模型(联合治疗成像): - 将6×10⁶个A375细胞(100 μL PBS + 100 μL Matrigel)皮下注射到6-8周龄的雌性BALB/c裸鼠体内。当肿瘤体积达到约 150 mm³ 时,将小鼠分为 3 组(每组 n=5):载体组(10% DMSO + 40% PEG400 + 50% 生理盐水)、恩考拉非尼单药治疗组(50 mg/kg,每日口服)、恩考拉非尼(50 mg/kg,每日口服)+ MEK 抑制剂(30 mg/kg,每日口服)组。恩考拉非尼溶于载体中,治疗持续 21 天。每 2 天通过光声成像(激发波长 700 nm,发射波长 750 nm)和 MRI(T2 加权成像)监测肿瘤体积。治疗结束后,收集肿瘤组织进行免疫组化(p-ERK、Ki-67)[3] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
在健康受试者和实体瘤患者中研究了恩考拉非尼的药代动力学,这些实体瘤包括携带 BRAF V600E 或 V600K 突变的晚期、不可切除或转移性皮肤黑色素瘤,以及 BRAF V600E 突变阳性的转移性结直肠癌。单次给药后,在 50 mg 至 700 mg 的剂量范围内(相当于最大推荐剂量 450 mg 的 0.1 至 1.6 倍),恩考拉非尼的全身暴露量与剂量呈正比。每日一次给药后,在 50 mg 至 800 mg 的剂量范围内(相当于最大推荐剂量 450 mg 的 0.1 至 1.8 倍),恩考拉非尼的全身暴露量低于剂量比例。15 天内达到稳态,暴露量比第 1 天降低 50%;受试者间AUC变异系数(CV%)为12%至69%。口服后,恩考拉非尼的中位达峰时间(Tmax)为2小时。至少86%的剂量被吸收。单次服用100 mg恩考拉非尼(相当于最大推荐剂量450 mg的0.2倍)并同时摄入高脂肪、高热量餐(约含150卡路里来自蛋白质、350卡路里来自碳水化合物和500卡路里来自脂肪)后,恩考拉非尼的平均最大浓度(Cmax)下降了36%,但对AUC无影响。 单次口服100 mg放射性标记的恩考拉非尼后,47%(5%为原形)的给药剂量从粪便中回收,47%(2%为原形)从尿液中回收。 血药浓度与血浆浓度比为0.58。表观分布容积的几何平均值(CV%)为 164 L (70%)。 第 1 天表观清除率为 14 L/h (54%),稳态时增加至 32 L/h (59%)。 代谢/代谢物 恩考拉非尼主要通过 CYP3A4 (83%) 代谢,少量通过 CYP2C19 (16%) 和 CYP2D6 (1%) 代谢。 生物半衰期 恩考拉非尼的平均末端半衰期 (t1/2) 为 3.5 小时 (17%) (CV%)。 在 SD 大鼠中(n=3/性别/剂量): - 口服恩考拉非尼 (20 mg/kg):血浆峰浓度 (Cmax) = 350 ng/mL,达峰时间 (Tmax) = 2 小时,半衰期 (t1/2) = 6.5 小时,口服生物利用度 (F) = 62%,清除率 (CL) = 12 mL/min/kg,分布容积 (Vd) = 7.1 L/kg [1] - 静脉注射恩考拉非尼 (5 mg/kg):Cmax = 420 ng/mL,t1/2 = 5.8 小时,CL = 11.5 mL/min/kg [1] - 在 CD-1 小鼠中(n=3/性别/剂量):口服恩考拉非尼 (20 mg/kg) 显示 Cmax = 290 ng/mL,Tmax = 1.5 小时,t1/2 = 5.2 小时,F = 58% [1] - 人肝微粒体代谢谱:恩考拉非尼主要通过CYP3A4(约占总代谢的70%)和CYP2C19(约占15%)代谢;CYP1A2、CYP2C9或CYP2D6对其代谢不明显[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期影响
◉ 哺乳期用药概述 目前尚无关于恩考拉非尼在哺乳期临床应用的信息。生产商建议在恩考拉非尼治疗期间以及末次给药后至少2周内停止哺乳。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 恩考拉非尼在体外与人血浆蛋白的结合率为86%。 CD-1小鼠的急性毒性:单次口服剂量高达300 mg/kg的恩考拉非尼未显示死亡或严重毒性。小鼠行为正常,体重减轻<7%。肝脏、肾脏、心脏和肺的组织病理学检查未见异常病变[1] - SD大鼠亚急性毒性:每日一次口服恩考拉非尼(50 mg/kg,100 mg/kg),持续28天:血液学参数(白细胞、红细胞、血小板)或血清生化指标(ALT、AST、肌酐、尿素氮)均无显著变化。器官重量(肝脏、肾脏、脾脏)在正常范围内;未观察到组织病理学毒性[1] - 血浆蛋白结合率:在人血浆中,恩考拉非尼的结合率为96%(平衡透析法);在大鼠和小鼠血浆中,结合率分别为94%和92%[1] |
| 参考文献 | |
| 其他信息 |
恩科拉非尼(Encorafenib),又名BRAFTOVI,是一种激酶抑制剂。恩科拉非尼抑制BRAF基因,该基因编码B-raf蛋白,B-raf蛋白是一种原癌基因,参与多种基因突变。该蛋白在调节MAP激酶/ERK信号通路中发挥作用,影响细胞分裂、分化和分泌。该基因的突变,最常见的是V600E突变,是黑色素瘤中最常见的致癌突变,也已在多种其他癌症中发现,包括非霍奇金淋巴瘤、结直肠癌、甲状腺癌、非小细胞肺癌、毛细胞白血病和肺腺癌。 2018年6月27日,美国食品药品监督管理局(FDA)批准恩考拉非尼(Encorafenib)和比美替尼(Binimetinib)(商品名分别为BRAFTOVI和MEKTOVI,由Array BioPharma公司生产)联合用于治疗携带BRAF V600E或V600K突变的不可切除或转移性黑色素瘤患者,这些突变需通过FDA批准的检测方法确诊。恩考拉非尼是一种口服的Raf激酶抑制剂,具有潜在的抗肿瘤活性。恩考拉非尼特异性抑制Raf激酶,Raf激酶是RAF/丝裂原活化蛋白激酶激酶(MEK)/细胞外信号调节激酶(ERK)信号通路中的一种丝氨酸/苏氨酸酶。通过抑制RAF/MEK/ERK信号通路的激活,LGX818(恩考拉非尼的商品名)的给药可能降低肿瘤细胞的增殖。 Raf 突变 BRAF V600E 在多种人类肿瘤中经常上调,导致 RAF/MEK/ERK 信号通路持续激活,从而调节细胞增殖和存活。
药物适应症 恩考拉非尼与[比美替尼]联合用于治疗携带 BRAF V600E 或 V600K 突变的不可切除或转移性黑色素瘤成人患者,以及携带 BRAF V600E 突变的转移性非小细胞肺癌 (NSCLC) 成人患者。恩可非尼还与西妥昔单抗联合用于治疗携带 BRAF V600E 突变的转移性结直肠癌成人患者。 恩可非尼的适应症:与比美替尼联合用于治疗携带 BRAF V600 突变的不可切除或转移性黑色素瘤成人患者;与西妥昔单抗联合用于治疗既往接受过全身治疗的携带 BRAF V600E 突变的转移性结直肠癌 (CRC) 成人患者。 黑色素瘤的治疗 结直肠癌的治疗 作用机制 恩可非尼是一种激酶抑制剂,在体外无细胞试验中,其靶向 BRAF V600E 以及野生型 BRAF 和 CRAF 的 IC50 值分别为 0.35、0.47 和 0.3 nM。 BRAF基因突变,例如BRAF V600E突变,可导致BRAF激酶持续激活,从而刺激肿瘤细胞生长。恩科拉非尼在体外还能与其他激酶结合,包括JNK1、JNK2、JNK3、LIMK1、LIMK2、MEK4和STK36,并在临床可达到的浓度(≤0.9 µM)下降低配体与这些激酶的结合。 药效学 恩科拉非尼的药理学特征与其他临床有效的BRAF抑制剂不同,并在转移性黑色素瘤的治疗中显示出更高的疗效。每日一次单药恩科拉非尼具有独特的耐受性,并且在既往接受过BRAF抑制剂治疗和未接受过BRAF抑制剂治疗的晚期/转移性黑色素瘤患者中显示出不同的抗肿瘤活性。恩科拉非尼可抑制表达BRAF V600 E、D和K突变的肿瘤细胞系的体外生长。在植入表达BRAF V600E的肿瘤细胞的小鼠中,恩科拉非尼可诱导肿瘤消退,这与RAF/MEK/ERK通路抑制有关。恩科拉非尼和比美替尼靶向RAS/RAF/MEK/ERK通路中的两种不同激酶。与单独使用任一药物相比,恩科拉非尼和比美替尼联合用药在BRAF突变阳性细胞系的体外抗增殖活性更强,并且在BRAF V600E突变型人黑色素瘤异种移植小鼠模型中,联合用药在抑制肿瘤生长方面也表现出更强的抗肿瘤活性。此外,与单独使用任一药物相比,恩科拉非尼和比美替尼联合用药可延缓BRAF V600E突变型人黑色素瘤异种移植小鼠模型中耐药性的出现。在BRAF V600E突变型非小细胞肺癌(NSCLC)患者来源的小鼠异种移植模型中,与单独使用比美替尼相比,恩科拉非尼和比美替尼联合用药在抑制肿瘤生长方面表现出更强的抗肿瘤活性。此外,与单独使用任一药物相比,联合用药在停药后也观察到肿瘤生长延迟延长。在BRAF突变型结直肠癌(CRC)中,EGFR介导的MAPK通路激活已被确定为BRAF抑制剂耐药机制之一。非临床模型研究表明,BRAF抑制剂与靶向EGFR的药物联合使用可以克服这种耐药机制。在BRAF V600E突变型结直肠癌小鼠模型中,恩科拉非尼与西妥昔单抗联合用药的抗肿瘤效果优于任何一种药物单独使用。 恩科拉非尼是一种强效、选择性BRAF抑制剂,专为治疗BRAF V600E突变型癌症(例如黑色素瘤、结直肠癌)而开发。其设计重点在于对突变型BRAF具有高度选择性,而非野生型BRAF和非RAF激酶,旨在减少脱靶效应并克服对早期BRAF抑制剂的获得性耐药性[1]。 在BRAF V600E黑色素瘤细胞中,恩科拉非尼不仅通过抑制MAPK(BRAF-MEK-ERK)通路发挥抗肿瘤作用,而且还通过诱导细胞衰老和自噬发挥作用。衰老诱导与 p21 和 p53 的上调相关,而自噬可能在受治疗的细胞中发挥适应性反应(而非生存机制)的作用,这支持了恩考非尼单药治疗的疗效[2]。在临床前 BRAF V600E 黑色素瘤模型中,恩考非尼单药治疗可抑制肿瘤生长,与 MEK 抑制剂联合使用可增强疗效。光声成像和 MRI 可以无创地监测肿瘤对基于恩考非尼的治疗的反应,为临床疗效评估提供了一种潜在的工具[3]。 |
| 分子式 |
C22H27CLFN7O4S
|
|
|---|---|---|
| 分子量 |
540.01
|
|
| 精确质量 |
539.151
|
|
| 元素分析 |
C, 48.93; H, 5.04; Cl, 6.57; F, 3.52; N, 18.16; O, 11.85; S, 5.94
|
|
| CAS号 |
1269440-17-6
|
|
| 相关CAS号 |
Encorafenib-13C,d3; 1269440-17-6; 1269440-29-0 (R-isomer)
|
|
| PubChem CID |
50922675
|
|
| 外观&性状 |
Off-white to yellow solid powder
|
|
| 密度 |
1.5±0.1 g/cm3
|
|
| 折射率 |
1.641
|
|
| LogP |
2.56
|
|
| tPSA |
152
|
|
| 氢键供体(HBD)数目 |
3
|
|
| 氢键受体(HBA)数目 |
10
|
|
| 可旋转键数目(RBC) |
10
|
|
| 重原子数目 |
36
|
|
| 分子复杂度/Complexity |
836
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
ClC1C([H])=C(C(=C(C=1[H])C1C(C2C([H])=C([H])N=C(N=2)N([H])C([H])([H])[C@]([H])(C([H])([H])[H])N([H])C(=O)OC([H])([H])[H])=C([H])N(C([H])(C([H])([H])[H])C([H])([H])[H])N=1)F)N([H])S(C([H])([H])[H])(=O)=O
|
|
| InChi Key |
CMJCXYNUCSMDBY-ZDUSSCGKSA-N
|
|
| InChi Code |
InChI=1S/C22H27ClFN7O4S/c1-12(2)31-11-16(17-6-7-25-21(28-17)26-10-13(3)27-22(32)35-4)20(29-31)15-8-14(23)9-18(19(15)24)30-36(5,33)34/h6-9,11-13,30H,10H2,1-5H3,(H,27,32)(H,25,26,28)/t13-/m0/s1
|
|
| 化学名 |
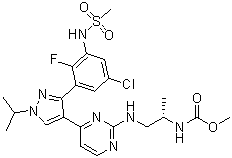
methyl N-[(2S)-1-[[4-[3-[5-chloro-2-fluoro-3-(methanesulfonamido)phenyl]-1-propan-2-ylpyrazol-4-yl]pyrimidin-2-yl]amino]propan-2-yl]carbamate
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (4.63 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (4.63 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (4.63 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 2.5 mg/mL (4.63 mM) in 5% DMSO + 40% PEG300 + 5% Tween80 + 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 5 中的溶解度: ≥ 2.5 mg/mL (4.63 mM) (饱和度未知) in 5% DMSO + 95% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 6 中的溶解度: 5%DMSO+40%PEG300+5%Tween80+50%ddH2O: 100mg/ml 配方 7 中的溶解度: 16.67 mg/mL (30.87 mM) in 50% PEG300 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8518 mL | 9.2591 mL | 18.5182 mL | |
| 5 mM | 0.3704 mL | 1.8518 mL | 3.7036 mL | |
| 10 mM | 0.1852 mL | 0.9259 mL | 1.8518 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Encorafenib and Binimetinib With or Without Nivolumab in Treating Patients With Metastatic Radioiodine Refractory BRAF V600 Mutant Thyroid Cancer
CTID: NCT04061980
Phase: Phase 2 Status: Active, not recruiting
Date: 2024-11-18
Fig. 1. LGX818 suppresses the ERK/MAPK pathway, inhibits proliferation and induces cell cycle arrest in BRAFV600E melanoma cells.Cancer Lett.2016 Jan 28;370(2):332-44. |
Fig. 2.LGX818 downregulates CyclinD1 dependent of DYRK1B, but not GSK3β.Cancer Lett.2016 Jan 28;370(2):332-44. |
Fig. 3. Apoptosis is not involved in LGX818-mediated melanoma cell growth inhibition.Cancer Lett.2016 Jan 28;370(2):332-44. |
Fig. 4. LGX818 induces senescence in BRAFV600E melanoma cells.Cancer Lett.2016 Jan 28;370(2):332-44. |
Fig. 5. LGX818 enhances autophagic flux and induces autophagy via inhibition of the mTOR pathway in BRAFV600E melanoma cells.Cancer Lett.2016 Jan 28;370(2):332-44. |
Fig. 6. Autophagy is involved in LGX818-induced senescence in BRAFV600E melanoma cells.Cancer Lett.2016 Jan 28;370(2):332-44. |