| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
Eprinomectin (2.5-50 μM; 0-48 h) significantly inhibits DU145 cell viability (IC50: 12.5 μM), colony formation and migration ability, and induces G0/G1 phase cell cycle arrest [1].
Eprinomectin (10-50 μM; 48 h) induces apoptosis and autophagy, increases reactive oxygen species production and endoplasmic reticulum stress, and promotes β-catenin nucleocytoplasmic translocation in DU145 cells [1]. |
|---|---|
| 体外研究 (In Vitro) |
Eprinomectin (2.5-50 μM; 0-48 h) 显著抑制 DU145 细胞活力 (IC50: 12.5 μM)、菌落形成和迁移能力,并诱导 G0/G1 期细胞周期停滞 [1]。
Eprinomectin (10-50 μM; 48 h) 诱导细胞凋亡和自噬,增加活性氧产生和内质网应激,并促进 DU145 细胞中 β-catenin 核质易位 [1]。 Eprinomectin以浓度依赖的方式显著抑制前列腺癌细胞系(DU145、LNCaP、VCaP、22RV1)的活力。在DU145细胞中的半数抑制浓度(IC50)为12.5 µM。在50 µM时观察到最大的活力抑制。DU145细胞(激素非依赖性)相比其他细胞系表现出更高的敏感性。[1] 在克隆形成实验中,Eprinomectin显著减少DU145细胞形成的克隆数量和大小,在5 µM浓度下即可减少约50%。[1] 在伤口愈合实验中,Eprinomectin在10 µM和25 µM浓度下,以浓度和时间依赖的方式抑制DU145细胞的迁移能力。[1] Eprinomectin诱导DU145细胞发生G0/G1期细胞周期阻滞,处于G1期的细胞比例从对照组的49.68%增加到50 µM EP处理组的71.7%。它下调细胞周期标志物cyclin D1、cyclin D3、CDK4和c-Myc的表达。[1] 实时荧光定量PCR显示,Eprinomectin下调DU145细胞中癌症干细胞标志物(Oct3/4、Nanog、Sox-2、ALDH1、CD44)和调节CSC特性的基因(β-catenin、c-Myc、cyclin D1)的表达。免疫荧光证实了β-连环蛋白从细胞核到细胞质的转位。[1] Eprinomectin以浓度依赖的方式抑制DU145细胞中碱性磷酸酶的活性。[1] Annexin V/PI染色和流式细胞术显示,Eprinomectin以浓度依赖的方式诱导DU145细胞凋亡。它激活cleaved caspase-3,增加促凋亡蛋白BAD和DNA损伤标志物pH2AX,减少PARP-1,并下调抗凋亡标志物(MCL-1、c-IAP-1、XIAP、survivin、TCTP)。其抗增殖作用可被广谱半胱天冬酶抑制剂减弱。[1] Eprinomectin以浓度依赖的方式诱导DU145细胞产生活性氧。其抗增殖作用可被抗氧化剂N-乙酰半胱氨酸减弱。[1] 免疫荧光和蛋白质印迹证据表明,Eprinomectin诱导DU145细胞自噬,表现为自噬标志物Beclin-1、Atg-5、LC-3II和p62的表达增加。[1] Eprinomectin诱导DU145细胞内质网应激,表现为内质网应激标志物PERK、Ero1-α和PDI的表达增加。这种内质网应激被认为有助于诱导自噬。[1] |
| 体内研究 (In Vivo) |
埃普利诺菌素 (0.08-0.5 mg/kg; 局部吸管给药; 14 天) 在牛体内具有杀虫、杀虫和杀螨活性[2]。牛体内药代动力学分析[1]
|
| 细胞实验 |
细胞活力测定[1]
细胞系:DU145细胞 浓度:2.5、5、10、25和50 μM 孵育时间:48小时 结果:显著抑制细胞活力。 Western Blot分析[1] 细胞系:DU145细胞 浓度:10、25和50 μM 孵育时间:48小时 结果:以浓度依赖性方式促进促凋亡标志物BAD和DNA损伤标志物pH2AX和caspase-9的蛋白表达。通过降低PARP-1抑制DNA修复。 细胞活力实验(MTT法): 将前列腺癌细胞接种于96孔板,待融合度达60-70%时,用不同浓度的Eprinomectin(2.5至100 µM)处理48小时。然后加入MTT染料孵育3小时。溶解生成的甲臜晶体后,在590 nm波长下测量吸光度,计算相对于未处理对照组的细胞活力百分比。[1] 克隆形成实验: 将约500个DU145细胞接种于六孔板。细胞贴壁后,用不同浓度的Eprinomectin(5至100 µM)处理,并培养2周,定期更换培养基。然后固定细胞集落,用结晶紫染色,冲洗、干燥后在光学显微镜下计数。[1] 伤口愈合/迁移实验: 将DU145细胞在24孔板中培养至100%融合。用移液器吸头划痕,并移除脱落细胞。加入含有Eprinomectin(10或25 µM)的新鲜培养基。在0、24和48小时使用光学显微镜拍摄伤口图像。使用软件计算伤口开放面积的百分比以评估迁移抑制情况。[1] 流式细胞术细胞周期分析: 用Eprinomectin(10、25、50 µM)处理DU145细胞48小时后收集细胞,固定,用RNase A处理,并用碘化丙啶染色。使用流式细胞仪分析DNA含量,以确定细胞在不同细胞周期阶段的分布。[1] 基因表达分析(实时荧光定量PCR): 使用Triazole-氯仿法从经或未经Eprinomectin(25 µM,48小时)处理的DU145细胞中提取总RNA。合成cDNA并用于实时荧光定量PCR,以分析靶基因(如CSC标志物、β-catenin通路基因)的表达水平。使用2^(-ΔΔCt)法计算相对基因表达量。[1] 碱性磷酸酶实验: 用Eprinomectin(10、25、50 µM)处理DU145细胞48小时后固定。加入新鲜配制的ALP染色液并在暗处孵育。去除染色液后,在光学显微镜下观察细胞,并使用图像分析软件量化染色强度。[1] 凋亡实验(Annexin V/PI染色及流式细胞术): 对于显微镜观察,用Eprinomectin处理的DU145细胞用Annexin V-FITC和PI染色,并使用共聚焦显微镜分析。对于流式细胞术,处理的细胞用Annexin V和PI染色,分析至少10,000个事件以量化早期和晚期凋亡细胞的百分比。[1] 免疫荧光: 在腔室载玻片上培养的DU145细胞经Eprinomectin处理后,进行固定、透化和封闭。然后与针对靶蛋白(如β-catenin、cleaved caspase-3、Beclin-1、LC-3、PERK、PDI)的一抗孵育,接着与FITC标记的二抗孵育。细胞核用DAPI复染。使用共聚焦显微镜捕获荧光图像并分析荧光强度。[1] 活性氧测量: 用Eprinomectin处理的DU145细胞与荧光探针DCFDA共孵育。清洗后,在荧光显微镜下观察。使用图像分析软件量化与ROS水平成比例的荧光强度。[1] 蛋白质印迹法: 从经Eprinomectin处理的DU145细胞制备蛋白裂解液。等量蛋白通过SDS-PAGE分离并转移至硝酸纤维素膜。封闭膜后,与特异性一抗孵育过夜,然后与相应的二抗孵育。使用增强化学发光法显示蛋白条带,并使用图像分析软件进行定量。β-肌动蛋白用作上样对照。[1] |
| 动物实验 |
动物模型:感染性线虫或牛绒毛虫感染的泽西雄性小牛[2]
剂量:0.08、0.16、0.2、0.24 和 0.5 mg/kg 给药途径:用滴管从尾根至肩胛皮肤表面局部给药;持续 14 天 结果:在最低剂量 (0.08 mg/kg) 下,除匐毛细线虫 (87%) 和囊尾蚴 (88%) 外,对大多数成虫体内寄生虫均达到最大或接近最大疗效。 治疗后第 14 天,所有剂量组的控制率均 ≥ 95%,并在为期 6 周的试验期间维持在该疗效水平或接近该水平。 |
| 参考文献 |
|
| 其他信息 |
依普利诺菌素(Eprinomectin)是伊维菌素的半合成大环内酯衍生物,属于阿维菌素类药物。它最初用作牛的广谱抗寄生虫药。[1]
本研究提出了依普利诺菌素对抗转移性去势抵抗性前列腺癌(mCRPC)细胞的多方面作用机制:它诱导细胞周期阻滞、细胞凋亡(通过caspase激活和活性氧ROS)、自噬(通过内质网应激),并通过破坏β-catenin信号通路抑制癌症干细胞样特性。[1] 该研究表明,依普利诺菌素具有作为晚期前列腺癌(尤其是转移性和耐药表型)新用途治疗药物的潜力。[1] |
| 分子式 |
C50H75NO14;C49H73NO14
|
|---|---|
| 分子量 |
914.13
|
| CAS号 |
123997-26-2
|
| 相关CAS号 |
Eprinomectin-d3
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.23
|
| 熔点 |
163-166 ºC
|
| 闪点 |
2 °C
|
| LogP |
5.469
|
| tPSA |
178.93
|
| SMILES |
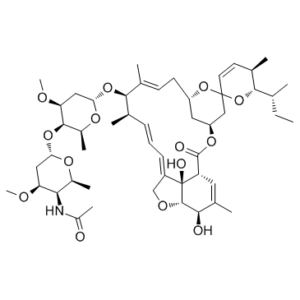
C[C@H]1[C@@H](NC(C)=O)[C@@H](OC)C[C@H](O[C@@H]2[C@H](C)O[C@@H](O[C@@H](/C(C)=C/C[C@@H](C3)OC4(O[C@@H]([C@@H](CC)C)[C@H](C)C=C4)C[C@H]3OC5=O)[C@@H](/C=C/C=C6CO[C@@H]7[C@@]\6(O)[C@H]5C=C(C)[C@H]7O)C)C[C@@H]2OC)O1
|
| InChi Key |
WPNHOHPRXXCPRA-TVXIRPTOSA-N
|
| InChi Code |
InChI=1S/C49H73NO14/c1-25(2)43-28(5)17-18-48(64-43)23-35-20-34(63-48)16-15-27(4)44(26(3)13-12-14-33-24-57-46-42(52)29(6)19-36(47(53)60-35)49(33,46)54)61-40-22-38(56-11)45(31(8)59-40)62-39-21-37(55-10)41(30(7)58-39)50-32(9)51/h12-15,17-19,25-26,28,30-31,34-46,52,54H,16,20-24H2,1-11H3,(H,50,51)/b13-12-,27-15-,33-14-/t26-,28-,30-,31-,34+,35-,36-,37+,38-,39-,40-,41+,42+,43+,44-,45+,46+,48+,49+/m0/s1
|
| 化学名 |
Avermectin B1, 4''-(acetylamino)-4''-deoxy-, (4''R)-
|
| 别名 |
MK 397; MK-397; MK397; Eprinex; 4'-epi-acetylamino-4'-deoxy-avermectin B1a
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : 100~125 mg/mL (~136.74 )
Ethanol :~ 100 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (2.73 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (2.73 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (2.73 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 10% DMSO+40% PEG300+5% Tween-80+45% Saline: ≥ 2.5 mg/mL (2.73 mM) 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.0939 mL | 5.4697 mL | 10.9394 mL | |
| 5 mM | 0.2188 mL | 1.0939 mL | 2.1879 mL | |
| 10 mM | 0.1094 mL | 0.5470 mL | 1.0939 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。