| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
BTK (Ki = 0.91 nM); BTK C481R (Ki = 1.3 nM); BTK C481S (Ki = 1.6 nM); BTK T474M (Ki = 3.4 nM); BTK T474I (Ki = 12.6 nM)
GDC-0853 only inhibits 3 out of 286 off-target kinases in a broad panel of human kinase biochemical assays when tested at 1 μM. The selectivity for Btk is >100-fold against each of these three off-targets, according to the calculated IC50 values: Bmx (153-fold), Fgr (168-fold), and Src (131-fold). GDC-0853 inhibits the signaling of monocyte FcγR and B-cell BCR. The average residence time of GDC-0853 with Btk in the in vitro biochemical Btk enzyme assay is 18.3 ± 2.8 hours. GDC-0853 blocks cellular autophosphorylation of WT Btk and the C481S mutant[1]. GDC-0853 treatment of CLL (chronic lymphocytic leukemia) cells in vitro prior to BCR stimulation results in decreased BTK phosphorylation and decreased activation of downstream targets such as PLCγ2, AKT, and ERK. GDC-0853 decreases activation, hinders migration, and inhibits NF-κB-dependent transcription. GDC-0853 does not influence T-cell receptor activation and does not inhibit EGFR or ITK in the cellular system[3]. |
|---|---|
| 体外研究 (In Vitro) |
在一系列人类激酶生化检测中,当浓度为 1 μM 时,GDC-0853 仅抑制 286 种脱靶激酶中的 3 种。根据计算的 IC50 值,Btk 对这三种脱靶的选择性均 >100 倍:Bmx(153 倍)、Fgr(168 倍)和 Src(131 倍)。 GDC-0853 抑制单核细胞 FcγR 和 B 细胞 BCR 的信号传导。在体外生化 Btk 酶测定中,GDC-0853 与 Btk 的平均停留时间为 18.3 ± 2.8 小时。 GDC-0853 阻断 WT Btk 和 C481S 突变体的细胞自磷酸化[1]。在 BCR 刺激之前,GDC-0853 在体外对 CLL(慢性淋巴细胞白血病)细胞进行处理,导致 BTK 磷酸化降低,并降低 PLCγ2、AKT 和 ERK 等下游靶标的激活。 GDC-0853 减少激活、阻碍迁移并抑制 NF-κB 依赖性转录。 GDC-0853 不影响 T 细胞受体激活,也不抑制细胞系统中的 EGFR 或 ITK[3]。
Fenebrutinib在人类全血中能有效抑制抗IgM诱导的B细胞CD69表达,IC₅₀为8.0 ± 6.0 nM。 在人类全血中抑制抗IgM诱导的Btk Y223自磷酸化,IC₅₀为11 ± 4.2 nM。 在分离的原代人类B细胞中,抑制抗IgM诱导的Btk Y223磷酸化,IC₅₀为3.1 ± 0.7 nM。 抑制抗IgM和CD40L诱导的B细胞增殖,IC₅₀分别为1.2 nM和1.4 nM。 抑制人单核细胞中FcγRIII触发的TNFα产生,IC₅₀为1.3 nM。 通过跳稀实验测定,其与Btk的靶点停留时间为18.3 ± 2.8小时。 |
| 体内研究 (In Vivo) |
GDC-0853 在通过腹腔注射 0.2 mg/kg 或口服 1 mg/kg 给药的大鼠中具有 27.4 mL/min/kg 的中等清除率和优异的生物利用度 (F=65%)。血浆半衰期(t1/2)为2.2小时,分布容积(Vd)为5.42 L/kg,血浆清除率为27.4 mL/min/kg。 GDC-0853 在狗中也显示出积极的 PK 特征。在犬类毒理学研究中,3.8 小时的半衰期(Clp 10.9 mL/min/kg,Vd 2.96 L/kg)进一步实现了足够的暴露)和高口服生物利用度(85%)。大鼠和狗对 GDC-0853 的耐受性良好,并且总体上具有良好的安全性。 GDC-0853有助于治疗由B细胞或骨髓细胞介导的自身免疫性疾病,包括类风湿性关节炎。 GDC-0853 在两项研究中显示出优异的耐受性:单次递增剂量 (SAD) 试验(0.5 mg 至 600 mg)和持续 14 天的多次递增剂量 (MAD) 研究(250 mg BID 至 500 mg QD)。两项研究均表明没有剂量限制性毒性,也没有严重的不良事件。 GDC-0853 表现出剂量成比例的线性药代动力学并且吸收良好[1]。 GDC-0853 和其他结构多样的 BTK 抑制剂在 Sprague-Dawley (SD) 大鼠中给药 7 天或更长时间会导致胰腺病变,包括富含色素的巨噬细胞、炎症、纤维化和多灶性胰岛中心出血以及邻近的小叶外分泌腺泡细胞萎缩、变性和炎症。在高得多的暴露量下,在小鼠或狗中没有看到类似的结果[2]。
类风湿关节炎和狼疮的临床前疗效[1] 为了评估GDC-0853 (29)的体内疗效,我们在B细胞和骨髓细胞依赖性炎症性关节炎模型中进行了测试。发生胶原诱导关节炎的雌性Lewis大鼠(30只)口服16天,其中29只每天服用一次(0.06、0.25、1、4和16 mg/kg QD)(图8A)或两次(0.125、0.5和2 mg/kg BID)(图8B)。29 . QD(图8A)和BID(图8B)给药方案后脚踝厚度的剂量依赖性降低。此外,29项研究显示,剂量反应对踝关节组织病理学参数(炎症、肿块、软骨损伤、骨吸收;数据未显示)。我们还评估了以曲线下面积(AUC)表示的踝关节直径作为疗效参数。与各自的疾病对照相比,QD组16 mg/kg(减少99%)、4 mg/kg(89%)、1 mg/kg(71%)和0.25 mg/kg 29(26%)或BID组2 mg/kg(96%)、0.5 mg/kg(79%)和0.125 mg/kg 29(50%)的大鼠脚踝直径AUC显著降低至正常水平。QD 16 mg/kg剂量和BID 2 mg/kg剂量29与地塞米松的疗效相当(略有改善)。在研究过程中,大鼠的踝关节直径没有变化,正常大鼠的踝关节直径明显小于CIA大鼠(P < 0.05)。 Fenebrutinib在大鼠胶原诱导性关节炎模型中,每日一次(0.06–16 mg/kg)或每日两次(0.125–2 mg/kg)口服给药,能剂量依赖性减轻踝关节肿胀。 血浆浓度在大鼠全血pBtk IC₇₀(27 nM)以上维持12小时,与显著的疗效相关(踝关节肿胀减少约75%)。 |
| 酶活实验 |
BTK 激酶assay。[1]
Btk激酶的活性和抑制作用是根据先前发表的肽磷酸化测定和使用基因泰克表达和纯化的野生型和突变型Btk酶进行评估的。Btk蛋白使用纯化后的蛋白,未采取特殊的活化措施。抑制常数(Ki)由抑制剂滴定数据计算如下。Btk分数活性(vi /vo)与试验品浓度进行拟合,数据使用Genedata筛选软件(Genedata;巴塞尔,瑞士)到紧密结合抑制方程2来计算表观抑制常数,Ki app。 激酶选择性。[1] Btk抑制剂激酶的选择性在浓度为1µM时,在多达287个重组人激酶活性和结合试验中进行评估,如脂质激酶、丝氨酸/苏氨酸激酶、细胞质激酶和受体酪氨酸激酶。结合实验追踪ATP位点结合探针的位移,而激酶活性实验量化肽磷酸化或ADP的产生。对于每个激酶,活性测定中使用的ATP浓度通常在实验确定的表观米切里斯常数(Kmapp)值的两倍以内,而结合测定中使用的竞争结合示踪剂浓度通常在实验确定的解离常数(Kd)值的三倍以内。对于每一种激酶,抑制剂都是重复测试的,并且报告了抑制的平均百分比。同样的测定法用于10点抑制剂滴定,以确定对在测试浓度下被抑制近80%或超过80%的激酶产生50%抑制(IC50)的抑制剂浓度。 激酶试验[3] 将160 ng人重组野生型和C481S BTK与DMSO或1µM GDC-0853孵育30分钟。然后将重组蛋白与50µM三磷酸腺苷和5µg聚肽(4:1,Glu:Tyr)在1倍反应缓冲液中室温结合30分钟,使肽底物磷酸化。然后用ADP-glo激酶试剂和激酶检测试剂分别淬灭和定量反应。使用DTX880plate阅读器测量发光。 肝微粒体代谢稳定性测定[1] 在人、小鼠和大鼠肝微粒体中评估了试验化合物的代谢稳定性。最终孵育液中含有:1µM试验化合物,1 mM NADPH, 0.5 mg/mL微粒体蛋白,0.1 M磷酸钾缓冲液(pH 7.4)。在5分钟的预孵育期后,将NADPH和测试化合物添加到磷酸盐缓冲盐水稀释的微粒体中,启动酶促反应。分别于37℃孵育0、20、40、60 min,采用LC-MS/MS测定所得化合物浓度。基于微粒体稳定性数据的内在清除率使用底物耗尽法确定,并使用充分搅拌模型缩放到肝脏清除率。 肝细胞代谢稳定性测定[1] 实验用小鼠、大鼠、狗、食蟹猴和人肝细胞进行了代谢稳定性分析。台盼蓝法测定细胞的膜完整性。将测试化合物(1µM, 0.1% DMSO)与细胞(50万个细胞/mL)在37°C的95%空气/5% CO2气氛中孵育0,20,40或60分钟。通过LC-MS/MS测定肝细胞孵育中测试化合物的浓度。使用底物耗尽法确定内在清除率,并使用充分搅拌模型(见上)缩放到肝脏清除率。 GDC-0853停留时间测定[1] Btk酶(10 nM)与GDC-0853 (11 nM)或DMSO在50 mM HEPES缓冲液(pH 7.5)中室温孵育2 h。孵育后,将Btk样品稀释200倍至含有ATP和肽底物1的实验混合物中,大约每2.5分钟监测一次未反应的底物肽和磷酸化肽产物的水平,持续8.5 h。与GDC-0853预孵育的Btk形成的产物的进展曲线符合描述活性恢复的方程4: 通过监测Btk催化的合成肽底物磷酸化来评估Btk酶抑制活性。抑制剂的Ki值至少进行三次重复测定。 采用跳稀实验测定解离动力学。将预孵育了Fenebrutinib的Btk稀释至测定体系中,活性恢复延迟表明解离缓慢。数据拟合一级解离模型以计算停留时间。 |
| 细胞实验 |
细胞Btk磷酸化。[1]
GDC-0853和ibrutinib对细胞野生型Btk和Btk C481S突变体Y223磷酸化的影响在瞬时转染的HEK293T细胞中进行了评估。 B细胞和单核细胞检测[1] 采用FicollPaque PLUS分离法从外周血单个核细胞(PBMCs)中分离人B细胞或单核细胞,并按照制造商说明进行磁性细胞分选负选择。用10或25µg/mL山羊抗igm - f (ab’)2或10µg/mL CD40L刺激人B细胞,用[3H]胸腺嘧啶掺入法检测细胞增殖。人单核细胞用40µg/mL固定的HSA/anti - HSA ic孵育。ELISA法检测fc - γ -活化后TNFα的生成。<人力资源> 用二甲基亚砜(DMSO)或GDC-0853处理的细胞同样成粒,然后在含有DMSO或GDC-0853的10%胎牛血清RPMI-1640培养基中重悬。在几天内进行的实验包括每天添加药物和更换培养基。[3] NK细胞介导的ADCC[3] 效应NK细胞从美国红十字会获得的白细胞中分离出来,与装载放射性Cr51的靶CLL细胞以效应靶比25:1孵育。用DMSO、1µM GDC-0853或1µM ibrutinib处理纯化NK细胞1小时后,CLL细胞与曲妥珠单抗、阿仑单抗、利妥昔单抗、ofatumumab或obinutuzumab以10µg/mL的浓度孵育,并与NK细胞共培养,使其溶解。共培养4小时后,收集上清并用PerkinElmer Wizard2 γ计数器测量辐射。β衰变测量根据无nk细胞共培养组与基线CLL裂解和洗涤剂处理CLL组完全裂解进行缩放。 在人类全血中,用抗IgM刺激后,通过流式细胞术测量CD19⁺ B细胞上CD69的表达。细胞与化合物共孵育并刺激过夜。 在人类全血中,抗IgM刺激后使用抗磷酸化Btk抗体检测Btk Y223磷酸化水平。 在分离的原代人类B细胞中,使用磷酸化特异性抗体和增殖实验测量抗IgM诱导的Btk磷酸化和增殖。 在人类单核细胞中,刺激后测量FcγRIII触发的TNFα产生。 |
| 动物实验 |
Sprague-Dawley、Wistar-Han 和 Fischer-344 大鼠(6 至 12 周龄)
5 或 10 mL/kg 口服 大鼠全血 pBtk 检测 [1] Sprague-Dawley 大鼠采用二氧化碳窒息法处死。通过心脏穿刺采集血液至肝素抗凝管中。将大鼠全血与 GDC-0853 进行滴定(起始浓度为 6 µM,然后进行 3 倍稀释,得到 11 点稀释曲线),于 37 ℃ 孵育 4 小时。然后加入等体积的含有蛋白酶和磷酸酶抑制剂的 MSD 裂解缓冲液处理血液。取 35 µL 裂解液加入预先包被有 100 ng/孔总抗 BTK 抗体的 MSD 板中,并在室温下振荡孵育 2 小时。孔板用TBST缓冲液洗涤三次,然后加入12 µg/mL的抗兔pBTK抗体检测液,室温下持续摇动孵育2小时。洗涤后,孔板加入1 µg/mL的磺基标签抗兔抗体,室温下持续摇动孵育45分钟。孵育结束后,孔板最后用S34 TBST缓冲液洗涤,并在每个孔中加入150 µL MSD读数缓冲液,使用MSD Sector Imager 6000成像系统检测pBTK水平。IC50值使用Prism软件计算。布鲁顿酪氨酸激酶(BTK)是Tec家族胞质酪氨酸激酶的成员,参与B细胞和髓系细胞信号传导。BTK小分子抑制剂正被研究用于治疗多种血液系统癌症和自身免疫性疾病。 GDC-0853 ((S)-2-(3'-(羟甲基)-1-甲基-5-((5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基)氨基)-6-氧代-1,6-二氢-[3,4'-联吡啶]-2'-基)-7,7-二甲基-3,4,7,8-四氢-2H-环戊并[4,5]吡咯并[1,2-a]吡嗪-1(6H)-酮) 是一种选择性可逆的口服小分子 BTK 抑制剂,目前正在开发用于治疗类风湿性关节炎和系统性红斑狼疮。在Sprague-Dawley (SD)大鼠中,连续7天或更长时间给予GDC-0853和其他结构各异的BTK抑制剂,可导致胰腺病变,表现为以胰岛为中心的多灶性出血、炎症、纤维化以及富含色素的巨噬细胞浸润,并伴有邻近小叶外分泌腺泡细胞的萎缩、变性和炎症。在小鼠或犬中,即使暴露剂量更高,也未观察到类似结果。在连续4至7天给予GDC-0853后,胰岛周围血管出现出血,其组织学特征与衰老SD大鼠自发发生的病变相似。这表明GDC-0853可能加剧年轻动物体内已存在的病变。葡萄糖负荷试验后,葡萄糖稳态出现紊乱;然而,这种情况仅在给药28天后出现,且与胰腺病变的发生或严重程度无直接关联。评估胰腺内分泌和外分泌功能的其他常见血清生物标志物未见变化。此外,这些病变难以通过多普勒超声、计算机断层扫描或磁共振成像检测到。我们的结果表明,大鼠胰腺病变可能是BTK抑制剂的类效应,可能会加剧以胰岛为中心的病理变化,而这种病理变化不太可能与人类相关。[3] 在胶原诱导性关节炎大鼠模型中,雌性Lewis大鼠用II型胶原蛋白免疫,并每日一次(0.06、0.25、1、4、16 mg/kg)或每日两次(0.125、0.5、2 mg/kg)口服芬布替尼,持续16天。每日测量踝关节直径。 在大鼠和犬中采用盒式给药法进行药代动力学研究。大鼠分别接受0.2 mg/kg静脉注射和1.0 mg/kg口服给药;犬分别接受0.2 mg/kg静脉注射和0.5 mg/kg口服给药。采集血样进行血浆浓度分析。 |
| 药代性质 (ADME/PK) |
每日一次口服1、4和16 mg/kg的GDC-0853 (29)可使血浆药物浓度维持在高于大鼠全血pBtk抑制效力(通过抑制Btk Y223自磷酸化测定,IC50 = 9 nM,IC70 = 27 nM,IC90 = 135 nM)的水平,且在24小时给药周期内至少维持12小时。每日两次口服0.125、0.5和2 mg/kg的GDC-0853(图9B)也可使血浆药物浓度维持在高于IC50、IC70和IC90水平的水平,且在12小时给药周期内至少维持6小时。每日一次 (QD) 1 mg/kg 和每日两次 (BID) 0.5 mg/kg 的剂量,其血浆浓度至少在 24 小时内约 12 小时内超过全血 pBtk IC70 (27 nM)。这种暴露-疗效关系表明,血浆浓度需超过 IC70 29 倍并维持 12 小时才能达到疗效,疗效定义为踝关节肿胀减少约 75%。每日一次 (QD) 4 mg/kg 剂量组的靶点覆盖率更高,在 24 小时内超过 IC90,并进一步提高了疗效。非共价抑制剂对 Btk 的抑制作用也在系统性红斑狼疮 (SLE) 小鼠模型中进行了评估。 (14) 综上所述,我们非共价Btk抑制剂在体内展现出的显著疗效,以及化合物29优异的临床前药理学、药代动力学和体外安全性,使我们有信心推进该分子的耐受性研究。[1]
在大鼠中,Fenebrutinib的清除率为27.4 mL/min/kg,分布容积为5.42 L/kg,半衰期为2.2 h,口服生物利用度为65%。 在犬中,清除率为10.9 mL/min/kg,分布容积为2.96 L/kg,半衰期为3.8 h,口服生物利用度为85%。 相关类似物的人肝微粒体预测肝清除率为7.2–17 mL/min/kg。 |
| 毒性/毒理 (Toxicokinetics/TK) |
在旨在评估该分子安全性的研究中,GDC-0853 (29)在大鼠和犬中均表现出良好的耐受性,并显示出总体上良好的安全性。在最敏感的临床前动物模型——犬中,未观察到不良反应剂量 (NOAEL) 比目标有效暴露量高出 80 倍以上,即在 12 小时内超过 IC70 浓度(来自人全血 CD69 检测)。在 Sprague-Dawley 大鼠中,GDC-0853 (29)和其他结构不同的 Btk 抑制剂已被证明在临床相关剂量下与以胰岛为中心的胰腺病变相关。经过对品系和物种敏感性差异、Btk基因敲除(KO)小鼠以及XLA突变人类病例文献报道的全面调查,我们得出结论:Sprague-Dawley品系大鼠中GDC-0853相关的胰腺病变是Btk抑制剂在鼠类中特异性、品系差异性、靶向作用的结果,与人类无关。对未经治疗的Btk KO Sprague-Dawley大鼠胰腺的组织学评估也支持了这一结论,结果显示其胰腺病理与GDC-0853组相同。由于其良好的安全性,且观察到的胰腺毒性是鼠特异性现象,我们选择GDC-0853 (29)作为临床开发的先导候选药物。[1]
芬布替尼在原代人肝细胞中未显示细胞毒性(IC₅₀ > 300 μM)。 Ames试验和微核试验结果均为阴性,表明其遗传毒性风险低。 hERG通道抑制作用低(IC₅₀ > 30 μM)。 在Sprague-Dawley大鼠中观察到胰腺病变,但被认为是鼠特异性靶向效应,与人类无关。 在犬中,未观察到不良反应的剂量水平高于有效暴露量的80倍以上。 |
| 参考文献 | |
| 其他信息 |
芬布替尼正在临床试验NCT03174041(GDC-0853与咪达唑仑、伊曲康唑、瑞舒伐他汀和辛伐他汀的药物相互作用研究)中进行研究。
芬布替尼是一种口服的布鲁顿酪氨酸激酶(BTK)抑制剂,具有潜在的抗肿瘤活性。给药后,芬布替尼抑制BTK的活性,并阻止B细胞抗原受体(BCR)信号通路的激活。这既能阻止B细胞活化,又能阻止BTK介导的下游生存通路的激活,从而抑制过表达BTK的恶性B细胞的生长。BTK是Src相关BTK/Tec家族胞质酪氨酸激酶的成员,在B细胞恶性肿瘤中过表达;它在B淋巴细胞的发育、活化、信号传导、增殖和存活中发挥着重要作用。 药物适应症 治疗多发性硬化症 芬布替尼是一种非共价Btk抑制剂,其结合模式与伊布替尼等共价抑制剂正交,因此能够保留对Btk C481S突变的活性。 它对Btk具有高度选择性,对其他激酶的抑制作用较弱,在1 μM浓度下仅抑制286个非靶激酶中的3个。 它已进入类风湿性关节炎、系统性红斑狼疮和慢性自发性荨麻疹的II期临床试验。 |
| 分子式 |
C37H44N8O4
|
|---|---|
| 分子量 |
664.7965
|
| 精确质量 |
664.348
|
| 元素分析 |
C, 66.85; H, 6.67; N, 16.86; O, 9.63
|
| CAS号 |
1434048-34-6
|
| 相关CAS号 |
1434048-34-6;2128304-54-9 (HCl);2128304-53-8 (mesylate);2128304-55-0 (sulfate);
|
| PubChem CID |
86567195
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.4±0.1 g/cm3
|
| 沸点 |
936.3±65.0 °C at 760 mmHg
|
| 闪点 |
520.0±34.3 °C
|
| 蒸汽压 |
0.0±0.3 mmHg at 25°C
|
| 折射率 |
1.725
|
| LogP |
1.59
|
| tPSA |
119Ų
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
9
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
49
|
| 分子复杂度/Complexity |
1340
|
| 定义原子立体中心数目 |
1
|
| SMILES |
O1C([H])([H])C([H])(C1([H])[H])N1C([H])([H])C([H])([H])N(C2=C([H])N=C(C([H])=C2[H])N([H])C2C(N(C([H])([H])[H])C([H])=C(C=2[H])C2C([H])=C([H])N=C(C=2C([H])([H])O[H])N2C(C3=C([H])C4=C(C([H])([H])C(C([H])([H])[H])(C([H])([H])[H])C4([H])[H])N3C([H])([H])C2([H])[H])=O)=O)[C@@]([H])(C([H])([H])[H])C1([H])[H]
|
| InChi Key |
WNEODWDFDXWOLU-QHCPKHFHSA-N
|
| InChi Code |
InChI=1S/C37H44N8O4/c1-23-18-42(27-21-49-22-27)9-10-43(23)26-5-6-33(39-17-26)40-30-13-25(19-41(4)35(30)47)28-7-8-38-34(29(28)20-46)45-12-11-44-31(36(45)48)14-24-15-37(2,3)16-32(24)44/h5-8,13-14,17,19,23,27,46H,9-12,15-16,18,20-22H2,1-4H3,(H,39,40)/t23-/m0/s1
|
| 化学名 |
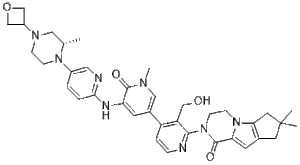
10-[3-(hydroxymethyl)-4-[1-methyl-5-[[5-[(2S)-2-methyl-4-(oxetan-3-yl)piperazin-1-yl]pyridin-2-yl]amino]-6-oxopyridin-3-yl]pyridin-2-yl]-4,4-dimethyl-1,10-diazatricyclo[6.4.0.02,6]dodeca-2(6),7-dien-9-one
|
| 别名 |
RG-7845; GDC-0853; RG7845; GDC 0853; RG 7845; GDC0853; Fenebrutinib [INN]; (S)-2-(3'-(hydroxymethyl)-1-methyl-5-((5-(2-methyl-4-(oxetan-3-yl)piperazin-1-yl)pyridin-2-yl)amino)-6-oxo-1,6-dihydro-[3,4'-bipyridin]-2'-yl)-7,7-dimethyl-3,4,7,8-tetrahydro-2H-cyclopenta[4,5]pyrrolo[1,2-a]pyrazin-1(6H)-one;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ≥ 23 mg/mL (~34.6 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 1 mg/mL (1.50 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 10.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1 mg/mL (1.50 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 10.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 1 mg/mL (1.50 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.5042 mL | 7.5211 mL | 15.0421 mL | |
| 5 mM | 0.3008 mL | 1.5042 mL | 3.0084 mL | |
| 10 mM | 0.1504 mL | 0.7521 mL | 1.5042 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
A PHASE II, RANDOMIZED, DOUBLE-BLIND, PLACEBO-CONTROLLED STUDY OF THE SAFETY AND EFFICACY OF GDC-0853 IN PATIENTS WITH
CTID: null
Phase: Phase 2 Status: Completed
Date: 2016-11-16
Representative photomicrographs of pancreatic histopathology observed in Sprague-Dawley rats following daily oral administration of GDC-0853 for 21 or 28 days are presented.J Pharmacol Exp Ther. 2017 Jan;360(1):226-238. |
Exposure to GDC-0853 in Sprague-Dawley rats relative to BTK (on-target) and off-target (BMX, FGR, SRC) kinase half-maximal inhibitory concentrations (IC50) is presented.
Strain sensitivity to BTK inhibitor–induced pancreatic lesions is presented.J Pharmacol Exp Ther. 2017 Jan;360(1):226-238. |
Relative Btk transcript expression (dCT; delta Cycle Threshold) in pancreatic tissue from humans and Sprague-Dawley rats is presented.
Glucose and insulin levels in Sprague-Dawley rats following administration of GDC-0853 are presented.J Pharmacol Exp Ther. 2017 Jan;360(1):226-238. |
Amylase, lipase, insulin, and fructosamine levels in Sprague-Dawley rats (n≤ 15 per sex per group) following administration of GDC-0853 are presented.J Pharmacol Exp Ther. 2017 Jan;360(1):226-238. |
Ultrasound imaging of the pancreas in Sprague-Dawley rats following administration of GNE-309 (n= 8 males per group) or GDC-0853 (n= 16 males per group) is presented.J Pharmacol Exp Ther. 2017 Jan;360(1):226-238. |
Molecular structures of BTK inhibitors GDC-0853, GNE-309, ibrutinib, and spebrutinib.J Pharmacol Exp Ther. 2017 Jan;360(1):226-238. |