| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
RIP3 (IC50 = 20.8 nM)
HS-1371 shows an inhibitory effect on S227 auto-phosphorylation of RIP3 at the basal level. It completely inhibits TNF-induced necroptosis signaling, as evidenced by the absence of RIP3 and MLKL phosphorylation in HT-29 cells. By preventing the formation of necrosome complexes, HS-1371's inhibition of RIP3 kinase activity demonstrates disruption of MLKL recruitment. HS-1371 prevents the necroptosis that TNF causes in cells. It prevents necroptotic cell death caused by RIP3 but does not prevent apoptotic cell death[1]. |
|---|---|
| 体外研究 (In Vitro) |
HS-1371 在基础水平上显示出对 RIP3 S227 自磷酸化的抑制作用。它完全抑制 TNF 诱导的坏死性凋亡信号传导,HT-29 细胞中不存在 RIP3 和 MLKL 磷酸化就证明了这一点。通过阻止坏死体复合物的形成,HS-1371 对 RIP3 激酶活性的抑制表明 MLKL 招募受到破坏。 HS-1371 可防止 TNF 在细胞中引起的坏死性凋亡。它可以防止 RIP3 引起的坏死性细胞死亡,但不能防止凋亡性细胞死亡[1]。
HS-1371 以 ATP 竞争性和时间非依赖性的方式直接结合到 RIP3 的 ATP 结合口袋。[1] 在 HT-29 细胞中,HS-1371 以剂量依赖的方式抑制 RIP3 的基础 S227 位点自身磷酸化。[1] 在用 TSZ (TNFα + Smac 模拟物 + zVAD) 处理以诱导坏死性凋亡的 HT-29 细胞中,预先用 HS-1371 (5 μM) 处理能完全阻断 TNF 诱导的 RIP3 磷酸化及其下游的 MLKL 磷酸化,效果与已知的 RIP3 抑制剂达拉非尼相似。[1] HS-1371 (5 μM) 能将 HT-29 细胞从 TSZ 诱导的坏死性凋亡中拯救出来,恢复细胞活力。这种保护作用是剂量依赖性的。[1] HS-1371 也能抑制 TRAIL 诱导的坏死性凋亡(表现为减少的 RIP3 和 MLKL 磷酸化),并以剂量依赖的方式保护 HT-29 细胞免受 TRAIL+Smac+zVAD 诱导的细胞死亡。[1] HS-1371 不抑制 TNF 诱导的细胞凋亡(由 TNF+CHX 或 TNF+Smac 模拟物诱导),表明其对坏死性凋亡具有特异性。[1] 在异位表达 RIP3 的 HeLa 和 H2009 细胞中,HS-1371 以剂量依赖的方式抑制基础和 TSZ 诱导的 RIP3 及 MLKL 磷酸化,并保护这些细胞免受 TSZ 诱导的死亡。[1] HS-1371 能预防小鼠 L929 细胞中 TNF+zVAD 诱导的坏死性凋亡以及小鼠胚胎成纤维细胞 (MEF) 中 TNF+CHX+zVAD 诱导的坏死性凋亡,抑制 MLKL 磷酸化和细胞死亡。[1] 在 HT-29 细胞中,在 TSZ 诱导后(最多 5 小时)给予 HS-1371 仍能部分抑制 MLKL 磷酸化并显著降低细胞毒性。[1] 在 RAW264.7 巨噬细胞中,HS-1371 降低了 LPS 诱导的促炎细胞因子 IL-1β、IL-6 和 TNF-α 的表达。[1] |
| 酶活实验 |
Reaction Biology Corp 使用放射激酶测定 ([γ-32P]ATP) 来确定所有化合物对 RIP3 的抑制活性。新鲜制备的反应缓冲液中的髓磷脂碱性蛋白 (MBP)(20 mM HEPES (pH 7.5)、10 mM MgCl2、1 mM EGTA、0.02% BRIJ-35、0.02 mg/mL BSA、0.1 mM Na3VO4、2 mM DTT 和1% DMSO)用于测量RIP3的酶活性。将每种假定的 RIP3 抑制剂以特定浓度溶解在 100% DMSO 中,用 epMotion 5070 的 DMSO 溶液进行系列稀释,然后进行测试。反应缓冲液中添加了人 RIP3 和 20 μM 肽底物 (MBP)。使用Acoustic技术(Echo550;纳升范围)将溶解在DMSO中的候选抑制剂给予激酶反应混合物,然后将反应混合物在室温下孵育20分钟。将终浓度为 10 μM 的 ATP 和比活度为 10 μCi/μL 的 33P-ATP 添加到反应混合物中,开始酶促反应。让反应混合物在室温下静置两小时后,然后使用过滤结合技术测量放射性。剩余激酶活性相对于载体(二甲基亚砜)反应的百分比用于计算给定浓度下抑制剂的生化效力。然后使用 PRISM 程序获得 IC50 值和曲线拟合。由于其对多种激酶(包括 RIP3)的高生化效力,ATP 竞争性抑制剂星形孢菌素 (STSP) 在本研究中被用作阳性对照。
使用放射性激酶实验测定 HS-1371 对 RIP3 激酶的抑制活性。将重组人 RIP3 激酶和肽底物(髓鞘碱性蛋白,MBP)溶解于反应缓冲液中。将 HS-1371(溶于 DMSO)的系列稀释液加入到激酶反应混合物中。通过添加 [γ-33P]ATP 启动酶促反应。孵育后,使用滤膜结合法监测放射性,以测量与溶剂对照组相比剩余的激酶活性百分比。从剂量反应曲线获得 IC50 值。[1] 进行了作用机制研究以确定 HS-1371 是否为 ATP 竞争性抑制剂。将 RIP3 酶与 HS-1371 预孵育。反应用不同浓度的 ATP 启动,并测量初始反应速度。数据绘制为米氏方程图和双倒数图。随着 HS-1371 浓度增加,ATP 的表观 Km 值增加,且双倒数图中的线在 y 轴上相交,表明是 ATP 竞争性抑制。[1] |
| 细胞实验 |
Nec-1 (40 μM)、DAB (5 μM) 或 HS-1371 在 HT-29 细胞中预处理 2 小时,然后给予 TSZ 4 小时。抗 RIP3 抗体用于免疫沉淀细胞裂解物。
免疫印迹分析和免疫沉淀[1] 细胞在冷磷酸盐缓冲盐水(PBS)中冲洗,在含有20 mM Tris的M2缓冲液中裂解,pH为7,0.5% NP-40, 250 mM NaCl, 3 mM EDTA, 3 mM EGTA, 2 mM DTT, 0.5 mM PMSF, 20 mM β-甘油磷酸,1 mM vanadate钠和1 μg/mL lepeptin。细胞提取物进行western blot分析。对于免疫沉淀,将裂解物与抗体和蛋白a -琼脂糖珠混合并沉淀过夜或在4°C下沉淀4小时。结合蛋白在SDS中煮沸去除,SDS- page溶解,增强化学发光观察免疫印迹。 细胞毒性测定[1] 使用四氮唑染料比色法(MTT法)在570 nm处测定细胞活力。PI染色用碘化丙啶定量。根据制造商的说明,使用CellTiter-Glo发光细胞活力测定试剂盒定量乳酸脱氢酶(LDH)泄漏。在490 nm处读取LDH吸光度,并给出重复的平均值±STDEV。 免疫荧光染色[1] HT-29细胞在4%多聚甲醛中固定10分钟。为了染色phospho-MLKL,细胞用0.25% Triton X-100渗透10分钟。在阻断缓冲液(DPBS中10%胎牛血清)中孵育30分钟后,将phospho-MLKL的一抗在4℃下孵育过夜,fitc偶联的二抗(山羊抗兔IgG, 1:250,稀释)在室温下孵育1小时。使用含有DAPI的挂载培养基进行反染。共聚焦显微镜拍摄代表性图像。 为了评估对 RIP3 磷酸化的影响,用不同浓度的 HS-1371 处理 HT-29 细胞指定时间。然后裂解细胞,使用针对磷酸化 RIP3 (S227)、总 RIP3、磷酸化 MLKL 和总 MLKL 的抗体,通过蛋白质印迹分析裂解物。肌动蛋白用作上样对照。[1] 为了评估对坏死性凋亡的保护作用,将细胞(如 HT-29、HeLa-RIP3、H2009-RIP3、L929、MEF)用 HS-1371 或溶剂预处理一段时间(例如 2 小时)。然后通过添加特定的刺激组合(例如 TSZ:TNFα + Smac 模拟物 + zVAD;TCZ:TNFα + 放线菌酮 + zVAD;TNF+zVAD)诱导坏死性凋亡。孵育一段时间(例如 6-24 小时)后,使用 MTT、乳酸脱氢酶释放或碘化丙啶染色等方法测量细胞活力。同时,制备细胞裂解物用于坏死性凋亡标志物的蛋白质印迹分析。[1] 为了分析磷酸化 MLKL 转位的免疫荧光,在存在或不存在 HS-1371 的情况下,用 TSZ 处理 HT-29 细胞。固定并透化细胞,用抗磷酸化 MLKL 的抗体染色,再用荧光二抗染色。用 DAPI 复染细胞核,并通过共聚焦显微镜捕获图像。[1] 为了测试对 RIP3 的依赖性,用靶向 RIP3 或 MLKL 的慢病毒 shRNA 感染 HT-29 细胞以实现敲低。通过蛋白质印迹确认敲低效率。然后用 TSZ 和 HS-1371 处理这些细胞,并评估细胞活力。[1] 为了研究后处理效果,首先用 TSZ 处理 HT-29 细胞以诱导坏死性凋亡。在 TSZ 添加后的不同时间点(例如 1、3、5、7 小时)加入 HS-1371。继续孵育细胞,并在实验结束时分析细胞活力和 RIP3/MLKL 的磷酸化状态。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
在HT-29细胞中,四种受试激酶抑制剂(包括HS-1371)在高浓度(10 μM)下处理24小时后,经MTT法检测,均显示出一定的细胞毒性。[1]
|
| 参考文献 | |
| 其他信息 |
坏死性凋亡是一种程序性细胞死亡,通常发生在细胞凋亡缺陷的情况下。受体相互作用蛋白激酶3 (RIP3,或RIPK3) 是坏死性凋亡的核心参与者,其激酶活性对于下游坏死性凋亡信号通路至关重要。由于RIP3激酶活性与多种疾病相关,因此开发特异性RIP3抑制剂是一种极具吸引力的治疗策略。在本研究中,我们通过对以激酶为靶点的化合物库进行广泛筛选,鉴定出一种高效的RIP3抑制剂HS-1371。HS-1371以ATP竞争性和时间非依赖性的方式直接与RIP3结合,这揭示了其作用机制。此外,该化合物抑制了TNF诱导的坏死性凋亡,但并未抑制TNF诱导的细胞凋亡,表明这种新型抑制剂通过抑制RIP3激酶活性,对RIP3介导的坏死性凋亡具有特异性抑制作用。我们的研究结果表明,HS-1371可能作为一种潜在的预防或治疗药物,用于治疗涉及RIP3过度激活的疾病。[1]
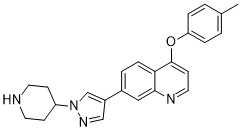
HS-1371(7-(1-(哌啶-4-基)-1H-吡唑-4-基)-4-(对甲苯氧基)喹啉)是通过筛选以激酶为靶点的化合物库而发现的一种有效的RIP3抑制剂。 [1] 分子对接模拟表明,HS-1371与RIP3的ATP结合位点结合,与Met98和Val28的骨架形成氢键,并与Phe97、Thr95、Asp161和Lys51等残基发生疏水相互作用。[1] 该研究提出,HS-1371可能作为一种潜在的预防或治疗药物,用于治疗涉及RIP3过度激活的疾病,例如中毒性表皮坏死松解症(TEN)、脓毒症和其他炎症性疾病。[1] HS-1371特异性抑制RIP3介导的坏死性凋亡,但不影响TNF诱导的细胞凋亡或NF-κB信号通路激活。[1] |
| 分子式 |
C24H24N4O
|
|
|---|---|---|
| 分子量 |
384.473565101624
|
|
| 精确质量 |
384.195
|
|
| 元素分析 |
C, 74.97; H, 6.29; N, 14.57; O, 4.16
|
|
| CAS号 |
2158197-70-5
|
|
| 相关CAS号 |
|
|
| PubChem CID |
134817449
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
4
|
|
| tPSA |
52
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
4
|
|
| 可旋转键数目(RBC) |
4
|
|
| 重原子数目 |
29
|
|
| 分子复杂度/Complexity |
517
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
CC1=CC=C(C=C1)OC2=C3C=CC(=CC3=NC=C2)C4=CN(N=C4)C5CCNCC5
|
|
| InChi Key |
VPVLPCIBKVWFDT-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C24H24N4O/c1-17-2-5-21(6-3-17)29-24-10-13-26-23-14-18(4-7-22(23)24)19-15-27-28(16-19)20-8-11-25-12-9-20/h2-7,10,13-16,20,25H,8-9,11-12H2,1H3
|
|
| 化学名 |
4-(4-methylphenoxy)-7-(1-piperidin-4-ylpyrazol-4-yl)quinoline
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 1.67 mg/mL (4.34 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 16.7 mg/mL澄清的DMSO储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1.67 mg/mL (4.34 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 16.7mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 1.67 mg/mL (4.34 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6010 mL | 13.0049 mL | 26.0098 mL | |
| 5 mM | 0.5202 mL | 2.6010 mL | 5.2020 mL | |
| 10 mM | 0.2601 mL | 1.3005 mL | 2.6010 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Identification of HS-1371 as a novel RIP3 kinase inhibitor.. From: HS-1371, a novel kinase inhibitor of RIP3-mediated necroptosis.Exp Mol Med.2018 Sep 20;50(9):125. |
|---|
HS-1371 protects cells from TNF-induced necroptosis.. From: HS-1371, a novel kinase inhibitor of RIP3-mediated necroptosis.Exp Mol Med.2018 Sep 20;50(9):125. |
Possibility of HS-1371 as a drug for necroptosis-related diseases.. From: HS-1371, a novel kinase inhibitor of RIP3-mediated necroptosis.Exp Mol Med.2018 Sep 20;50(9):125. |
HS-1371 had an inhibitory effect on RIP3 kinase activity in various cell lines.. From: HS-1371, a novel kinase inhibitor of RIP3-mediated necroptosis.Exp Mol Med.2018 Sep 20;50(9):125. |
|---|
HS-1371 only rescues cells from RIP3-dependent necroptosis.. From: HS-1371, a novel kinase inhibitor of RIP3-mediated necroptosis.Exp Mol Med.2018 Sep 20;50(9):125. |
Novel inhibitors can block RIP3 S227 phosphorylation.. From: HS-1371, a novel kinase inhibitor of RIP3-mediated necroptosis.Exp Mol Med.2018 Sep 20;50(9):125. |