| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Both radiolabeled inhibitors have high affinity for their respective enzymes and are selective ligands based on their in vitro binding characteristics. In rat cerebral cortex, 3H-Ro 19-6327 had KD and Bmax values of 18.4 nM and 3.45 pmol/mg protein, respectively [1]. Lazabemide's IC50 values are as follows: 86 μM for NA uptake, 123 μM for 5HT uptake, and >500 μM for DA uptake, respectively[1]. Human MAO-B and MAO-A are inhibited by lazabemide (5 μM) with IC50 values of 6.9 nM and >10 nM, respectively. It inhibits rat MAO-B and MAO-A in enzymatic experiments with IC50 values of 37 nM and >10 μM, respectively [2]. In terms of their capacity to trigger the release of endogenous monoamines from synaptosomes, lazabemide and L-deprenyl are not the same. Thus, compared to L-deprenyl, lazabemide (500 μM) caused a greater release of 5 HT, but it was less successful in releasing DA. On the other hand, lazabemide is essentially inert upon 5-HT and DA release [2]. In renal tubular epithelial cells treated with 50 microM L-DOPA, lazabemide (250 nM) effectively suppresses DOPAC production without increasing the concentration of freshly generated DA [3].
|
|---|---|
| 体外研究 (In Vitro) |
两种放射性标记抑制剂对其各自的酶具有高亲和力,并且基于其体外结合特性是选择性配体。在大鼠大脑皮层中,3H-Ro 19-6327 的 KD 和 Bmax 值分别为 18.4 nM 和 3.45 pmol/mg 蛋白质 [1]。 Lazabemide 的 IC50 值如下:NA 摄取为 86 μM,5HT 摄取为 123 μM,DA 摄取为 >500 μM[1]。人 MAO-B 和 MAO-A 被拉扎贝胺 (5 μM) 抑制,IC50 值分别为 6.9 nM 和 >10 nM。它在酶促实验中抑制大鼠 MAO-B 和 MAO-A,IC50 值分别为 37 nM 和 >10 μM [2]。就触发突触体释放内源性单胺的能力而言,拉扎贝胺和 L-deprenyl 并不相同。因此,与 L-丙炔苯丙胺相比,拉扎贝胺 (500 μM) 引起更多的 5 HT 释放,但在释放 DA 方面不太成功。另一方面,拉扎贝胺在释放 5-HT 和 DA 时基本上呈惰性 [2]。在用 50 microM L-DOPA 处理的肾小管上皮细胞中,拉扎贝米 (250 nM) 有效抑制 DOPAC 的产生,而不增加新产生的 DA 浓度 [3]。
Lazabemide (³H-Ro 19-6327) 在大鼠中枢神经系统、外周器官和人死后脑组织切片中表现出对 MAO-B 的高亲和力、可饱和且具有药理学特异性的结合。³H-Ro 19-6327 与大鼠大脑额叶皮层结合的平衡解离常数 (K_D) 为 18.4 nM,最大结合容量 (B_max) 为 3.45 pmol/mg 蛋白。其结合可被已知的 MAO-B 抑制剂(如 L-司来吉兰)竞争性抑制,而不被 MAO-A 抑制剂抑制,证实了其对 MAO-B 的选择性。 [1] 使用 ³H-Ro 19-6327 进行的定量酶放射自显影揭示了 MAO-B 在显微区域的详细分布和丰度。在大鼠脑中,MAO-B 在室周器、室管膜、嗅神经层(内部)、丘脑室旁核、乳头体核、中缝核和小脑 Bergmann 胶质细胞中最为丰富。在大鼠外周组织中,在内分泌胰腺、肝脏(门静脉周围 > 中央区)、附睾和十二指肠中发现了高丰度。 [1] 在人类死后脑组织切片中,MAO-B 结合位点(用 ³H-Ro 19-6327 显示)通常比 MAO-A 位点更丰富。在室管膜细胞、齿状回多形层、中缝背核、黑质网状部和脚间核中发现了高水平表达。 [1] |
| 体内研究 (In Vivo) |
与相当的媒介物处理对照相比,Lazabemide 预处理显示出较低的 DOPAC 水平,并且 Lazabemide (3 mg/kg) 抑制缺血再灌注诱导的羟自由基生成 [4]。
|
| 酶活实验 |
使用组织切片定量酶放射自显影技术测定了氚标记的 Lazabemide (³H-Ro 19-6327) 与 MAO-B 的体外结合特性。 [1]
将新鲜冷冻的大鼠和人类死后组织的冷冻切片(12 μm)贴在载玻片上。切片在含有 50 mM Tris、120 mM NaCl、1 mM MgCl₂、5 mM KCl 和 0.5 mM EGTA 的缓冲液(pH 7.4)中与 ³H-Ro 19-6327 一起孵育。在 20°C 下孵育 90 分钟以达到稳态。 [1] 非特异性结合通过将相邻切片与 1 μM L-司来吉兰(针对 ³H-Ro 19-6327)或 50 μM L-司来吉兰(用于饱和实验)共同孵育来确定。孵育后,切片在冰浴缓冲液中冲洗(30秒 + 30秒 + 60秒),然后在冰浴蒸馏水中快速冲洗以去除未结合的配体。 [1] 进行了结合动力学(结合/解离)和饱和实验。对于饱和实验,切片与浓度递增的 ³H-Ro 19-6327(1-250 nM)一起孵育。通过将组织擦拭到玻璃纤维滤膜上进行液体闪烁计数,或将标记的切片与氚敏感胶片接触 3 周,然后使用计算机辅助图像分析系统进行光密度分析来量化放射性。使用校准标准品将光密度值转换为 pmol/mg 蛋白。 [1] 通过将切片与 20 nM ³H-Ro 19-6327 以及不同浓度(1 pM 至 1 mM)的竞争性 MAO 抑制剂(如 L-司来吉兰、Ro 41-1049)一起孵育来进行竞争结合实验,以确定 IC₅₀ 值。 [1] |
| 细胞实验 |
大鼠前脑突触小体摄取实验: 从大鼠前脑匀浆中获得粗突触小体制备物。突触小体在含有 MAO 抑制剂帕吉林 (10 µM) 的 Krebs 缓冲液中,于 37°C 预孵育 5 分钟,存在或不存在测试药物(Lazabemide、Ro 16-6491 或 L-司来吉兰)。随后,加入浓度为 3 nM 的氚标记胺类([³H]NA、[³H]DA 或 [³H]5-HT),继续孵育 4 分钟。反应通过 4°C 离心终止。将沉淀洗涤两次并溶解,通过液体闪烁光谱法测量放射性。在 4°C 下孵育的样品中的摄取值作为空白对照。 [2]
突触小体内源性胺类释放实验: 为了研究药物诱导的释放,将突触小体在含有帕吉林 (10 µM) 和通用摄取抑制剂双氯芬辛 (1 µM) 的 Krebs 缓冲液中于 37°C 预孵育 5 分钟,以尽量减少再摄取。然后将样品在存在或不存在测试药物的情况下再孵育 15 分钟。离心后,将沉淀物在内标物存在下用高氯酸匀浆。使用反相 HPLC 结合库仑检测法分析上清液中的内源性 NA、DA 和 5-HT 含量。 [2] 大鼠血小板 [¹⁴C]5-HT 摄取实验: 将富血小板血浆 (PRP) 与测试药物(存在或不存在)在 37°C 预孵育 5 分钟。然后加入 [¹⁴C]5-HT (1 µM),继续孵育 5 分钟。通过离心沉降血小板,洗涤并裂解。测定裂解液中的放射性和蛋白质含量。 [2] 大鼠血小板 [¹⁴C]5-HT 释放实验: 将 PRP 与 [¹⁴C]5-HT (1 µM) 在 37°C 预孵育 10 分钟。然后洗涤血小板并重悬于缓冲液中。将此悬浮液等分试样与测试药物(存在或不存在)在 37°C 重新孵育 60 分钟。沉降和洗涤后,裂解血小板沉淀,并测量剩余的放射性。 [2] |
| 参考文献 | |
| 其他信息 |
拉扎贝胺(Lazabemide)是一种新型、高选择性、可逆的MAO-B抑制剂。研究开展时,该药物正处于治疗帕金森病的II期临床试验阶段。[1]
该研究主要利用拉扎贝胺(氚标记放射性配体)作为研究工具,通过定量酶放射自显影技术绘制MAO-B的分布和丰度图谱,为组织化学和免疫组织化学方法提供了一种灵敏且定量的替代方法。[1] 拉扎贝胺结合所揭示的MAO-B分布表明,其生理功能可能包括在星形胶质细胞和室管膜细胞中清除痕量胺(例如苯乙胺),并可能防止血清素能神经元中假性神经递质的积累。[1] |
| 分子式 |
C8H10N3OCL
|
|---|---|
| 分子量 |
199.6375
|
| 精确质量 |
199.051
|
| CAS号 |
103878-84-8
|
| 相关CAS号 |
Lazabemide hydrochloride;103878-83-7
|
| PubChem CID |
71307
|
| 外观&性状 |
Light yellow to yellow solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
397.4±37.0 °C at 760 mmHg
|
| 闪点 |
194.2±26.5 °C
|
| 蒸汽压 |
0.0±0.9 mmHg at 25°C
|
| 折射率 |
1.572
|
| LogP |
-0.01
|
| tPSA |
68.01
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
13
|
| 分子复杂度/Complexity |
177
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
JZXRLKWWVNUZRB-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C8H10ClN3O/c9-6-1-2-7(12-5-6)8(13)11-4-3-10/h1-2,5H,3-4,10H2,(H,11,13)
|
| 化学名 |
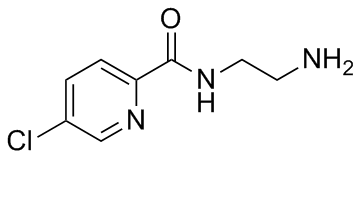
N-(2-aminoethyl)-5-chloropyridine-2-carboxamide
|
| 别名 |
Ro 19-6327; Ro-19-6327; Ro 19 6327
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~5 mg/mL (~25.05 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 0.5 mg/mL (2.50 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 5.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 0.5 mg/mL (2.50 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 5.0 mg/mL 澄清 DMSO 储备液加入 900 μL 20% SBE-β-CD 生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 0.5 mg/mL (2.50 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 5.0090 mL | 25.0451 mL | 50.0902 mL | |
| 5 mM | 1.0018 mL | 5.0090 mL | 10.0180 mL | |
| 10 mM | 0.5009 mL | 2.5045 mL | 5.0090 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。