| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Cysteine proteases; CANP; Cathepsin C
|
|---|---|
| 体外研究 (In Vitro) |
体外活性:Loxistatin Acid (E-64C) 作为硫醇蛋白酶抑制剂,可抑制完整血小板中的钙蛋白酶活性。 E-64C 抑制神经元嗜铬细胞调节的分泌囊泡中的 β 分泌酶活性,并减少 Aβ 的产生,这表明了阿尔茨海默病的治疗策略。
E-64d,E-64c的膜渗透性衍生物,硫醇蛋白酶抑制剂(Tamai等人(1986)J.Pharmacobio Dyn。9672-677),测试其抑制完整血小板钙蛋白酶活性的能力。钙蛋白酶活性是通过肌动蛋白结合蛋白和塔林(钙蛋白酶的两种已知底物)的蛋白水解来测量的。在裂解前用E-64c/(非渗透性)或E-64d孵育血小板可防止裂解后的蛋白水解。当血小板与E-64c/Loxistatin Acid或E-64d一起孵育,然后在裂解前洗涤以去除药物时,只有E-64d抑制了蛋白水解。当血小板与E-64c/Loxistatin Acid或E-64d一起孵育,然后用A23187加钙(一种激活板内钙蛋白酶的治疗方法)激活时,只有E-64d抑制了蛋白水解。这些结果表明,E-64d可以进入完整的细胞并抑制钙蛋白酶。[1] Z-Val-Lys-Met-MCA切割活性的DTT敏感性表明,半胱氨酸蛋白酶的参与通常需要还原条件。半胱氨酸蛋白酶抑制剂Loxistatin Acid完全抑制嗜铬囊泡β-分泌酶活性;半胱氨酸蛋白酶抑制剂C和对羟基苯甲酸汞(PHMB)也抑制了该活性。苯甲基磺酰氟(PMSF)是一种丝氨酸蛋白酶抑制剂,具有部分抑制作用(Hook等人,2002)。糜蛋白酶抑制剂的抑制与半胱氨酸或丝氨酸蛋白酶活性有关。天冬氨酸和金属蛋白酶抑制剂的作用很小。嗜铬小泡中的β-分泌酶活性不受他汀类取代肽抑制剂的抑制(Hook等人,2002),该抑制剂代表瑞典突变型β-分泌酶类切割位点(Sinha等人,1999),表明嗜铬小囊泡β-分泌蛋白酶活性对切割大多数AD患者中表达的野生型β-分泌物位点具有特异性(Price等人,1998;Selkoe,19982001)。显然,E64c/Loxistatin Acid的显著抑制表明半胱氨酸蛋白酶在嗜铬囊泡中对β-分泌酶活性起作用。[4] 半胱氨酸蛋白酶作为β-分泌酶活性的证明:调节分泌泡中Aβ的产生和细胞APP的裂解[4] E64c/Loxistatin Acid抑制分离的完整分泌囊泡中Aβ(1-40)的产生,进一步说明了半胱氨酸蛋白酶活性对Aβ(1-40)产生的预测作用(图5a)。此外,当嗜铬细胞用E64c/Loxistatin Acid的细胞渗透性类似物E64d处理时,APP的12-14kDaβ-分泌酶产物的产生受到抑制(图5b;Hook等人,2002)。这些结果暗示半胱氨酸蛋白酶在神经元嗜铬细胞中APP的β分泌酶加工中起作用[4]。 |
| 体内研究 (In Vivo) |
营养不良鸡胸肌中组织蛋白酶B和组织蛋白酶H的总活性(413号线)比对照鸡(412号线)高约两倍,营养不良鸡该肌肉中组织蛋白酶D的活性高约3倍。当将合成的强效巯基抑制剂E-64-c/Loxistatin Acid以不同剂量每天皮下注射到营养不良的鸡(L413)中80天时,组织蛋白酶B和组织蛋白酶H的活性降低到对照鸡的水平(第412行),但组织蛋白酶D的活性没有变化,组织蛋白酶D在体外对LoxistatinAcid/E-64-c不敏感。[2]
大鼠左侧大脑中动脉闭塞3天后,左侧大脑半球的微管相关蛋白2(MAP2)水平显著降低至对照水平的29+/-16.3%。由于MAP2是钙蛋白酶的底物之一,因此合成钙蛋白酶抑制剂E-64c/Loxistatin Acid以400mg/kg的剂量每天两次给药,持续3天,第一剂在缺血发生前给药。E-64c在体内显著抑制了这种耗竭(P小于0.05),使MAP2水平增加到对照水平的55+/-25.7%。E-64c/Loxistatin Acid对缺血诱导的髓鞘相关糖蛋白耗竭没有显著影响。使用假手术大鼠作为对照。我们的研究结果表明,钙蛋白酶部分参与MAP2的降解,钙蛋白酶抑制剂的使用可能是治疗脑缺血的一种有用的临床方法。[3] 在营养不良鸡的胸肌中,Loxistatin Acid (E-64C) 可使组织蛋白酶 B 和组织蛋白酶 H 的活性增加正常化。E-64C 抑制大鼠大脑中动脉闭塞后脑蛋白的缺血性降解。 |
| 酶活实验 |
β-分泌酶测定中在没有还原剂的情况下纯化BACE 1时缺乏半胱氨酸蛋白酶活性的检测[4]
令人感兴趣的是,从人脑组织中纯化BACE 1所使用的测定不包括还原条件(Sinha等人,1999)。该测定中没有还原剂,这解释了从脑组织中纯化如何产生BACE 1,而在还原条件下对分泌囊泡的研究检测到半胱氨酸蛋白酶作为β-分泌酶的活性(Hook等人,2002)。有趣的是,对BACE 1敲除小鼠的研究表明,神经元中的β-分泌酶活性降低。然而,这些研究在没有还原条件和存在大量半胱氨酸蛋白酶抑制剂Loxistatin Acid/E64c的情况下测量了β-分泌酶的活性(Roberds等人,2001)。因此,这些研究无法确定半胱氨酸蛋白酶。 |
| 动物实验 |
犬:本研究选取83只平均体重11.2 kg的杂种犬。通过静脉注射硫喷妥钠(7 mg/kg)使犬只失去意识。A组(n = 17)在血管闭塞前和再灌注后分别静脉注射溶于饱和碳酸氢钠溶液的E-64c(100 mg/kg),而B组(n = 17)在上述时间段内仅注射溶剂。剩余的49只犬(C组和D组)在同一水平永久结扎左前降支(LAD)。在结扎前和结扎后1小时,分别静脉注射溶剂(D组;n = 25)或洛司他汀酸(100 mg/kg)。估计心肌内洛司他汀酸的分子浓度是总mCANP的1000倍,E-64c的剂量旨在用于潜在的临床实践。
|
| 毒性/毒理 (Toxicokinetics/TK) |
123664 大鼠腹腔注射 LD50 2140 mg/kg 行为:嗜睡(总体活动抑制);行为:共济失调;肺、胸腔或呼吸:呼吸困难。《药品研究》,17(736),1986
123664 大鼠静脉注射 LD50 >1 gm/kg。《药品研究》,17(736),1986 123664 小鼠腹腔注射 LD50 2400 mg/kg 行为:嗜睡(总体活动抑制);行为:共济失调;肺部、胸部或呼吸:呼吸困难 Iyakuhin Kenkyu。医疗用品研究。, 17(736), 1986 123664 小鼠静脉注射 LD50 >1 gm/kg Iyakuhin Kenkyu。医疗用品研究,17(736),1986 |
| 参考文献 | |
| 其他信息 |
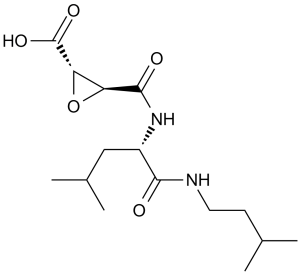
E-64c 是亮氨酸衍生物。
本文重点关注β-淀粉样蛋白 (Aβ) 肽在调节性分泌途径中的产生和分泌,以及该过程与阿尔茨海默病中毒性Aβ积累的关系。新发现表明,大部分Aβ以活性依赖的方式通过神经元中的调节性分泌途径产生和分泌。只有少量细胞Aβ通过基础的、组成型分泌途径分泌。因此,调节性分泌囊泡含有主要的β-分泌酶,这些酶负责产生大部分分泌的Aβ。对神经元嗜铬细胞调节性分泌囊泡中β-分泌酶活性的研究表明,半胱氨酸蛋白酶占β-分泌酶活性的大部分。BACE 1存在于调节性分泌囊泡中,但仅提供一小部分β-分泌酶活性。此外,半胱氨酸蛋白酶活性倾向于切割野生型β-分泌酶位点,这与大多数阿尔茨海默病(AD)病例相关。相反,BACE 1 倾向于切割瑞典突变型β-分泌酶位点,该位点在少数AD患者中表达。这些新发现引出了一个统一的假说:半胱氨酸蛋白酶是主要调控分泌途径中Aβ产生的主要β-分泌酶,而BACE 1是次要组成型分泌途径中Aβ产生的主要β-分泌酶。这些结果表明,抑制多种蛋白酶可能是降低Aβ产生、治疗阿尔茨海默病的一种策略。[4] 半胱氨酸蛋白酶作为β-分泌酶在调控分泌囊泡(a)和神经元嗜铬细胞(b)中产生Aβ的证据。 a:半胱氨酸蛋白酶抑制剂E64c/洛西他汀酸抑制嗜铬细胞囊泡中Aβ(1–40)的生成。将裂解的嗜铬细胞囊泡在37°C(pH 5.5,用DTT调节)下孵育不同时间,分别在有(实心圆点)或无(空心圆点)半胱氨酸蛋白酶抑制剂E64c(10 μM)的情况下进行。采用放射免疫分析法测定不同孵育时间下Aβ(1–40)的含量。b:半胱氨酸蛋白酶抑制剂减少嗜铬细胞中APP衍生的β-分泌酶产物。通过抗Aβ(1–40)抗体在SDS-PAGE凝胶上进行免疫沉淀和放射自显影,检测到了β-分泌酶产生的12–14 kDa 35S-COOH末端APP片段。与未刺激的对照组(泳道1)相比,佛波醇肉豆蔻酸酯(PMA)刺激了12–14 kDa COOH末端片段的生成(泳道2)。然而,E64c/洛西他汀酸的细胞渗透性类似物E64d降低了β-分泌酶产生的APP COOH末端产物的生成(泳道3)。[4] |
| 分子式 |
C15H26N2O5
|
|
|---|---|---|
| 分子量 |
314.38
|
|
| 精确质量 |
314.184
|
|
| 元素分析 |
C, 57.31; H, 8.34; N, 8.91; O, 25.45
|
|
| CAS号 |
76684-89-4
|
|
| 相关CAS号 |
|
|
| PubChem CID |
123664
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.2±0.1 g/cm3
|
|
| 沸点 |
596.4±50.0 °C at 760 mmHg
|
|
| 闪点 |
314.5±30.1 °C
|
|
| 蒸汽压 |
0.0±3.6 mmHg at 25°C
|
|
| 折射率 |
1.504
|
|
| LogP |
1.36
|
|
| tPSA |
108.03
|
|
| 氢键供体(HBD)数目 |
3
|
|
| 氢键受体(HBA)数目 |
5
|
|
| 可旋转键数目(RBC) |
9
|
|
| 重原子数目 |
22
|
|
| 分子复杂度/Complexity |
422
|
|
| 定义原子立体中心数目 |
3
|
|
| SMILES |
O=C([C@H]1O[C@@H]1C(N[C@H](C(NCCC(C)C)=O)CC(C)C)=O)O
|
|
| InChi Key |
SCMSYZJDIQPSDI-SRVKXCTJSA-N
|
|
| InChi Code |
InChI=1S/C15H26N2O5/c1-8(2)5-6-16-13(18)10(7-9(3)4)17-14(19)11-12(22-11)15(20)21/h8-12H,5-7H2,1-4H3,(H,16,18)(H,17,19)(H,20,21)/t10-,11-,12-/m0/s1
|
|
| 化学名 |
(2S,3S)-3-[[(2S)-4-methyl-1-(3-methylbutylamino)-1-oxopentan-2-yl]carbamoyl]oxirane-2-carboxylic acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (6.62 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (6.62 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (6.62 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: Saline: 2mg/mL 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.1809 mL | 15.9043 mL | 31.8086 mL | |
| 5 mM | 0.6362 mL | 3.1809 mL | 6.3617 mL | |
| 10 mM | 0.3181 mL | 1.5904 mL | 3.1809 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。