| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 10g |
|
||
| Other Sizes |
|
| 靶点 |
Progesterone receptor; Endogenous Metabolite
Phosphatidylinositol 3-Kinase (PI3K)/Akt/Nuclear Factor-kappaB (NF-κB) Pathway: Medroxyprogesterone acetate (MPA) activates this pathway to upregulate cyclin D1 [1] - Cell Adhesion Molecules (VCAM-1, ICAM-1): MPA upregulates their expression in endothelial cells [2] |
|---|---|
| 体外研究 (In Vitro) |
在类固醇剥夺的 HUVEC 中,醋酸甲羟孕酮(10 和 0.5 nM,48 小时)抑制 eNOS 表达 [2]。 Medroxyprogesteroneacetate(10和0.5nM,16小时)降低内皮粘附分子(VCAM-1和ICAM-1蛋白)的表达,从而防止白细胞粘附到人内皮细胞(类固醇剥夺的HUVEC)上[2]。在类固醇剥夺的 HUVEC 中,醋酸甲羟孕酮(10 和 0.5 nM,2 小时)可减少 NF-κB 核易位 [2]。
1. 人乳腺癌细胞增殖诱导([1]): 用MPA(10–1000 nM)处理T47D和MCF-7(PR阳性乳腺癌)细胞48小时,呈浓度依赖促进增殖。100 nM时,T47D细胞活力较对照升高35%,MCF-7升高30%(MTT实验)。蛋白质印迹法显示,100 nM MPA使cyclin D1蛋白水平在T47D中升高2.5倍,MCF-7中升高2倍;用PI3K抑制剂(LY294002,10 μM)或NF-κB抑制剂(PDTC,20 μM)处理后,MPA诱导的cyclin D1上调和增殖被阻断(活力仅较对照高10%)[1] 2. 单核细胞-内皮细胞相互作用增强([2]): 人脐静脉内皮细胞(HUVECs)用MPA(10–1000 nM)处理24小时,100 nM时VCAM-1 mRNA升高3倍,ICAM-1 mRNA升高2.5倍(实时PCR),对应蛋白水平分别升高2.8倍和2.2倍(蛋白质印迹法)。在流动条件(1 dyn/cm²)下,100 nM MPA使荧光标记的THP-1单核细胞与HUVECs的黏附率升高40%(荧光显微镜计数)[2] 3. 甲状腺癌细胞细胞因子下调([6]): 用MPA(1–10 μM)处理KTC-2(间变性甲状腺癌)细胞48小时,10 μM时IL-6分泌降低55%(ELISA),PTHrP mRNA降低60%(实时PCR)。MTT实验显示,10 μM MPA对细胞活力无显著影响(活力>90%)[6] 4. 无神经保护作用([5]): 大鼠原代海马神经元在谷氨酸损伤前用MPA(1–10 μM)处理,MPA未减少神经元死亡(乳酸脱氢酶释放与损伤对照无差异),也未上调神经保护蛋白(BDNF、Bcl-2)[5] |
| 体内研究 (In Vivo) |
大鼠灌胃给予 5 mg/kg 醋酸甲羟孕酮,观察到 AUC0-2535.9 ng·h/mL,t1/2 为 10.2 小时,Cmax 为 377.9 ng/mL [3]。在 14 天的过程中,口服醋酸甲羟孕酮(0.05-0.2 mg/kg/天)的大鼠显示,除肾上腺外的所有组织中别孕酮水平均有所增加,并且海马中的 β-END 水平发生了变化 [4]。
甲羟孕酮(27.7 μg/天,皮下注射)虽能增强血栓形成,但能抑制动脉血管血栓形成[3]。 MPA和MPA + e2治疗的动物表现出加重的血栓反应,表现为稳定闭塞的时间显著缩短。MPA的促血栓作用与ETP升高平行,而血小板活化不受影响。此外,MPA + E2减少了α -平滑肌肌动蛋白阳性细胞的数量,增加了斑块基质中的透明质酸。有趣的是,总斑块负担减少了MPA,但MPA + E2没有变化[3]。 结论和意义:长期服用MPA和MPA + E2可增加apoe缺陷小鼠动脉血栓形成,尽管MPA对动脉粥样硬化有抑制作用。凝血酶形成增加,平滑肌含量减少和非胶原斑块基质重塑可能参与促血栓作用。因此,MPA对动脉血栓形成和动脉粥样硬化的影响不同[3]。 甲羟孕酮醋酸酯(MPA)和MPA + e2治疗的动物表现出加重的血栓反应,表现为稳定闭塞的时间显著缩短。MPA的促血栓作用与ETP升高平行,而血小板活化不受影响。此外,MPA + E2减少了α -平滑肌肌动蛋白阳性细胞的数量,增加了斑块基质中的透明质酸。有趣的是,MPA降低了总斑块负担,但MPA + E2没有改变。 结论和意义:长期服用MPA和MPA + E2可增加apoe缺陷小鼠动脉血栓形成,尽管MPA对动脉粥样硬化有抑制作用。凝血酶形成增加,平滑肌含量减少和非胶原斑块基质重塑可能参与促血栓作用。因此,MPA对动脉血栓形成和动脉粥样硬化的影响是不同的。[4] 1. 小鼠血栓与动脉粥样硬化影响([3]): - 血栓模型:8–10周龄雄性C57BL/6小鼠皮下注射MPA(1、5、10 mg/kg/天),连续14天。10 mg/kg剂量使尾出血时间缩短30%,三氯化铁诱导的颈动脉血栓形成率升高40%。 - 动脉粥样硬化模型:12周龄ApoE⁻/⁻小鼠口服MPA(5 mg/kg/天),连续12周。主动脉根部斑块面积较对照增加25%,巨噬细胞浸润增多(CD68免疫组化)[3] 2. 大鼠无神经保护作用([5]): 10周龄雌性SD大鼠在海马缺血再灌注损伤前,皮下注射MPA(2 mg/kg/天),连续7天。MPA未减少梗死体积(TTC染色),也未改善认知功能(Morris水迷宫逃避潜伏期无缩短)[5] |
| 酶活实验 |
卵巢激素黄体酮在不同的神经变性实验模型中具有神经保护作用。在神经系统中,孕酮通过5 α还原酶代谢为5 α -二氢孕酮(DHP)。DHP随后通过3 -羟基类固醇脱氢酶催化的可逆反应还原为3 -,5 -四氢孕酮(THP)。[5]
醋酸甲羟孕酮(MPA)诱导乳腺癌细胞增殖的机制尚不清楚。本研究探讨了MPA影响孕激素受体(PR)阳性T47D人乳腺癌细胞中cyclin D1表达的机制。MPA (10 nM)处理48 h,细胞增殖率达到1.6倍。MPA诱导细胞周期蛋白D1表达(诱导率为3.3倍),选择性PR拮抗剂RU486阻断MPA诱导的细胞增殖和细胞周期蛋白D1表达(抑制率为23%)。MPA使转染PRB而不转染PRA的MCF-7细胞中cyclin D1的蛋白水平(诱导率为2.2倍)和启动子活性(诱导率为2.7倍)均升高。虽然MPA转录激活了cyclin D1的表达,但cyclin D1启动子没有孕激素应答元件相关序列。我们进一步研究了cyclin D1表达调控的机制。由于cyclin D1启动子包含三个假定的核因子- kappab (NFkappaB)结合基序,并且NFkappaB是Akt的底物,因此我们研究了磷脂酰肌醇3-激酶(PI3K)/Akt/NFkappaB级联对cyclin D1对MPA的反应的影响。MPA诱导Akt瞬时磷酸化(5 min诱导2.7倍),PI3K抑制剂(wortmannin)处理可减弱MPA诱导的cyclin D1表达上调(抑制40%)和细胞增殖(抑制40%)。MPA还诱导了NFkappaBalpha抑制剂(IkappaBalpha)的磷酸化(诱导率为2.3倍),而wortmannin处理可减弱MPA诱导的IkappaBalpha磷酸化(抑制率为60%)。用IkappaBalpha磷酸化抑制剂(BAY 11-7085)或特异性NFkappaB核易位抑制剂(SN-50)处理可以减弱mpa诱导的cyclin D1表达上调(分别抑制80%和50%)和细胞增殖(分别抑制55%和34%)。由于MPA诱导Akt的短暂磷酸化,且cyclin D1启动子不含孕酮响应元件相关序列,因此MPA通过PRB通过PI3K/Akt/NFkappaB级联上调cyclin D1表达诱导细胞增殖可能是非基因组机制[1]。 本文首次利用秀丽隐杆线虫(Cunninghamella elegans)、玫瑰毛霉(Trichothecium roseum)和铅毛霉(Mucor plumbeus)研究了甲氧孕酮(1)的真菌转化。得到的代谢物如下:6β,20-dihydroxymedroxyprogesterone(2), 12个β-hydroxymedroxyprogesterone(3), 6β,11β-dihydroxymedroxyprogesterone(4), 16β-hydroxymedroxyprogesterone(5), 11α,17-dihydroxy-6α-methylpregn-4-ene-3, 20-dione (6), 11-oxo-medroxyprogesterone(7) 6α-methyl-17α-hydroxypregn-1, 4-diene-3, 20-dione(8)和6β-hydroxymedroxyprogesterone(9), 15β-hydroxymedroxyprogesterone(10), 6α-methyl-17α,11β-dihydroxy-5α-pregnan-3, 20-dione(11), 11个β-hydroxymedroxyprogesterone(12)和11α,20-dihydroxymedroxyprogesterone(13)。在所有微生物转化产物中,新分离的生物转化产物13对SH-SY5Y细胞的增殖活性最强。化合物12、5、6、9、11和3对SH-SY5Y肿瘤细胞系也显示出一定程度的活性(活性由高到低)。从未报道过的生物转化产物2显示出对乙酰胆碱酯酶最有效的抑制活性。进行分子模拟研究是为了了解观察到的实验活动,也为了获得更多关于生物转化产物与酶之间的结合模式和相互作用的信息。[4] |
| 细胞实验 |
免疫荧光[2]
细胞类型:100 ng/ml LPS 处理的内皮细胞 测试浓度:10 和 0.5 nM 孵育时间:2h 实验结果:抑制NF-κB核转位。 在HUVECs中,通过实时PCR检测粘附分子mRNA水平。免疫细胞化学和酶联免疫吸附测定蛋白表达。为了模拟单核细胞粘附内皮细胞,我们使用了一个流动室系统来评估孕激素对U937单核细胞粘附HUVEC单层的影响。我们还研究了小干扰rna对粘附分子的抑制作用。[2] 从甲状腺癌复发伴甲状腺乳头状癌间变性的恶性胸腔积液中建立了一种新的甲状腺癌细胞系KTC-2。核型分析显示有109条染色体。皮下细胞注射在胸腺或严重联合免疫缺陷疾病(SCID)小鼠中产生小的退行性肿瘤。组织学检查显示间变性肿瘤细胞被突出的单核细胞包围。检测到甲状腺球蛋白、甲状腺转录因子-1和PAX-8的表达,但未检测到甲状腺过氧化物酶和促甲状腺激素(TSH)受体。生化分析显示分泌白介素(IL)-6、甲状旁腺激素相关蛋白(PTHrP)和粒细胞-巨噬细胞集落刺激因子。已知所有细胞因子均可诱导间变性甲状腺癌患者的副肿瘤综合征。我们之前的研究表明,醋酸甲羟孕酮(MPA)可降低人乳腺癌细胞IL-6和PTHrP的分泌。为了研究这些细胞因子的分泌调节机制,我们给KTC-2细胞注射MPA。MPA呈剂量依赖性降低IL-6和PTHrP的分泌及mRNA表达。雄激素受体和糖皮质激素受体(GR)均有表达,孕激素受体未见表达。地塞米松能降低IL-6和PTHrP的分泌,而双氢睾酮和孕酮不能。这些结果表明,MPA作为GR介导的糖皮质激素,可降低KTC-2细胞中IL-6和PTHrP的分泌。KTC-2细胞系可能是开发抗间变性甲状腺癌引起的副肿瘤综合征新策略的合适模型。[6] 1. 乳腺癌细胞实验([1]): - 细胞培养:T47D/MCF-7细胞接种于含10%胎牛血清的RPMI 1640培养基,96孔板(5×10³细胞/孔)或6孔板(2×10⁵细胞/孔)。 - 药物处理:贴壁24小时后,用MPA(10–1000 nM)单独或与PI3K抑制剂(LY294002,10 μM)/NF-κB抑制剂(PDTC,20 μM)共处理48小时。 - 检测: 1. 增殖:MTT实验(570 nm吸光度)计算活力; 2. 蛋白表达:蛋白质印迹法检测cyclin D1、p-Akt、p-NF-κB(以β-肌动蛋白为内参)[1] 2. 内皮-单核细胞相互作用实验([2]): - 细胞培养:HUVECs接种于24孔板(1×10⁵细胞/孔)培养至融合;THP-1单核细胞用CM-DiI荧光染料标记。 - 药物处理:HUVECs用MPA(10–1000 nM)处理24小时,加入THP-1细胞(5×10⁴细胞/孔),在流动条件(1 dyn/cm²)下孵育30分钟。 - 检测: 1. 黏附:荧光显微镜计数黏附的THP-1细胞; 2. 基因/蛋白:实时PCR检测VCAM-1/ICAM-1 mRNA,蛋白质印迹法检测对应蛋白[2] 3. 甲状腺癌细胞实验([6]): - 细胞培养:KTC-2细胞接种于含10%胎牛血清的DMEM培养基,6孔板(1×10⁵细胞/孔)。 - 药物处理:用MPA(1–10 μM)处理48小时。 - 检测: 1. 细胞因子分泌:ELISA检测培养上清中IL-6; 2. 基因表达:实时PCR检测PTHrP mRNA(以GAPDH为内参)[6] |
| 动物实验 |
载脂蛋白E (ApoE)-/-小鼠接受双侧卵巢切除术,并分别接受安慰剂、MPA(27.7 μg/天)和MPA+17β-雌二醇(E2;1.1 μg/天)治疗90天,同时喂以西式饮食。采用光血栓模型检测血栓反应,通过荧光激活细胞分选 (FACS) 分析(CD62P)检测血小板活化,并通过内源性凝血酶生成潜能 (ETP) 检测凝血酶生成。此外,还测定了主动脉斑块负荷和主动脉根部斑块组成。[3]
卵巢切除术和激素治疗[7] 大鼠被随机分为五组:假手术组(卵巢完整)、卵巢切除组 (OVX)、卵巢切除+孕酮组 (OVX+PROG)、卵巢切除+低剂量MPA组和卵巢切除+高剂量MPA组。在行为学测试前约两个月,所有大鼠均接受了卵巢切除术(OVX)或假手术。所有大鼠均采用异氟烷吸入麻醉。接受卵巢切除术的大鼠在皮肤和腹膜上进行双侧背外侧切口,结扎并切除卵巢和子宫角尖端。然后缝合肌肉和皮肤。接受假手术的大鼠进行相同的皮肤切口和缝合。手术时,将含有丙二醇(溶剂)、孕酮(PROG;21 mg溶于2 mL丙二醇)或醋酸甲羟孕酮(MPA)(低剂量:14 mg;高剂量:21 mg,溶于2 mL丙二醇)的Alzet渗透泵(2ML4)植入颈背皮下。在整个行为学测试和处死过程中持续给药。剂量参考既往研究(Zhang、Fishman 和 Huang,1999),并乘以 10 以补偿小鼠到大鼠体重的差异。术后,大鼠接受利马迪尔(Rimadyl,5 mg/mL/kg)镇痛,并注射生理盐水(2 mL)以防止脱水。动物每 31-32 天接受一次泵植入手术;行为学测试在首次泵植入后 66 天开始。因此,在行为测试和处死过程中持续进行激素给药。[7] 1. 小鼠血栓/动脉粥样硬化方案 ([3]): - 血栓模型: 1. 动物选择:8-10 周龄雄性 C57BL/6 小鼠(每组 n=6),随机分为对照组、1、5、10 mg/kg 的 MPA 组。 2. 药物制备:将 MPA 溶于芝麻油中(0.1、0.5、1 mg/mL)。 3. 给药:皮下注射(0.1 mL/10 g 体重),每日一次,持续 14 天。 4. 检测:测量尾部出血时间;氯化铁诱导颈动脉血栓形成,记录血栓形成率。 - 动脉粥样硬化模型: 1. 动物选择:12周龄ApoE⁻/⁻小鼠(每组n=6),喂以高脂饮食。 2. 药物制备:MPA悬浮于0.5% CMC + 0.1% Tween 80溶液中(0.5 mg/mL)。 3. 给药:每日一次,灌胃(10 mL/kg),持续12周。 4. 检测:取主动脉根部切片进行H&E染色(斑块区域)和CD68免疫组化(巨噬细胞)[3]。 2. 大鼠神经保护方案([5]): - 动物选择:10周龄雌性Sprague-Dawley大鼠(每组n=5),随机分为对照组、损伤组、损伤+MPA。 - 药物配制:MPA溶于5%乙醇+95%生理盐水(0.2 mg/mL)。 - 给药途径:皮下注射(10 mL/kg),每日一次,连续7天(首次注射于缺血前24小时)。 - 检测:通过TTC染色测量海马梗死体积;通过Morris水迷宫(逃避潜伏期)评估认知功能[5]。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服醋酸甲羟孕酮 (MPA) 的吸收因制剂而异。1000mg 口服剂量平均血药浓度峰值 (Cmax) 为 145-315nmol/L,而 500mg 口服剂量平均血药浓度峰值 (Cmax) 为 33-178nmol/L,达峰时间 (Tmax) 为 1-3 小时,滞后时间为半小时。500mg 口服 MPA 的 AUC 为 543.4-1981.1nmol/L/h,具体数值取决于制剂。肌注 MPA 的血药浓度峰值 (Cmax) 为 4.69±1.52nmol/L,达峰时间为 4.75±2.09 天,AUC 为 81.58±27.64 天·mol/L。皮下注射醋酸甲羟孕酮(MPA)的血药浓度峰值(Cmax)为3.83±1.56 nmol/L,达峰时间(Tmax)为6.52±2.07天,曲线下面积(AUC)为72.26±38.73天·mol/L。然而,MPA的药代动力学也可能因注射部位而异。 大部分醋酸甲羟孕酮(MPA)以葡萄糖醛酸苷结合物的形式经尿液排出,少量以硫酸盐结合物排出。粪便中也可检测到葡萄糖醛酸苷结合物。由于尿液中的代谢物谱差异不显著,且放射性标记研究不易获得,因此难以确定尿液和粪便中代谢物与母体化合物的确切比例。 醋酸甲羟孕酮的分布容积为20±3升。 醋酸甲羟孕酮(MPA)的平均清除率为1668±146升/天或21.9±4.3升/公斤/天。由于MPA药代动力学存在较高的患者间差异,据报道其清除率为1600-4000升/天。 代谢/代谢物 醋酸甲羟孕酮经β-羟基化生成代谢物6-β-羟基(M-2)、2-β-羟基(M-4)和1-β-羟基醋酸甲羟孕酮(M-3)。 M-2 和 M-4 进一步代谢为 2β,6β-二羟基甲羟孕酮 (M-1)。M-3 进一步代谢为 1,2-脱氢甲羟孕酮醋酸酯 (M-5)。 甲羟孕酮醋酸酯已知的代谢产物包括 M-3、甲羟孕酮醋酸酯和 M-2。 主要代谢途径:肝脏。 排泄途径:口服后,MPA 在肝脏中主要通过羟基化代谢,随后进行结合反应,最终经尿液排出。大多数 MPA 代谢物以葡萄糖醛酸苷结合物的形式经尿液排出,仅有少量以硫酸盐形式排出。 半衰期:50 天 生物半衰期 口服醋酸甲羟孕酮 (MPA) 的吸收半衰期为 15-30 分钟,生物半衰期为 40-60 小时。肌注 MPA 的吸收半衰期为 0.86±0.30 天,消除半衰期为 24.03±21.74 天。皮下注射 MPA 的吸收半衰期为 1.05±0.56 天,消除半衰期为 30.90±15.11 天。 |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性总结
孕激素可自由扩散到女性生殖道、乳腺、下丘脑和垂体中的靶细胞,并与孕激素受体结合。孕激素与受体结合后,会减缓下丘脑促性腺激素释放激素 (GnRH) 的释放频率,并抑制排卵前黄体生成素 (LH) 的峰值。 1. 体外毒性: - MPA (10 μM) 对 KTC-2 细胞无细胞毒性(细胞活力 >90%,MTT 法)[6] - MPA (1–10 μM) 未诱导神经元坏死(乳酸脱氢酶释放量 <15% vs. 对照组)[5] 2. 体内毒性: - 小鼠接受 MPA (1–10 mg/kg/天,14–84 天) 治疗后,ALT/AST、BUN 或体重均无变化 [3] - 大鼠接受 MPA (2 mg/kg/天,7天)未见肝肾损伤(血清生化指标正常)[5] |
| 参考文献 |
[1]. Medroxyprogesterone acetate induces cell proliferation through up-regulation of cyclin D1 expression via phosphatidylinositol 3-kinase/Akt/nuclear factor-kappaB cascade in human breast cancer cells. Endocrinology. 2005 Nov;146(11):4917-25.
[2]. Medroxyprogesterone acetate enhances monocyte-endothelial interaction under flow conditions by stimulating the expression of cell adhesion molecules. J Clin Endocrinol Metab. 2014 Jun;99(6):2188-97. [3]. Differential effects of medroxyprogesterone acetate on thrombosis and atherosclerosis in mice. Br J Pharmacol. 2009 Dec;158(8):1951-60. [4]. Medroxyprogesterone derivatives from microbial transformation as anti-proliferative agents and acetylcholineterase inhibitors (combined in vitro and in silico approaches). Steroids. 2020 Dec;164:108735. [5]. Reduced metabolites mediate neuroprotective effects of progesterone in the adult rat hippocampus. The synthetic progestin medroxyprogesterone acetate (Provera) is not neuroprotective. J Neurobiol.2006 Aug;66(9):916-28; [6]. Medroxyprogesterone acetate decreases secretion of interleukin-6 and parathyroid hormone-related protein in a new anaplastic thyroid cancer cell line, KTC-2. Thyroid.2003;13(3):249-58; [7]. Medroxyprogesterone acetate impairs memory and alters the GABAergic system in aged surgically menopausal rats. Neurobiol Learn Mem.2010;93(3):444-53. |
| 其他信息 |
根据世界卫生组织国际癌症研究机构 (IARC) 的说法,醋酸甲羟孕酮可能致癌。根据州或联邦政府的标签要求,它可能具有发育毒性。
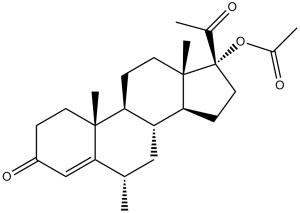
醋酸甲羟孕酮是一种无臭的白色至类白色微晶粉末。(NTP, 1992) 醋酸甲羟孕酮是一种乙酸酯,由甲羟孕酮的 17α-羟基与乙酸的羧基缩合而成。它是一种广泛用于更年期激素治疗和仅含孕激素避孕的孕激素。它具有多种功能,包括孕激素、雄激素、女性避孕药、合成口服避孕药、佐剂、抑制剂、抗氧化剂和抗肿瘤药。它是一种甾体酯、乙酸酯、20-氧代甾体、3-氧代-Δ⁴甾体和皮质类固醇。其功能与甲羟孕酮相关。 醋酸甲羟孕酮 (MPA) 是一种孕酮衍生物,其代谢稳定性更高,因此具有更优的药代动力学特性。MPA 可用于治疗继发性闭经、子宫内膜增生、异常子宫出血、骨质疏松症、更年期血管舒缩症状、外阴和阴道萎缩、避孕、缓解子宫内膜异位症疼痛,也可用于子宫内膜癌和肾癌的姑息治疗。醋酸甲羟孕酮于 1959 年 6 月 18 日获得 FDA 批准。 醋酸甲羟孕酮是性激素孕酮的合成乙酸衍生物。醋酸甲羟孕酮 (NCI04) 醋酸甲羟孕酮(INN、USAN、BAN),又称17'-羟基-6'-甲基孕酮醋酸酯,通常缩写为MPA,是一种甾体类孕激素,是人类激素孕酮的合成衍生物。它可用作避孕药、激素替代疗法药物,并用于治疗子宫内膜异位症以及其他多种适应症。MPA是其母体化合物甲羟孕酮 (MP) 的更强效衍生物。虽然甲羟孕酮有时被用作醋酸甲羟孕酮的同义词,但通常使用的药物是MPA而非MP。 一种源自17-羟孕酮的合成孕激素。它是一种长效避孕药,口服或肌注均有效,也曾用于治疗乳腺和子宫内膜肿瘤。 药物适应症 醋酸甲羟孕酮 (MPA) 口服片适用于治疗继发性闭经,降低绝经后妇女子宫内膜增生的发生率,以及治疗由激素失衡而非器质性病变引起的异常子宫出血。含有 MPA 和结合雌激素的口服片适用于预防绝经后骨质疏松症,以及治疗中度至重度更年期症状,例如血管舒缩症状、外阴萎缩和阴道萎缩。皮下注射 MPA 适用于预防妊娠和治疗子宫内膜异位症相关疼痛。肌注醋酸甲羟孕酮(MPA)适用于预防妊娠,高浓度时可用于子宫内膜癌或肾癌的姑息治疗。 FDA标签 作用机制 醋酸甲羟孕酮(MPA)抑制促性腺激素的产生,从而阻止卵泡成熟和排卵,这是其发挥避孕作用的原因。此作用还会使子宫内膜变薄。MPA可减少子宫内膜上皮细胞中的核雌激素受体和DNA合成。 MPA 还能诱导某些癌细胞系发生 p53 依赖性凋亡,并抑制 GABA-A 受体。 药效学 醋酸甲羟孕酮 (MPA) 抑制促性腺激素的产生,减少子宫内膜上皮细胞中的核雌激素受体和 DNA 合成,并诱导癌细胞系发生 p53 依赖性凋亡。MPA 口服片剂的半衰期为 40-60 小时,其他制剂的半衰期可能更长,因此其作用持续时间较长。MPA 的治疗窗较宽,患者每日口服剂量可从 5mg 到每周注射 1000mg 不等。长期使用 MPA 与骨密度降低有关,青春期服用 MPA 的患者峰值骨量可能低于未接受治疗的患者,这也会增加未来患骨质疏松症和骨折的风险。 1.药物背景([1][3]): 醋酸甲羟孕酮是一种合成孕激素,广泛用于避孕、激素替代疗法和激素敏感性癌症(例如乳腺癌、子宫内膜癌)的治疗[1][3] 2. 作用机制([1][2][6]): - 在乳腺癌细胞中:激活PI3K/Akt/NF-κB通路,上调细胞周期蛋白D1,促进细胞增殖[1] - 在内皮细胞中:上调VCAM-1/ICAM-1,增强单核细胞黏附,促进血管炎症[2] - 在甲状腺癌细胞中:下调IL-6和PTHrP的分泌,可能抑制肿瘤进展[6] 3.局限性([5]): 与孕酮(内源性孕激素)不同,MPA由于无法代谢为具有神经活性的还原代谢物,因此缺乏神经保护作用[5] |
| 分子式 |
C24H34O4
|
|
|---|---|---|
| 分子量 |
386.52
|
|
| 精确质量 |
386.245
|
|
| 元素分析 |
, 74.58; H, 8.87; O, 16.56
|
|
| CAS号 |
71-58-9
|
|
| 相关CAS号 |
Medroxyprogesterone acetate;71-58-9; 520-85-4
|
|
| PubChem CID |
6279
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.1±0.1 g/cm3
|
|
| 沸点 |
496.4±45.0 °C at 760 mmHg
|
|
| 熔点 |
206-207 °C(lit.)
|
|
| 闪点 |
213.2±28.8 °C
|
|
| 蒸汽压 |
0.0±1.3 mmHg at 25°C
|
|
| 折射率 |
1.539
|
|
| LogP |
4.11
|
|
| tPSA |
60.44
|
|
| 氢键供体(HBD)数目 |
0
|
|
| 氢键受体(HBA)数目 |
4
|
|
| 可旋转键数目(RBC) |
3
|
|
| 重原子数目 |
28
|
|
| 分子复杂度/Complexity |
767
|
|
| 定义原子立体中心数目 |
7
|
|
| SMILES |
C[C@H]1C[C@@H]2[C@H](CC[C@]3([C@H]2CC[C@@]3(C(=O)C)OC(=O)C)C)[C@@]4(C1=CC(=O)CC4)C
|
|
| InChi Key |
PSGAAPLEWMOORI-PEINSRQWSA-N
|
|
| InChi Code |
InChI=1S/C24H34O4/c1-14-12-18-19(22(4)9-6-17(27)13-21(14)22)7-10-23(5)20(18)8-11-24(23,15(2)25)28-16(3)26/h13-14,18-20H,6-12H2,1-5H3/t14-,18+,19-,20-,22+,23-,24-/m0/s1
|
|
| 化学名 |
(6S,8R,9S,10R,13S,14S,17R)-17-acetyl-6,10,13-trimethyl-3-oxo-2,3,6,7,8,9,10,11,12,13,14,15,16,17-tetradecahydro-1H-cyclopenta[a]phenanthren-17-yl acetate
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 1 mg/mL (2.59 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 10.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1 mg/mL (2.59 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 10.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 1 mg/mL (2.59 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5872 mL | 12.9359 mL | 25.8719 mL | |
| 5 mM | 0.5174 mL | 2.5872 mL | 5.1744 mL | |
| 10 mM | 0.2587 mL | 1.2936 mL | 2.5872 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。