| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Antifungal agent; 1, 3-beta-D-glucan synthesis
Micafungin Sodium (FK463) targets fungal β-1,3-glucan synthase (IC50 = 0.01–0.1 μM for Candida albicans β-1,3-glucan synthase; MIC range = 0.03–1 μg/mL against clinically relevant Candida species) [4][5] Micafungin Sodium (FK463) shows no significant inhibition of mammalian cell enzymes at therapeutic concentrations [3][4] |
|---|---|
| 体外研究 (In Vitro) |
米卡芬净是一种抗真菌剂,已知可抑制白色念珠菌中 1,3-β-D-葡聚糖的合成。在测试的 18 株铜绿假单胞菌分离株中,有 13 株米卡芬净显着降低了生物膜生物量。在测试的所有 9 株铜绿假单胞菌分离株中,米卡芬净降低了编码细胞壁 1,3-β-D-葡聚糖的 ndvB 的表达。此外,它还降低了藻酸盐和薄膜生物膜编码基因(分别为 algC 和 pelC)的表达。真菌实验:米卡芬净降低了藻酸盐和薄膜生物膜编码基因(分别为algC和pelC)的表达。
米卡芬净钠(Micafungin Sodium; FK463) 以0.1 μg/mL浓度处理24小时,抑制铜绿假单胞菌生物膜形成75%,降低生物膜生物量和代谢活性 [1] 米卡芬净钠(Micafungin Sodium; FK463) 对念珠菌属具有强效抗真菌活性:白色念珠菌MIC₉₀ = 0.03 μg/mL,光滑念珠菌MIC₉₀ = 0.125 μg/mL,克柔念珠菌MIC₉₀ = 0.25 μg/mL,热带念珠菌MIC₉₀ = 0.5 μg/mL(微量稀释法)[4][5] 米卡芬净钠(Micafungin Sodium; FK463) 以0.2 μg/mL浓度与KB425796-C联用,对烟曲霉表现出协同抗真菌活性,使KB425796-C的MIC从8 μg/mL降至1 μg/mL(部分抑菌浓度指数 = 0.5)[2] 米卡芬净钠(Micafungin Sodium; FK463) 以1 μg/mL浓度处理48小时,抑制烟曲霉菌丝生长80%,减少真菌细胞壁中β-1,3-葡聚糖合成90% [3][4] 米卡芬净钠(Micafungin Sodium; FK463) 在浓度高达64 μg/mL时,对人上皮细胞(HEp-2)或成纤维细胞无细胞毒性 [4][5] |
| 体内研究 (In Vivo) |
在败血症烟曲霉感染的小鼠模型中,米卡芬净 (0.1 mg/kg) 使小鼠的存活率提高至 20%。当米卡芬净 (0.1 mg/kg) 与 KB425796-C (32 mg/kg) 组合时,小鼠在感染后 31 天的存活率增加至 100%。而未经治疗的小鼠仅存活了 6 天。
米卡芬净钠(Micafungin Sodium; FK463) 以0.5 mg/kg/天的剂量静脉注射小鼠,持续7天,改善播散性念珠菌病(白色念珠菌)小鼠的存活率,从对照组的20%升至85%,肾脏真菌载量减少99% [3] 米卡芬净钠(Micafungin Sodium; FK463) 以1 mg/kg/天的剂量静脉注射,联合KB425796-C(5 mg/kg/天口服)治疗烟曲霉肺曲霉病小鼠,持续10天:存活率从KB425796-C单药组的30%升至70%,肺真菌载量减少85% [2] 米卡芬净钠(Micafungin Sodium; FK463) 以2 mg/kg/天的剂量静脉注射小鼠,持续5天,抑制新型隐球菌在小鼠体内的播散,脑和脾脏真菌载量分别减少90%和88% [3] 米卡芬净钠(Micafungin Sodium; FK463) 以0.3 mg/kg/天的剂量静脉注射烟曲霉感染小鼠,减少肺组织炎症,中性粒细胞浸润降低65%,促炎细胞因子(TNF-α、IL-6)水平降低55%–60% [2] |
| 酶活实验 |
本研究通过减少细胞外基质β-D-葡聚糖形成单元的合成,评估了米卡芬净对选定铜绿假单胞菌分离株生物膜形成的潜在影响。使用微量滴定板法在体外监测最佳治疗剂量10 mg ml(-1)米卡芬净对生物膜产生的影响。在大多数分离物中,生物膜形成的表型减少是显著的(基于平均光密度;p<0.05)。此外,使用定量逆转录PCR评估了海藻酸盐和膜生物膜编码基因(分别为algC和pelC)以及细胞壁1,3-β-D-葡聚糖编码基因(ndvB)的相对基因表达。对于所有测试的基因,与未经处理的样本相比,米卡芬净处理的样本的mRNA转录水平也显著降低(p<0.05)。总之,本研究表明米卡芬金是一种破坏铜绿假单胞菌生物膜结构的潜在药物,可以暴露和治疗核心浮游细胞[1]。
真菌β-1,3-葡聚糖合成酶活性实验:白色念珠菌细胞膜组分与米卡芬净钠(Micafungin Sodium; FK463)(0.001–1 μM)、UDP-葡萄糖(底物)及反应缓冲液在30°C孵育2小时;特异性染色结合分光光度法定量合成的β-1,3-葡聚糖,经剂量-反应曲线计算IC50值 [4][5] 酶选择性实验:30种哺乳动物酶(如哺乳动物葡聚糖合成酶、激酶)与米卡芬净钠(Micafungin Sodium; FK463)(10 μg/mL)及各自底物孵育;放射测量法或比色法检测酶活性,评估选择性 [3][4] |
| 细胞实验 |
将每种真菌分离物在酵母-麦芽糖 (YM) 琼脂肉汤中于 30°C 静态培养 24 小时。在YM肉汤培养基中,将新型隐球菌YC203在30℃和200rpm振荡下培养20小时。用无菌盐水洗涤培养的细胞一次,得到细胞悬浮液。在无菌盐水中收获烟曲霉 FP1305 的孢子,在马铃薯葡萄糖琼脂 (PDA) 斜面上培养四天后,通过纱布过滤收集孢子。添加 L-谷氨酰胺(不含钠)的 RPMI 1640 培养基的抗真菌活性使用微肉汤稀释法在 96 孔培养板中对所有分离株(新型隐球菌除外)进行测量,并用 0.165 m MOPS 缓冲至 pH 7.0。 YNBD(酵母氮基葡萄糖)培养基用于新型隐球菌。在测定中,将1×105 CFU/孔的测试微生物接种到每个孔中,然后将板在37℃下孵育20或48小时。显微镜观察确定两个终点:MEC(定义为真菌生长的显着下降)和 MIC(定义为生长的完全抑制)。
抗真菌MIC实验:临床分离的念珠菌属和烟曲霉接种于96孔板(1×10³ CFU/孔),用米卡芬净钠(Micafungin Sodium; FK463)(0.001–64 μg/mL)处理48小时(念珠菌)或72小时(曲霉菌);MIC₉₀定义为抑制90%真菌生长的最低浓度 [4][5] 生物膜抑制实验:铜绿假单胞菌接种于96孔板培养形成生物膜;加入米卡芬净钠(Micafungin Sodium; FK463)(0.01–2 μg/mL),24小时后结晶紫染色定量生物膜生物量;MTT实验检测代谢活性 [1] 协同作用实验:烟曲霉用米卡芬净钠(Micafungin Sodium; FK463)(0.01–4 μg/mL)与KB425796-C(0.1–16 μg/mL)联用处理72小时;计算部分抑菌浓度指数以确定协同作用 [2] 菌丝生长抑制实验:烟曲霉分生孢子接种于含米卡芬净钠(Micafungin Sodium; FK463)(0.05–2 μg/mL)的琼脂平板,孵育48小时;显微镜测量菌丝长度 [3] |
| 动物实验 |
将2.0×10⁶个烟曲霉FP1305孢子经静脉注射入8组共10只7周龄雌性DBA/2小鼠体内。各组小鼠分别接受以下治疗:腹腔注射(ip)安非他明(AMPH),每日一次(qd);皮下注射(sc)米卡芬净,剂量分别为0.1、0.32或1 mg/kg体重(qd);皮下注射米卡芬净,剂量分别为0.1、0.32或1 mg/kg体重(qd);此外,腹腔注射KB425796-C,剂量为32 mg/kg,每日两次(bid);以及注射生理盐水(bid)。于第1天和第2天给药。治疗结束后,每组5只小鼠于次日处死。无菌取出肾脏和肝脏后,在5 mL无菌生理盐水中匀浆。将匀浆液进行10倍系列稀释,涂布于PDA培养基上,然后在37℃培养48小时。计算每克组织中的菌落形成单位(CFU)数。攻毒后31天内,每天监测每组剩余5只小鼠的存活率。
播散性念珠菌病模型:ICR小鼠经静脉注射感染白色念珠菌(1×10⁶ CFU/只);感染24小时后,小鼠经静脉注射米卡芬净钠(FK463)(0.1–2 mg/kg/天,溶于生理盐水)治疗7天;监测存活率 14 天,并通过 CFU 测定法定量肾脏中的真菌负荷 [3] 肺曲霉病模型:BALB/c 小鼠经鼻内感染烟曲霉分生孢子(5×10⁶ CFU/只);感染后 4 小时,小鼠接受米卡芬净钠 (FK463)(0.5–1 mg/kg/天,静脉注射)加 KB425796-C(5 mg/kg/天,口服)治疗 10 天;评估存活率和肺部真菌负荷 [2] 播散性隐球菌病模型:C57BL/6 小鼠经静脉注射感染新型隐球菌(2×10⁵ CFU/只);小鼠接受米卡芬净钠(FK463)(0.3–2 mg/kg/天,静脉注射)治疗5天;采用菌落形成单位(CFU)测定法测定脑和脾脏中的真菌负荷[3] |
| 药代性质 (ADME/PK) |
小鼠静脉注射米卡芬净钠(FK463)(1 mg/kg)后,其终末半衰期(t1/2)为3.5小时,血浆峰浓度(Cmax)为12 μg/mL,曲线下面积(AUC₀–∞)为45 μg·h/mL [3]。米卡芬净钠(FK463)广泛分布于各组织,肾脏、肝脏和肺脏中的浓度最高(给药后2小时组织/血浆比值为3.2–4.8)[3]。约80%的药物在72小时内以原形经粪便排出,10%经尿液排出[3]。米卡芬净钠(FK463)在人体内的血浆蛋白结合率为99%。血浆中含量为98%,小鼠血浆中含量为98%[4]
|
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期用药
◉ 哺乳期用药概述 目前尚无米卡芬净在哺乳期使用的信息。由于米卡芬净与血浆蛋白的结合率超过99%,且口服生物利用度低,因此不太可能进入乳汁并被婴儿吸收。4个月以下婴儿可安全地静脉注射米卡芬净。从乳汁中吸收的量可能远低于婴儿剂量。如果母亲需要使用米卡芬净,这并非停止母乳喂养的理由。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 米卡芬净钠 (FK463) 在小鼠中显示出较低的急性毒性:LD50 = 50 mg/kg(静脉注射)[3] 在大鼠中长期给药(2 mg/kg/天,持续 28 天)未引起血清 ALT、AST、BUN 或肌酐水平的显著变化,表明无明显的肝毒性或肾毒性[3][4] 当 米卡芬净钠 (FK463) 与两性霉素联合使用时,未观察到显著的药物相互作用B 或氟康唑在体外和体内的疗效[2][3] |
| 参考文献 |
|
| 其他信息 |
米卡芬净钠是一种有机钠盐,也是一种抗生素抗真菌药物。
米卡芬净钠是米卡芬净的钠盐形式,米卡芬净是一种半合成棘白菌素类抗生素,来源于真菌Coleophoma empetri的天然产物,具有抗真菌活性。与其他环状脂肽类抗生素一样,米卡芬净以非竞争性方式抑制真菌特异性酶1,3-β-D-葡聚糖合成酶,该酶是合成真菌细胞壁重要成分1,3-β-D-葡聚糖所必需的。通过抑制1,3-β-D-葡聚糖的合成,细胞壁被削弱,导致渗透性溶解,最终导致真菌细胞死亡。 一种环状脂六肽棘白菌素类抗真菌药物,用于治疗和预防念珠菌病。 另见:米卡芬净(具有活性部分)。 药物适应症 米卡芬净适用于:成人、16岁及以上青少年和老年人,用于治疗侵袭性念珠菌病;适用于适合静脉治疗的食管念珠菌病患者;用于接受异基因造血干细胞移植的患者或预计中性粒细胞减少症(绝对中性粒细胞计数<500个/µl)持续10天或以上的患者的念珠菌感染预防。儿童(包括新生儿)和 16 岁以下青少年:用于治疗侵袭性念珠菌病;用于接受异基因造血干细胞移植的患者或预计出现中性粒细胞减少症(绝对中性粒细胞计数 < 500 个/µl)10 天或以上的患者预防念珠菌感染。使用 Mycamine 的决定应考虑发生肝肿瘤的潜在风险。因此,仅当其他抗真菌药物不适用时才应使用米卡芬净。 米卡芬净钠 (FK463)是一种水溶性脂肽类抗真菌药物,属于棘白菌素类[3][4][5] 其抗真菌机制包括抑制真菌β-1,3-葡聚糖合成酶,阻断细胞壁合成,最终导致真菌细胞裂解[3][4][5] 米卡芬净钠 (FK463)对念珠菌属和曲霉属真菌,包括氟康唑耐药菌株,均具有强效活性[4][5] 它能抑制铜绿假单胞菌生物膜的形成,提示其在治疗生物膜相关感染方面具有潜在应用价值[1] 临床上,它适用于治疗侵袭性念珠菌病、食管念珠菌病和侵袭性曲霉病。免疫功能低下患者[3][4] 该化合物对真菌酶的选择性远高于哺乳动物酶,因此具有良好的安全性[3][5] |
| 分子式 |
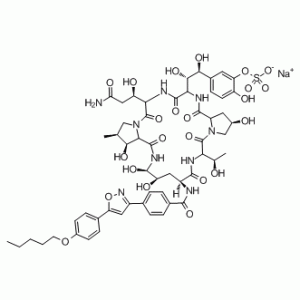
C56H70N9NAO23S
|
|---|---|
| 分子量 |
1292.26
|
| 精确质量 |
1291.42
|
| 元素分析 |
C, 52.05; H, 5.46; N, 9.76; Na, 1.78; O, 28.48; S, 2.48
|
| CAS号 |
208538-73-2
|
| 相关CAS号 |
Micafungin;235114-32-6
|
| PubChem CID |
23666118
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
518.52
|
| 氢键供体(HBD)数目 |
15
|
| 氢键受体(HBA)数目 |
24
|
| 可旋转键数目(RBC) |
18
|
| 重原子数目 |
90
|
| 分子复杂度/Complexity |
2580
|
| 定义原子立体中心数目 |
15
|
| SMILES |
O=C1[C@@]([H])(NC([C@@]([H])(NC([C@]2([H])C[C@H](CN2C([C@@]([H])(NC([C@H](C[C@H]([C@H](NC([C@]2([H])[C@H]([C@H](CN21)C)O)=O)O)O)NC(C1C=CC(C2=NOC(C3C=CC(=CC=3)OCCCCC)=C2)=CC=1)=O)=O)[C@H](O)C)=O)O)=O)[C@H](O)[C@H](C1C=CC(=C(C=1)OS(O)(=O)=O)O)O)=O)[C@H](O)CC(=O)N.[Na]
|
| InChi Key |
KOOAFHGJVIVFMZ-WZPXRXMFSA-M
|
| InChi Code |
InChI=1S/C56H71N9O23S.Na/c1-4-5-6-17-86-32-14-11-28(12-15-32)39-21-33(63-87-39)27-7-9-29(10-8-27)49(75)58-34-20-38(70)52(78)62-54(80)45-46(72)25(2)23-65(45)56(82)43(37(69)22-41(57)71)60-53(79)44(48(74)47(73)30-13-16-36(68)40(18-30)88-89(83,84)85)61-51(77)35-19-31(67)24-64(35)55(81)42(26(3)66)59-50(34)76;/h7-16,18,21,25-26,31,34-35,37-38,42-48,52,66-70,72-74,78H,4-6,17,19-20,22-24H2,1-3H3,(H2,57,71)(H,58,75)(H,59,76)(H,60,79)(H,61,77)(H,62,80)(H,83,84,85);/q;+1/p-1/t25-,26+,31+,34-,35-,37+,38+,42-,43-,44-,45-,46-,47-,48-,52+;/m0./s1
|
| 化学名 |
sodium 5-((1S,2S)-2-((2R,6S,9S,11R,12R,14aS,15S,16S,20S,23S,25aS)-20-((R)-3-amino-1-hydroxy-3-oxopropyl)-2,11,12,15-tetrahydroxy-6-((R)-1-hydroxyethyl)-16-methyl-5,8,14,19,22,25-hexaoxo-9-(4-(5-(4-(pentyloxy)phenyl)isoxazol-3-yl)benzamido)tetracosahydro-1H-dipyrrolo[2,1-c:2',1'-l][1,4,7,10,13,16]hexaazacyclohenicosin-23-yl)-1,2-dihydroxyethyl)-2-hydroxyphenyl sulfate
|
| 别名 |
FK463; FK 463; FK-463; Funguard; Mycamine; FK463; Micafungin Na; FK463 Sodium; Micafungin sodium salt; Micafungin sodium
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮和光照。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : 32 ~100 mg/mL (24.76 ~77.38 mM )
Water : ~100 mg/mL (~77.38 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (1.93 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (1.93 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (1.93 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 10% DMSO+40% PEG300+5% Tween-80+45% Saline: ≥ 2.5 mg/mL (1.93 mM) 配方 5 中的溶解度: 50 mg/mL (38.69 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. 配方 6 中的溶解度: 50 mg/mL (38.69 mM) in Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.7738 mL | 3.8692 mL | 7.7384 mL | |
| 5 mM | 0.1548 mL | 0.7738 mL | 1.5477 mL | |
| 10 mM | 0.0774 mL | 0.3869 mL | 0.7738 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04728971 | NOT YET RECRUITING | Drug:Micafungin Sodium 50 MG Injection Drug:Caspofungin Acetate |
Liver Transplantation | Shanghai General Hospital, Shanghai Jiao Tong University School of Medicine |
2022-10-01 | Phase 4 |
| NCT05784844 | RECRUITING | Drug:Meropenem Drug:Micafungin |
Febrile Neutropenia | Wake Forest University Health Sciences |
2024-08 | Phase 4 |
| NCT04738955 | UNKNOWN STATUS | Drug:Micafungin Sodium | Hematological Tumors Patients With High Risk Factors of Invasive Fungal Disease |
Shandong Provincial Hospital | 2021-02-01 | Phase 4 |
| NCT02678598 | COMPLETED | Drug:Micafungin | Invasive Fungal Infections | Astellas Pharma China,Inc. | 2015-03 | |
| NCT03174457 | COMPLETED | Drug:Micafungin | Invasive Fungal Infections | Astellas Pharma Singapore Pte.Ltd. | 2017-06-21 |
|
|
|