| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
APJ ( IC50 = 1.75 μM )
Apelin (APJ) receptor: Functionally antagonizes APJ, with >37-fold selectivity over the angiotensin II type 1 (AT1) receptor; shows no significant binding activity against 29 other GPCRs, except for <50% inhibition (I) at 10 μM against κ-opioid receptor and <70%I at 10 μM against benzodiazepinone receptor [1] - Apelin receptor (APLNR): Inhibits the apeliPLNR axis to suppress cholangiocarcinoma (CCA) growth [2] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:将细胞(血管紧张素 II 受体样 1 (AGTRL-1) 细胞系(DiscoveRx,目录号 93-0250C2))以 1000 个细胞/孔(1536 板,Corning)接种在 4 μL 中并培养过夜(16 -18 小时),37°C,5% CO2,100% 湿度,然后将 60 nL DMSO 对照或 2 mM DMSO 储备测试化合物转移到每个孔中,然后加入 2 μL 30 nM Apelin-13 至阴性对照和测试化合物孔,以及阳性对照孔中加入 2 μL 测定培养基(补充有 10% hi-FBS、1×青霉素/链霉素的 F12 营养混合物 HAM)。这样得到的测试化合物的最终浓度为 20 μM,最终 DMSO 为 1%。检测在室温下孵育 90 分钟,然后用 3 μL 检测试剂(PathHunter 检测试剂(DiscoveRx,目录号 93-0001))显色 60 分钟,并在 Perkin Elmer ViewLux 上读取发光读数。激酶测定:使用两种互补的 APJ 功能测定来评估 ML221 对 apelin-13 介导的 APJ 激活的拮抗作用;抑制 cAMP 和募集 β-arrestin。在两种测定中,增加 ML221 的浓度会拮抗固定浓度的 Ap13 (EC80 = 10 nM),计算出的 IC50 在 cAMP 测定中等于 0.70 μM,在 β-arrestin 测定中等于 1.75 μM。细胞测定:根据制造商的说明(Phoenix Pharmaceuticals, INC.),使用 Apelin-36(人)EIA 试剂盒,从 H69 和选定的 CCA 细胞系的上清液(37°C 孵育 48 小时)测量 Apelin 水平。根据方案一式三份制备未稀释的样品(50 mL)。在微孔板分光光度计(VersaMax,Molecular Devices,Sunnyvale,CA)上测量 450 nm 处的吸光度 OD。使用 PRISM® 软件 (GraphPad) 制作标准曲线并计算每个样品中 apelin 的浓度。数据表示为平均浓度±SEM。
APJ 拮抗活性检测:在 cAMP 实验和 β-抑制蛋白募集实验中,ML221 均能以浓度依赖性方式拮抗 Ap13 介导的 APJ 激活,实验数据以 Ap13 抑制率的平均值±标准误(mean ± SEM%)表示,并采用四参数逻辑斯蒂模型拟合剂量-效应曲线 [1] - GPCR 选择性分析:10 μM 浓度的 ML221 对 29 种受试 GPCR 无显著结合活性,仅对 κ-阿片受体(抑制率<50%)和苯二氮䓬酮受体(抑制率<70%)表现出微弱活性 [1] - 胆管癌细胞增殖抑制:通过实时定量聚合酶链反应(rtPCR,n=5)检测发现,ML221 可剂量依赖性降低 Mz-ChA-1 胆管癌细胞中增殖标志物(Ki-67、PCNA)的基因表达。在划痕愈合实验中,10 μM 浓度的 ML221 可在 6、12、24 和 48 h 显著抑制 Mz-ChA-1 细胞的增殖和迁移,但处理 24 h 后对细胞侵袭能力无显著影响 [2] - 胆管癌血管生成因子抑制:rtPCR(n=5)结果显示,ML221 可剂量依赖性降低 Mz-ChA-1 细胞中血管生成因子(VEGF-A、Ang-1、Ang-2)的基因表达。在 HuH-28 和 SG231 胆管癌细胞系中,10 μM 浓度的 ML221 可显著下调 Ki-67 及血管生成因子(VEGF-A、VEGF-C、Ang-1、Ang-2)的基因表达 [2] - 对正常胆管细胞的影响:在正常 H69 胆管细胞中,10 μM 浓度的 ML221 处理 24 h 后,可上调 Ki-67 基因表达,但显著下调血管生成因子(VEGF-A、VEGF-C、Ang-1、Ang-2)的表达(rtPCR 检测)[2] |
| 体内研究 (In Vivo) |
将八周龄的雄性 BALB/c 裸鼠 (nu/nu) 饲养在温度和光照受控的环境中,可自由获取饮用水和啮齿动物食物。将 300 万个 Mz-ChA-1 细胞悬浮在细胞外基质凝胶中,并皮下注射到这些裸鼠的后侧。通过尾静脉注射每周 3 次对小鼠进行 ML221 (150 μg/kg) 治疗,持续 4 周。使用电子卡尺每周测量肿瘤生长3次,体积测定如下:肿瘤体积(mm 3 )=长度(mm)×宽度(mm)×高度(mm)。允许肿瘤生长直至达到 Baylor Scott & White Healthcare IACUC 肿瘤负荷政策规定的最大允许肿瘤负荷。治疗4周后,用戊巴比妥钠(50mg/kg ip)对小鼠实施安乐死。使用购自 ScyTek Laboratories, INC 的 H&E 染色试剂盒进行苏木精和伊红 (H&E) 染色。通过阳性 IHC 染色和细胞角蛋白-19 (CK-19)(一种胆管细胞特异性标记物)的免疫印迹,证实肿瘤主要是 CCA 细胞。 IHC 和免疫印迹用于证明 APLNR、p-ERK 和 t-ERK 的表达。使用购自 abcam 的小鼠单克隆抗 α 微管蛋白抗体,将 α 微管蛋白用作相对对照。通过测量增殖标记物(PCNA、Ki-67)、血管生成标记物(VEGF-A、VEGF-C、Ang-1 和 Ang-2)和肿瘤进展标记物(Vimentin、MMP-9、MMP-3)(Qiagen)使用上述方案进行 rtPCR。
异种移植肿瘤生长抑制:将 Mz-ChA-1 胆管癌细胞接种于裸鼠(nu/nu)侧腹,建立肿瘤异种移植模型。治疗组(n=12)通过尾静脉注射给予 150 μg/kg 剂量的 ML221,对照组(n=9)不进行治疗。结果显示,ML221 可显著降低 Mz-ChA-1 肿瘤体积。肿瘤苏木精-伊红(H&E)染色显示治疗组与对照组存在差异;免疫印迹检测发现 ML221 治疗组肿瘤中 p-ERK 和 t-ERK 表达降低;rtPCR 检测显示增殖标志物(PCNA、Ki-67)、血管生成因子(VEGF-A、VEGF-C、Ang-1、Ang-2)及肿瘤进展标志物(波形蛋白、MMP-9、MMP-3)的基因表达均下调 [2] |
| 酶活实验 |
ML221 对 apelin-13 介导的 APJ 激活的拮抗作用通过两种互补的 APJ 功能测定进行评估:β-arrestin 募集和 cAMP 抑制。在两种测定中,增加 ML221 的浓度会拮抗固定浓度的 Ap13 (EC80 = 10 nM),计算出的 IC50 在 cAMP 测定中等于 0.70 μM,在 β-arrestin 测定中等于 1.75 μM。
APJ 拮抗作用的 cAMP 实验:培养表达 APJ 的细胞,加入 Ap13(激活 APJ)和不同浓度的 ML221。通过检测细胞内 cAMP 水平,评估 ML221 对 Ap13 介导的 APJ 激活的抑制作用。实验数据以 Ap13 抑制率的平均值±标准误表示,并拟合四参数逻辑斯蒂曲线以确定浓度依赖性拮抗效应 [1] - APJ 拮抗作用的 β-抑制蛋白募集实验:使用表达 APJ 的细胞,检测 Ap13 诱导的 β-抑制蛋白募集。加入不同浓度的 ML221 后,定量分析 β-抑制蛋白募集程度。与 cAMP 实验类似,结果以 Ap13 抑制率的平均值±标准误表示,并拟合四参数逻辑斯蒂曲线 [1] - GPCR 结合选择性实验:检测 10 μM 浓度的 ML221 对 31 种 GPCR(包括 APJ、AT1、κ-阿片、苯二氮䓬酮受体及 29 种其他 GPCR)的结合活性。结合活性以抑制率(%I)量化,除对 κ-阿片受体(<50%I)和苯二氮䓬酮受体(<70%I)有微弱活性外,对其他受体均无显著活性 [1] |
| 细胞实验 |
bEnd 的扩增。与 ML221 (0-30 μM) 孵育 24 小时后,使用 BrdU 掺入测定和 MTT 测定对 3 个细胞进行评估。 bEnd 是一种小鼠内皮细胞系 Dulbecco 改良的 Eagle 培养基,用 10% 热灭活胎牛血清增强,用于维持三个细胞。对于 MTT 和 BrdU 掺入测定,将细胞以 2.5 × 104/孔的密度接种在 24 孔培养板中。为了进行 BrdU 掺入测定,将 10 μM BrdU 添加到培养基中。 2小时后用4%多聚甲醛固定细胞10分钟。链霉亲和素异硫氰酸荧光素与生物素化的山羊抗小鼠 IgG 抗体相结合,可以实现一抗的可视化。要检测细胞核,请使用 Hoechst 33342。每个 Hoechst 阳性细胞的 BrdU 阳性细胞数用于计算 BrdU 掺入率。
细胞中 APJ 介导的激活抑制实验:培养表达 APJ 的细胞,以 Ap13 作为 APJ 激动剂,加入不同浓度的 ML221。在 cAMP 实验中,孵育后检测细胞内 cAMP 水平,评估 ML221 对 Ap13 诱导的 APJ 激活的抑制作用;在 β-抑制蛋白募集实验中,使用特异性检测激活型 GPCR 与 β-抑制蛋白结合的系统,量化 ML221 对 Ap13 介导的 β-抑制蛋白募集的影响。每个实验均重复进行,获取抑制率的平均值±标准误,并绘制剂量-效应曲线 [1] - 胆管癌细胞增殖及标志物分析实验:培养 Mz-ChA-1、HuH-28、SG231 胆管癌细胞及 H69 正常胆管细胞,加入不同浓度的 ML221(关键实验使用 10 μM 浓度),作用特定时间(基因表达检测为 24 h,划痕愈合实验为 6~48 h)。通过 rtPCR 检测增殖标志物(Ki-67、PCNA)和血管生成因子(VEGF-A、VEGF-C、Ang-1、Ang-2)的表达;采用划痕愈合实验,在细胞单层上制造划痕,多个时间点监测细胞迁移,评估增殖和迁移能力;使用侵袭实验试剂盒检测细胞侵袭能力,ML221 处理时间为 24 h [2] - APLNR 表达的免疫荧光和流式细胞术实验:固定 H69 和 Mz-ChA-1 细胞,用 APLNR 特异性抗体进行免疫荧光染色,观察 APLNR 的定位;流式细胞术实验中,收集细胞并与 APLNR 抗体孵育,分析并量化 APLNR 表达水平,比较胆管癌细胞与正常胆管细胞的差异 [2] - apelin 分泌的 ELISA 实验:收集胆管癌细胞(Mz-ChA-1、HuH-28、SG231)和 H69 细胞的培养上清液,使用 apelin 特异性 ELISA 试剂盒检测 apelin 浓度,比较恶性细胞与正常细胞的分泌水平 [2] |
| 动物实验 |
150 μg/kg;每周3次,尾静脉注射,持续4周。
雄性BALB/c裸鼠(nu/nu),8周龄。 裸鼠异种移植瘤模型:本研究使用裸鼠(nu/nu)。将Mz-ChA-1胆管癌细胞注射到小鼠侧腹,建立肿瘤异种移植模型。肿瘤形成后,治疗组(n=12)尾静脉注射150 μg/kg剂量的ML221,对照组(n=9)不进行任何治疗。定期监测肿瘤大小并计算肿瘤体积。实验结束时,处死小鼠并取出肿瘤组织。收集的肿瘤组织进行H&E染色(用于组织病理学分析)、免疫印迹(检测CK-19、p-ERK、t-ERK表达)和实时PCR(检测增殖、血管生成和肿瘤进展标志物的基因表达)[2] |
| 参考文献 | |
| 其他信息 |
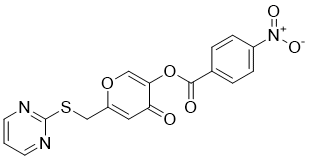
4-硝基苯甲酸[4-氧代-6-[(2-嘧啶基硫代)甲基]-3-吡喃基]酯是一种硝基苯甲酸。
ML221(化学名称:4-氧代-6-((嘧啶-2-基硫代)甲基)-4H-吡喃-3-基 4-硝基苯甲酸酯)是通过对约330,600个化合物的MLSMR化合物库进行高通量筛选(HTS)发现的。其合成方法和构效关系(SAR)(基于曲酸骨架)也已报道[1]。 - apeliPJ系统是心血管稳态的关键调节因子,与心血管疾病的发病机制相关;它还在能量代谢和胃肠道功能中发挥作用。 ML221 作为一种强效的 APJ 功能拮抗剂,为研究该系统提供了一种工具[1]。胆管癌 (CCA) 的五年生存率较低。apeliPLNR 轴在 CCA 组织和细胞中过度表达(经 IHC、rtPCR、免疫荧光、流式细胞术和 ELISA 证实)。ML221 通过靶向该轴抑制 CCA 的生长,提示其具有作为新型 CCA 肿瘤靶向治疗药物的潜力[2]。 |
| 分子式 |
C17H11N3O6S
|
|
|---|---|---|
| 分子量 |
385.04
|
|
| 精确质量 |
385.037
|
|
| 元素分析 |
C, 52.99; H, 2.88; N, 10.90; O, 24.91; S, 8.32
|
|
| CAS号 |
877636-42-5
|
|
| 相关CAS号 |
|
|
| PubChem CID |
7217941
|
|
| 外观&性状 |
Off-white to yellow solid powder
|
|
| LogP |
3.372
|
|
| tPSA |
153.41
|
|
| 氢键供体(HBD)数目 |
0
|
|
| 氢键受体(HBA)数目 |
9
|
|
| 可旋转键数目(RBC) |
6
|
|
| 重原子数目 |
27
|
|
| 分子复杂度/Complexity |
646
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
O=C(C1C=CC([N+](=O)[O-])=CC=1)OC1C(=O)C=C(CSC2N=CC=CN=2)OC=1
|
|
| InChi Key |
UASIRTUMPRQVFY-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C17H11N3O6S/c21-14-8-13(10-27-17-18-6-1-7-19-17)25-9-15(14)26-16(22)11-2-4-12(5-3-11)20(23)24/h1-9H,10H2
|
|
| 化学名 |
[4-oxo-6-(pyrimidin-2-ylsulfanylmethyl)pyran-3-yl] 4-nitrobenzoate
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2 mg/mL (5.19 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5971 mL | 12.9857 mL | 25.9713 mL | |
| 5 mM | 0.5194 mL | 2.5971 mL | 5.1943 mL | |
| 10 mM | 0.2597 mL | 1.2986 mL | 2.5971 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Representative dose response curve for ML221.Bioorg Med Chem Lett. 2012 Nov 1; 22(21): 6656–6660. |
|---|
GPCR profiling panel forML221.Bioorg Med Chem Lett. 2012 Nov 1; 22(21): 6656–6660. |
A: Positive APLNR staining by IHC in four human CCA tissues (bottom row) compared to adjacent non-malignant liver tissues (top row).Cancer Lett.2017Feb 1;386:179-188. |
A: Treatment of benign human cholangiocytes (H69) with 10 μM of ML221 over 24 h increased Ki-67 gene expression, but significantly decreased expression of angiogenic factors (VEGF-A, VEGF-C, Ang-1, and Ang-2) via rtPCR. B. Treatment of HuH-28 cholangiocarcinoma cells with 10 μM of ML221 over 24 h significantly decreased Ki-67 gene expression, as well as angiogenic factors (VEGF-A, VEGF-C, Ang-1, and Ang-2) via rtPCR. C. Treatment of SG231 cholangiocarcinoma cells with 10 μM of ML221 over 24 h significantly decreased Ki-67 gene expression, as well as angiogenic factors (VEGF-A, VEGF-C, Ang-1, and Ang-2) via rtPCR. Cancer Lett.2017Feb 1;386:179-188. |
|---|
A: Apelin treatment promotes Mz-ChA-1 gene expression of Ki-67 and PCNA (left), whereas, ML221 treatment decreases Mz-ChA-1 gene expression of Ki-67 and PCNA in a dose dependent manner (n = 5) via rtPCR. B: Gene expression of angiogenic factors (VEGF-A, Ang-1, and Ang-2) is increased when Mz-ChA-1 cells are treated with increasing concentrations of apelin (left), whereas, gene expression is decreased with increasing concentrations of ML221, an APLNR antagonist (right) (n = 5) via rtPCR. C: 10 μM of ML221 treatment significantly decreases cell proliferation and migration at 6, 12, 24, and 48 h during wound-healing assay (* = P < 0.05). D: Mz-ChA-1 cell invasiveness did not significantly change following treatment with 10 μM of ML221 for 24 h compared to untreated control cells.Cancer Lett.2017Feb 1;386:179-188. |
A: Parenteral administration of ML221 in nu/nu mice decreases Mz-ChA-1 tumor size (bottom row) compared to untreated control tumors (top row). B: Mz-ChA-1 tumor volume significantly increases in untreated control tumors (n = 9) compared to ML221 treated tumors (n = 12). C: H&E staining of control (left) and ML221 treated (right) Mz-ChA-1 tumors isolated from nu/nu mice.
A: Immunoblots of protein isolated from control and ML221 treated Mz-ChA-1 tumors shows expression of CK-19. p-ERK and t-ERK expression is decreased in ML221 treated Mz-ChA-1 tumors compared to untreated Mz-ChA-1 tumors. B: Control and ML221 treated Mz-ChA-1 tumors demonstrate positive staining for CK-19, a cholangiocyte specific marker, shown by IHC. C: IHC shows positive staining for APLNR in control and ML221 treated Mz-ChA-1 tumors. D. Mz-ChA-1 tumors treated with ML221 demonstrated decreased gene expression of proliferative markers (PCNA, Ki-67), angiogenic factors (VEGF-A, VEGF-C, Ang-1, and Ang-2), and markers of tumor progression (Vimentin, MMP-9, MMP-3) via rtPCR. |