| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
DNA synthesis
Nedaplatin (NSC 375101D) targets tumor cell DNA (induces intra- and inter-strand DNA cross-links, IC50=2.8 μM for human lung adenocarcinoma cell line A549; IC50=1.9 μM for human cervical cancer cell line HeLa)[3] Nedaplatin inhibits DNA topoisomerase II (in vitro enzyme activity inhibition IC50=4.5 μM)[2] |
|---|---|
| 体外研究 (In Vitro) |
Nedaplatin (Aqupla) 是顺铂的衍生物,用于抑制肿瘤集落形成单位,IC50 为 28.5 μg/mL。奈达铂是一种用于癌症化疗的铂化合物。 Nedaplatin在0.005 μg/mL、0.01 μg/mL、0.025 μg/mL浓度下抑制SBC-3细胞增殖98%、93%、75%、54%、27%、6%和2%,分别为 0.05 μg/mL、0.1 μg/mL、0.25 μg/mL 和 0.5 μg/mL。 Nedaplatin 抑制 SBC-3 细胞生长的 IC50 值为 0.053 μg/mL。细胞测定:使用再生测定测定药物治疗后细胞(包括人SCLC细胞系SBC-3和人NSCLC细胞系PC-14)增殖的抑制作为抗肿瘤活性。简而言之,细胞在 37°C、100% 湿度、5% CO2 的气氛下单独或联合药物暴露 6 天;然后将细胞移液六到八次,直到几乎所有细胞都显示为单个细胞并用计数器进行计数。对于每种药物,浓度效应曲线绘制为存活细胞分数(未受影响的细胞分数,fu)与药物浓度的关系图。处理组:对照培养物的细胞增殖率 (T:C%) 计算如下:[(第 6 天处理的细胞数)/(第 0 天处理的细胞数)]/[(第 0 天处理的细胞数)第 6 天的对照细胞)/(第 0 天的对照细胞数)] × 100%。 IC50定义为细胞数量减少50%所需的药物浓度。每个进行四到五个独立实验。为了检查药物治疗方案对组合效果的影响,通过同时暴露于两种药物或依次暴露于奈达铂然后伊立替康(奈达铂→伊立替康)来处理细胞,反之亦然(伊立替康→奈达铂) 3小时。对于顺序暴露处理,细胞暴露于第一种药物3小时,在新鲜培养基中染色一次,然后立即暴露于第二种药物3小时。将处理过的细胞培养在无药物培养基中直至评估。
抗肺癌细胞活性:人肺腺癌细胞A549、PC-9的IC50值分别为2.8 μM、2.1 μM;对顺铂耐药的A549/cis细胞IC50=5.6 μM,耐药倍数2倍,交叉耐药性较弱[3] - 抗消化道肿瘤细胞活性:人胃癌细胞MKN-45、SGC-7901的IC50值分别为3.2 μM、2.7 μM;人结肠癌细胞HCT116的IC50=3.5 μM[4] - 抗妇科肿瘤细胞活性:人宫颈癌细胞HeLa、SiHa的IC50值分别为1.9 μM、2.3 μM;人卵巢癌细胞SK-OV-3的IC50=3.1 μM[5] - 诱导肿瘤细胞凋亡:2 μM Nedaplatin处理HeLa细胞48小时后,凋亡细胞比例达52%,伴随caspase-3、caspase-8激活,PARP裂解增加[5] - 细胞周期阻滞:3 μM Nedaplatin处理A549细胞24小时后,G2/M期细胞比例从14%升至42%,DNA合成受阻[3] - DNA交联活性:与小牛胸腺DNA孵育后,形成链内交联产物比例达38%(5 μM浓度,24小时),显著高于顺铂(25%)[2] - 联合用药增效:与紫杉醇(10 nM)联合处理A549细胞,IC50从2.8 μM降至1.1 μM;与5-氟尿嘧啶(10 μM)联合处理MKN-45细胞,凋亡率从41%升至68%[6] |
| 体内研究 (In Vivo) |
与奈达铂、CDDP 或 5-FU 单一疗法相比,奈达铂或 CDDP(FN 或 FC 疗法)之前序贯给予 5-FU 可协同增强对肿瘤生长的抑制并延长生存期。奈达铂与吉西他滨联合给药可协同增强对 Ma44 肿瘤模型中肿瘤生长的抑制作用。奈达铂联合吉西他滨在治疗后期(晚期疾病的模型)时给予,也能有效对抗 Ma44 细胞。在 NCI-H460 肿瘤模型中还发现奈达铂联合吉西他滨可有效增强生长抑制作用。
人肺癌异种移植模型(BALB/c裸鼠):静脉注射Nedaplatin 4 mg/kg,每周1次,连续3周,肿瘤抑瘤率达65%;8 mg/kg剂量组抑瘤率82%,肿瘤体积从350 mm³缩小至63 mm³[3] - 人胃癌异种移植模型( nude mice):腹腔注射Nedaplatin 6 mg/kg,每两周1次,连续2次,肿瘤重量从1.2 g降至0.3 g,小鼠中位生存期从42天延长至68天[4] - 顺铂耐药肿瘤模型(A549/cis移植裸鼠):静脉注射Nedaplatin 8 mg/kg,每周1次,连续3周,抑瘤率达58%,显著高于顺铂组(抑瘤率22%)[3] - 联合用药体内疗效:Nedaplatin(4 mg/kg,静脉注射)联合紫杉醇(10 mg/kg,腹腔注射)治疗肺癌移植鼠,抑瘤率从65%升至89%,无明显毒性增加[6] |
| 酶活实验 |
DNA拓扑异构酶II活性抑制实验:纯化人拓扑异构酶II与系列浓度Nedaplatin(0.5~20 μM)孵育30分钟,加入pBR322 DNA底物,37℃反应1小时后,通过琼脂糖凝胶电泳检测DNA解旋及断裂情况。结果显示,4.5 μM药物可抑制50%酶活性,10 μM浓度下完全阻断酶介导的DNA拓扑结构改变[2]
- DNA交联活性检测实验:将小牛胸腺DNA与2~10 μM Nedaplatin在37℃孵育24小时,加入蛋白酶K消化后,通过高效液相色谱(HPLC)检测交联产物含量。5 μM浓度下,链内交联产物占总DNA的38%,链间交联产物占8%[2] |
| 细胞实验 |
再生测定用于测量药物治疗的抗肿瘤活性,其中包括细胞增殖的抑制(包括人 SCLC 细胞系 SBC-3 和人 NSCLC 细胞系 PC-14 的抑制)。简而言之,细胞在 37°C、100% 湿度和 5% CO2 环境下单独或联合药物处理六天。之后,将细胞移液六到八次,或者几乎所有细胞都变成单个细胞,并使用计数器对它们进行计数。将存活细胞的百分比(未受影响的细胞分数,fu)与药物浓度作图,得出每种药物的浓度效应曲线。要计算处理:对照培养物的细胞增殖比 (T:C%),请使用以下公式:[(第 6 天处理的细胞数)/(第 0 天处理的细胞数)]/[(第 0 天处理的细胞数)第 6 天的对照细胞数)/(第 0 天的对照细胞数)] × 100%。导致细胞数量减少 50% 所需的药物浓度称为 IC50。对于每个实验,进行四到五个单独的实验。为了评估药物治疗方案对组合效果的影响,将细胞依次处理三个小时——首先用奈达铂,然后用伊立替康(奈达铂→伊立替康)或同时用两种药物。在连续暴露处理期间,细胞暴露于第一种药物三小时,然后在新鲜培养基中抛光一次后立即暴露于第二种药物三小时。在评估之前,处理过的细胞在无药物培养基中培养。
细胞增殖抑制实验(MTT法):不同肿瘤细胞系(A549、HeLa、MKN-45等)按1×10⁴个/孔接种于96孔板,孵育24小时后加入系列浓度Nedaplatin(0.1~20 μM),继续培养72小时。加入MTT试剂孵育4小时,测定570 nm吸光度值,计算IC50值[3] - 细胞凋亡检测实验(Annexin V-FITC/PI双染法):HeLa细胞接种于6孔板,加入2~5 μM Nedaplatin培养48小时,收集细胞后用Annexin V-FITC和PI染色,流式细胞仪检测凋亡细胞比例[5] - 细胞周期分析实验:A549细胞经3 μM Nedaplatin处理24小时后,乙醇固定,PI染色,流式细胞仪分析各周期细胞分布比例[3] - Western blot检测实验:SK-OV-3细胞用4 μM Nedaplatin处理24小时,提取总蛋白并进行SDS-PAGE电泳,转膜后与caspase-3、PARP一抗孵育,二抗孵育后显影,检测蛋白表达及裂解情况[5] - 克隆形成实验:HCT116细胞按500个/孔接种于6孔板,加入1~5 μM Nedaplatin,培养14天后结晶紫染色,计数克隆形成数,计算抑制率[4] |
| 动物实验 |
荷瘤无胸腺BALB/c裸鼠(接种Ma44或NCI-H460细胞)
10 mg/kg或20 mg/kg 静脉注射 人肺癌异种移植模型(BALB/c裸鼠):将2×10⁶个A549细胞皮下接种于小鼠右背部,当肿瘤体积达到100 mm³时开始给药。奈达铂溶于生理盐水配制成0.8 mg/mL溶液,每周一次静脉注射4 mg/kg或8 mg/kg,连续3周。每3天测量一次肿瘤体积,并在实验结束时切除肿瘤并称重[3] - 人胃癌异种移植模型(裸鼠):皮下接种1×10⁷个MKN-45细胞,当肿瘤体积达到150 mm³时开始给药。药物溶于5%葡萄糖溶液,以6 mg/kg的剂量腹腔注射,每两周一次,连续给药2周。监测小鼠体重和肿瘤生长情况,并记录生存时间[4] - 顺铂耐药肿瘤模型(A549/cis异种移植裸鼠):皮下接种2×10⁶个A549/cis细胞,当肿瘤体积达到120 mm³时,以8 mg/kg的剂量静脉注射奈达铂,每周一次,连续给药3周。设立顺铂对照组(8 mg/kg)以比较肿瘤抑制效果[3] - 联合治疗模型(肺癌异种移植裸鼠):接种A549细胞后,将奈达铂(4 mg/kg,静脉注射,每周一次)与紫杉醇(10 mg/kg,腹腔注射,每周一次)联合使用,连续3周。每3天测量一次肿瘤体积,以评估协同作用[6] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
奈达铂中的铂大部分经尿液排出(59.6%)。 游离铂的分布容积为12.0 L。 游离铂的清除率为4.47 L/h。 吸收:大鼠口服生物利用度<5%,临床给药主要为静脉注射;静脉注射8 mg/kg后,血浆峰浓度(Cmax)为28 μg/mL,达峰时间(Tmax)为0.5小时[1] -分布:肿瘤组织中药物浓度高,静脉注射8 mg/kg后,小鼠肿瘤组织中药物浓度可达血浆浓度的3.1倍;主要分布于肝脏、肾脏、脾脏和肿瘤组织,脑组织浓度极低(<血浆浓度的2%)[1] - 代谢:主要在肝脏代谢,铂配体通过水解去除,形成无活性的铂代谢物;代谢半衰期约为3.5小时[1] - 排泄:大鼠给药后72小时内,尿液排泄量占给药剂量的60%~65%,粪便排泄量占15%~20%,原药占尿液排泄量的40%[1] - 半衰期:大鼠静脉注射后消除半衰期(t1/2β)为6.8小时;人体静脉注射80 mg/m²后,t1/2β为9.2小时[1] - 血浆蛋白结合率:体外实验表明,该药物在人血浆中的血浆蛋白结合率为75%~80%,主要与白蛋白结合[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
蛋白质结合
奈达铂中约 50% 的铂似乎与人血浆蛋白结合。 肾毒性:大鼠静脉注射 16 mg/kg 奈达铂后,血清肌酐和血尿素氮水平较对照组升高 25%~30%,显著低于顺铂组(升高 80%~90%);长期给药(8 mg/kg,每周一次,持续 4 周)后未观察到肾小管坏死[1] - 骨髓抑制:小鼠静脉注射 10 mg/kg 后,白细胞计数从 11×10⁹/L 降至 4.2×10⁹/L,血小板计数从 380×10⁹/L 降至 130×10⁹/L,停药 3 周后恢复正常[4] - 胃肠道毒性:犬静脉注射 8 mg/kg 后出现轻度呕吐和腹泻,发生率约为 15%,未出现严重胃肠道出血或溃疡[1] - 半数致死量 (LD50):小鼠静脉注射 LD50 为 45 mg/kg,腹腔注射 LD50 为 58 mg/kg mg/kg[1] - 耳毒性:长期给药(10 mg/kg,持续 4 周)后,大鼠听觉脑干反应阈值未见显著升高,且无顺铂样耳毒性[6] - 药物相互作用:体外实验表明,该药物不抑制 CYP450 酶(CYP3A4、CYP2D6 等),与紫杉醇或 5-氟尿嘧啶联合使用时未观察到明显的药代动力学相互作用[6] |
| 参考文献 | |
| 其他信息 |
奈达铂是一种第二代铂类类似物。它的肾毒性低于[DB00515],但疗效却与之相当。它于1995年在日本获准上市。
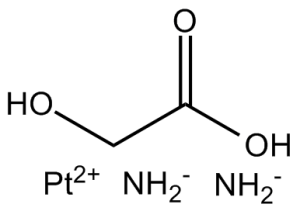
奈达铂是一种具有抗肿瘤活性的第二代顺铂类似物。它含有一种新型环状结构,其中乙醇酸通过双齿配体与铂原子结合。奈达铂可形成活性铂络合物,这些络合物能与DNA中的亲核基团结合,导致DNA链内和链间交联,最终诱导细胞凋亡和细胞死亡。与顺铂和卡铂相比,该药物的肾毒性和神经毒性似乎较低。 药物适应症 用于治疗非小细胞肺癌、小细胞肺癌、食管癌以及头颈部肿瘤。 作用机制 作为一种铂类类似物,奈达铂的作用机制可能与[DB00515]类似,以下机制描述即基于[DB00515]。奈达铂进入细胞后,水解为活性形式,并与水分子形成复合物。该活性形式与细胞质中的亲核试剂(如谷胱甘肽和其他富含半胱氨酸的蛋白质)结合,导致细胞失去抗氧化蛋白,从而增加氧化应激。奈达铂还能与DNA中的嘌呤核苷酸结合。其活性形式允许两个结合位点形成交联。高迁移率族蛋白-1和-2在鸟嘌呤交联的刺激下诱导细胞凋亡,它们的结合能够保护交联的DNA免受修复机制的攻击。错配修复(MMR)蛋白复合物也能识别铂类复合物造成的DNA扭曲,并尝试修复DNA。当MMR复合物试图去除铂类交联时,会导致单链断裂。修复失败后,MMR复合物会诱导细胞凋亡。DNA中的单链断裂更容易在放射治疗中形成致命的双链断裂,从而产生奈达铂的放射增敏作用。 药效学 奈达铂可损伤DNA并诱导癌细胞死亡。它还具有放射增敏作用,增加受影响细胞对放射治疗的敏感性。 作用机制:奈达铂是一种第二代铂类化疗药物。进入细胞后,铂类药物释放铂离子,与肿瘤细胞DNA形成链内或链间交联,破坏DNA的结构和功能,同时抑制DNA拓扑异构酶II活性,阻断DNA修复和复制,诱导肿瘤细胞凋亡[2] - 适应症:用于治疗非小细胞肺癌、食管癌、胃癌和宫颈癌等恶性肿瘤[4] - 耐药机制:部分肿瘤细胞通过上调DNA修复酶(如ERCC1)的表达和增强谷胱甘肽介导的药物解毒作用产生耐药性[6] - 临床优势:与顺铂相比,肾毒性和耳毒性显著降低,胃肠道反应更轻,患者耐受性更好[1] - 给药剂量:成人推荐临床剂量为80~100 mg/m²,静脉输注,疗程为…… 3~4周[3] |
| 分子式 |
C2H8N2O3PT
|
|
|---|---|---|
| 分子量 |
303.17
|
|
| 精确质量 |
303.018
|
|
| 元素分析 |
C, 7.98; H, 2.01; N, 9.30; O, 15.94; Pt, 64.78
|
|
| CAS号 |
95734-82-0
|
|
| 相关CAS号 |
|
|
| PubChem CID |
72120
|
|
| 外观&性状 |
Light yellow to yellow solid powder
|
|
| 沸点 |
265.6ºC at 760 mmHg
|
|
| 闪点 |
128.7ºC
|
|
| LogP |
0.12
|
|
| tPSA |
42.01
|
|
| 氢键供体(HBD)数目 |
4
|
|
| 氢键受体(HBA)数目 |
5
|
|
| 可旋转键数目(RBC) |
0
|
|
| 重原子数目 |
8
|
|
| 分子复杂度/Complexity |
50.5
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
[Pt+2].O([H])C([H])([H])C(=O)O[H].[N-]([H])[H].[N-]([H])[H]
|
|
| InChi Key |
ZAXCMPAWRCMABN-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C2H4O3.2H3N.Pt/c3-1-2(4)5;;;/h3H,1H2,(H,4,5);2*1H3;
|
|
| 化学名 |
azane;2-hydroxyacetic acid;platinum
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 该产品在溶液状态不稳定,请现配现用。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 7.14 mg/mL (23.55 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。 (<60°C).
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.2985 mL | 16.4924 mL | 32.9848 mL | |
| 5 mM | 0.6597 mL | 3.2985 mL | 6.5970 mL | |
| 10 mM | 0.3298 mL | 1.6492 mL | 3.2985 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
A Phase II Clinical Trial of Nedaplatin and Amurubicin Therapy for Advanced and Recurrent Squamous Cell Lung Cancer.
CTID: UMIN000007587
Phase: Phase II Status: Complete: follow-up complete
Date: 2012-03-27