| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
MAP4K2 (IC50 = 21.7 nM); TAK1 (IC50 = 149 nM); LYN (IC50 = 12.9 nM); GSK (IC50 = 56.4 nM); ABL,ARG (IC50 = 75.2 nM); FER (IC50 = 82.3 nM); SRC (IC50 = 113 nM); Eph B2 (IC50 = 672 nM); ZAK (IC50 = 698 nM); Eph A2 (IC50 = 773 nM); Eph B4 (IC50 = 999 nM); ZC1/HGK (IC50 = 3250 nM); RAF1 (IC50 = 7590 nM)
NG25 is a potent dual TAK1 and MAP4K2 inhibitor, with IC50s of 149 nM and 21.7 nM, respectively. Additionally, NG25 effectively inhibits a number of kinases, including LYN, CSK, FER, p38α, ABL, ARG, and SRC, with respective IC50 values of 12.9, 56.4, 82.3, 102, 75.2, and 113 nM[1]. NG25 completely inhibits the secretion of IFNα and IFNβ when stimulated by CL097 or CpG B or A, respectively[2]. All tested breast cancer cell lines experience a dose-dependent reduction in cell viability after NG25 treatment. The cytotoxic effect of Dox on breast cancer cells is enhanced by NG25 (2 μM)[3]. NG-25 (also referred to as compound 1) is a type II kinase inhibitor. Its primary targets are Transforming Growth Factor β-Activated Kinase 1 (TAK1, MAP3K7) with an IC₅₀ of 149 nM and Mitogen-Activated Protein Kinase Kinase Kinase Kinase 2 (MAP4K2, GCK) with an IC₅₀ of 21.7 nM. It also inhibits p38α (MAPK14) and ABL kinase. Other kinases showing inhibition in profiling include ZAK, LYN, SRC, FER, FES, and EPH-family kinases. [1] |
|---|---|
| 体外研究 (In Vitro) |
NG25 是一种有效的 TAK1 和 MAP4K2 双重抑制剂,IC50 分别为 149 nM 和 21.7 nM。此外,NG25 还能有效抑制多种激酶,包括 LYN、CSK、FER、p38α、ABL、ARG 和 SRC,IC50 值分别为 12.9、56.4、82.3、102、75.2 和 113 nM[1]。当 CL097 或 CpGB 或 A 分别刺激时,NG25 完全抑制 IFNα 和 IFNβ 的分泌[2]。所有测试的乳腺癌细胞系在 NG25 处理后都会出现剂量依赖性细胞活力下降。 NG25 (2 μM) 增强了 Dox 对乳腺癌细胞的细胞毒作用[3]。
在小鼠 L929 细胞中,100 nM 的 NG-25 (1) 能有效降低 TNFα 诱导的 IKKα/β 磷酸化并抑制 IκB-α 降解,效果与不可逆 TAK1 抑制剂 37 (5Z-7-oxozeaenol) 相当。[1] 在 IL-1α 刺激的 293 IL-1R 细胞和小鼠胚胎成纤维细胞(MEFs)中,NG-25 (1) 以剂量依赖性方式抑制下游 p105、p38 和 JNK1/2 的磷酸化。[1] 在 LPS 刺激的小鼠 RAW 细胞中,NG-25 (1) 抑制 p105、p38 和 JNK1/2 的磷酸化。[1] 在 TLR7 激动剂 CL097 刺激的人 Gen2.2 细胞中,1 µM 的 NG-25 (1) 阻断了信号传导。[1] NG-25 (1) 对 BCR-ABL 依赖的 Ba/F3 细胞具有抗增殖活性。[1] |
| 酶活实验 |
IRF7 在大肠杆菌中作为与谷胱甘肽 S-转移酶 (GST) 的融合蛋白产生,后者被 PreScission 蛋白酶分解。通过 PreScission 蛋白酶消化,IRF7 从 GST 和谷胱甘肽-Sepharose 中释放出来,GST-IRF7 被谷胱甘肽-Sepharose 捕获。昆虫 Sf21 细胞表达 His6 标记形式的 IKKβ 和 TBK1,这些形式已被磷酸化而变得有活性,然后将这些纯化形式用于次氮基三乙酸镍-琼脂糖亲和层析。 Millipore 公司销售活性 GST-IKKα,然后进行测试。
NG-25 对多种激酶的抑制活性通过生化酶活实验测定。对于 TAK1 和 MAP4K2,IC₅₀ 值使用商业激酶谱分析服务(SelectScreen)测定。该实验测量化合物对激酶酶活性的抑制。[1] 此外,使用体外 ATP 位点竞争结合实验(KinomeScan)在 10 µM 或 1 µM 浓度下对超过 420 种激酶进行了全激酶组选择性谱分析。[1] |
| 细胞实验 |
在 96 孔板中,将 3.5×105 Gen 2.2 细胞或 Flt3-DC 在不加或加指定浓度抑制剂的情况下孵育 1 小时。然后用 1 M CpG(A 型或 B 型)、1 μg/mL CL097 或 1 μg/mL R848 刺激它们。 5 或 12 小时后收集细胞培养物上清液,通过离心澄清,并储存在 80°C 等待细胞因子水平分析。将未刺激的细胞在不存在或存在抑制剂的情况下孵育 12 小时,以进行细胞活力测定。细胞固定后,使用流式细胞术测定活细胞的百分比。
用于基于细胞的激酶抑制谱分析时,用 5 µM 和 0.5 µM 的 NG-25 处理 A375 黑色素瘤细胞,裂解后使用 KINativ 技术进行探针标记。该方法测量化合物在细胞裂解物中保护激酶免于被赖氨酸反应性 ATP 或 ADP-生物素探针标记的能力,表明其在细胞环境中的靶点结合。[1] 为评估对下游信号的抑制,L929 细胞用化合物(例如 100 nM)预处理 30 分钟,然后用 TNFα 刺激 5 分钟。裂解细胞后,通过 Western blot 分析 IKKα/β 的磷酸化和 IκB-α 的水平。[1] 类似地,293 IL-1R 细胞、MEFs 和 RAW 细胞用不同浓度的 NG-25 预处理 1 小时,然后用 IL-1α 或 LPS 刺激 30 分钟。通过 Western blot 分析 p105、p38 和 JNK1/2 的磷酸化。[1] Gen2.2 细胞用化合物(1 µM)预处理 1 小时,然后用 CL097 刺激 30 分钟,随后进行 Western blot 分析。[1] 在 Ba/F3 细胞(BCR-ABL 依赖型和亲本型)中评估抗增殖活性。细胞与系列稀释的化合物共培养 48 小时,使用发光细胞活力测定法测量细胞活力。[1] |
| 动物实验 |
雄性瑞士白化小鼠
1 mg/kg 静脉注射或口服 在雄性瑞士白化小鼠中进行了药代动力学研究。对于静脉注射(IV),将NG-25配制成20% (v/v)羟丙基-β-环糊精的25 mM磷酸钠缓冲液溶液,经尾静脉以1 mg/kg的剂量给药。 对于口服(PO),将NG-25配制成0.5% (w/v)羧甲基纤维素钠(Na CMC)和0.1% (v/v)吐温-80的混悬液,经灌胃以10 mg/kg的剂量给药。 在给药后不同时间点(例如,0.083、0.25、0.5、1、2、4、6、8、12、24 h)采集血样。分离血浆并储存,用于LC/MS/MS生物分析。[1] |
| 药代性质 (ADME/PK) |
小鼠静脉注射1 mg/kg NG-25后,其半衰期 (T₁/₂) 为2.03 h,清除率 (CL) 为80.8 mL min⁻¹ kg⁻¹,稳态分布容积 (Vₛₛ) 为11.9 L/kg。口服10 mg/kg NG-25后,最大血浆浓度 (Cmax) 为316 ng/mL,达峰时间 (Tmax) 为0.5 h,浓度-时间曲线下面积 (AUC) 为1369 h·ng/mL。口服生物利用度 (F) 为70.2%。[1]
|
| 毒性/毒理 (Toxicokinetics/TK) |
在细胞实验所用的浓度下(细胞因子分泌实验最高浓度为 400 nM,蛋白质印迹实验最高浓度为 2 μM),NG-25 对 Gen2.2 细胞的活力没有影响,这已在对照实验中得到证实。[2]
|
| 参考文献 |
|
| 其他信息 |
NG-25是利用II型抑制剂的药效团模型和全激酶组分析发现的。
它与TAK1的DFG-out构象结合,这已通过2.4 Å共晶结构(PDB:4O91)得到证实。其结合涉及与铰链区(Ala107)的氢键、与Glu77和Asp175骨架的连接酰胺以及与激活环上Ile153和His154羰基的哌嗪尾部的氢键。 由于其可逆的抑制模式以及与共价抑制剂5Z-7-oxozeaenol相比独特的脱靶效应,它可作为TAK1的药理学探针。 结构修饰得到了对MAP4K2(例如化合物17)或p38α(例如化合物11)选择性更高的类似物。[1] |
| 分子式 |
C29H30F3N5O2
|
|---|---|
| 分子量 |
537.5760
|
| 精确质量 |
537.235
|
| 元素分析 |
C, 64.79; H, 5.63; F, 10.60; N, 13.03; O, 5.95
|
| CAS号 |
1315355-93-1
|
| 相关CAS号 |
NG25 trihydrochloride;2108554-00-1
|
| PubChem CID |
53340664
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
6.332
|
| tPSA |
76.98
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
8
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
39
|
| 分子复杂度/Complexity |
808
|
| 定义原子立体中心数目 |
0
|
| SMILES |
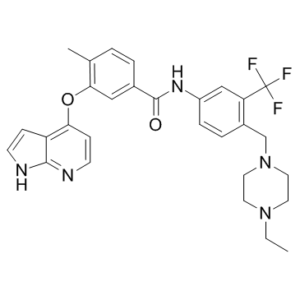
FC(C1C([H])=C(C([H])=C([H])C=1C([H])([H])N1C([H])([H])C([H])([H])N(C([H])([H])C([H])([H])[H])C([H])([H])C1([H])[H])N([H])C(C1C([H])=C([H])C(C([H])([H])[H])=C(C=1[H])OC1C([H])=C([H])N=C2C=1C([H])=C([H])N2[H])=O)(F)F
|
| InChi Key |
SMPGEBOIKULBCT-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C29H30F3N5O2/c1-3-36-12-14-37(15-13-36)18-21-6-7-22(17-24(21)29(30,31)32)35-28(38)20-5-4-19(2)26(16-20)39-25-9-11-34-27-23(25)8-10-33-27/h4-11,16-17H,3,12-15,18H2,1-2H3,(H,33,34)(H,35,38)
|
| 化学名 |
N-[4-[(4-ethylpiperazin-1-yl)methyl]-3-(trifluoromethyl)phenyl]-4-methyl-3-(1H-pyrrolo[2,3-b]pyridin-4-yloxy)benzamide
|
| 别名 |
NG25; NG-25; NG 25
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 16.7~25 mg/mL (31.0~46.1 mM)
Ethanol: ~3 mg/mL (~5.6 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (4.65 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (4.65 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (4.65 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8602 mL | 9.3009 mL | 18.6019 mL | |
| 5 mM | 0.3720 mL | 1.8602 mL | 3.7204 mL | |
| 10 mM | 0.1860 mL | 0.9301 mL | 1.8602 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。