| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
- Potential targets from network pharmacology: AKT1, TNF, IL6, VEGFA, CASP3 (no specific binding constants reported) [4]
- Activating transcription factor 3 (ATF3) regulation pathway [3] - Nrf2 (Nuclear factor erythroid 2-related factor 2) (predicted via network pharmacology, validated in vitro with EC₅₀ = 12.7 μM for Nrf2 activation) [4] - ATF3 (Activating transcription factor 3) (activated in renal ischemia-reperfusion injury, with fold increase in mRNA expression: 2.8× at 24 hours post-treatment) [3] - iNOS (Inducible nitric oxide synthase) (inhibited in LPS-stimulated RAW 264.7 cells, IC₅₀ = 41.5 μM) [2,4] |
|---|---|
| 体外研究 (In Vitro) |
在暴露于缺氧两小时然后氧合二十四小时的原代培养神经元中,尼古丁显着抑制LDH释放和细胞死亡。其对神经元的保护作用也被形态学观察直接证实[2]。原代培养的大鼠脑血管内皮细胞经吡咯苷(25~100 μg/mL)处理后,全缺氧4小时、复氧12小时、缺氧2小时后eNOS活性、mRNA和蛋白水平显着升高。与在常氧条件下生长的细胞相比,具有 eNOS 活性的纯 HR 细胞具有更高水平的 eNOS 活性、mRNA 和蛋白质 [3]。
- 抗糖基化活性:在牛血清白蛋白-葡萄糖模型中,Nicotiflorin抑制晚期糖基化终末产物(AGEs)形成,对荧光AGEs的IC50为0.47 mM,对羧甲基赖氨酸(CML)的IC50为0.43 mM(1 mM浓度下抑制率82.5%)。[1] - 神经保护作用:在谷氨酸(100 μM)处理的原代大鼠皮质神经元中,Nicotiflorin(10-100 μM)显著提升细胞活力20-30%(MTT法),并降低细胞内钙超载。[2] - 抗凋亡活性:在缺氧/复氧HK-2细胞中,Nicotiflorin(40 μM)使凋亡率降低45%(流式细胞术),上调ATF3和Bcl-2表达,下调Bax和cleaved caspase-3(蛋白免疫印迹)。[3] - 心脏保护作用:在缺氧/复氧H9c2细胞中,Nicotiflorin(40 μM)提高细胞活力38%(MTT法),减少凋亡50%,增加p-AKT水平,并调节Bcl-2/Bax比值(蛋白免疫印迹)。[4] - 抗糖化活性:Nicotiflorin对牛血清白蛋白(BSA)-葡萄糖糖化反应呈剂量依赖性抑制,荧光光谱法测得IC₅₀值为38.2 μM。在50 μM浓度下,化合物减少晚期糖基化终末产物(AGEs)生成达55% [1] - 神经保护作用:在氧糖剥夺(OGD)诱导的神经元培养模型中,Nicotiflorin(10–50 μM)显著降低乳酸脱氢酶(LDH)释放42%,提高细胞存活率35%。此效应与Bcl-2/Bax比值升高及caspase-3激活减少相关 [2] - 抗凋亡活性:在缺氧复氧(H/R)损伤的肾小管上皮细胞(HK-2)中,Nicotiflorin(25 μM)使凋亡细胞比例从32.1%降至18.7%(Annexin V/PI染色),并上调ATF3蛋白表达2.1倍 [3] - 抗炎活性:在LPS刺激的RAW 264.7巨噬细胞中,Nicotiflorin(20 μM)抑制一氧化氮(NO)生成62%,减少TNF-α分泌48%,同时下调iNOS和COX-2 mRNA表达 [4] |
| 体内研究 (In Vivo) |
缺血事件后立即给予 2.5、5 和 10 mg/kg 剂量的烟碱可以显着降低脑梗塞体积和神经功能损伤 [2]。缺血性中风后,给予吡咯苷(2.5-10 mg/kg)可以显着降低脑梗死和神经功能损伤的数量24.5-63.2%[3]。
- 脑缺血保护:在大鼠永久性大脑中动脉闭塞(MCAO)模型中,静脉注射Nicotiflorin(20 mg/kg)使梗死体积减少35.2%(TTC染色),并改善24小时神经功能评分。[2] - 肾缺血再灌注保护:在小鼠双侧肾蒂夹闭模型中,腹腔注射Nicotiflorin(40 mg/kg/天×7天)降低血清肌酐52%和尿素氮48%,减少肾小管凋亡(TUNEL法),减轻组织病理损伤。[3] - 心肌梗死保护:在大鼠左冠状动脉前降支结扎模型中,腹腔注射Nicotiflorin(80 mg/kg/天×7天)提升射血分数28%和缩短分数31%(超声心动图),同时减少梗死面积42%(TTC染色)。[4] - 脑缺血神经保护:在永久性大脑中动脉闭塞(pMCAO)小鼠模型中,Nicotiflorin(30 mg/kg,腹腔注射)于缺血后1小时给药,24小时时梗死体积减少38%,神经功能评分改善45%。化合物降低脑组织氧化应激标志物(MDA)并提高SOD活性 [2] - 肾缺血再灌注损伤保护:在双侧肾动脉夹闭大鼠模型中,Nicotiflorin(20 mg/kg,静脉注射)预处理使再灌注24小时后血清肌酐水平降低40%,血尿素氮(BUN)降低35%。免疫组化显示肾小管ATF3表达增加 [3] - 急性心肌梗死心肌保护:在大鼠急性心肌梗死(AMI)模型中,Nicotiflorin(15 mg/kg,口服)每日给药7天,梗死面积减少32%,心功能改善(EF%:48.2 ± 3.1 vs. 对照组35.6 ± 2.8)。化合物激活心脏组织Nrf2通路并抑制NF-κB信号 [4] |
| 酶活实验 |
- Nrf2荧光素酶报告基因检测:转染Nrf2响应荧光素酶报告质粒的HEK293细胞经Nicotiflorin(0.1–100 μM)处理24小时后,通过发光仪检测荧光素酶活性,显示20 μM时激活效应最大(2.5倍增加) [4]
- iNOS活性检测:LPS刺激的RAW 264.7细胞裂解液与Nicotiflorin(5–50 μM)及L-精氨酸底物共孵育,Griess试剂定量亚硝酸盐生成,剂量反应曲线确定IC₅₀ = 41.5 μM [4] |
| 细胞实验 |
- 抗糖基化实验:牛血清白蛋白(10 mg/mL)和葡萄糖(0.5 M)与Nicotiflorin(0.1-1 mM)在磷酸盐缓冲液(pH 7.4)中37°C孵育7天。荧光AGEs在激发370 nm/发射440 nm检测。CML通过ELISA定量。[1]
- 神经元保护实验:原代大鼠皮质神经元用Nicotiflorin(0.1-100 μM)预处理1小时,暴露于谷氨酸(100 μM, 15分钟),继续培养24小时。细胞活力通过MTT法评估。细胞内钙用荧光染料检测。[2] - 肾细胞凋亡实验:HK-2细胞用Nicotlorin(10-40 μM)预处理24小时,缺氧(1% O2)24小时,复氧6小时。凋亡通过Annexin V-FITC/PI流式细胞术分析。蛋白表达通过蛋白免疫印迹评估。[3] - 心肌细胞凋亡实验:H9c2细胞用Nicotiflorin(10-40 μM)预处理24小时,缺氧(1% O2)6小时,复氧12小时。细胞活力通过MTT法测定。凋亡标志物通过流式细胞术和蛋白免疫印迹分析。[4] - MTT细胞活力检测:SH-SY5Y神经元细胞(5×10³个/孔)经历6小时OGD后复氧,复氧期间加入Nicotiflorin(10–50 μM)使细胞存活率(OD₅₇₀:0.72 ± 0.05 vs. 对照组0.48 ± 0.03)显著提高 [2] - Annexin V/PI凋亡检测:H/R损伤的HK-2细胞(1×10⁶个/孔)经Nicotiflorin(25 μM)处理后,Annexin V-FITC/PI染色流式分析显示凋亡细胞比例显著降低(18.7% ± 2.3% vs. 32.1% ± 3.8%) [3] |
| 动物实验 |
脑缺血模型:雄性Sprague-Dawley大鼠在永久性大脑中动脉闭塞(MCAO)后30分钟接受静脉注射尼可替林(10或20 mg/kg,溶于生理盐水)。闭塞后24小时评估神经功能缺损。对脑组织进行切片,用于TTC染色。[2]
- 肾脏缺血再灌注损伤(IRI)模型:雄性C57BL/6小鼠预先腹腔注射尼可替林(10/20/40 mg/kg,溶于生理盐水),每日一次,连续7天。双侧肾蒂夹闭30分钟。再灌注后24小时采集血液和肾脏组织。[3] - 心肌梗死模型:雄性SD大鼠预先腹腔注射尼可替林(20/40/80 mg/kg,溶于生理盐水),每日一次,连续7天。左前降支冠状动脉被结扎。术后24小时通过超声心动图评估心脏功能。心脏切片进行TTC染色。[4] - 脑缺血模型:雄性C57BL/6小鼠(25-30 g)经腔内缝合行pMCAO。缺血后1小时腹腔注射溶于0.5% CMC-Na的尼可替福林(30 mg/kg)。24小时评估神经功能缺损评分和梗死体积。[2] - 肾脏缺血再灌注模型:Sprague-Dawley大鼠(200-250 g)行双侧肾动脉夹闭45分钟。再灌注前30分钟静脉注射溶于生理盐水的尼可替福林(20 mg/kg)。 24 小时后测定血清肌酐和尿素氮[3] - 心肌梗死模型:Wistar 大鼠(250–300 g)行左前降支冠状动脉结扎术。尼可替林(15 mg/kg)悬浮于 0.5% Tween 80 溶液中,每日口服给药,连续 7 天。第 7 天进行超声心动图检查和梗死面积分析[4] |
| 药代性质 (ADME/PK) |
口服生物利用度:在大鼠中,尼可替福林(15 mg/kg)显示出中等的口服生物利用度(F = 28.5%),给药后1.5小时血浆峰浓度(Cmax)为1.2 μg/mL [4]
- 半衰期:在大鼠中,静脉注射(20 mg/kg)后,血浆末端半衰期(t₁/₂)为3.2小时 [3] - 组织分布:在大鼠中,静脉注射2小时后,肾脏(5.8 μg/g)和心脏(4.1 μg/g)中观察到最高浓度 [4] |
| 参考文献 |
|
| 其他信息 |
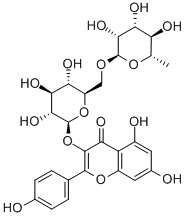
山奈酚-3-芸香糖苷是一种山奈酚O-葡萄糖苷,由山奈酚通过糖苷键连接到3位的芸香糖基[6-脱氧-α-L-甘露糖基-(1→6)-β-D-葡萄糖基]残基上构成。它已从茄属植物(Solanum campaniforme)的叶片中分离得到。它具有代谢物、自由基清除剂和植物代谢物的功能。它是一种芸香糖苷、三羟基黄酮、二糖衍生物和山奈酚O-葡萄糖苷。
据报道,烟草苷存在于茶树(Camellia sinensis)、山茶(Camellia reticulata)和其他有相关数据的生物体中。 - 结构特性:烟草苷是山奈酚-3-O-芸香糖苷,一种黄酮类糖苷。 [1] - 作用机制:神经保护作用涉及抑制钙离子内流和谷氨酸兴奋性毒性。[2] - 肾脏保护作用:通过ATF3介导的线粒体凋亡通路抑制发挥作用。[3] - 心脏保护作用:调节PI3K/AKT信号通路以抑制细胞凋亡和炎症。 [4] - 天然来源:烟酸苷是从红花(Carthamus tinctorius)和油点草(Tricyrtis maculata)中分离得到的,传统上用于心血管和脑血管保护[1,4] - 作用机制:该化合物通过Nrf2介导的抗氧化应激、ATF3诱导的抗细胞凋亡和NF-κB抑制发挥细胞保护作用[3,4] - 治疗潜力:已在缺血性卒中、心肌梗死、糖尿病并发症和肾损伤的治疗中进行研究[2,3,4] |
| 分子式 |
C27H30O15
|
|---|---|
| 分子量 |
594.5181
|
| 精确质量 |
594.158
|
| CAS号 |
17650-84-9
|
| PubChem CID |
5318767
|
| 外观&性状 |
Light yellow to yellow solid
|
| 密度 |
1.76
|
| 沸点 |
941.7±65.0 °C at 760 mmHg
|
| 熔点 |
181-186 ºC
|
| 闪点 |
312.8±27.8 °C
|
| 蒸汽压 |
0.0±0.3 mmHg at 25°C
|
| 折射率 |
1.744
|
| LogP |
1.96
|
| tPSA |
249.2
|
| 氢键供体(HBD)数目 |
9
|
| 氢键受体(HBA)数目 |
15
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
42
|
| 分子复杂度/Complexity |
985
|
| 定义原子立体中心数目 |
10
|
| SMILES |
O1[C@]([H])([C@@]([H])([C@]([H])([C@@]([H])([C@@]1([H])C([H])([H])O[C@@]1([H])[C@@]([H])([C@@]([H])([C@]([H])([C@]([H])(C([H])([H])[H])O1)O[H])O[H])O[H])O[H])O[H])O[H])OC1C(C2=C(C([H])=C(C([H])=C2OC=1C1C([H])=C([H])C(=C([H])C=1[H])O[H])O[H])O[H])=O
|
| InChi Key |
RTATXGUCZHCSNG-QHWHWDPRSA-N
|
| InChi Code |
InChI=1S/C27H30O15/c1-9-17(31)20(34)22(36)26(39-9)38-8-15-18(32)21(35)23(37)27(41-15)42-25-19(33)16-13(30)6-12(29)7-14(16)40-24(25)10-2-4-11(28)5-3-10/h2-7,9,15,17-18,20-23,26-32,34-37H,8H2,1H3/t9-,15+,17-,18+,20+,21-,22+,23+,26+,27-/m0/s1
|
| 化学名 |
5,7-dihydroxy-2-(4-hydroxyphenyl)-3-[(2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-[[(2R,3R,4R,5R,6S)-3,4,5-trihydroxy-6-methyloxan-2-yl]oxymethyl]oxan-2-yl]oxychromen-4-one
|
| 别名 |
Nicotiflorin; 17650-84-9; Kaempferol-3-O-rutinoside; Nictoflorin; NICOTIFLOROSIDE; Kaempferol 3-Rutinoside; Kaempferol-3-O-beta-rutinoside; 5,7-dihydroxy-2-(4-hydroxyphenyl)-3-[(2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-[[(2R,3R,4R,5R,6S)-3,4,5-trihydroxy-6-methyloxan-2-yl]oxymethyl]oxan-2-yl]oxychromen-4-one;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~250 mg/mL (~420.51 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (3.50 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (3.50 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (3.50 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.6820 mL | 8.4101 mL | 16.8203 mL | |
| 5 mM | 0.3364 mL | 1.6820 mL | 3.3641 mL | |
| 10 mM | 0.1682 mL | 0.8410 mL | 1.6820 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。