| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
PARP-1 ( Kd = 9 nM ); PARP-2 ( Kd = 1390 nM )
PARP-1 (IC50 = 1.3 nM); PARP-2 (IC50 = 120 nM) [1] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:NMS-P118 被发现在体外比 PARP-1/-2 双重抑制剂奥拉帕尼(现在以 Lynparza 上市)的骨髓毒性更低。 NMS-P118 被证明是代谢稳定的,它会适度抑制测试的八种亚型中的两种细胞色素 P450 家族成员(CYP-2B6 IC50:8.15 μM;CYP-2D6 IC50:9.51 μM)。根据物种不同,其阻碍骨髓细胞增殖的能力比奥拉帕尼低 5 至 60 倍以上。激酶检测:NMS-P118 在 56 种不同激酶(ABL、ACK1、AKT1、ALK、AUR1、AUR2、BRK、BUB1、CDC7/DBF4、CDK2/CYCA、CHK1、CK2、EEF2K、EGFR1、ERK2、EphA2、FAK)上进行分析, FGFR1, FLT3, GSK3beta, Haspin, IGFR1, IKK2, IR, JAK1, JAK2, JAK3, KIT, LCK, LYN, MAPKAPK2, MELK, MET, MNK2, MPS1, MST4, NEK6, NIM1, P38alpha, PAK4, POLYDATINGFRb, POLYDATINK1 、PERK、PIM1、PIM2、PKAα、PKCβ、PLK1、RET、SULU1、Syk、TLK2、TRKA、TYK2、VEGFR2、ZAP70)。所有测试的酶的 IC50 值均 >10 μM。细胞测定:使用前将 NMS-P118 溶解在 DMSO 中并用适当的培养基稀释。 PARP-1 抑制剂的细胞活性通过测量 HeLa 细胞 (ECACC) 中过氧化氢诱导的 PAR 形成的抑制来评估。通过免疫细胞化学测量细胞 PAR 水平,并使用 ArrayScan vTi 仪器进行定量。
NMS-P118强效抑制重组人PARP-1酶活性,IC50为1.3 nM,对PARP-2的选择性高达92倍 [1] 它抑制BRCA1突变的MDA-MB-436乳腺癌细胞增殖,IC50为4.7 nM;抑制BRCA2突变的CAPAN-1胰腺癌细胞增殖,IC50为3.2 nM [1] 该化合物阻断A2780卵巢癌细胞中的DNA单链断裂修复,免疫荧光检测显示20 nM时γ-H2AX灶点增加5.8倍 [1] Western blot分析显示,NMS-P118(10 nM)诱导MDA-MB-436细胞中PARP-1切割(89 kDa片段)和caspase-3激活,表明诱导凋亡 [1] 15 nM时抑制HT-29结肠癌细胞克隆形成率达78%,并在U2OS细胞中降低同源重组(HR)修复效率65% [1] 在浓度高达500 nM时,未观察到对其他DNA修复酶(如ATM、ATR)的显著抑制 [1] |
| 体内研究 (In Vivo) |
NMS-P118 被证明是代谢稳定的,它会适度抑制测试的八种同工型中的两种细胞色素 P450 家族成员(CYP-2B6 IC50,8.15 μM;CYP-2D6 IC50,9.51 μM)。 NMS-P118 体内清除率低,口服生物利用度完全。 NMS-P118 在大鼠中以 10 mg/kg 静脉注射给药以及以 10 和 100 mg/kg 口服给药的药代动力学特征与在小鼠中观察到的情况相似,口服生物利用度 >65%,并且暴露与剂量呈线性关系。其治疗在给药后 1、2 和 6 小时显着降低瘤内 PAR 水平,并在 24 小时观察到 PAR 水平部分恢复。 NMS-P118 在 BRCA1 突变的 MDA-MB-436 和 BRCA2 缺陷的 Capan-1 人类肿瘤异种移植物中显示出优异的 ADME 和药代动力学特征,在小鼠和大鼠中具有高口服利用度,并且作为单药以及与替莫唑胺联合使用均具有高功效模型,分别。
小鼠口服NMS-P118,剂量为10、30、60 mg/kg,每日一次,治疗28天后,对MDA-MB-436(BRCA1突变)异种移植瘤的生长抑制率分别为52%、76%和88% [1] 在CAPAN-1(BRCA2突变)异种移植模型中,每日口服40 mg/kg剂量与溶媒对照组相比,肿瘤体积减少82%,同时肿瘤组织中γ-H2AX表达增加 [1] 药效学分析显示,NMS-P118(30 mg/kg)抑制肿瘤PARP活性79%,并在治疗组小鼠中诱导DNA损伤(γ-H2AX升高)[1] 在BRCA缺陷的三阴性乳腺癌(TNBC)患者来源异种移植(PDX)模型中,NMS-P118(50 mg/kg,口服,每日一次)实现部分肿瘤退缩(肿瘤缩小42%)[1] |
| 酶活实验 |
NMS-P118 具有 56 种不同的激酶谱(ABL、ACK1、AKT1、ALK、AUR1、AUR2、BRK、BUB1、CDC7/DBF4、CDK2/CYCA、CHK1、CK2、EEF2K、EGFR1、ERK2、EphA2、FAK、FGFR1) , FLT3, GSK3beta, Haspin, IGFR1, IKK2, IR, JAK1, JAK2, JAK3, KIT, LCK, LYN, MAPKAPK2, MELK, MET, MNK2, MPS1, MST4, NEK6, NIM1, P38alpha, PAK4, POLYDATINGFRb, POLYDATINK1, PERK 、PIM1、PIM2、PKAα、PLK1、RET、SULU1、Syk、TLK2、TRKA、TYK2、VEGFR2、ZAP70)。对于每种测试的酶,IC50 值均大于 10 μM[1]。
采用重组人PARP-1和PARP-2酶评估抑制活性。实验在含有烟酰胺腺嘌呤二核苷酸(NAD+)、组蛋白(底物)和系列稀释的NMS-P118的缓冲液中进行。反应混合物在37°C孵育60分钟后,通过均相时间分辨荧光(HTRF)结合PAR特异性抗体定量聚腺苷二磷酸核糖(PAR)聚合物的生成量,从剂量-反应曲线计算IC50值 [1] 结合亲和力实验:采用表面等离子体共振(SPR)检测与PARP-1的相互作用。将PARP-1固定在传感器芯片上,注入系列稀释的NMS-P118,通过传感图推导结合动力学参数(ka、kd、KD),PARP-1的KD值为0.8 nM [1] |
| 细胞实验 |
NMS-P118 在使用前用适当的介质稀释并溶解在 DMSO 中。通过评估 HeLa 细胞 (ECACC) 中过氧化氢诱导的 PAR 形成的抑制作用,确定 PARP-1 抑制剂的细胞活性。 ArrayScan vTi 用于在通过免疫细胞化学测定细胞 PAR 水平后对其进行定量[1]。
癌细胞增殖实验:MDA-MB-436、CAPAN-1和HT-29细胞以2×103个细胞/孔接种到96孔板中,过夜贴壁。加入系列稀释的NMS-P118,在37°C、5% CO2环境中孵育72小时。采用比色法检测细胞活力,确定抗增殖IC50 [1] DNA损伤实验:A2780细胞用NMS-P118(0.1-50 nM)处理24小时后,固定、透化,用抗γ-H2AX抗体染色,共聚焦显微镜成像并计数荧光灶点 [1] 凋亡实验:MDA-MB-436细胞用NMS-P118(0-50 nM)处理48小时,制备细胞裂解液,通过Western blot用抗切割型PARP-1、抗切割型caspase-3抗体及总蛋白对照抗体检测 [1] 克隆形成实验:HT-29细胞以500个细胞/孔接种到6孔板中,加入NMS-P118(0-30 nM),孵育14天后,结晶紫染色并计数克隆,评估抑制效果 [1] |
| 动物实验 |
已在大鼠身上进行了专门的药代动力学研究,以考察化合物的口服生物利用度和药代动力学特征。NMS-P118 设计用于静脉推注,其溶液为 20% DMSO + 40% PEG 400 的 5% 乳糖溶液。NMS-P118 混悬液(含 0.5% 甲基纤维素)用于口服给药。每种给药途径均设置一个 100 mg/kg 剂量的口服给药组和一个 10 mg/kg 剂量的单次给药组。每项研究均使用三只雄性动物[1]。MDA-MB-436 异种移植瘤模型:将 5×10⁶ 个 MDA-MB-436 细胞皮下植入雌性裸鼠体内。当肿瘤体积达到 150–200 mm³ 时,将小鼠随机分为载体组和治疗组。 NMS-P118以0.5%羟丙基纤维素+0.1%吐温80配制,每日一次口服给药,剂量分别为10、30和60 mg/kg,持续28天。每周测量两次肿瘤体积和体重[1]
CAPAN-1异种移植模型:将1×10⁷个CAPAN-1细胞皮下接种到雄性裸鼠体内。当肿瘤体积达到200 mm³时开始治疗,每日口服NMS-P118 40 mg/kg,持续30天。在研究结束时收集肿瘤样本进行γ-H2AX免疫组织化学分析[1] TNBC PDX模型:将患者来源的TNBC肿瘤组织块植入雌性NOD/SCID小鼠体内。当肿瘤体积达到 250 mm³ 时,每日口服一次 NMS-P118(50 mg/kg),持续 21 天。采用游标卡尺测量法监测肿瘤生长情况 [1] |
| 药代性质 (ADME/PK) |
在小鼠中,单次口服20 mg/kg剂量的NMS-P118的生物利用度为64%[1]。静脉注射10 mg/kg剂量后,该化合物在小鼠体内的血浆半衰期(t1/2)为5.4小时[1]。在大鼠中,口服生物利用度为59%(20 mg/kg剂量),血浆t1/2为6.1小时[1]。该化合物具有良好的肿瘤渗透性,在MDA-MB-436异种移植小鼠中,口服给药4小时后,肿瘤/血浆浓度比为4.6[1]。在人肝微粒体中,该化合物代谢稳定性高,半衰期为280分钟[1]。在大鼠体内,该化合物的分布容积(Vd)为1.0 L/kg,表明其组织渗透性中等[1]。
|
| 毒性/毒理 (Toxicokinetics/TK) |
在一项为期28天的大鼠重复给药毒性研究中,口服剂量高达100 mg/kg/天的NMS-P118未引起显著的体重减轻或血液学参数异常[1]。NMS-P118在人血浆中的血浆蛋白结合率为94%,在小鼠血浆中为92%,在大鼠血浆中为90%[1]。在100 mg/kg/天的剂量下,观察到血清ALT和AST水平轻度且可逆的升高,但未检测到肝组织病理学改变[1]。在治疗剂量下,未观察到显著的骨髓抑制(PARP抑制剂常见的毒性)[1]。
|
| 参考文献 | |
| 其他信息 |
NMS-P118 是一种强效、口服且高选择性的 PARP-1 抑制剂,专为治疗 BRCA 缺陷型和 DNA 修复缺陷型癌症而开发 [1]。其作用机制是抑制 PARP-1 介导的 DNA 单链断裂修复,导致 DNA 损伤积累,并在同源重组 (HR) 修复缺陷的癌细胞中产生合成致死性 [1]。该化合物在 BRCA1/2 突变型乳腺癌、胰腺癌、卵巢癌和三阴性乳腺癌以及其他 HR 缺陷型恶性肿瘤中显示出治疗潜力 [1]。它对 PARP-1 的选择性远高于 PARP-2 和其他 DNA 修复酶,从而降低了脱靶毒性的风险 [1]。
|
| 分子式 |
C20H24F3N3O2
|
|
|---|---|---|
| 分子量 |
395.42
|
|
| 精确质量 |
395.18
|
|
| 元素分析 |
C, 60.75; H, 6.12; F, 14.41; N, 10.63; O, 8.09
|
|
| CAS号 |
1262417-51-5
|
|
| 相关CAS号 |
|
|
| PubChem CID |
49843531
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 沸点 |
508.3±50.0 °C at 760 mmHg
|
|
| 闪点 |
261.2±30.1 °C
|
|
| 蒸汽压 |
0.0±1.3 mmHg at 25°C
|
|
| 折射率 |
1.591
|
|
| LogP |
0.15
|
|
| tPSA |
66.6
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
3
|
|
| 重原子数目 |
28
|
|
| 分子复杂度/Complexity |
614
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
FC1(C([H])([H])C([H])([H])C([H])(C([H])([H])C1([H])[H])N1C([H])([H])C([H])([H])C([H])(C([H])([H])C1([H])[H])N1C(C2C(C(N([H])[H])=O)=C([H])C(=C([H])C=2C1([H])[H])F)=O)F
|
|
| InChi Key |
ARYVAQSYRLZVQD-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C20H24F3N3O2/c21-13-9-12-11-26(19(28)17(12)16(10-13)18(24)27)15-3-7-25(8-4-15)14-1-5-20(22,23)6-2-14/h9-10,14-15H,1-8,11H2,(H2,24,27)
|
|
| 化学名 |
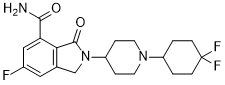
2-[1-(4,4-difluorocyclohexyl)piperidin-4-yl]-6-fluoro-3-oxo-1H-isoindole-4-carboxamide
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|---|
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5290 mL | 12.6448 mL | 25.2896 mL | |
| 5 mM | 0.5058 mL | 2.5290 mL | 5.0579 mL | |
| 10 mM | 0.2529 mL | 1.2645 mL | 2.5290 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。