| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
shp2 (IC50 = 0.318 μM); shp1 (IC50 = 0.355 μM)
SHP2 (protein tyrosine phosphatase, PTP) ( binds to the catalytic cleft) [1] - SHP1 (protein tyrosine phosphatase, PTP) (cross-inhibited in vitro) [1] - Dual-specificity phosphatase 26 (DUSP26) (competitive inhibition mode) [2][3] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:NSC-87877 是一种新型、有效、细胞渗透性的 SHP-1 和 SHP-2 PTP(蛋白酪氨酸磷酸酶)小分子抑制剂,IC50 分别为 55 和 318 nM。蛋白质磷酸化在控制细胞活动的许多调节机制中发挥着关键作用,因此涉及多种疾病。磷酸化的细胞平衡通过蛋白激酶和磷酸酶的作用来调节。因此,这些调节蛋白已成为药物开发的有希望的靶标。 NSC-87877 以剂量依赖性方式降低双特异性蛋白磷酸酶 26 (DUSP26) 的磷酸酶活性。 NSC-87877 和 DUSP26 的动力学研究揭示了竞争性抑制。NSC-87877 有效抑制 DUSP26 介导的 p38 去磷酸化,p38 是丝裂原激活蛋白激酶 (MAPK) 家族的成员。由于 DUSP26 与未分化甲状腺癌 (ATC) 细胞的存活有关,因此 NSC-87877 可能成为治疗 ATC 的治疗试剂。激酶测定:将六组氨酸标记的 DUSP26 (1 μg) 与各种 NSC-87877浓度(0、10 或 50 μM)在 PTP 测定缓冲液中在 37 °C 下预混合 15 分钟,然后在活性磷酸化 p38 (10 ng) 在 37 °C 下持续 15 分钟。通过将预孵育的样品与补充有 20 μM ATP/10 μCi 的激酶反应缓冲液(20 mM Tris-HCl (pH 7.5)、20 mM MgCl2、0.1 mM 原钒酸钠和 1 mM DTT)混合来启动激酶测定反应。 γ-32P]ATP 和 1 μg GST 激活转录因子 2 (ATF2) 作为底物。 30°C 30 分钟后,通过添加 SDS-PAGE 样品缓冲液终止反应,并通过 SDS-PAGE 分离激酶反应产物进行放射自显影。为了确认 DUSP26 不会使 ATF2 去磷酸化,通过与 p38 一起孵育对 ATF2 进行 32P 标记。孵育后,将样品与或不与 DUSP26 一起在 30 °C 下进一步孵育 30 分钟,然后通过 SDS-PAGE 进行解析。将凝胶干燥并暴露于X射线胶片。免疫复合物激酶测定。对于免疫复合物激酶测定,将 HEK 293 细胞与 HA-p38 和 FLAG-DUSP26 表达质粒共转染。转染 48 小时后,用 NSC-87877(0-100 μM,3 小时)预处理细胞,然后用 H2O2 刺激(1 mM,30 分钟)。通过离心澄清细胞提取物,并用抗HA琼脂糖珠对上清液进行免疫沉淀。将珠子用 PTP 裂解缓冲液洗涤一次,用含有 20 mM Tris-HCl (pH 7.5)、150 mM NaCl、5 mM EDTA、2 mM DTT 和 1 mM PMSF 的溶液洗涤两次,然后用含有20 mM Tris–HCl (pH 7.5) 和 20 mM MgCl2。然后将珠子重悬于含有 20 μM ATP 和 0.3 μCi [γ-32P]ATP 以及 1 μg GST-ATF2 的激酶反应缓冲液(20 mM Tris-HCl (pH 7.5)、20 mM MgCl2 和 1 mM DTT)中在 30°C 下保持 30 分钟。通过 SDS-PAGE 分离激酶反应的产物。将凝胶干燥并曝光于胶片上。体外磷酸酶测定和动力学分析。根据前述方法,在 96 孔微量滴定板测定中,使用底物 3-O-甲基荧光素磷酸盐 测量磷酸酶的活性,其浓度随每种酶的 Km 的变化而变化。 NSC-87877和 OMFP 分别溶解在 H2O 和 DMSO 中。所有反应均在终浓度 1% DMSO 下进行。最终的孵育混合物(150 μl)针对酶活性进行了优化,由 30 mM Tris-HCl (pH 7)、75 mM NaCl、1 mM 乙二胺四乙酸 (EDTA)、0.1 mM 二硫苏糖醇 (DTT)、0.33% 牛血清白蛋白组成(BSA) 和 100 nM PTP。通过添加 OMFP 启动反应,37°C 下孵育时间为 30 分钟。使用多孔板读数器(激发滤光片,485 nm;发射滤光片,535 nm)测量产物的荧光发射。该反应在实验期间呈线性,并且与酶和底物浓度成正比。半最大抑制常数 (IC50) 定义为导致 PTP 活性降低 50% 的抑制剂浓度。使用曲线拟合程序 Prism 3.0 (GraphPad Software, San Diego, CA) 确定 Lineweaver-Burk 图的半最大抑制常数和最佳曲线拟合。所有实验一式三份进行并且重复至少三次。使用活性磷酸化 MAPK 进行去磷酸化测定。将六组氨酸标签的 DUSP26 (1 µg) 与活性磷酸化 p38 (10 ng)、ERK (10 ng) 或 JNK (50 ng) 在 PTP 测定缓冲液 (30 mM Tris-HCl (pH 7), 75 mM NaCl、1 mM EDTA、0.1 mM DTT 和 0.33% BSA),并在 37°C 下孵育 30 分钟。为了确定 NSC-87877 是否在体外下调 DUSP26 对 p38 的作用,将 1 μg DUSP26 与 10 ng 活性磷酸化 p38 和各种 NSC-87877 浓度(0、10 或 100 μM)在 30 μl 反应体积中混合并在 37°C 下孵育 30 分钟。使用磷酸-MAPK 抗体对样品进行蛋白质印迹分析以检查 MAPK 的磷酸化状态。细胞测定:收获细胞,然后在 50 mM Tris-HCl (pH 8)、300 mM NaCl、1% NP-40 和 1 mM 苯甲基磺酰氟 (PMSF) 中超声裂解。裂解液在 4°C、4000 rpm 下澄清 30 分钟。通过重力流将上清液施加到 Ni-NTA 树脂柱 。用 20 mM Tris–HCl (pH 8)、500 mM NaCl、50 mM 咪唑洗涤树脂,并用 20 mM Tris–HCl (pH 8)、500 mM NaCl、200–300 mM 咪唑洗脱。将洗脱的蛋白质用 20 mM Tris-HCl、100 mM NaCl、30% 甘油、0.5 mM PMSF 透析过夜,然后储存于 -80 °C。
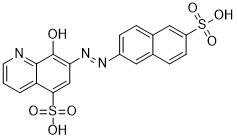
NSC-87877(化学名称:8-羟基-7-(6-磺基萘-2-基)偶氮-喹啉-5-磺酸)是一种强效且选择性的SHP2 PTP抑制剂。它在体外交叉抑制SHP1,但对其他PTPs(包括PTP1B、HePTP、DEP1、CD45和LAR)具有选择性 [1] - 它在细胞培养中抑制表皮生长因子(EGF)诱导的SHP2 PTP、Ras和Erk1/2激活,且不阻断EGF诱导的Gab1酪氨酸磷酸化或Gab1-Shp2结合。它还可抑制Gab1-Shp2嵌合体介导的Erk1/2激活,但不影响佛波醇12-肉豆蔻酸酯13-乙酸酯介导的不依赖Shp2的Erk1/2激活 [1] - NSC-87877以剂量依赖性方式抑制DUSP26磷酸酶活性,与DUSP26呈竞争性抑制动力学特征。它能有效阻断DUSP26介导的p38 MAP激酶去磷酸化 [2] - 在神经母细胞瘤(NB)细胞系(IMR32、NB-19、SH-SY5Y、SK-N-SH、SK-N-AS、SHEP)中,NSC-87877表现出剂量和时间依赖性的生长抑制作用并诱导凋亡。不同NB细胞系的IC₅₀值存在差异,从0.25 μM浓度开始即可观察到明显的细胞毒性 [3] - 用NSC-87877处理可增加NB细胞中p53在Ser37和Ser46位点的磷酸化,激活p53,并增强下游p38效应蛋白(HSP27和MAPKAPK2)的激活。它还诱导凋亡标志物PARP和caspase-3的裂解 [3] - NB细胞中NSC-87877的细胞毒性可通过shRNA敲低p53表达或用SB203580抑制p38活性部分逆转。它还能抑制NB细胞在软琼脂实验中的锚定非依赖性生长 [3] |
| 体内研究 (In Vivo) |
在 NB 肾内小鼠模型中,NSC-87877 治疗可减少肿瘤生长并增加 p53 和 p38 活性。 NSC-87877 抑制 DUSP26 是一种通过激活 p53 和 p38 丝裂原激活蛋白激酶 (MAPK) 肿瘤抑制途径在体外和体内诱导 NB 细胞细胞毒性的有效策略。
NSC-87877对NB肿瘤生长的影响[3] 为了在体内测试小分子抑制DUSP26的效果,我们使用了一个完善的肾内NB肿瘤小鼠模型将具有荧光素酶表达水平的SH-SY5Y细胞注射到雌性裸鼠左肾。肿瘤生长10天后,小鼠ig注射安慰剂对照(control)或30 mg/kg NSC-87877,每天1次,连续15天。小鼠每周ig注射荧光素并进行生物发光成像监测。图7a显示了在治疗第1天具有相似生物发光信号的等效肿瘤负荷和治疗第15天信号的差异。第15天行尸检,称肿瘤重量。对照组肿瘤显著大于nsc -87877治疗组(P<0.01;图7 b)。 在NB肾内异种移植小鼠模型(雌性NCr裸鼠植入荧光素酶标记的SH-SY5Y细胞)中,30 mg/kg NSC-87877腹腔注射15天,可显著抑制肿瘤生长,表现为肿瘤重量减轻和生物发光信号减弱 [3] - 与载体对照组相比,NSC-87877处理组小鼠的肿瘤组织中,p53(磷酸化p53 Ser46)和p38通路(磷酸化MAPKAPK2、磷酸化HSP27)的激活增强。处理组肿瘤组织中还检测到PARP和caspase-7的裂解 [3] |
| 酶活实验 |
在与活性磷酸化p38 (10 ng)在37℃下进一步孵育15分钟之前,将6 - his标记的DUSP26 (1 μg)与各种NSC-87877浓度(0、10或50 μM)在PTP实验缓冲液中预混合。从预孵育的样品开始,加入激酶反应缓冲液(20 mM Tris-HCl (pH 7.5), 20 mM MgCl2, 0.1 mM正钒酸钠和1 mM DTT),以及20 μM ATP/10 μCi [γ-32P]ATP和1 μg gst激活转录因子2 (ATF2)作为底物,开始激酶测定反应。激酶反应产物通过SDS-PAGE分离进行放射自显影,30℃下加入SDS-PAGE样品缓冲液30分钟后停止反应。为了验证DUSP26不会使ATF2去磷酸化,我们通过p38孵育对ATF2进行32P标记。样品在30°C下加或不加DUSP26孵育30分钟,使用SDS-PAGE对结果进行解析。干燥后,将凝胶暴露于x射线胶片中。
免疫复合物激酶试验。将HA-p38和FLAG-DUSP26表达质粒共转染HEK 293细胞,进行免疫复合物激酶检测。转染48 h后用H2O2 (1 mM, 30 min)刺激细胞,预处理NSC-87877 (0-100 μM, 3 h)。使用抗ha琼脂糖珠,离心去除多余的液体后免疫沉淀细胞提取物。珠粒用PTP裂解缓冲液处理一次,150 mM NaCl, 5 mM EDTA, 2 mM DTT和1 mM PMSF处理两次,再用20 mM Tris-HCl (pH 7.5), 20 mM MgCl2和5 mM EDTA的混合物处理一次。随后,将微球再次悬浮在含有20 μM ATP、0.3 μCi [γ-32P]ATP和1 μg GST-ATF2的激酶反应缓冲液(20 mM Tris-HCl (pH 7.5)、20 mM MgCl2和1 mM DTT)中,30℃下悬浮1小时。采用SDS-PAGE技术对激酶反应产物进行分离。胶片在干燥后暴露在凝胶中。 磷酸酶体外测定及动力学评价。使用基于先前发表的技术的96孔微滴板测定,使用底物3- o -甲基荧光素磷酸酯在每种酶的Km浓度不同的情况下评估磷酸酶的活性。用H2O和DMSO分别溶解NSC-87877和OMFP。每个反应都以1% DMSO为终浓度进行。最终孵育液(150 μl)含有30 mM Tris-HCl (pH 7)、75 mM NaCl、1 mM乙二胺四乙酸(EDTA)、0.1 mM二硫苏糖醇(DTT)、0.33%牛血清白蛋白(BSA)和100 nM PTPs。对该混合物的酶活性进行了优化。加入OMFP启动反应,37℃孵育30分钟。使用多孔板读取器(GENios Pro;激发滤波器,485 nm;发射滤光片(535 nm),测定产物的荧光发射。在整个实验过程中,反应与酶和底物的浓度呈线性关系。抑制剂的半最大抑制常数(IC50)定义为PTP活性下降50%的浓度。使用曲线拟合软件Prism 3.0获得Lineweaver-Burk图的最佳拟合曲线和半最大抑制常数。每个实验至少重复三次,一组三次。 使用活性磷酸化的mapk进行去磷酸化检测。在PTP实验缓冲液(30 mM Tris-HCl (pH 7)、75 mM NaCl、1 mM EDTA、0.1 mM DTT和0.33% BSA)中,将6 - his标记的DUSP26 (1 μg)与活性磷酸化的p38 (10 ng)、ERK (10 ng)或JNK (50 ng)混合。然后将混合物在37℃下孵育30分钟。在30 μl反应体积下,将1 μg DUSP26与10 ng活性磷酸化p38及不同浓度NSC-87877(0、10、100 μM)联合,观察NSC-87877是否下调DUSP26对p38的体外作用。然后将混合物在37℃下孵育30分钟。使用phospho-MAPK抗体,对样品进行Western blotting分析,以确定mapk的磷酸化状态。 PTP活性抑制实验:制备包含纯化的SHP2、SHP1或其他PTPs(PTP1B、HePTP、DEP1、CD45、LAR)与磷酸肽底物的反应混合物。向反应混合物中加入不同浓度的NSC-87877并孵育指定时间。通过检测磷酸根的释放,确定对PTP活性的抑制作用并评估选择性 [1] - DUSP26磷酸酶活性实验:制备包含纯化DUSP26和p38 MAP激酶底物的反应混合物。与不同浓度的NSC-87877共同孵育,通过检测底物的去磷酸化水平测量磷酸酶活性。进行动力学分析以确定抑制模式(竞争性抑制)[2] |
| 细胞实验 |
细胞收获后,通过在 50 mM Tris-HCl (pH 8)、300 mM NaCl、1% NP-40 和 1 mM PMSF(苯甲基磺酰氟)中超声处理进行裂解。 4°C 下 30 分钟,裂解物在 4000 rpm 下澄清。 Ni-NTA 树脂柱 通过重力流接收上清液。使用 20 mM Tris–HCl (pH 8)、500 mM 氯化钠和 200–300 mM 咪唑进行洗脱步骤后,用 20 mM Tris–HCl (pH 8)、50 mM 咪唑和 500 mM 氯化钠冲洗树脂。用 20 mM Tris-HCl、100 mM NaCl、30% 甘油和 0.5 mM PMSF 透析过夜后,洗脱的蛋白质储存在 -80 °C。
细胞活力和增殖实验:将NB细胞系或其他靶细胞接种到96孔板中。用0.25 μM至50 μM浓度的NSC-87877处理24-72小时。采用MTT法(检测540 nm处吸光度)评估细胞活力并计算IC₅₀值。长期增殖分析中,每24小时监测细胞生长,持续5-9天 [3] - Western blot分析:用指定浓度和时间的NSC-87877处理细胞。裂解细胞、提取总蛋白、经SDS-PAGE分离后转移至膜上。用针对靶蛋白(p-SHP2、Ras、Erk1/2、p-p53、p53、p-p38、HSP27、MAPKAPK2、PARP、caspase-3、caspase-7、β-肌动蛋白)的抗体孵育,检测蛋白表达、磷酸化或裂解情况 [1][3] - 软琼脂集落形成实验:将NB细胞接种到含琼脂、培养基和不同浓度NSC-87877的六孔板中。孵育2-3周后,用MTT染色集落,计数并量化锚定非依赖性生长能力 [3] - shRNA敲低挽救实验:将p53 shRNA或非沉默对照shRNA转染至NB细胞。将转染后的细胞接种到96孔板中,用NSC-87877处理48-72小时,通过MTT法评估细胞活力,验证p53在药物诱导细胞毒性中的作用 [3] - p38抑制挽救实验:将NB细胞接种到96孔板中,用5 μM SB203580(p38抑制剂)或载体预处理,然后加入不同浓度的NSC-87877。通过MTT法测量细胞活力,评估p38通路在药物诱导细胞毒性中的作用 [3] |
| 动物实验 |
雌性裸鼠肾内神经母细胞瘤 (NB) 肿瘤小鼠模型。
30 mg/kg。 腹腔注射,每日一次,持续 15 天。 RNA 干扰和 NSC-87877 对原位小鼠模型中 NB 细胞生长的影响[3] 使用雌性 Nu-nude 小鼠(Taconic Biosciences,美国纽约州哈德逊)进行 NSC-87877 的体内试验,并与对照组进行比较。如前所述30,将 SH-SY5Y 转导的荧光素酶细胞 (SY5Y-Luc) 和 SH-SY5Y 转导的 shDUSP26-1 细胞植入左肾。植入 10 天后对小鼠进行成像并测量通量。使用 5 × 107 总通量 (p/s) 的阈值来标准化接受治疗的小鼠。实验分为两组,一组腹腔注射NSC-87877(剂量为30 mg/kg/天),另一组腹腔注射等体积的0.9%氯化钠溶液作为对照。15天后进行尸检并测量肿瘤重量。为进行磷酸化免疫印迹分析,将SH-SY5Y-Luc植入三只小鼠的肾脏。当达到预先设定的通量阈值后,两只小鼠接受30 mg/kg的NSC-87877治疗,另一只小鼠接受对照注射。分别在注射NSC-87877后12小时和24小时处死小鼠并进行尸检。立即用液氮速冻肿瘤组织,以便后续提取蛋白质。将10 mg肿瘤组织研磨,与蛋白裂解缓冲液混合,通过22G针头抽吸,冰上孵育30分钟提取蛋白。[3] 肾内异种移植模型:将荧光素酶标记的SH-SY5Y细胞植入雌性NCr裸鼠的左肾。通过生物发光成像确认肿瘤建立后,将小鼠随机分为治疗组和对照组(每组n≥3)。治疗组腹腔注射NSC-87877,剂量为30 mg/kg,每日一次,连续15天;对照组注射生理盐水。每周使用生物发光成像监测肿瘤生长情况。研究结束时,处死小鼠,解剖肿瘤,称重,并提取蛋白进行Western blot分析。[3] |
| 参考文献 |
|
| 其他信息 |
8-氧代-7-[(6-磺基-2-萘基)肼基]-5-喹啉磺酸是一种萘磺酸。
Shp2 是一种非受体蛋白酪氨酸磷酸酶 (PTP),由 PTPN11 基因编码。它参与生长因子诱导的丝裂原活化蛋白 (MAP) 激酶 Erk1 和 Erk2 (Erk1/2) 的激活,并与致癌细菌幽门螺杆菌的致病性有关。此外,在儿童白血病和努南综合征中发现了 Shp2 功能获得性突变。因此,小分子 Shp2 PTP 抑制剂是评估 Shp2 作为治疗靶点以及进行 Shp2 功能化学生物学研究的必要试剂。通过筛选美国国家癌症研究所 (NCI) 多样性化合物库,我们鉴定出 8-羟基-7-(6-磺基萘-2-基)重氮基喹啉-5-磺酸 (NSC-87877) 是一种有效的 Shp2 PTP 抑制剂。分子建模和定点突变研究表明,NSC-87877 与 Shp2 PTP 的催化裂隙结合。NSC-87877 在体外对 Shp1 具有交叉抑制作用,但对 Shp2 的选择性高于其他 PTP(PTP1B、HePTP、DEP1、CD45 和 LAR)。值得注意的是,NSC-87877 可抑制表皮生长因子 (EGF) 诱导的细胞培养物中 Shp2 PTP、Ras 和 Erk1/2 的激活,但不会阻断 EGF 诱导的 Gab1 酪氨酸磷酸化或 Gab1-Shp2 的结合。此外,NSC-87877抑制了Gab1-Shp2嵌合体对Erk1/2的激活,但对佛波醇酯(PMA)诱导的Shp2非依赖性Erk1/2激活没有影响。这些结果表明,NSC-87877是首个能够在细胞培养中抑制Shp2 PTP且无明显脱靶效应的PTP抑制剂。我们的研究还首次提供了Shp2介导EGF诱导的Erk1/2 MAP激酶激活的药理学证据。[1]蛋白质磷酸化在许多调控细胞活动的机制中发挥着关键作用,因此与多种疾病相关。细胞内磷酸化平衡受蛋白激酶和磷酸酶的调控。因此,这些调控蛋白已成为药物研发的潜在靶点。本研究通过体外磷酸酶活性测定筛选蛋白酪氨酸磷酸酶(PTPs),以鉴定可被8-羟基-7-(6-磺基萘-2-基)重氮基喹啉-5-磺酸(NSC-87877)抑制的PTPs。NSC-87877是一种强效的SHP-1和SHP-2 PTPs抑制剂。双特异性蛋白磷酸酶26(DUSP26)的磷酸酶活性可被该抑制剂以剂量依赖的方式降低。NSC-87877与DUSP26的动力学研究表明二者之间存在竞争性抑制关系。NSC-87877能有效抑制DUSP26介导的丝裂原活化蛋白激酶(MAPK)家族成员p38的去磷酸化。由于DUSP26参与间变性甲状腺癌(ATC)细胞的存活,NSC-87877可能成为治疗ATC的潜在药物。[2] 双特异性蛋白磷酸酶26 (DUSP26) 在高危神经母细胞瘤 (NB) 中过表达,并通过抑制p53功能导致化疗耐药。体外实验表明,DUSP26也能有效抑制p38 MAP激酶。我们假设抑制DUSP26将以p53和/或p38介导的方式降低NB细胞的生长。NSC-87877(8-羟基-7-[(6-磺基-2-萘基)偶氮]-5-喹啉磺酸)是一种新型DUSP26小分子抑制剂,可有效抑制NB细胞系的生长并诱导其凋亡。用靶向DUSP26的小发夹RNA(shRNA)处理的NB细胞系在体外和体内均表现出增殖缺陷。用NSC-87877处理NB细胞系会导致p53磷酸化(Ser37和Ser46)和活化增加,下游p38效应蛋白(热休克蛋白27 (HSP27) 和MAP激酶活化蛋白激酶2 (MAPKAPK2))活化增加,以及聚ADP核糖聚合酶/caspase-3裂解增加。用shRNA敲低p53表达以及用SB203580(4-[4-(4-氟苯基)-2-(4-甲亚磺酰基苯基)-1H-咪唑-5-基]吡啶)抑制p38活性可部分逆转DUSP26抑制引起的细胞毒性。在肾内小鼠神经母细胞瘤(NB)模型中,NSC-87877 治疗可降低肿瘤生长并增强 p53 和 p38 的活性。这些结果共同表明,使用 NSC-87877 抑制 DUSP26 是一种有效的策略,可通过激活 p53 和 p38 丝裂原活化蛋白激酶 (MAPK) 肿瘤抑制通路,在体外和体内诱导 NB 细胞毒性。[3] NSC-87877 是通过筛选美国国家癌症研究所 (NCI) 多样性化合物库而鉴定出的 Shp2 PTP 抑制剂。分子建模和定点诱变研究表明,它与Shp2的催化裂隙结合[1] - 它是首个能够在细胞培养中抑制Shp2 PTP且无明显脱靶效应的PTP抑制剂,提供了Shp2介导EGF诱导的Erk1/2 MAP激酶激活的药理学证据[1] - DUSP26在高危神经母细胞瘤(NB)中过表达,并通过抑制p53功能导致化疗耐药。靶向DUSP26的NSC-87877代表了一种治疗神经母细胞瘤和未分化甲状腺癌(ATC)的潜在策略[2][3] |
| 分子式 |
C19H13N3O7S2
|
|
|---|---|---|
| 分子量 |
459.45
|
|
| 精确质量 |
459.019
|
|
| 元素分析 |
C, 49.67; H, 2.85; N, 9.15; O, 24.38; S, 13.96
|
|
| CAS号 |
56990-57-9
|
|
| 相关CAS号 |
NSC-87877 disodium;56932-43-5
|
|
| PubChem CID |
92577
|
|
| 外观&性状 |
Light brown to black solid powder
|
|
| 密度 |
1.7±0.1 g/cm3
|
|
| 折射率 |
1.758
|
|
| LogP |
0.12
|
|
| tPSA |
183.34
|
|
| 氢键供体(HBD)数目 |
3
|
|
| 氢键受体(HBA)数目 |
10
|
|
| 可旋转键数目(RBC) |
4
|
|
| 重原子数目 |
31
|
|
| 分子复杂度/Complexity |
883
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
N1C=CC=C2C(S(=O)(O)=O)=CC(/N=N/C3C=CC4C=C(S(O)(=O)=O)C=CC=4C=3)=C(O)C=12
|
|
| InChi Key |
XGMFVZOKHBRUTL-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C19H13N3O7S2/c23-19-16(10-17(31(27,28)29)15-2-1-7-20-18(15)19)22-21-13-5-3-12-9-14(30(24,25)26)6-4-11(12)8-13/h1-10,23H,(H,24,25,26)(H,27,28,29)
|
|
| 化学名 |
8-hydroxy-7-[(6-sulfonaphthalen-2-yl)diazenyl]quinoline-5-sulfonic acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.53 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1.67 mg/mL (3.63 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 16.7 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 View More
配方 3 中的溶解度: 3.33 mg/mL (7.25 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶 (<60°C). 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.1765 mL | 10.8826 mL | 21.7652 mL | |
| 5 mM | 0.4353 mL | 2.1765 mL | 4.3530 mL | |
| 10 mM | 0.2177 mL | 1.0883 mL | 2.1765 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Inhibitory effect of NSC-87877 in DUSP26 and kinetic analysis of DUSP26 inhibition by NSC-87877.Biochem Biophys Res Commun.2009 Apr 17;381(4):491-5. |
|---|
DUSP26 specifically dephosphorylates and inhibits p38, and NSC-87877 inhibits the action of DUSP26 on p38.Biochem Biophys Res Commun.2009 Apr 17;381(4):491-5. |
NSC-87877 inhibits the action of DUSP26 on p38in vivo.Biochem Biophys Res Commun.2009 Apr 17;381(4):491-5. |
NSC-87877 shows decreased cell proliferation in NB cell lines.Cell Death Dis. 2015 Aug; 6(8): e1841. |
|---|
Knockdown of DUSP26 inhibits NB growthin vivo.Cell Death Dis. 2015 Aug; 6(8): e1841. |
NSC-87877 induces apoptosis in NB cell linesin vitro.Cell Death Dis. 2015 Aug; 6(8): e1841. |
Inhibition of p38 or p53 results in increased cell viability despite treatment with NSC-87877.Cell Death Dis. 2015 Aug; 6(8): e1841. |
|---|
Inhibition of p38 results in decreased expression of p38 and p53 downstream proteins.Cell Death Dis. 2015 Aug; 6(8): e1841. |
NSC-87877 affects tumor growth, as well as p38 and p53 pathway expressionin vivo.Cell Death Dis. 2015 Aug; 6(8): e1841. |