| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
hCB1 ( Ki = 0.7 nM ); rCB1 ( Ki = 2.8 nM )
Cannabinoid receptor 1 (CB1) (Ki = 0.9 nM, human; IC50 = 1.2 nM for [³H]-CP55940 binding inhibition) [1][2] - Cannabinoid receptor 2 (CB2) (Ki = 850 nM, human; >940-fold lower affinity than CB1) [1][2] - No significant affinity for other GPCRs (e.g., μ-opioid, dopamine D2 receptors) (Ki > 10000 nM) [2] |
|---|---|
| 体外研究 (In Vitro) |
CP-945598 HCl 抑制 CB1 受体,具有中等的未结合微粒体清除率、低 hERG 亲和力和足够的 CNS 渗透性。 CP-945598 HCl 对人类 CB2 受体具有低亲和力,Ki 为 7.6 μM。激酶测定:由稳定转染人 CB-1 受体 cDNA 的 CHOK1 细胞制备膜。 GTPγ [35S] 结合测定以 96 孔 FlashPlate 格式重复进行,每孔使用 100 pM GTPγ [35S] 和 10μg 膜,测定缓冲液由 50 mM Tris HCl,pH 7.4、3 mM MgCl2,pH 7.4、10 组成mM MgCl2、20 mM EGTA、100 mM NaCl、30 µM GDP、0.1% 牛血清白蛋白和以下蛋白酶抑制剂:100 μg/mL 杆菌肽、100 μg/mL 苯甲脒、5 μg/mL 抑肽酶、5 μg/mL 亮肽素。然后将测定混合物与浓度逐渐增加的拮抗剂(10-10M 至 10-5 M)一起孵育 10 分钟,并用大麻素激动剂 CP-55,940 (10 μM) 进行攻击。测定在 30°C 下进行 1 小时。然后将 FlashPlates 在 2000 g 下离心 10 分钟。然后使用 Wallac Microbeta 对 GTPγ [35S] 结合的刺激进行定量。 EC50 计算是使用 GraphPad 的 Prism 完成的。反向激动是在不存在激动剂的情况下测量的。细胞测定:Otenabant (CP-945,598) 在结合 (Ki = 0.7 nM) 和功能测定 (Ki = 0.2 nM) 中对人 CB1 受体表现出亚纳摩尔效力。该化合物对人类 CB2 受体具有低亲和力 (Ki = 7600 nM)。
Otenabant (CP-945598) HCl(奥滕巴坦盐酸盐)是强效、高选择性大麻素受体1(CB1)拮抗剂,对CB2活性极低[1][2] - 在表达人CB1的HEK293细胞中,Otenabant (CP-945598) HCl(0.001-100 nM)剂量依赖性抑制[³H]-CP55940结合,IC50为1.2 nM,阻断CB1介导的环腺苷酸(cAMP)积累抑制[1][2] - 在小鼠下丘脑组织外植体中,Otenabant (CP-945598) HCl(0.1-10 μM)逆转CB1激动剂诱导的食欲素分泌抑制,使食欲素释放增加30-45%[1] - 在人脂肪细胞中,Otenabant (CP-945598) HCl(1-5 μM)抑制CB1介导的脂肪生成,减少甘油三酯积累40%[1] - 浓度高达100 μM时,对表达人CB2的CHO细胞中CB2介导的ERK磷酸化无影响[2] |
| 体内研究 (In Vivo) |
服用合成 CB1 受体激动剂 CP-55940 后,CP-945598 HCl 可逆转四种大麻素激动剂介导的行为(运动活动、体温过低、镇痛和僵住)。 CP-945598 HCl 在啮齿类动物急性食物摄入模型中表现出剂量依赖性厌食活性,并增加能量消耗和脂肪氧化。 CP-945598 还急剧刺激大鼠的能量消耗并降低呼吸商,表明代谢转变为增加脂肪氧化。在饮食诱导的肥胖小鼠的 10 天体重减轻研究中,10 mg/kg 的 CP-945598 可促进 9% 的媒介物调整体重减轻。
在饮食诱导肥胖(DIO)小鼠中,口服Otenabant (CP-945598) HCl(0.3-3 mg/kg/天,连续28天)剂量依赖性降低体重18-30%,减少食物摄入22-35%[1] - 在DIO大鼠中,口服Otenabant (CP-945598) HCl(1-10 mg/kg/天,连续21天)减少内脏脂肪量25-40%,改善胰岛素敏感性(HOMA-IR降低30%)[1] - 在小鼠高架十字迷宫实验中,口服Otenabant (CP-945598) HCl(3 mg/kg)诱导轻度焦虑样行为,减少开臂探索时间25%[1] - 小鼠治疗剂量(高达3 mg/kg/天)下未观察到显著镇静或共济失调[1] |
| 酶活实验 |
膜由已永久转染人类 CB-1 受体 cDNA 的 CHOK1 细胞制成。 GTPγ [35S] 结合测定以 96 孔 FlashPlate 格式重复进行,每孔使用 100 pM GTPγ [35S] 和 10μg 膜,测定缓冲液由 50 mM Tris HCl,pH 7.4、3 mM MgCl2,pH 组成7.4、10 mM MgCl2、20 mM EGTA、100 mM NaCl、30 µM GDP、0.1% 牛血清白蛋白和蛋白酶抑制剂 100 μg/mL 杆菌肽、100 μg/mL 苯甲脒、5 μg/mL 抑肽酶和 5 μg/ mL 亮肽素。与逐渐升高的拮抗剂浓度(10-10M 至 10-5 M)一起孵育 10 分钟后,用大麻素激动剂 CP-55,940 (10 μM) 对测定混合物进行攻击。测定在 30°C 下进行一小时。随后将 FlashPlates 在 2000 g 下离心 10 分钟。接下来,利用 Wallac Microbeta 测量 GTPγ [35S] 结合的刺激。 GraphPad Prism 用于计算 EC50。不存在激动剂用于测量反向激动。
CB1/CB2受体结合实验:制备表达人CB1/CB2的细胞膜制剂,与[³H]-CP55940(0.5 nM)及不同浓度的Otenabant (CP-945598) HCl(0.0001-10000 nM)在25°C孵育60分钟。在过量未标记CP55940存在下测定非特异性结合,过滤分离结合态配体,定量放射性强度以计算Ki值[1][2] - CB1介导的cAMP实验:表达人CB1的HEK293细胞经Otenabant (CP-945598) HCl(0.001-100 nM)预处理30分钟后,用毛喉素(10 μM)联合CB1激动剂(1 μM)刺激30分钟。ELISA法定量细胞内cAMP水平,评估CB1阻断活性[2] |
| 细胞实验 |
下丘脑食欲素分泌实验:小鼠下丘脑组织外植体接种于24孔板,经Otenabant (CP-945598) HCl(0.1-10 μM)联合CB1激动剂(1 μM)处理24小时。ELISA法定量上清液中食欲素水平[1]
- 脂肪细胞脂肪生成实验:人脂肪细胞接种于96孔板,经Otenabant (CP-945598) HCl(1-5 μM)处理72小时。比色法测定甘油三酯积累[1] - CB2信号实验:表达人CB2的CHO细胞经Otenabant (CP-945598) HCl(0.1-100 μM)预处理30分钟后,用CB2激动剂(1 μM)刺激15分钟。Western blot检测ERK磷酸化[2] |
| 动物实验 |
本研究选用14周龄雄性C57/Bl6/6J小鼠进行DIO体重减轻研究,这些小鼠此前已喂食高脂饮食(45%的能量来自脂肪)六周。年龄匹配的对照组小鼠喂食标准饲料,其平均体重至少超出实验组小鼠体重范围五个标准差。小鼠成对饲养。所有小鼠在实验开始时的平均体重为38.9±0.5 g。第0天:将小鼠随机分配至各治疗组(每组n=10)。在接下来的十天里,小鼠每天分别给予赋形剂或10 mg/kg(口服)CP-945,598。给药时间约为12小时黑暗周期开始前半小时。每日记录小鼠的食物消耗量和体重。计算每日和累积的食物消耗量以及累积体重,并进行方差分析和均值比较。统计学显著性定义为 P < 0.05。
饮食诱导肥胖 (DIO) 小鼠模型:雄性 C57BL/6 小鼠喂食高脂饮食(60% 脂肪)8 周以诱导肥胖。将盐酸奥替那班 (CP-945598) 悬浮于 0.5% CMC-Na 溶液中,以 0.3、1 和 3 mg/kg/天的剂量口服给药,持续 28 天。评估体重、食物摄入量和脂肪量 [1] - 饮食诱导肥胖 (DIO) 大鼠模型:雄性 Sprague-Dawley 大鼠喂食高脂饮食(45% 脂肪)12 周以诱导肥胖。将盐酸奥替那班 (CP-945598) 悬浮于 0.5% CMC-Na 溶液中,以 1、3 和 10 mg/kg/天的剂量口服给药,持续 21 天。测定了胰岛素敏感性和内脏脂肪量[1] - 高架十字迷宫小鼠模型:雄性ICR小鼠(20-25 g)在测试前30分钟经口灌胃给予溶于0.5% CMC-Na的盐酸奥替那班(CP-945598)(3 mg/kg)。记录开放臂探索时间[1] |
| 药代性质 (ADME/PK) |
口服生物利用度:人体口服后约为70%;大鼠口服后约为78%[1]
- 消除半衰期:人体为12-14小时;大鼠为9.5小时[1] - 血浆蛋白结合率:人血浆中为97-99%(浓度范围:0.1-10 μg/mL)[1][2] - 分布:大鼠分布容积(Vd)为1.9 L/kg,广泛分布于脑和脂肪组织[1] - 代谢:主要在肝脏经CYP3A4代谢为无活性代谢物[1] - 排泄:65-70%的剂量以代谢物形式经粪便排出;25-30%经尿液排出;<3%以原形排出[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
急性毒性:大鼠口服LD50 > 500 mg/kg;小鼠 > 400 mg/kg [1]
- 亚慢性毒性(DIO小鼠28天口服给药):剂量高达3 mg/kg/天时未见明显的肝毒性或肾毒性;10 mg/kg/天时出现轻微的短暂性焦虑[1] - 治疗剂量下血清肌酐、BUN、ALT/AST或血液学参数均无显著变化[1] - 药物相互作用:可被强效CYP3A4抑制剂(例如酮康唑)抑制,AUC增加1.8倍;与口服降血糖药无相互作用[1] |
| 参考文献 |
|
| 其他信息 |
盐酸奥替那班(CP-945598)是一种强效、高选择性的CB1受体拮抗剂,最初开发用于治疗肥胖症和代谢综合征[1][2]。其核心机制是阻断中枢神经系统(减少食物摄入)和外周组织(抑制脂肪细胞脂肪生成)中CB1介导的信号传导,从而减轻体重并改善代谢[1]。该药物曾进入肥胖症的临床试验阶段,但由于担心其与其他CB1拮抗剂类似的轻微精神副作用(焦虑)而终止[1]。对CB1受体相对于CB2受体的高选择性最大限度地减少了对免疫细胞的脱靶效应,使其能够专注于代谢和中枢神经系统相关的作用[2]。良好的口服生物利用度和较长的消除半衰期使其具有每日一次给药的潜力[1]。
|
| 分子式 |
C25H26CL3N7O
|
|
|---|---|---|
| 分子量 |
546.88
|
|
| 精确质量 |
545.126
|
|
| 元素分析 |
C, 54.91; H, 4.79; Cl, 19.45; N, 17.93; O, 2.93
|
|
| CAS号 |
686347-12-6
|
|
| 相关CAS号 |
Otenabant; 686344-29-6
|
|
| PubChem CID |
16223963
|
|
| 外观&性状 |
White solid powder
|
|
| 熔点 |
275-276℃ (decomposition)
|
|
| LogP |
6.181
|
|
| tPSA |
101.96
|
|
| 氢键供体(HBD)数目 |
3
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
6
|
|
| 重原子数目 |
36
|
|
| 分子复杂度/Complexity |
729
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
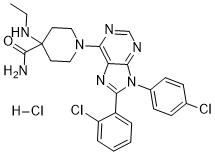
[H]Cl.ClC1=CC=CC=C1C2=NC3=C(N4CCC(NCC)(C(N)=O)CC4)N=CN=C3N2C5=CC=C(Cl)C=C5
|
|
| InChi Key |
KPYUQCJBZGQHPL-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C25H25Cl2N7O.ClH/c1-2-31-25(24(28)35)11-13-33(14-12-25)22-20-23(30-15-29-22)34(17-9-7-16(26)8-10-17)21(32-20)18-5-3-4-6-19(18)27;/h3-10,15,31H,2,11-14H2,1H3,(H2,28,35);1H
|
|
| 化学名 |
1-[8-(2-chlorophenyl)-9-(4-chlorophenyl)purin-6-yl]-4-(ethylamino)piperidine-4-carboxamide;hydrochloride
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|---|
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8286 mL | 9.1428 mL | 18.2855 mL | |
| 5 mM | 0.3657 mL | 1.8286 mL | 3.6571 mL | |
| 10 mM | 0.1829 mL | 0.9143 mL | 1.8286 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT00645463 | Completed | Drug: CP-945,598 | Obesity | Pfizer | March 2007 | Phase 1 |
| NCT00644839 | Completed | Drug: CP-945,598 | Obesity | Pfizer | April 2008 | Phase 1 |
| NCT00645216 | Completed | Drug: CP-945,598 | Obesity | Pfizer | June 2007 | Phase 1 |
| NCT00134199 | Completed | Drug: CP-945,598 Drug: sibutramine |
Obesity | Pfizer | March 2005 | Phase 2 Phase 3 |
| NCT00706537 | Completed | Drug: Active treatment Drug: Placebo |
Non-Alcoholic Steatohepatitis (NASH) |
Pfizer | July 2008 | Phase 1 |