| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
JAK3 (IC50 = 0.7 nM); JAK1 (IC50 = 3.9 nM); JAK2 (IC50 = 5 nM); Tyk2 (IC50 = 4.8 nM)
Peficitinib (ASP-015K, JNJ-54781532) is a potent, orally active Janus kinase (JAK) inhibitor with preferential activity against JAK1, JAK2, and JAK3, and moderate activity against TYK2. In recombinant human enzyme assays: - IC50 for JAK1 = 3.9 nM, IC50 for JAK2 = 5.6 nM, IC50 for JAK3 = 1.3 nM; - IC50 for TYK2 = 52 nM; - No significant inhibition of non-JAK kinases (e.g., EGFR, SRC, MAPK) at concentrations up to 10 μM (IC50 > 1000 nM for all tested non-JAK kinases) [1] |
|---|---|
| 体外研究 (In Vitro) |
氢溴酸佩菲替尼(0-100 nM;3 天)以浓度依赖性方式抑制 IL-2 驱动的 T 细胞增殖[1]。氢溴酸培菲替尼 (10-1000 nM) 在大鼠全血中的平均 IC50 为 124 nM,在人类细胞中的平均 IC50 为 127 nM,以浓度依赖性方式抑制 IL-2 诱导的 STAT5 磷酸化[1]。
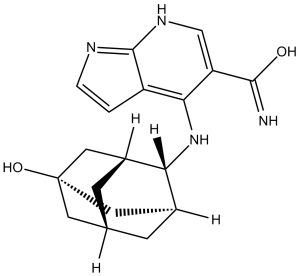
佩菲替尼的体外活性[1] pecicitinib的结构如图1所示。佩菲替尼对JAK活性的抑制呈浓度依赖性,IC50值分别为3.9 nM (JAK1)、5.0 nM (JAK2)、0.7 nM (JAK3)和4.8 nM (TYK2)(表1)。在相同的实验条件下,托法替尼的IC50值为3.7 nM (JAK1)、3.1 nM (JAK2)、0.8 nM (JAK3)和16 nM (TYK2)。这两种化合物都表现出对JAK3最有效的抑制活性。对JAK3的选择性比对JAK2的选择性高约7倍,比对托法替尼的选择性高4倍。 T细胞JAK-STAT信号抑制:在抗CD3/抗CD28抗体刺激的人外周血CD4+ T细胞中,Peficitinib(ASP-015K, JNJ-54781532) (0.1–100 nM)剂量依赖性抑制增殖:IC50 = 4.2 nM(72小时CFSE稀释法)。10 nM浓度下,磷酸化STAT3(p-STAT3,Tyr705)降低85%,磷酸化STAT5(p-STAT5,Tyr694)降低90%(蛋白质印迹法),JAK-STAT靶基因(IL-2、IFN-γ)表达降低65–70%(qPCR)[1] - 炎症因子分泌抑制:在脂多糖(LPS,1 μg/mL)或IL-6(10 ng/mL)刺激的人外周血单个核细胞(PBMC)中,Peficitinib(ASP-015K, JNJ-54781532) (0.5–50 nM)剂量依赖性降低细胞因子产生: - 10 nM使LPS诱导的TNF-α降低75%,IL-6降低80%(ELISA); - 20 nM抑制IL-6诱导的STAT3激活(p-STAT3降低90%),并抑制IL-6驱动的急性期蛋白(CRP)表达70%(qPCR)[1] - 正常细胞无细胞毒性:在人皮肤成纤维细胞和未刺激的PBMC中,Peficitinib(ASP-015K, JNJ-54781532) (≤1 μM)处理72小时后存活率>90%(MTT法),无显著凋亡(Annexin V/PI染色)[1] |
| 体内研究 (In Vivo) |
在佐剂诱导的关节炎大鼠模型中,氢溴酸培菲替尼(1-30 mg/kg;口服;每天一次,持续 24 天)在预防和治疗剂量方案中均表现出剂量依赖性有效性[1]。
在口服治疗的研究中,培菲替尼对AIA大鼠的足跖肿胀(ED50为2.7 mg/kg)和足跖骨破坏具有预防作用[1]。
值得注意的是,培菲替尼剂量依赖性地改善了AIA大鼠的足跖肿胀,并抑制了il -2诱导的STAT5磷酸化。更有趣的是,在输液泵实验中,诱导50%爪肿胀抑制的血浆浓度为29.0 ng/mL (88.9 nM),这似乎与体外全血实验中STAT5磷酸化的IC50一致(124 nM,图3B)。这些发现进一步提示jak1 /3介导的STAT5磷酸化程度可能与AIA的发病机制相关。综上所述,这些数据表明,体外il -2诱导的STAT5磷酸化测定可能是一种有用的药效学标志物,全血测定中STAT5磷酸化的抑制作用可以预测培菲替尼在AIA模型中的作用[1]。 此外,在人全血中观察到il -2诱导的STAT5磷酸化,且培菲替尼浓度依赖性地抑制STAT5磷酸化,其IC50值与大鼠全血相似。这一结果表明,在大鼠和人之间,培菲替尼对STAT5的磷酸化模式不存在种间差异[1]。 大鼠佐剂诱导关节炎(AIA)模型疗效:6–8周龄雄性Lewis大鼠通过后爪皮下注射弗氏完全佐剂(FCA)构建AIA模型,从FCA注射后第10天(关节炎发作)开始给予Peficitinib(ASP-015K, JNJ-54781532) (3 mg/kg、10 mg/kg、30 mg/kg,口服,每日1次)处理: - 30 mg/kg剂量使关节炎评分(每爪0–4分,总分0–16)从溶剂组的10.2降至3.5(P<0.001,第21天); - 关节组织病理学:30 mg/kg剂量较溶剂组减少骨侵蚀70%、软骨损伤65%、炎症细胞浸润80%; - 血清细胞因子:30 mg/kg剂量较溶剂组降低IL-6 75%、TNF-α 65%、IL-1β 60%(ELISA); - 所有处理组体重无显著下降(<3%),与溶剂组相当[1] - 关节组织JAK-STAT激活抑制:AIA大鼠关节匀浆中,Peficitinib(ASP-015K, JNJ-54781532) (30 mg/kg)较溶剂组降低p-JAK1(85%)、p-JAK2(75%)、p-STAT3(80%)水平(蛋白质印迹法),并下调关节组织IL-6和TNF-α mRNA表达70–75%(qPCR)[1] |
| 酶活实验 |
激酶分析[1]
人类JAK1、2、3和TYK2激酶结构域是市售的,使用链霉亲和素包被的96孔板进行检测。反应混合物中含有15 mM Tris-HCl (pH 7.5)、0.01%吐温20、2 mM二硫苏糖醇、10 mM MgCl2、250 nM Biotin-Lyn-Substrate-2(用于JAK1、2和3)或Biotin-IRS1-Substrate(用于TYK2)和ATP(最终浓度为200 μM [JAK1]、10 μM [JAK2]、8 μM [JAK3]和4 μM [TYK2])。将培菲替尼或托法替尼溶解在二甲亚砜中。通过添加激酶结构域启动反应,然后在室温下孵育1小时。使用磷酸酪氨酸特异性ELISA,使用酶标抗磷酸酪氨酸抗体,以生物素- lyn -底物-2或生物素- irs -底物的磷酸化速率来测量激酶活性。在ATP浓度为10 μM的条件下,对培菲替尼进行TYK2激酶检测。 重组JAK激酶活性实验(基于HTRF): 1. 将纯化的人JAK1、JAK2、JAK3或TYK2(各0.2 μg/mL)与生物素化STAT肽底物(JAK1/JAK2/TYK2用STAT3底物,JAK3用STAT5底物;各1 μg/mL)、ATP(10 μM)在实验缓冲液(50 mM Tris-HCl pH 7.5、10 mM MgCl₂、1 mM DTT)中37°C孵育15分钟。 2. 加入系列浓度的Peficitinib(ASP-015K, JNJ-54781532) (0.01–1000 nM),继续孵育30分钟。 3. 用20 mM EDTA终止反应,随后加入抗磷酸化STAT穴状化合物抗体(特异性识别STAT3的Tyr705或STAT5的Tyr694)和链霉亲和素-铕偶联物。 4. 检测时间分辨荧光(激发光340 nm,发射光665 nm/620 nm比值)以定量磷酸化STAT,将激酶活性剩余百分比(较溶剂组)拟合四参数逻辑模型计算IC50[1] |
| 细胞实验 |
细胞增殖测定[1]
细胞类型:雄性Lewis大鼠的脾细胞 测试浓度: 0 -100 nM 孵育时间: 3 天 实验结果: 以浓度依赖性方式抑制 IL-2 诱导的 T 细胞增殖,IC50 为 10 nM。 大鼠T细胞的增殖[1] 将雄性Lewis大鼠脾细胞悬浮于添加10%胎牛血清和50 μM 2-巯基乙醇的RPMI1640中,浓度为1.5 × 106个细胞/mL。用刀豆蛋白A在37℃下培养大鼠脾细胞24 h,诱导IL-2受体表达。然后将脾细胞与IL-2和指定浓度的培非替尼或托法替尼在96孔组织培养板中孵育。孵育3天后,将alamarBlue®添加到每个测试孔中,然后孵育4-6小时。在545 nm的激发波长和590 nm的发射波长下测量荧光强度。所有实验都进行了三次,实验分别进行了四次或一次,分别使用了培非替尼或托法替尼。对于每个个体,分别用细胞和培养基单独培养的孔作为空白,用不含JAK抑制剂的IL-2刺激细胞作为对照。为了计算JAK抑制剂的抑制率,空白和对照分别被指定为100%和0%的抑制率。 人CD4+ T细胞增殖实验(CFSE稀释法): 1. 磁珠分选法从PBMC中分离人CD4+ T细胞,用CFSE(5 μM)37°C标记15分钟。 2. 标记T细胞(1×10⁵细胞/孔)接种于96孔板,用抗CD3(2 μg/mL)和抗CD28(1 μg/mL)抗体刺激,同时加入Peficitinib(ASP-015K, JNJ-54781532) (0.1–100 nM)。 3. 72小时后,流式细胞术检测CFSE稀释程度评估增殖,通过非增殖细胞百分比计算IC50[1] - PBMC炎症因子分泌实验(ELISA): 1. 人PBMC(1×10⁶细胞/mL)接种于24孔板,用Peficitinib(ASP-015K, JNJ-54781532) (0.5–50 nM)预处理1小时。 2. 用LPS(1 μg/mL)或IL-6(10 ng/mL)刺激细胞,37°C、5% CO₂孵育24小时。 3. 收集培养上清,夹心ELISA法检测TNF-α、IL-6或IL-1β浓度,计算较溶剂组的细胞因子抑制百分比[1] - Jurkat细胞p-STAT蛋白质印迹实验: 1. Jurkat T细胞(2×10⁵细胞/孔)用无血清培养基饥饿4小时,随后用Peficitinib(ASP-015K, JNJ-54781532) (0.1–50 nM)处理1小时。 2. 用IL-6(10 ng/mL)刺激细胞30分钟,含蛋白酶/磷酸酶抑制剂的RIPA缓冲液裂解细胞。 3. 30 μg蛋白经10% SDS-PAGE电泳后转移至PVDF膜,4°C过夜孵育抗p-STAT3(Tyr705)、抗p-STAT5(Tyr694)或抗STAT3/5(内参)抗体。 4. 膜与HRP标记二抗孵育,ECL显色可视化条带,密度分析法定量p-STAT相对总STAT的水平[1] |
| 动物实验 |
动物/疾病模型: 7周龄雌性Lewis大鼠,佐剂诱导关节炎(AIA)模型[1]
剂量: 1、3、10和30 mg/kg 给药途径: 口服,每日一次,持续24天 实验结果: 剂量为1 mg/kg或更高时,显著抑制爪体积的增加,ED50值为2.7 mg/kg(95%置信区间:1.5–4.2 mg/kg)。在 10 mg/kg 或更高剂量下,骨破坏评分显著降低;在 30 mg/kg 剂量下,爪肿胀和骨破坏评分几乎完全缓解。 在口服给药方案中,四个佐剂注射组每天一次服用溶于 0.5% 甲基纤维素 (MC) 的 peficitinib(剂量分别为 1、3、10 和 30 mg/kg)。正常组和对照组大鼠仅服用 0.5% MC。采用上述同一组大鼠,分别进行预防性和治疗性两种不同的给药方案。在预防性给药方案中,大鼠在佐剂注射后第二天开始,连续 24 天每天服用 peficitinib 或 0.5% MC。在佐剂注射后第4、10、15、21和25天测量体重,并在佐剂注射后第10、15、21和25天测量爪体积。对于治疗剂量方案,根据第15天的体重和左后爪体积增加情况,将注射佐剂的大鼠平均分组。大鼠在第15至24天接受peficitinib或0.5% MC治疗,并在佐剂注射后第15、18、21和25天测量体重和爪体积。[1] 在预防和治疗剂量方案中,在测量体重和爪体积后,于第25天处死大鼠,并收集每只动物的左后爪。在腹腔输注方案中,将培非替尼溶解于聚乙二醇和等体积的500 mM乙酸溶液中,浓度分别为1、2和4 mg/mL,并在佐剂注射后第9天通过腹腔输注给药。输注泵在无菌条件下植入,并使用异氟烷麻醉。剂量水平计算为每只大鼠每日约0.12、0.24和0.48 mg,或每公斤体重每日约0.75、1.5和3 mg。正常组和对照组大鼠均接受了输注泵植入手术,并给予赋形剂。在佐剂注射后第0、9、15、18、21和24天测量体重和爪体积。[1] 大鼠佐剂诱导关节炎 (AIA) 模型方案:1. 雄性Lewis大鼠(6-8周龄,180-220 g)在实验前适应环境7天。第0天,通过向右后爪皮下注射0.1 mL含有热灭活结核分枝杆菌的弗氏完全佐剂 (FCA) 来诱导AIA。2. 在FCA注射后第10天(出现关节炎症状:爪肿胀≥0.5 mm vs. 基线),将大鼠随机分为4组(每组n=6):- 载体组:0.5%甲基纤维素PBS溶液,灌胃,每日一次; - 培非替尼(ASP-015K,JNJ-54781532)3 mg/kg组:溶于0.5%甲基纤维素溶液,灌胃给药,每日一次;- 培非替尼(ASP-015K,JNJ-54781532)10 mg/kg组:溶剂和给药途径与3 mg/kg组相同;- 培非替尼(ASP-015K,JNJ-54781532)30 mg/kg组:溶剂和给药途径与3 mg/kg组相同。3. 治疗持续11天(至FCA给药后第21天)。每日测量体重和关节炎评分(每爪0-4分:0 = 正常,1 = 轻度肿胀,2 = 中度肿胀,3 = 重度肿胀,4 = 关节畸形;总分0-16分)。4. 第21天,处死大鼠。采集血液样本用于检测血清细胞因子(ELISA)。取后肢关节组织,固定于10%福尔马林溶液中,脱钙,石蜡包埋,进行组织病理学分析(苏木精-伊红染色),以评估骨侵蚀、软骨损伤和炎症浸润[1]。 |
| 药代性质 (ADME/PK) |
一项使用雌性SD大鼠进行为期4周的重复口服给药研究,以3 mg/kg剂量给予peficitinib,药代动力学数据显示,血浆峰浓度(Cmax)为367 ng/mL,AUC为834 ng·h/mL,谷浓度(Ctrough)为2.9 ng/mL(未发表数据)。结合本研究的药代动力学数据,在ED50时,Cmax估计为330 ng/mL,AUC为751 ng·h/mL,Ctrough为2.6 ng/mL。[1]
在我们研究持续输注效应时,测定了腹腔输注peficitinib的血浆浓度,并估计爪肿胀的EC50为29.0 ng/mL。因此,AUC 计算为 696 ng·h/mL (29.0 ng/mL × 24 h)——与口服 peficitinib 的暴露水平相似,尽管持续输注和口服给药的血浆浓度变化有所不同。这些发现表明,peficitinib 对 AIA 模型中爪肿胀的疗效取决于 AUC 而不是 Cmax 或 Ctrough,这为临床给药方案的设计提供了潜在的重要见解。[1] 大鼠口服生物利用度:雄性 Lewis 大鼠(200–250 g)通过灌胃(10 mg/kg)或静脉注射(2 mg/kg)接受 peficitinib(ASP-015K,JNJ-54781532):- 口服生物利用度 = 78%; - 口服给药:血浆峰浓度(Cmax)= 4.5 μg/mL,达峰时间(Tmax)= 1.2 小时,末端半衰期(t1/2)= 5.3 小时,血浆浓度-时间曲线下面积(AUC0-24h)= 25.8 μg·h/mL; - 静脉给药:Cmax = 10.2 μg/mL,t1/2 = 4.9 h,AUC0-∞ = 33.1 μg·h/mL [1] - 血浆蛋白结合率:在人血浆中,Peficitinib(ASP-015K,JNJ-54781532)的蛋白结合率为 94%(通过 37°C 平衡透析法测定)[1] - AIA 大鼠组织分布:AIA 大鼠口服 Peficitinib(ASP-015K,JNJ-54781532)(30 mg/kg)后 2 小时,关节组织浓度为 5.2 μg/g,脾脏浓度为 4.8 μg/g,分别约为血浆浓度(4.3 μg/mL)的 1.2 倍和 1.1 倍。 [1] |
| 毒性/毒理 (Toxicokinetics/TK) |
大鼠重复给药毒性(28 天):雄性/雌性 Lewis 大鼠(每性别每组 n=4)接受 Peficitinib(ASP-015K,JNJ-54781532)(5 mg/kg、30 mg/kg、100 mg/kg,口服,每日一次)28 天:- 未观察到死亡;未观察到不良反应水平(NOAEL)为 30 mg/kg;- 在 100 mg/kg 时:观察到轻度淋巴细胞减少症(淋巴细胞计数比对照组减少 23%),但未检测到肝脏、肾脏或脾脏的组织病理学变化。血清ALT、AST、肌酐和BUN水平保持在正常范围内[1]
- AIA模型体内安全性:在接受Peficitinib(ASP-015K,JNJ-54781532)(剂量高达30 mg/kg,口服,11天)治疗的AIA大鼠中: - 未观察到明显的毒性反应(例如嗜睡、腹泻、食欲减少); - 体重变化与载体组相当(差异<3%); - 血清电解质和肝肾功能参数(ALT、AST、肌酐、BUN)均正常[1] |
| 参考文献 | |
| 其他信息 |
Peficitinib 已被用于研究银屑病、药效学、药物相互作用、溃疡性结肠炎和类风湿性关节炎等疾病的治疗和基础科学的试验中。
作用机制:Peficitinib(ASP-015K,JNJ-54781532)通过竞争性抑制 JAK1、JAK2 和 JAK3(JAK-STAT 信号通路中的关键激酶)发挥抗炎作用。它通过阻止 STAT 蛋白(例如 STAT3、STAT5)的磷酸化来阻断其活化,从而抑制促炎细胞因子(IL-6、TNF-α、IL-1β)的转录和活化 T 细胞的增殖——这些是类风湿性关节炎等自身免疫性疾病发病机制中的关键过程[1] - 治疗潜力:来自大鼠 AIA 模型的临床前数据支持 Peficitinib(ASP-015K,JNJ-54781532)作为治疗类风湿性关节炎 (RA) 和其他 JAK-STAT 介导的自身免疫性疾病的候选药物。其口服生物利用度高、组织分布良好(尤其对炎症关节),且治疗剂量下毒性低,使其适合长期口服给药[1] - 药物设计特点:Peficitinib(ASP-015K,JNJ-54781532)旨在靶向多种JAK亚型(JAK1/JAK2/JAK3),从而广泛抑制炎症信号通路,同时保持对非JAK激酶的选择性,以最大限度地减少脱靶副作用[1] |
| 分子式 |
C18H22N4O2
|
|
|---|---|---|
| 分子量 |
326.39
|
|
| 精确质量 |
326.174
|
|
| 元素分析 |
C, 66.24; H, 6.79; N, 17.17; O, 9.80
|
|
| CAS号 |
944118-01-8
|
|
| 相关CAS号 |
Peficitinib hydrobromide;1353219-05-2;Peficitinib hydrochloride;1353219-06-3
|
|
| PubChem CID |
57928403
|
|
| 外观&性状 |
Light yellow to yellow solid powder
|
|
| 密度 |
1.5±0.1 g/cm3
|
|
| 折射率 |
1.777
|
|
| LogP |
3.26
|
|
| tPSA |
105.02
|
|
| 氢键供体(HBD)数目 |
4
|
|
| 氢键受体(HBA)数目 |
4
|
|
| 可旋转键数目(RBC) |
3
|
|
| 重原子数目 |
24
|
|
| 分子复杂度/Complexity |
525
|
|
| 定义原子立体中心数目 |
2
|
|
| SMILES |
C1[C@@H]2CC3(C[C@@H](C2NC4=C5C=CNC5=NC=C4C(=O)N)CC1C3)O
|
|
| InChi Key |
DREIJXJRTLTGJC-JQCLMNFQSA-N
|
|
| InChi Code |
InChI=1S/C18H22N4O2/c19-16(23)13-8-21-17-12(1-2-20-17)15(13)22-14-10-3-9-4-11(14)7-18(24,5-9)6-10/h1-2,8-11,14,24H,3-7H2,(H2,19,23)(H2,20,21,22)/t9?,10-,11+,14?,18?
|
|
| 化学名 |
4-[[(1R,3S)-5-hydroxy-2-adamantyl]amino]-1H-pyrrolo[2,3-b]pyridine-5-carboxamide
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (7.66 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (7.66 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.0638 mL | 15.3191 mL | 30.6382 mL | |
| 5 mM | 0.6128 mL | 3.0638 mL | 6.1276 mL | |
| 10 mM | 0.3064 mL | 1.5319 mL | 3.0638 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03971253 | Recruiting | Drug: Peficitinib | Rheumatoid Arthritis (RA) | Astellas Pharma Inc | September 2, 2019 | |
| NCT04143477 | Completed | Drug: peficitinib | Healthy Volunteers | Astellas Pharma China, Inc. | December 5, 2019 | Phase 1 |
| NCT02531191 | Completed | Drug: peficitinib | Healthy Volunteers | Astellas Pharma Inc | June 21, 2015 | Phase 1 |
| NCT02111317 | Completed | Drug: ASP015K Drug: verapamil |
Healthy Subjects Pharmacokinetics of ASP015K |
Astellas Pharma Global Development, Inc. |
October 2013 | Phase 1 |
American College of Rheumatology (ACR) response rates at week 12 (full analysis set population).Ann Rheum Dis.2016 Jun;75(6):1057-64. |
 |
|