| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
A3AR; IB-MECA acts as an agonist at the A₃-adenosine receptor. Its affinity for the rat brain A₃-adenosine receptor is reported with a Kᵢ value of 1.1 nM [1].
|
|---|---|
| 体外研究 (In Vitro) |
在大鼠 RBL-2H3 肥大细胞中,IB-MECA 可刺激磷酸肌醇分解,通过 [³H]IP₁ 的积累来测定。该作用对 [³H]IP₁ 积累的 EC₅₀ 值为 8.5 ± 1.7 μM [1]。
IB-MECA 在 RBL-2H3 细胞中可引起细胞内钙水平 ([Ca²⁺]ᵢ) 的浓度依赖性升高。该反应的效力强于其对磷酸肌醇分解的作用,EC₅₀ 值为 0.11 ± 0.005 μM。它是所测试化合物中针对该效应最有效的药物之一 [1]。 与 NECA(设为 100%)相比,IB-MECA 在升高 [Ca²⁺]ᵢ 方面的相对效能为 55%,相对较高 [1]。 Piclidenoson能够抑制Forskolin刺激的cAMP水平,在OVCAR-3细胞和Caov-4细胞中的EC50分别为0.82 μM和1.2 μM[2]。 Piclidenoson (0.0001-100 μM;48小时)以剂量依赖的方式显着降低人卵巢系的细胞活力,对OVCAR-3和Caov-4细胞的IC50分别为32.14 μM和45.37 μM[2]。 Piclidenoson (0.001-100 μM;48小时)通过半胱天冬酶途径途径途径。 Cell Proliferation Assay[2] Cell Line: OVCAR-3 cells, Caov-4 cells Concentration: 0.0001-100 μM Incubation Time: 48 Ⅲ系透明度[2]。小时 结果:导致细胞活力呈剂量依赖性降低。细胞凋亡分析[2] 细胞系:OVCAR-3 细胞、Caov-4 细胞 浓度:0.1 μM、1 μM、10 μM、50 μM、100 μM 孵育时间:48 小时 结果:某一浓度下细胞凋亡百分比显着增加依赖方式。 Western Blot分析[2] 细胞系:OVCAR-3细胞、Caov-4细胞 浓度:1 μM、10 μM、100 μM 孵育时间:48小时 结果:Bcl-2表达明显降低,Bax表达增加蛋白质。 |
| 体内研究 (In Vivo) |
动物模型:3月龄B10CBAF1雄性小鼠(平均30 g)[1] 剂量:105 μg/kg 给药方式:腹腔注射,0.5 Piclidenoson (105 μg/kg;ip) 提高 γ 辐射小鼠的休眠率[3]。照射后 h 结果:与对照受照射小鼠相比,平均存活时间显着增加。
• 对接受 8.5 Gy γ 射线致死剂量全身照射的雄性B10CBAF1小鼠,于照射后 0.5 小时腹腔单次给予Piclidenoson (IB-MECA)(105 μg/kg),可使小鼠平均存活时间(MST)显著提升至 23.3 天(95% 置信区间:20.3;26.3),与对照组的 18.1 天(95% 置信区间:15.1;21.1)相比,log-rank 检验 P=0.020;单药处理组小鼠的 30 天累积存活率(CPS)为 56.0%(95% 置信区间:34.8;72.7),高于对照组的 28.0%(95% 置信区间:12.4;46.0),但 Fisher 精确检验显示无统计学意义(P=0.084)[3] • 对 8.5 Gy γ 射线照射的雄性B10CBAF1小鼠,联合给予Piclidenoson (IB-MECA)(照射后 0.5 小时腹腔单次 105 μg/kg)和美洛昔康(照射后 1 小时腹腔单次 20 mg/kg),使小鼠 MST 达到 24.9 天(95% 置信区间:21.9;27.8),较对照组提升的统计学显著性最高(P=0.003),且是所有处理组中唯一使 CPS 产生统计学显著升高的方案,CPS 达 68.0%(95% 置信区间:46.1;82.5),与对照组相比 P=0.010 [3] • 在亚致死剂量 γ 射线照射的小鼠中,Piclidenoson (IB-MECA)与美洛昔康联合给药时,二者的造血刺激作用可相互增强 [3] • 在受辐射的哺乳动物机体中,Piclidenoson (IB-MECA)可刺激造血祖细胞增殖和骨髓粒细胞系统活化,同时作为骨髓造血的稳态调节剂发挥作用 [3] • 若在小鼠受照射后 24 小时及更晚时间开始给予Piclidenoson (IB-MECA),即使给药 2~9 次,也无法对致死剂量照射小鼠的存活指标产生显著影响 [3] • Piclidenoson (IB-MECA)可诱导粒细胞集落刺激因子(G-CSF)的产生,该因子有助于缓解辐射诱导的细胞凋亡,减轻辐射损伤 [3] |
| 细胞实验 |
在大鼠 RBL-2H3 肥大细胞中,IB-MECA 可刺激磷酸肌醇分解,通过 [³H]IP₁ 的积累来测定。该作用对 [³H]IP₁ 积累的 EC₅₀ 值为 8.5 ± 1.7 μM [1]。
IB-MECA 在 RBL-2H3 细胞中可引起细胞内钙水平 ([Ca²⁺]ᵢ) 的浓度依赖性升高。该反应的效力强于其对磷酸肌醇分解的作用,EC₅₀ 值为 0.11 ± 0.005 μM。它是所测试化合物中针对该效应最有效的药物之一 [1]。 与 NECA(设为 100%)相比,IB-MECA 在升高 [Ca²⁺]ᵢ 方面的相对效能为 55%,相对较高 [1]。 细胞系:OVCAR-3 细胞、Caov-4 细胞 浓度:0.0001-100 μM 孵育时间:48 小时 结果:导致细胞活力呈剂量依赖性降低。 |
| 动物实验 |
3月龄B10CBAF1雄性小鼠(平均30克)
105 μg/kg 腹腔注射,照射后0.5小时 • 实验动物:3月龄雄性B10CBAF1小鼠,平均体重30克,在受控条件下饲养,可自由摄取标准化颗粒饲料和盐酸处理过的自来水;所有动物实验程序均符合欧洲共同体指南,并经研究所伦理委员会批准[3] • 照射程序:小鼠接受全身γ射线照射,使用60Co源,剂量率为0.5 Gy/min,致死总剂量为8.5 Gy[3]• Piclidenoson (IB-MECA)药物制备:首先溶解于二甲基亚砜(DMSO)中,然后用无菌生理盐水稀释至最终DMSO浓度为2%[3] • 单独给予Piclidenoson (IB-MECA):在8.5 Gy γ射线照射后0.5小时,单次腹腔注射(ip) 105 μg/kg,体积为0.2 ml;该组对照小鼠在同一时间点腹腔注射含2% DMSO的溶剂[3] • 联合使用Piclidenoson (IB-MECA)和美洛昔康:Piclidenoson (IB-MECA)于照射后0.5小时单次腹腔注射105 μg/kg (0.2 ml),美洛昔康(溶于0.9%无菌生理盐水)于照射后1小时单次腹腔注射20 mg/kg (0.2 ml);总对照组在相应时间间隔接受两次溶剂注射[3] • 生存观察:每日记录实验小鼠的生存状况,直至照射后30天;该实验重复5次,每组5只动物(每组共25只动物)[3] • 统计分析:采用Kaplan-Meier方法分析生存时间,从Kaplan-Meier曲线得出中位生存时间(MST);采用log-rank检验比较各组间MST的差异,采用Fisher精确检验比较各组间CPS的差异,显著性水平设定为P≤0.05 [3] |
| 参考文献 |
|
| 其他信息 |
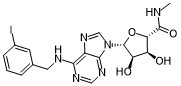
3-碘苄基-5'-N-甲基羧酰胺腺苷是腺苷的衍生物,其中5'-羟甲基被N-乙基羧酰胺基取代,且外环氨基上的一个氢原子被3-碘苄基取代。它是一种腺苷A3受体激动剂。它属于腺苷类化合物,是一种有机碘化合物和单羧酸酰胺。其功能与腺苷相关。
CF 101(通用名为IB-MECA)是一种用于治疗类风湿性关节炎的抗炎药。其独特的作用机制在于拮抗腺苷A3受体。CF101为口服药物,具有良好的安全性。它还被考虑用于治疗其他自身免疫性炎症性疾病,例如克罗恩病、银屑病和干眼症。 匹克利德诺森是一种口服生物利用度高的腺苷A3受体(A3AR)激动剂,具有潜在的抗炎活性。给药后,匹克利德诺森选择性地靶向、结合并激活细胞表面表达的A3AR,从而激活A3AR发挥关键作用的信号转导通路。这抑制了核因子-κB(NF-κB)信号传导,并抑制了炎症细胞因子(例如肿瘤坏死因子(TNF)和多种白细胞介素)的产生。 A3AR 是一种 G 蛋白偶联受体,在多种炎症性疾病和某些类型的癌症中发挥着关键作用。 药物适应症 已研究用于治疗癌症/肿瘤(未具体说明)、眼部疾病/感染、银屑病及银屑病相关疾病以及类风湿性关节炎。Can-Fite BioPharma 公司报告称,CF101 通过靶向腺苷 A3 受体,也可用于治疗克罗恩病,一种严重的胃肠道疾病。 作用机制 CF101 是一种 A3AR 激动剂。A3AR 在炎症细胞中高表达,并在外周血单核细胞中过表达,这反映了其在远端炎症过程中的作用。在正常组织中,腺苷 A3 受体的表达较低。用特定激动剂激活 A(3)AR 可使炎症细胞中的 NF-kappaB 信号通路失调,并启动免疫调节作用。 |
| 分子式 |
C18H19IN6O4
|
|---|---|
| 分子量 |
510.28
|
| 精确质量 |
510.051
|
| 元素分析 |
C, 42.37; H, 3.75; I, 24.87; N, 16.47; O, 12.54
|
| CAS号 |
152918-18-8
|
| 相关CAS号 |
152918-18-8
|
| PubChem CID |
123683
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
2.0±0.1 g/cm3
|
| 折射率 |
1.808
|
| LogP |
2.08
|
| tPSA |
134.42
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
8
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
29
|
| 分子复杂度/Complexity |
589
|
| 定义原子立体中心数目 |
4
|
| SMILES |
IC1=C([H])C([H])=C([H])C(=C1[H])C([H])([H])N([H])C1=C2C(=NC([H])=N1)N(C([H])=N2)[C@@]1([H])[C@@]([H])([C@@]([H])([C@@]([H])(C(N([H])C([H])([H])[H])=O)O1)O[H])O[H]
|
| InChi Key |
HUJXGQILHAUCCV-MOROJQBDSA-N
|
| InChi Code |
InChI=1S/C18H19IN6O4/c1-20-17(28)14-12(26)13(27)18(29-14)25-8-24-11-15(22-7-23-16(11)25)21-6-9-3-2-4-10(19)5-9/h2-5,7-8,12-14,18,26-27H,6H2,1H3,(H,20,28)(H,21,22,23)/t12-,13+,14-,18+/m0/s1
|
| 化学名 |
(2S,3S,4R,5R)-3,4-dihydroxy-5-(6-(3-iodobenzylamino)-9H-purin-9-yl)-N-methyltetrahydrofuran-2-carboxamide
|
| 别名 |
ALB-7208; ALB 7208; CF101; IB-MECA; CF-101; CF 101; ALB7208; IB MECA; Piclidenoson
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ≥ 45 mg/mL (~88.2 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (4.90 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (4.90 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (4.90 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9597 mL | 9.7985 mL | 19.5971 mL | |
| 5 mM | 0.3919 mL | 1.9597 mL | 3.9194 mL | |
| 10 mM | 0.1960 mL | 0.9799 mL | 1.9597 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04333472 | Completed | Drug: Piclidenoson Drug: Placebo |
COVID-19 Coronavirus Infection |
Can-Fite BioPharma | January 6, 2021 | Phase 2 |
| NCT00349466 | Completed | Drug: CF101 Drug: Placebo |
Keratoconjunctivitis Sicca | Can-Fite BioPharma | January 2007 | Phase 2 |
| NCT01034306 | Completed | Drug: CF101 Drug: Placebo control |
Rheumatoid Arthritis | University of Alberta | October 2010 | Phase 2 |
| NCT03168256 | Active Recruiting |
Drug: CF101 2mg Biological: Plerixafor |
Sickle Cell Disease | Sangamo Therapeutics | March 6, 2019 | Phase 1 Phase 2 |
| NCT02570542 | Active Recruiting |
Drug: Plerixafor Drug: CF101 3mg |
Can-Fite BioPharma | University of Chicago | September 15, 2018 | Phase 3 |