| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| Other Sizes |
|
| 靶点 |
Pradefovir is a PMEA prodrug that is cyclic diester. It is one of the HepDirect prodrugs made to be selectively and potently activated by oxidative processes mediated by the liver-based enzyme CYP3A4. With a Km of 60 μM, a maximum metabolic rate of 228 pmol/min/mg protein, and an intrinsic clearance rate of around 359 L/min, pradefovir is transformed into PMEA in human liver microsomes [1].
|
|---|---|
| 体外研究 (In Vitro) |
Pradefovir 是一种 PMEA 前药,是环状二酯。它是 HepDirect 前药之一,可被肝脏酶 CYP3A4 介导的氧化过程选择性且有效地激活。普拉德福韦的 Km 为 60 μM,最大代谢率为 228 pmol/min/mg 蛋白质,内在清除率约为 359 L/min,在人肝微粒体中转化为 PMEA [1]。
在人类肝微粒体中,Pradefovir 被 CYP3A4 代谢活化为 PMEA,其 Km 为 60 µM,最大代谢速率为 228 pmol/min/mg 蛋白,内在清除率约为 3.8 µl/min/mg 蛋白。[1] 浓度为 0.2、2 和 20 µM 的 Pradefovir 在人类肝微粒体中既不是 CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP2E1 或 CYP3A4 的直接抑制剂,也不是基于机制的抑制剂。[1] 酮康唑(一种 CYP3A4 抑制剂)和 CYP3A4 抑制性单克隆抗体 (MAb 3A4) 在人类肝微粒体中显著抑制了 pradefovir 向 PMEA 的转化,证实了 CYP3A4 在其代谢活化中的主要作用。0.5 µM 的酮康唑基本上完全抑制了该活化过程。[1] 在人类原代肝细胞培养中,浓度高达 10 µg/ml 的 pradefovir 未诱导 CYP1A2 或 CYP3A4/5 的酶活性。[1] |
| 体内研究 (In Vivo) |
连续八天,给大鼠口服 300 mg/kg 的普德福韦。大鼠体重、肝脏重量、肝脏重量与体重比、肝微粒体蛋白含量、总CYP含量、CYP1A、CYP2B、CYP3A酶活性水平,CYP1A1、CYP2B1/2、CYP3A1/2脱辅基蛋白含量,和 CYP4A1/3 均不受影响,表明普地福韦不会诱导大鼠体内的 CYP [1]。
在门静脉插管的大鼠中口服给予 pradefovir (30 mg/kg) 后,在给药后 5 分钟的系统血浆中检测到 PMEA,但在门静脉血浆中未检测到,这表明在大鼠体内,肝脏(而非小肠)是代谢活化的主要部位。[1] 大鼠每日口服 pradefovir (300 mg/kg/天,持续 8 天) 并未诱导 CYP1A、CYP2B 或 CYP3A 的酶活性或其脱辅基蛋白水平,表明 pradefovir 在大鼠中不是 CYP 诱导剂。[1] |
| 酶活实验 |
为确定负责 pradefovir 活化的 CYP 同工酶,将 pradefovir (1.63 µM) 与一组 cDNA 表达的人类 CYP 超微粒体(包括 1A1、1A2、1B1、2A6、2B6、2C8、2C9、2C18、2C19、2D6、2E1、3A4 和 3A5)一起孵育。只有 CYP3A4 在将 pradefovir 转化为 PMEA 方面显示出显著的活性。加入不同浓度的酮康唑(0、0.05、0.1、0.2、0.5、1 和 2 µM)以确认抑制作用。[1]
通过将 pradefovir (1.63 至 40.8 µM) 与混合的人类肝微粒体 (0.4 mg/ml) 孵育 15 分钟来研究酶动力学。反应遵循米氏动力学,动力学参数(Km、Vmax)通过 Lineweaver-Burk 图推导得出。[1] 通过在人类肝微粒体中共同孵育 pradefovir 与酮康唑或 CYP3A4 抑制性单克隆抗体来进行抑制研究。使用斜率对抑制剂浓度图测定酮康唑的抑制常数 (Ki) 为 12.5 nM,Dixon 图分析表明其为非竞争性抑制。[1] 为了评估 pradefovir 作为各种 CYP 同工酶的直接或基于机制的抑制剂,将 pradefovir (0.2, 2, 20 µM) 与人类肝微粒体和 CYP 特异性底物(CYP1A2 用非那西丁,CYP2C9 用双氯芬酸,CYP2C19 用 S-美芬妥英,CYP2D6 用丁呋洛尔,CYP2E1 用氯唑沙宗,CYP3A4 用睾酮)一起孵育。对于基于机制的抑制评估,pradefovir 在与底物加入前与微粒体和 NADPH 预孵育 15 分钟。通过 LC-MS/MS 测量代谢物形成。[1] |
| 动物实验 |
门静脉插管大鼠研究:大鼠禁食过夜后,经灌胃给予甲磺酸普拉德福韦(30 mg/kg)。分别于给药后2、5、10、20、40和60分钟,从门静脉和体循环静脉插管同时采集血样至肝素化试管中。离心分离血浆,并采用经验证的LC-MS/MS方法分析普拉德福韦和PMEA的浓度。[1]
大鼠酶诱导研究:大鼠每日口服普拉德福韦(300 mg/kg/天),连续8天。末次给药24小时后,处死大鼠并收集肝脏。测定了肝脏重量、体重、肝微粒体蛋白含量、总CYP含量以及特定酶活性(CYP1A、CYP2B、CYP3A)和载脂蛋白水平(CYP1A1、CYP2B1/2、CYP3A1/2、CYP4A1/3)。[1] |
| 药代性质 (ADME/PK) |
普拉德福韦主要通过肝脏CYP3A4代谢活化为活性形式PMEA。[1]
人肝微粒体中普拉德福韦转化为PMEA的固有清除率约为359 ml/min,低于肝血流量,表明并非所有普拉德福韦在人体内都能转化为PMEA。[1] 在大鼠中,口服给药后,普拉德福韦主要在肝脏转化为PMEA,根据门体浓度比较,肠道代谢的贡献极小。[1] 活性代谢物PMEA由于其在生理pH值下膦酸酯基团电离,口服吸收不良,导致多种动物的口服生物利用度较低。[1] 在服用放射性标记普拉德福韦的大鼠中,血浆PMEA的AUC约占总血浆放射性AUC的23%,尿液中PMEA的AUC也较低。 PMEA的排泄约占尿液放射性的66%,表明PMEA的形成是主要的代谢途径。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
普拉德福韦(浓度高达 20 µM)未显示对人肝微粒体中主要 CYP 酶(CYP1A2、2C9、2C19、2D6、2E1、3A4)的直接或机制性抑制作用,表明其通过 CYP 抑制发生代谢性药物相互作用的可能性较低。[1]
普拉德福韦(浓度高达 10 µg/ml)未诱导人肝细胞原代培养物中的 CYP1A2 或 CYP3A4/5。[1] 普拉德福韦(300 mg/kg/天,连续 8 天)未诱导大鼠体内的 CYP 酶,表现为肝脏重量、体重、微粒体蛋白、总 CYP 含量以及特定酶活性和载脂蛋白水平均未发生改变。[1] 前药设计普拉德福韦旨在增强肝脏靶向递送并降低PMEA的全身暴露,从而通过限制脱靶效应来提高安全性。[1] |
| 参考文献 | |
| 其他信息 |
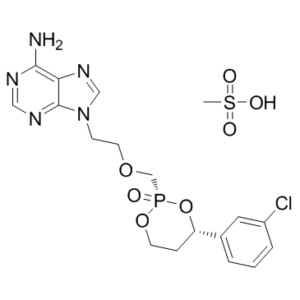
普拉地福韦甲磺酸盐(曾用名MB-06886、Hepavir B和雷莫福韦甲磺酸盐)是一种口服小分子化合物,属于阿德福韦的新型磷酸酯和膦酸酯前药系列。阿德福韦(Hepsera)是一种腺嘌呤的非环状膦酸酯类似物,用于治疗乙型肝炎病毒感染。由于阿德福韦吸收不良且肾毒性较高,普拉地福韦甲磺酸盐的设计旨在特异性靶向肝脏,降低对外部组织(尤其是肾脏)的风险,同时提高阿德福韦的疗效。普拉地福韦通过细胞色素P-450 (CYP) 3A4介导的氧化作用激活,CYP 3A4主要在肝脏中表达。这种新型前药在血浆和组织中均具有高度稳定性,并在临床前和临床研究中均显示出强大的抗乙肝病毒活性。普拉地福韦目前正处于治疗慢性乙型肝炎的II期临床试验阶段。
甲磺酸普拉地福韦是普拉地福韦的甲磺酸盐形式,普拉地福韦是一种环二酯类抗病毒前药,对乙型肝炎病毒(HBV)具有特异性活性。普拉地福韦主要通过肝酶(主要是CYP4503A4)在肝脏中代谢为阿德福韦。阿德福韦随后被细胞激酶磷酸化为活性形式阿德福韦二磷酸。阿德福韦二磷酸通过与天然底物dATP竞争,掺入病毒DNA中,抑制RNA依赖性DNA聚合酶。这会导致DNA链终止,最终抑制HBV复制。 另见:普拉地福韦(注释已移至)。 药物适应症 已研究用作Hepsera的前药,用于治疗乙型肝炎(病毒性肝炎)。 作用机制 普拉地福韦通过细胞色素P-450 (CYP) 3A4介导的氧化作用激活,CYP 3A4主要在肝脏中表达。这样,它就能选择性地提高Hepsera在肝脏中的浓度。 药效学 普拉地福韦通过细胞色素P-450 (CYP) 3A4介导的氧化作用激活,CYP 3A4主要在肝脏中表达。因此,普拉地福韦能使Hepsera在肝脏中浓缩,同时在其他组织中保持较低的浓度。这种新型前药是一种口服的小分子化合物,属于新型磷酸盐和膦酸盐药物系列。它在血浆和组织中均具有高度稳定性。 甲磺酸普拉地福韦(瑞莫福韦)是PMEA的环二酯前药,属于HepDirect类前药,这类前药旨在通过CYP3A4在肝脏中选择性激活。[1] 其激活机制涉及CYP3A4介导的氧化,生成带电中间体,该中间体被滞留在肝细胞内,并进一步转化为活性二磷酸代谢物PMEApp,后者可抑制HBV DNA聚合酶。[1] PMEA(活性形式)已在稳定转染的人肝细胞癌细胞系、感染鸭乙型肝炎病毒的原代鸭肝细胞以及鸭乙型肝炎模型中显示出抗HBV活性。[1] 与CYP3A4抑制剂(例如酮康唑)或诱导剂(例如,利福平)对普拉德福韦药代动力学的影响已被注意到,并且相关研究正在进行中。[1] 采用前药策略是为了克服母体药物PMEA口服生物利用度低的问题。[1] |
| 分子式 |
C13H23CLN5O7PS
|
|
|---|---|---|
| 分子量 |
519.90
|
|
| 精确质量 |
519.074
|
|
| CAS号 |
625095-61-6
|
|
| 相关CAS号 |
|
|
| PubChem CID |
9604653
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
4.573
|
|
| tPSA |
186.94
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
11
|
|
| 可旋转键数目(RBC) |
6
|
|
| 重原子数目 |
33
|
|
| 分子复杂度/Complexity |
668
|
|
| 定义原子立体中心数目 |
2
|
|
| SMILES |
CS(=O)(=O)O.C1CO[P@@](=O)(O[C@@H]1C2=CC(=CC=C2)Cl)COCCN3C=NC4=C(N=CN=C43)N
|
|
| InChi Key |
JXQUAHHUSMJUFV-HZPZRMRQSA-N
|
|
| InChi Code |
InChI=1S/C17H19ClN5O4P.CH4O3S/c18-13-3-1-2-12(8-13)14-4-6-26-28(24,27-14)11-25-7-5-23-10-22-15-16(19)20-9-21-17(15)23;1-5(2,3)4/h1-3,8-10,14H,4-7,11H2,(H2,19,20,21);1H3,(H,2,3,4)/t14-,28+;/m0./s1
|
|
| 化学名 |
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (192.34 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9234 mL | 9.6172 mL | 19.2345 mL | |
| 5 mM | 0.3847 mL | 1.9234 mL | 3.8469 mL | |
| 10 mM | 0.1923 mL | 0.9617 mL | 1.9234 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Ketoconazole inhibition of conversion of pradefovir to PMEA in human liver microsomes as a percentage of the control activity (mean;n= 2) versus the concentration of pradefovir.Antimicrob Agents Chemother.2006 Sep;50(9):2926-31. |
|---|
Determination ofKi(slope versus [I] plot) for ketoconazole on conversion of pradefovir to PMEA (mean;n= 2).Antimicrob Agents Chemother.2006 Sep;50(9):2926-31. |
MAb 3A4 inhibition of conversion of pradefovir to PMEA (mean;n= 2) in human liver microsomes.Antimicrob Agents Chemother.2006 Sep;50(9):2926-31. |