| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|

| 靶点 |
Human Endogenous Metabolite; The targets of Taurolithocholic acid sodium involve multiple cellular signaling pathways and receptors. It acts as a potent Ca²⁺ agonist, functioning through the regulation of intracellular calcium signaling. This compound selectively activates the epsilon isoform of protein kinase C (PKCε), inducing its translocation to hepatocellular membranes, which is a key mechanism underlying its cholestatic effects. Additionally, TLCA activates protein kinase B (PKB/Akt) via a PI3K-dependent pathway and participates in TGR5- and FXR-mediated signal transduction. In the nervous system, it inhibits radioligand binding to muscarinic M1 receptors but has no effect on M2 or M3 receptors.
|
|---|---|
| 体外研究 (In Vitro) |
在无细胞和细胞体系中,Taurolithocholic acid sodium显示出多种生物活性。在10 μM浓度下,TLCA选择性诱导PKCε亚型向肝细胞膜转位,转位率达47.9% ± 20.5%,而α、δ和ζ亚型不受影响。该化合物在5 μM浓度下可使PKCε的膜结合部分增加44.1% ± 40.2%,并刺激膜结合PKC活性增加60.5% ± 45.8%。在PI3K通路研究中,5 μM TLCA处理60分钟后使PKB/Akt磷酸化水平增加至对照组的194% ± 46%。此外,75 μM TLCA可显著增加表达NTCP的Hep3B细胞中caspase-3和caspase-7的活性,提示其具有促凋亡作用。
在低剂量 (5 µM) 下,Taurolithocholic acid /牛磺石胆酸 (TLCA) 往往会使 PKC e 亚型的膜相关部分提高 44.1% ± 40.2%[1]。移动 PKC 同工型的激活需要 PKC 的 epsilon 同工型选择性易位至肝细胞膜,这是由 TLCA (10 µM) 诱导的[1]。 蛋白激酶C(PKC)同工酶家族在肝细胞分泌的调节中起着关键作用。疏水性和胆汁淤积性胆汁酸,牛磺酸胆酸(TLCA),在分离的肝细胞中充当强效的钙离子激动剂。然而,其对PKC亚型的影响尚未阐明。在这里,我们研究了低微摩尔浓度的TLCA对PKC亚型分布和膜相关PKC活性的影响。使用蛋白质印迹和免疫荧光技术在短期培养的分离大鼠肝细胞中确定PKC亚型的分布。放射化学法测定PKC活性。Taurolithocholic acid /TLCA(10微摩尔/升)诱导εPKC选择性易位47.9%+/-20.5%(与对照组相比,P<.02;n=7),但α-、δ-和ζPKC未选择性易位至肝细胞膜,而佛波醇酯佛波醇12-肉豆蔻酸酯13-乙酸酯(PMA)(1微摩尔/L)导致所有可移动异构体α-、Δ-和εPKC易位,如免疫印迹所示。免疫荧光研究表明,TLCA(10微摩尔/升)选择性地将ε-PKC转运到分离的大鼠肝细胞联的小管膜,但PMA(1微摩尔/L)主要转运到细胞内和基底外侧膜。TLCA(10μmol/L)和PMA(1μmol/L)均能刺激膜结合PKC活性60.5%+/-45。分别为8%(与对照组相比P<0.05;n=5)和72.4%+/-37.2%(P<0.05;n=5)。较低浓度(5微摩尔/升)的TLCA效果较差。由于εPKC的激活与囊泡介导的分泌细胞膜蛋白靶向和插入的损伤有关,因此推测TLCA通过激活小管膜上的εPKC来降低肝细胞的胆汁分泌能力是有吸引力的。[1] 分离的大鼠肝细胞中PI3K依赖性PKB(PKB/Akt)活性[2] 磷酸化PKB(Ser-473)的量是PI3K通路激活的敏感读数(27,32),在短期培养中,肝细胞中的Taurolithocholic acid /牛磺酸/TLCA(5μmol/l)显著增强(图7),60分钟后达到对照组的194±46%(与对照组相比p<0.005;与TUDCA相比p<0.05;与TCA相比p<0.01)。相比之下,TUDCA(10μmol/升)仅短暂增加PKB活性,而TCA(10µmol/升,在所选实验条件下没有影响(图7)。因此,TLCA在体外显著影响了分离肝细胞中的PI3K活性,而TUDCA在低微摩尔浓度下给药时仅对PI3K通路产生轻微的短暂影响。 |
| 体内研究 (In Vivo) |
Taurolithocholic acid sodium在体内主要通过诱导胆汁淤积发挥作用。在离体灌注大鼠肝脏模型中,10 μM TLCA使胆汁流量减少51%,辣根过氧化物酶的胆汁分泌减少46%,Mrp2底物(2,4-二硝基苯基-S-谷胱甘肽)的分泌减少95%。在分离的大鼠肝细胞对中,2.5 μM TLCA使荧光胆汁酸的毛细胆管分泌减少50%。PI3K抑制剂wortmannin可显著逆转TLCA诱导的胆汁淤积效应。在神经炎症研究中,TLCA通过TGR5受体增强骨髓源性巨噬细胞的吞噬活性,促进髓鞘清除。人体研究表明,口服脂质耐受试验后2小时内,血清TLCA水平升高约5倍。
大鼠肝细胞对和灌注大鼠肝脏中的Taurolithocholic acid /牛磺石胆酸 (TLCA) 通过 PI3K 依赖性机制表现出胆汁淤积作用 [2]。 Taurolithocholic acid /牛磺酸胆酸(TLCA)是一种强效的胆汁淤积剂。我们最近的工作表明,TLCA通过蛋白激酶Cepsilon(PKCepsilon)依赖性机制损害肝胆分泌、运输蛋白插入肝细胞顶膜和胆汁流动。磷脂酰肌醇3-激酶(PI3K)的产物刺激PKCε。我们研究了PI3K在离体灌流大鼠肝脏(IPRL)和离体大鼠肝细胞偶联物(IRHC)中对TLCA诱导的胆汁淤积的作用。在IPRL中,TLCA(10微摩尔/升)使胆汁流量受损51%,使辣根过氧化物酶(囊泡分泌的标志物)的胆汁分泌受损46%,Mrp2底物2,4-二硝基苯基-S-谷胱甘肽受损95%,并刺激PI3K依赖性蛋白激酶B(PI3K活性的标志)受损154%,使PKEpsilon膜结合受损23%。在IRHC中,TLCA(2.5微摩尔/升)使荧光胆汁酸(胆酰甘氨酰荧光素)的小管分泌受损50%。选择性PI3K抑制剂渥曼青霉素(100 nmol/升)和抗胆固醇胆汁酸牛磺脱氧胆酸(TUDCA,25微摩尔/升)独立和相加地逆转了TLCA对IPRL中胆汁流量、胞吐、有机阴离子分泌、PI3K依赖性蛋白激酶B活性和PKCε膜结合的影响。渥曼青霉素还逆转了IRHC中受损的胆汁酸分泌。这些数据强烈表明,TLCA通过PI3K和PKCε依赖的机制发挥胆汁淤积作用,这些机制被牛磺脱氧胆酸以PI3K非依赖的方式逆转[2]。 |
| 酶活实验 |
Taurolithocholic acid sodium与受体的结合可通过多种体外方法进行评估。对于PKCε转位实验:分离大鼠肝细胞进行短期培养,加入10 μM TLCA处理,通过Western blotting检测各PKC亚型在膜组分和胞浆组分中的分布,并使用免疫荧光技术观察PKCε向毛细胆管膜的转位。对于PI3K/PKB活性测定:用5 μM TLCA处理肝细胞0-60分钟,收集细胞裂解液,使用磷酸化特异性抗体通过Western blotting检测PKB(Ser-473)的磷酸化水平。对于caspase活性测定:将表达NTCP的Hep3B细胞与75 μM TLCA共孵育,使用荧光底物法检测caspase-3和caspase-7的活性。
通过免疫印迹技术测定分离的大鼠肝细胞中PKB/Akt的活性。简而言之,在接种后4小时(见上文),细胞与Taurolithocholic acid /牛磺胆酸/TLCA(5μmol/l;浓度>5μmol/l时,TLCA在短期培养中对分离的肝细胞造成可见损伤)、TUDCA(10μmol/l)、TCA(10µmol/l)或仅使用载体Me2SO(对照,0.1%,v/v)孵育5、15、30和60分钟。然后将培养皿放在冰上,刮取细胞并立即冷冻(-80°C)。将休克冷冻细胞在冰冷的裂解缓冲液(1ml/100mg)中均质化,并如上所述进行处理[2]。 |
| 细胞实验 |
Taurolithocholic acid sodium在细胞实验中广泛用于研究胆汁淤积机制。典型流程(肝细胞对模型):分离大鼠肝细胞对,接种于培养板中,加入2.5 μM TLCA处理,使用荧光胆汁酸类似物(如胆酰甘氨酰氨基荧光素)评估毛细胆管分泌功能,通过荧光显微镜观察和定量分泌抑制率。对于巨噬细胞功能研究:分离骨髓源性巨噬细胞,在LPS诱导的炎症条件下与TLCA共孵育,通过流式细胞术检测吞噬活性,并通过qPCR检测CD36和TREM2等吞噬受体的表达变化。对于细胞活力检测,可使用MTT法评估TLCA的细胞毒性。
|
| 动物实验 |
通过测量肝细胞对浓度为 1 μmol/L 的胆酰甘氨酰胺荧光素 (CGamF) 的摄取和分泌到胆小管腔的情况来评估 IRHC 的胆汁酸分泌,方法如前所述。CGamF 的合成方法参照 Schteingart 等人的方法,由 Alan Hofmann 博士惠赠。分离 4 小时后,将肝细胞(置于盖玻片上)短暂转移至 HEPES 缓冲液中。然后,将细胞在 37 °C 下用以下溶液预处理 15 分钟:(i)0.1% (v/v) 的 Me2SO;(ii)100 nmol/L 沃特曼宁和 Me2SO;(iii)Me2SO 处理 5 分钟,然后用 2.5 μM 牛磺石胆酸/TLCA(溶于 0.1% (v/v) 的 Me2SO)处理 10 分钟;(iv)100 nmol/L 沃特曼宁和 Me2SO 处理 5 分钟,然后用 100 nmol/L 沃特曼宁和 2.5 μM 牛磺石胆酸/TLCA(溶于 0.1% (v/v) 的 Me2SO)处理 10 分钟;(v)Me2SO 处理 5 分钟,然后用 5 μmol/L 牛磺石胆酸/TLCA(溶于 0.1% (v/v) 的 Me2SO)处理 10 分钟。 (vi) 用 100 nmol/L 沃特曼宁和 Me2SO 处理 5 分钟,或用 100 nmol/L 沃特曼宁和 5 μmol/L 牛磺胆酸/TLCA 处理 10 分钟。然后将细胞转移至含有 1 μmol/L 荧光 CGamF 的 HEPES 缓冲液中,于 37 °C 孵育 5 分钟,以确保荧光胆汁酸充分加载,之后再转移回之前的培养皿中孵育 10 分钟(i-vi)。将盖玻片置于冰上的冰冷 HEPES 缓冲液中以终止肝细胞分泌,并立即使用蔡司 LSM 510 显微镜(纽约州索恩伍德)观察细胞。优化激光设置以获得合适的动态范围,避免荧光饱和。所有实验条件均使用相同的设置。由一位对实验条件不知情的实验人员(CJ Soroka)使用共聚焦激光扫描显微镜分析细胞。根据明场光学显微镜下清晰可见的管腔,选择成对细胞。然后快速扫描采集图像,以避免荧光猝灭。CGamF 的摄取(摄取量 = (F° 细胞 + F° 管腔)/μm2) 和分泌(分泌百分比 = [F° 管腔/(F° 细胞 + F° 管腔)] × 100)的定量分析方法与之前发表的方法相同,只是使用了 NIH Image 软件。[2]
Taurolithocholic acid sodium的体内研究主要采用大鼠胆汁淤积模型。典型流程:雄性Charles River大鼠(300-350 g)麻醉后行气管切开、颈静脉和颈动脉插管及胆总管插管。收集术后10分钟的胆汁作为基线,然后经颈静脉给予TLCA(剂量为2.75-5.0 μmol/100 g大鼠体重),持续60分钟每5分钟收集一次胆汁,同时采集血样9次。研究显示,TLCA剂量为5.0、3.75和2.75 μmol/100 g体重时,分别产生85%、68%和45%的胆汁淤积效应。在离体灌注大鼠肝脏模型中,使用10 μM TLCA灌流,通过测定胆汁流量、辣根过氧化物酶和谷胱甘肽-S-二硝基苯的分泌来评估胆汁淤积程度。 |
| 药代性质 (ADME/PK) |
Taurolithocholic acid sodium作为牛磺酸结合型胆汁酸,其药代动力学行为遵循胆汁酸的肠肝循环规律。计算预测的理化性质:LogP约为5.555,氢键供体数为2,氢键受体数为5,可旋转键数为7。该化合物在DMSO中的溶解度为100 mg/mL(约197.75 mM),在DMF中为25 mg/mL,在乙醇和PBS(pH 7.2)中溶解度较低(约1 mg/mL)。人体研究表明,口服脂质负荷后2小时内血清TLCA水平升高约5倍。储存条件:粉末在-20°C可稳定保存3年,4°C可保存2年;溶解后在-80°C可保存6个月,-20°C可保存1个月。该化合物仅供科研使用,不可用于人体。
|
| 毒性/毒理 (Toxicokinetics/TK) |
Taurolithocholic acid sodium被广泛用作诱导实验性肝内胆汁淤积的工具化合物,其毒性作用主要表现为胆汁淤积性肝损伤。在大鼠模型中,静脉注射TLCA(2.75-5.0 μmol/100 g体重)可剂量依赖性地诱导胆汁淤积,胆汁流量减少45%-85%。该化合物的毒性机制涉及PKCε依赖性和PI3K依赖性的毛细胆管分泌功能抑制。在细胞水平,75 μM TLCA可诱导表达NTCP的Hep3B细胞凋亡,表现为caspase-3和caspase-7活性升高。根据材料安全数据表,该化合物未被归类为危险物质,IARC、NTP和OSHA均未将其列为致癌物。该产品仅限科研使用,不可用于人体或兽医。
|
| 参考文献 |
|
| 其他信息 |
牛磺胆酸钠是一种胆汁酸,其功能与牛磺胆酸相关。
另见:牛磺胆酸钠(注释已移至)。 在本研究中,联合使用PI3K抑制剂不仅逆转了TLCA诱导的胆汁分泌障碍,而且逆转了乳酸脱氢酶释放所确定的细胞损伤(表I)。胆汁流量的改善本身不足以解释这一效应,因为TUDCA也改善了TLCA处理肝脏的胆汁分泌,但未能消除TLCA在IPRL中诱导的细胞损伤。未来需要开展更多研究来阐明PI3K在TLCA诱导的急性肝细胞损伤中的作用。 目前的数据表明,PI3K可能是未来抗胆汁淤积治疗策略的潜在靶点。然而,值得一提的是,PI3K 可能激活大鼠肝细胞中由疏水性胆汁酸牛磺鹅脱氧胆酸 (TCDCA) 处理的存活通路,从而在体外和体内保护肝细胞免受 TCDCA 诱导的损伤(Rust C,未发表的观察结果)。有趣的是,牛磺鹅脱氧胆酸诱导的存活通路在体外并不涉及 PKB 的激活。因此,不同的胆汁酸可能对肝细胞中 PI3K 和 PKB 介导的过程产生不同的影响。不同PI3K亚型的参与或在不同亚细胞区室的作用是否会导致胆汁酸对PI3K和PKB产生如此多样的影响,仍有待阐明。 总之,本研究表明,TLCA诱导的胆汁流动、肝胆胞吐、胆汁酸和其他有机阴离子分泌以及肝细胞损伤的损害是由PI3K依赖性机制和推测的PKCε依赖性机制介导的。TUDCA通过一种不依赖于PI3K的机制逆转了TLCA对胆汁分泌的抑制作用。[2] |
| 分子式 |
C26H44NNAO5S
|
|---|---|
| 分子量 |
505.69
|
| 精确质量 |
505.284
|
| CAS号 |
6042-32-6
|
| 相关CAS号 |
Taurolithocholic Acid-d5 sodium;1265476-97-8;Taurolithocholic acid-d4 sodium;2410279-97-7;Taurolithocholic acid-d4-1 sodium; 6042-32-6; 516-90-5
|
| PubChem CID |
23662757
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
5.555
|
| tPSA |
114.91
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
34
|
| 分子复杂度/Complexity |
832
|
| 定义原子立体中心数目 |
9
|
| SMILES |
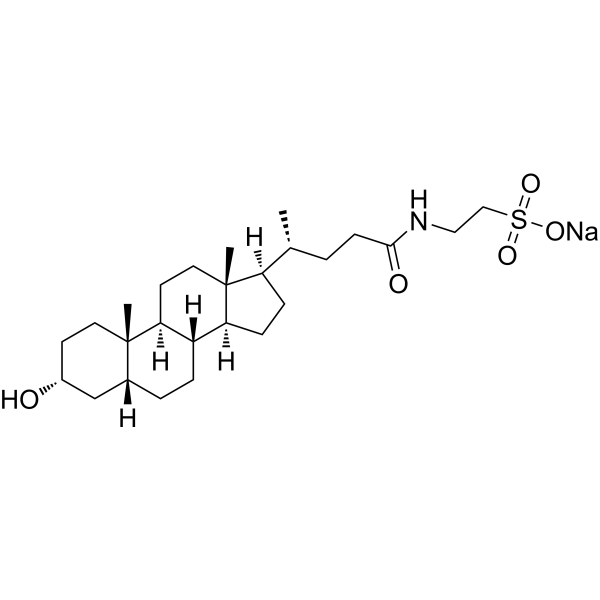
C[C@H](CCC(=O)NCCS(=O)(=O)[O-])[C@H]1CC[C@@H]2[C@@]1(CC[C@H]3[C@H]2CC[C@H]4[C@@]3(CC[C@H](C4)O)C)C.[Na+]
|
| InChi Key |
YAERYJYXPRIDTO-HRHHVWJRSA-M
|
| InChi Code |
InChI=1S/C26H45NO5S.Na/c1-17(4-9-24(29)27-14-15-33(30,31)32)21-7-8-22-20-6-5-18-16-19(28)10-12-25(18,2)23(20)11-13-26(21,22)3;/h17-23,28H,4-16H2,1-3H3,(H,27,29)(H,30,31,32);/q;+1/p-1/t17-,18-,19-,20+,21-,22+,23+,25+,26-;/m1./s1
|
| 化学名 |
sodium;2-[[(4R)-4-[(3R,5R,8R,9S,10S,13R,14S,17R)-3-hydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1H-cyclopenta[a]phenanthren-17-yl]pentanoyl]amino]ethanesulfonate
|
| 别名 |
Taurolithocholic acid sodium salt; 6042-32-6; Sodium taurolithocholate; Taurolithocholic Acid (Sodium Salt); 2-((R)-4-((3R,5R,8R,9S,10S,13R,14S,17R)-3-Hydroxy-10,13-dimethylhexadecahydro-1H-cyclopenta[a]phenanthren-17-yl)pentanamido)ethanesulfonic acid, sodium salt; MFCD00036746; CHEMBL2028239; CHEBI:229584;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮和光照。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 100 mg/mL (197.75 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.11 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (4.11 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (4.11 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9775 mL | 9.8875 mL | 19.7750 mL | |
| 5 mM | 0.3955 mL | 1.9775 mL | 3.9550 mL | |
| 10 mM | 0.1977 mL | 0.9887 mL | 1.9775 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。