| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
5-HT2A ( Ki = 0.17 nM ); α2c-adrenergic receptor ( Ki = 1.3 nM ); α2c-adrenergic receptor ( Ki = 1.3 nM ); D2 receptor ( Ki = 3.57 nM ); D3 receptor ( Ki = 3.6 nM ); D2L Receptor ( Ki = 4.16 nM )
|
|---|---|
| 体外研究 (In Vitro) |
体外活性:利培酮/Risperidone与 DA 和血清素 (5HT) 受体结合,特别是在纹状体和边缘结构的神经元中。利培酮显着影响脑神经生长因子 (NGF) 水平,表明它影响内源性生长因子的周转。利培酮显着降低额叶皮层、枕叶皮层和海马体中的 BDNF 浓度,并减少或增加特定大脑结构中的 TrkB 受体。利培酮显着增加大鼠前脑区域内侧前额皮质中 D(2) 的结合达 34%。 Risperidone 对大鼠前脑区域的 CPU (37%)、NAc (32%) 和 HIP (37%) 中的 D(4) 受体产生更大的上调。 Risperidone 显着抑制激活的小胶质细胞产生 NO 和促炎细胞因子。 Risperidone (1-50 mM) 通过抑制 P-gp 活性,显着增强 Caco-2 细胞中 Rh123 的细胞内积累,IC(50) 值为 5.87 mM。
小胶质细胞最近被认为是通过在中枢神经系统(CNS)中释放促炎细胞因子、一氧化氮(NO)和活性氧(ROS)来介导神经炎症的介质。因此,据报道,小胶质细胞在阿尔茨海默病(AD)和帕金森病(PD)等神经退行性疾病的病理学中起着重要作用。精神分裂症的病理机制尚不清楚,而最近的一些神经影像学研究表明,即使是精神分裂症也可能是一种神经退行性疾病。据报道,Risperidone/利培酮可以减少精神分裂症临床过程中MRI体积的减少。最近的许多研究表明,干扰素(IFN)-γ和细胞因子等免疫机制可能与精神分裂症的病理生理学有关。在本研究中,我们分别使用Griess试验、Western印迹和ELISA研究了利培酮对IFN-γ激活的小胶质细胞产生一氧化氮、诱导型一氧化氮合酶(iNOS)表达和炎性细胞因子白细胞介素(IL)-1β、IL-6和肿瘤坏死因子(TNF)-α的影响。与氟哌啶醇相比,利培酮显著抑制了活化小胶质细胞产生NO和促炎细胞因子。利培酮处理的细胞的iNOS水平远低于氟哌啶醇处理的细胞。抗精神病药物,尤其是利培酮,可能通过抑制小胶质细胞活化而具有抗炎作用,小胶质细胞不仅对神经元有直接毒性,而且对神经发生和少突胶质细胞发生也有抑制作用,据报道,这两者在精神分裂症的病理学中都起着至关重要的作用。[3] 利培酮/Risperidone(RSP)及其主要活性代谢产物9-羟基利培酮(帕利哌酮,PALI)是药物转运蛋白P-糖蛋白(P-gp)的底物。本研究的目的是研究RSP和PALI对P-糖蛋白介导的转运的体外影响。在LLC-PK1/MDR1细胞中检测罗丹明123(Rh123)和阿霉素(DOX)的细胞内积累,以评估RSP和PALI对P-gp的抑制作用。这两种化合物都以浓度依赖的方式显著增加了Rh123和DOX的细胞内积累。RSP抑制P-gp介导的Rh123和DOX转运的IC50值分别为63.26和15.78 μM,而PALI的IC50值>100 μM,表明PALI是一种效力较低的P-gp抑制剂。利用Caco-2和原代培养的大鼠脑微血管内皮细胞(RBMECs)研究RSP对作为P-gp底物的联合用药的肠道吸收和血脑屏障(BBB)转运的可能影响。RSP,1–50 μM,通过抑制P-gp活性显著增强Caco-2细胞中Rh123的细胞内积累,IC50值为5.87 μM.暴露于10 μM RSP,Rh123在Caco-2和RBMECs单层上的表观渗透系数在顶端到基底外侧方向上分别增加到2.02和2.63倍,但在基底外侧到顶端方向上分别降低到0.37和0.21倍。这些数据表明,RSP和PALI在较小程度上有可能通过抑制P-gp介导的转运来影响药物动力学,从而影响联合用药的药效学。然而,目前还没有解决这个问题的人类数据。特别是,RSP可能通过抑制P-gp介导的PALI穿过BBB内皮细胞的流出来促进其脑浓度,从而与其自身的活性代谢产物PALI相互作用[4]。 |
| 体内研究 (In Vivo) |
尽管雄性大鼠的催乳素和皮质酮显着升高,但利培酮不会显着影响体重增加(BWG)、食物摄入量(FI)、葡萄糖耐量或瘦素水平。利培酮显着增加雌性大鼠的 BWG 和 FI。利培酮 (0.05 mg/kg) 会增加白色脂肪组织 (WAT) 中的食物摄入量和瘦素基因表达,但大鼠体重增加率不受影响。利培酮 (0.5 mg/kg) 会导致大鼠体重增加减少,并增强 BAT 中的 Ucp1 基因表达和血清催乳素浓度。
抗精神病药物氟哌啶醇和利培酮/Risperidone广泛用于治疗精神分裂症。前一种药物主要作用于多巴胺(DA)D(2)受体,而利培酮结合DA和血清素(5HT)受体,特别是在纹状体和边缘结构的神经元中。最近的证据表明,神经营养因子也可能参与中枢神经系统(CNS)的抗精神病作用。我们之前报道过氟哌啶醇和利培酮显著影响脑神经生长因子(NGF)水平,表明这些药物会影响内源性生长因子的周转。脑源性神经营养因子(BDNF)支持发育和成熟脑DA神经元的存活和分化。我们假设氟哌啶醇或利培酮治疗会影响脑BDNF的合成/释放,并通过在食物中添加氟哌啶醇和利培酮治疗29天后测量大鼠脑区的BDNF和TrkB来验证这一假设。药物治疗对大脑区域的重量没有影响。然而,长期服用这些药物会改变脑内BDNF的合成或释放以及TrkB免疫反应性的表达。氟哌啶醇和利培酮均显著降低了额叶皮层、枕叶皮层和海马中的BDNF浓度,并降低或增加了选定脑结构中的TrkB受体。由于BDNF可以作用于多种中枢神经系统神经元,因此有理由假设这种神经营养因子脑水平的改变可能构成抗精神病药物的作用机制之一。这些观察结果也支持了神经营养因子在精神分裂症患者脑功能改变中发挥作用的可能性。[1] 通过定量体外受体放射自显影比较了非典型抗精神病药物奥氮平、利培酮Risperidone/和喹硫平长期治疗(28天)后大鼠前脑区域多巴胺(DA)D(1)样(D(1,D(5))和D(2)样(D2,D(3),D(4))受体家族成员的变化。奥氮平和利培酮显著增加了内侧前额叶皮层(MPC;67%和34%)、尾壳核(CPu;平均42%,25%)、伏隔核(NAc;37%,28%)和海马(HIP;53%,30%)中的D(2)结合,但喹硫平没有。奥氮平和利培酮,而不是喹硫平,在CPu(61%,37%)、NAc(65%,32%)和HIP(61%,37%)中产生了更大的D(4)受体上调。所有区域的D(1)样和D(3)受体均未因任何治疗而改变,表明它们在介导这些抗精神病药物作用中的作用很小。这些发现支持这样一种假设,即奥氮平和利培酮的抗精神病作用部分由MPC、NAc或HIP中的D(2)受体介导,也可能由CPu、NAc和HIP的D(4)受体介介导,但不在大脑皮层。奥氮平和利培酮在CPu中选择性上调D(2)受体可能反映了它们诱导一些锥体外系效应的能力。喹硫平不能改变DA受体,这表明非多巴胺能机制有助于其抗精神病作用。[2] 肥胖和相关代谢紊乱是一些抗精神病药物(AP)的重要副作用。目前可用的AP诱导大鼠体重增加(BWG)的动物模型是基于舒必利(SUL)的给药。然而,这种模式有重要的局限性。例如,SUL是一种纯多巴胺拮抗剂,而目前临床使用的大多数AP与参与食物摄入(FI)和代谢调节的多种神经递质受体相互作用。因此,我们评估了利培酮/Risperidone(RIS,0.125、0.25或0.5mg/kg,持续16天)对雄性和雌性大鼠BWG和FI的影响。还对雌性大鼠进行了12天内RIS(0.5 mg/kg)、SUL(20 mg/kg)和赋形剂(VEH)的比较。在雄性大鼠中,RIS对BWG、FI、葡萄糖耐量或瘦素水平没有显著影响,尽管催乳素和皮质酮显著升高。在女性中,两种AP都显著增加了BWG和FI,但SUL的效果更强。BWG与体脂增加显著相关。血清瘦素水平仅在SUL治疗的大鼠中升高。SUL组的葡萄糖曲线下面积(AUGC)明显较低,但所有治疗组的胰岛素曲线下面积相似。胰岛素曲线下面积(AUIC)和BWG仅在RIS组呈正相关。两种AP均显著增加催乳素和皮质酮。RIS显著提高了血清雌二醇水平,但SUL没有,但两组的孕酮水平相似。在RIS给药期间观察到的BWG和AUIC之间的正相关表明,该药物可能代表了人类AP给药的更好模型。通过测试其他剂量、给药途径和饮食类型,可以改善RIS诱导的大鼠肥胖动物模型。[5] 1.利培酮/Risperidone是一种非典型抗精神病药物,具有5-羟色胺5-HT2受体拮抗作用和较轻的多巴胺D2受体拮抗作用。2.体重过度增加是抗精神病药物的副作用之一。利培酮治疗比氟哌啶醇等传统抗精神病药物治疗导致患者体重增加更多。因此,本研究旨在通过检测瘦素(一种在白色脂肪组织(WAT)中产生的食欲调节激素)和解偶联蛋白(UCP)-1(一种促进棕色脂肪组织(BAT)能量消耗的物质)的表达,来解决利培酮诱导的大鼠体重变化的病因。3.8周龄雄性大鼠皮下注射利培酮(0.005、0.05或0.5mg/kg),每天两次,持续21天。每天监测体重和食物摄入量。在第21天,将大鼠斩首,并测量其血清瘦素和催乳素浓度。使用实时聚合酶链式反应扩增定量WAT和BAT中瘦素、Ucp1和β3肾上腺素受体(β3-AR)基因的表达水平。4.大鼠注射0.005 mg/kg利培酮可增加食物摄入量和体重增加率,并增加WAT中瘦素基因的表达。注射0.05mg/kg利培酮可增加WAT的食物摄入量和瘦素基因表达,但体重增加率不受影响。注射0.5mg/kg利培酮可减少体重增加,并增强BAT和血清催乳素浓度中的Ucp1基因表达。注射0.5mg/kg利培酮对WAT和BAT的血清瘦素浓度和β3-AR基因表达没有影响。5.尽管在注射利培酮的大鼠中观察到的食物摄入量的变化既不是由血清瘦素也不是催乳素浓度合理化的,但注射0.5mg/kg后体重增加率的降低在一定程度上可以解释为能量消耗的增加,正如BAT中UCP-1 mRNA表达水平的显著增加所揭示的那样。瘦素在利培酮诱导的体重增加变化中的作用仍有待澄清[6]。 |
| 细胞实验 |
细胞活力[3]
通过3-[4,5-二甲基噻唑-2-基]-2,5-二苯基溴化四唑(MTT)还原产物的比色测量来确定细胞存活率。在用或不用氟哌啶醇和利培酮/Risperidone处理后,从96孔板中取出原始培养基,在含有0.5mg/mL MTT的无酚红最低必需培养基的存在下,在37°C下孵育细胞2小时。然后向每个孔中加入100 mL的酸-异丙醇(0.04 mol/L盐酸),并将平板在37°C下孵育过夜,以溶解孔中形成的甲氮。MTT在活细胞的线粒体中被还原为甲氮。通过平板读数器在570nm波长下测量MTT减少。 亚硝酸盐产量评估[3] NO2-是一种稳定的最终产物,广泛用作培养细胞产生NO的指标,其积累是通过格里斯反应进行测定的。将6-3个细胞以每200μl/孔1×105/孔的比例铺在96孔组织培养板上,然后在有或没有氟哌啶醇或Risperidone/利培酮的情况下预孵育12小时,然后在37°C下有或没有50 U/ml IFN-γ的情况下孵育。48小时后,将无细胞上清液与等量的Griess试剂混合。样品在室温下孵育15分钟,随后使用平板读数器在540nm处读取吸光度。 Western印迹法检测诱导型一氧化氮合酶(iNOS)[3] 将6-3个小胶质细胞以每孔1.8×106个细胞的密度铺在35 mm的组织培养皿上,然后在有或没有氟哌啶醇或Risperidone/利培酮的情况下预孵育12小时,然后在37°C下在有或无50 U/ml IFN-γ的情况下孵育12 h。之后,用PBS(pH 7.4)洗涤细胞,并用含十二烷基硫酸钠(SDS)的样品缓冲液裂解。蛋白质在7.5%的SDS-聚丙烯酰胺凝胶中分离,并转移到硝化纤维膜上。将膜与5%脱脂奶粉一起孵育,以阻断非特异性结合。随后,将膜与iNOS抗体和β-actin抗体一起孵育。采用增强化学发光系统检测iNOS和β-actin的表达。用光密度扫描仪对条带强度进行定量。实验分别进行了三次。 细胞因子释放评估[3] 将6-3个细胞以每200μl/孔1×105/孔的比例铺在96孔组织培养板上,然后在有或没有氟哌啶醇或Risperidone/利培酮的情况下预孵育12小时,然后在37°C下有或没有50 U/ml IFN-γ的情况下孵育。48小时后,检测收集的培养基中细胞因子(IL-1β、IL-6和TNF-α)的积累。基于定量“夹心”酶免疫吸附技术,使用小鼠IL-1β、IL-6和TNF-α酶联免疫吸附试验(ELISA)试剂盒测量释放到培养基中的细胞因子。根据制造商的方案进行了分析。该测定的灵敏度为4pg/ml。 细胞内Rh123和DOX积累研究[4] 测量P-gp底物Rh123和DOX的细胞内积累,以评估LLC-PK1/MDR1和Caco-2细胞中的P-gp活性,而LLC-PK1被列为阴性对照(van der Sandt等人,2000)。达到融合后,细胞在37°C下预孵育30 用运输缓冲液(无血清DMEM,含25 mM N-2-羟基哌嗪-N′-2-乙磺酸,pH 7.4)。加入载体对照(0.5%二甲亚砜(DMSO))、特定浓度的RSP/Risperidone/利培酮、PALI或PSC833,然后加入5 μM的Rh123或10 添加μM的DOX,再添加60 最小孵化时间。孵育后,丢弃溶液,用冰冷的DPBS洗涤细胞三次,并用1%Triton X-100溶解。通过高效液相色谱法(HPLC)测定Rh123和DOX的荧光。通过构建Rh123和DOX标准曲线,根据荧光值确定浓度。每个样品中Rh123或DOX的量用Lowry测定法测定的蛋白质含量进行标准化。 Rh123运输研究[4] 当RBMEC或Caco-2细胞达到融合时,通过TEER值和荧光素(一种公认的细胞旁转运标志物)的转运速率来检查单层的完整性(van Bree等人,1988)。用DPBS冲洗合格的单层两次,并在37°C下用运输缓冲液预孵育30 min.总之,在单层的两侧分别加载0.5%DMSO、RSP/利培酮或PSC833,然后在基底外侧加入Rh123(5μM)进行基底外侧到顶端(B-A)转运研究,或在顶端侧加入Rh123进行顶端到基底外侧(A-B)转运研究。在指定时间,150 从接收器室中取出μl样品,每次取样后立即更换相同体积的接收器室溶液。通过HPLC测定Rh123的浓度。表观渗透系数Papp(cm/s)根据以下方程式计算. |
| 动物实验 |
本研究共使用了211只Long-Evans大鼠,其中雌性56只,雄性155只。将大鼠分为三组,每组数量大致相等,分别注射1.0 mg/kg利培酮、3.0 mg/kg利培酮或作为对照的利培酮溶液(溶剂)。在第一项实验中,使用了26只雄性大鼠(溶剂组和3.0 mg/kg利培酮组各9只,1.0 mg/kg利培酮组8只)。从出生后第49天开始,每天对这些大鼠进行20分钟的运动活性测试,直至出生后第53天。后续研究考察了早期利培酮治疗对大鼠运动活性的长期影响。在第三项实验中,研究了性别对早期服用利培酮对幼年成年大鼠运动能力的影响。该实验共纳入60只雄性大鼠(每组20只)和56只雌性大鼠(溶剂对照组和3.0 mg/kg剂量组各19只,1.0 mg/kg剂量组18只)。在第四项实验中,评估了早期服用利培酮的大鼠在成年期的逆转学习能力。该实验共纳入42只雄性大鼠(每组14只)。
药物处理[5] 将消旋的SUL和利培酮RIS分别溶于0.1 N HCl和酒石酸中,并将pH值调节至7.0。药物以0.1 cc/100 g的剂量皮下注射。 血液采样和口服葡萄糖耐量试验[5] 采用肌内注射由盐酸氯胺酮(50 mg/ml)、盐酸赛拉嗪(5 mg/kg)和醋丙嗪(1 mg/kg)配制的溶液进行全身麻醉。总注射量为1 ml/kg体重。于中午12:00在尾背动脉置入导管,并用肝素化(2 U/ml)生理盐水灌注。术后36小时进行口服葡萄糖耐量试验(葡萄糖,1 g/kg,灌胃),试验顺序采用平衡设计。在给予葡萄糖前后(0、30、60、90 和 120 分钟;共采集 0.6 毫升血液),将动物轻轻固定于塑料啮齿动物约束器中。葡萄糖耐量试验结束后立即拔出导管,两天后,大鼠禁食 6 小时后断头处死。采集躯干血用于激素测定。所有动物均在 17:00 至 19:00 之间按平衡顺序断头处死。为尽量减少应激对激素水平的影响,从处理动物到断头处死的时间间隔不超过 1 分钟。对尸体进行处理以进行体成分分析(见下文)。 实验 1:利培酮对雌性或雄性大鼠体重和食物摄入量的影响[5] 每种性别各 32 只动物随机分为 4 组,每组 8 只,分别接受以下处理之一:赋形剂(0.1 cc/kg)、利培酮/RIS 0.125、0.25 或 0.5 mg/kg,持续 16 天。已知这些剂量的利培酮对大鼠的运动行为影响甚微。体重增长和食物摄入量的测量方法如上所述。由于未对雄性大鼠进行其他研究,因此在第 14 天对接受赋形剂和 RIS 0.5 mg/kg 处理的大鼠进行口服葡萄糖耐量试验。检测所有血液样本的血清葡萄糖和胰岛素水平。实验结束时,立即对动物进行断头处死,并采集血样,检测瘦素、皮质酮和催乳素水平。 实验2:利培酮和舒必利对雌性大鼠体重、食物摄入量、葡萄糖耐量、阴道周期、激素水平和葡萄糖耐量的影响比较[5] 29只雌性大鼠被分为3组,分别接受以下三种治疗,持续12天:0.9%氯化钠溶液,0.1毫升/公斤(n=9);利培酮,0.5毫克/公斤(n=11);舒必利,20毫克/公斤(n=9)。该舒必利剂量已被证明在长期治疗后可诱导最大体重增加。在开始给药后第9天放置动脉导管,并在葡萄糖耐量试验完成后拔出。在第10天,动物禁食6小时,然后按照血液采样部分所述进行口服葡萄糖耐量试验。所有血液样本均检测了胰岛素和葡萄糖水平。在第12天断头取样,检测了基础血液样本中的瘦素、皮质酮、催乳素、孕酮和雌二醇浓度。 使用利培酮。8周龄雄性Sprague-Dawley大鼠,体重285-305克,单独饲养,保持12小时光照/12小时黑暗循环(早上6:00开灯),并可自由摄取标准啮齿动物饲料(CE-2;14.4 kJ/g,含12%脂肪、29%蛋白质和59%碳水化合物)和水。室温保持在23 ± 1°C。大鼠适应环境3天后,被分为四组实验组。其中三组大鼠在各自的饲养箱内,每天两次(上午9:00和下午18:00)在颈部皮下注射利培酮,浓度分别为0.005、0.05和0.5 mg/kg(n分别为5、6和5),持续21天。另10只大鼠在颈部皮下注射赋形剂(0.3%酒石酸溶液),同样每天两次(上午9:00和下午18:00),持续21天。每天上午9:00注射前,记录大鼠的体重和食物摄入量,精确到1.0 g。第21天,在下午18:00注射利培酮1小时后,将大鼠断头处死。从躯干血管采集血样,并将血清保存在−80°C直至进行激素测定。附睾白色脂肪组织和肩胛间棕色脂肪组织被迅速取出,并在RNA提取前保存在−80°C[6]。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
利培酮吸收良好。其绝对口服生物利用度为70%(CV=25%)。与溶液相比,片剂的相对口服生物利用度为94%(CV=10%)。 利培酮在肝脏中广泛代谢。与年轻健康受试者相比,健康老年人利培酮及其代谢产物9-羟基利培酮的肾清除率降低,消除半衰期延长。 利培酮的分布容积约为1~2 L/kg。 利培酮经肾脏清除。老年人和肌酐清除率(ClCr)在15~59 mL/min之间的患者的清除率降低,后者的清除率降低约60%。 利培酮吸收良好。利培酮的绝对口服生物利用度为70%(变异系数CV=25%)。与溶液相比,片剂的相对口服生物利用度为94%(变异系数CV=10%)。利培酮分布迅速,分布容积为1-2 L/kg。在血浆中,利培酮与白蛋白和α1-酸性糖蛋白结合。利培酮的血浆蛋白结合率为90%,其主要代谢物9-羟基利培酮的血浆蛋白结合率为77%。利培酮和9-羟基利培酮不会相互置换血浆蛋白结合位点。高浓度的磺胺二甲嘧啶(100 μg/mL)、华法林(10 μg/mL)和卡马西平(10 μg/mL)仅导致利培酮(10 ng/mL)和9-羟基利培酮(50 ng/mL)的游离分数略有增加,其临床意义尚不明确。 在每日1至16 mg(每日两次,每次0.5至8 mg)的剂量范围内,利培酮、其主要代谢物9-羟基利培酮以及利培酮加9-羟基利培酮的血浆浓度与剂量成正比。口服溶液或片剂后,利培酮的平均血浆峰浓度出现在约1小时。在快速代谢者中,9-羟基利培酮的峰浓度出现在约3小时,而在慢速代谢者中,则出现在约17小时。在快速代谢者中,利培酮的稳态浓度可在 1 天内达到;在慢速代谢者中,预计约需 5 天才能达到稳态。9-羟基利培酮的稳态浓度在 5-6 天内达到(在快速代谢者中测得)。 利培酮和 9-羟基利培酮存在于人乳中。 有关利培酮(共 6 种代谢物)的更多吸收、分布和排泄(完整)数据,请访问 HSDB 记录页面。 代谢/代谢物 利培酮主要经肝细胞色素 P450 2D6 同工酶代谢为 9-羟基利培酮(即帕利哌酮),其与利培酮的受体结合亲和力大致相同。羟基化作用依赖于去溴喹4-羟化酶,且利培酮的代谢受去溴喹4-羟化酶基因多态性的影响。利培酮还会发生少量N-去烷基化。 利培酮主要在肝脏代谢。其主要代谢途径是通过CYP2D6酶将利培酮羟基化为9-羟基利培酮。次要代谢途径是通过N-去烷基化。主要代谢产物9-羟基利培酮与利培酮具有相似的药理活性。因此,该药物的临床疗效取决于利培酮和9-羟基利培酮的联合浓度。CYP2D6,也称为去溴喹羟化酶,是许多抗精神病药、抗抑郁药、抗心律失常药和其他药物代谢的酶。 CYP 2D6 受遗传多态性影响(约 6%-8% 的白种人和极少数亚洲人 CYP 2D6 活性很低或没有活性,属于“弱代谢者”),并易受多种底物和一些非底物(尤其是奎尼丁)的抑制。CYP 2D6 强代谢者能迅速将利培酮转化为 9-羟基利培酮,而 CYP 2D6 弱代谢者转化速度则慢得多。尽管快代谢者体内利培酮浓度低于慢代谢者,而9-羟基利培酮浓度高于慢代谢者,但单次和多次给药后,快代谢者和慢代谢者体内利培酮和9-羟基利培酮的药代动力学特征相似。利培酮已知的代谢产物包括9-羟基利培酮、帕利哌酮、3-[2-[4-(6-氟-2-羟基-1,2-苯并恶唑-2-鎓-3-基)哌啶-1-基]乙基]-2,9-二甲基-6,7,8,9-四氢吡啶并[1,2-a]嘧啶-4-酮、3-乙基-2,9-二甲基-6,7,8,9-四氢吡啶并[1,2-a]嘧啶-4-酮等。 6-氟-3-(4-哌啶基)-1,2-苯并异噁唑。 主要经肝细胞色素P450 2D6同工酶代谢为9-羟基利培酮,后者与利培酮具有大致相同的受体结合亲和力。羟基化作用依赖于去溴喹4-羟化酶,且代谢受去溴喹4-羟化酶基因多态性的影响。利培酮也发生少量N-去烷基化反应。 消除途径:利培酮主要在肝脏代谢。在健康老年人中,利培酮及其代谢产物9-羟基利培酮的肾清除率均降低,消除半衰期较年轻健康受试者延长。 半衰期:20-24小时 生物半衰期 强代谢者为3小时,弱代谢者可达20小时 服用利培酮缓释片(Risperdal Consta)后,利培酮及其代谢产物9-羟基利培酮的表观半衰期为3至6天,血浆浓度呈单指数下降。利培酮的半衰期为3-6天,这与微球的侵蚀以及随后利培酮的吸收有关。 在快代谢者中,利培酮的表观半衰期为3小时(CV=30%),在慢代谢者中为20小时(CV=40%)。在快代谢者中,9-羟基利培酮的表观半衰期约为21小时(CV=20%),在慢代谢者中约为30小时(CV=25%)。单次和多次给药后,利培酮和9-羟基利培酮联合用药在快代谢者和慢代谢者中的药代动力学相似,总体平均消除半衰期约为20小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概述
阻断边缘系统中的多巴胺D2受体可缓解精神分裂症的阳性症状,例如幻觉、妄想以及行为和言语异常。阻断中脑皮质通路中的5-羟色胺2(5-HT2)受体可导致多巴胺过量和多巴胺传递增强,从而增强多巴胺传递并消除核心阴性症状。利培酮不影响黑质纹状体通路中的多巴胺受体,因此避免了锥体外系副作用。与其他 5-HT2 受体拮抗剂一样,利培酮也能与 α1-肾上腺素能受体结合,并较弱地与组胺 H1 和 α2-肾上腺素能受体结合。 毒性数据 LD50=82.1mg/kg(小鼠口服)。 药物相互作用 鉴于利培酮主要作用于中枢神经系统,当利培酮与其他中枢作用药物和酒精合用时应谨慎。 利培酮可能拮抗左旋多巴和多巴胺激动剂的作用。 当利培酮与酶诱导剂(例如卡马西平)合用时,利培酮的剂量应增加至患者常用剂量的两倍。当停用卡马西平等酶诱导剂时,可能需要降低利培酮的剂量[参见药物相互作用(7.1)]。利培酮与其他酶诱导剂(例如苯妥英钠、利福平和苯巴比妥)合用时,也可能出现类似情况。 长期服用氯氮平和利培酮可能会降低利培酮的清除率。 有关利培酮的更多相互作用(完整)数据(共10项),请访问HSDB记录页面。 肝毒性 长期服用利培酮的患者中,高达30%可能出现肝功能异常,通常在治疗的前8周内出现。ALT升高通常较轻、短暂,即使继续用药也可能恢复正常。已有报道称,部分患者出现更明显的ALT和碱性磷酸酶升高,伴或不伴症状,以及黄疸。损伤通常在开始服用利培酮后几天内发生,停药后迅速消退。也有报道称,部分患者在开始服用利培酮数月甚至数年后出现急性肝损伤伴黄疸。血清酶升高模式通常为胆汁淤积型,但也曾报道过肝细胞型和混合型病例。免疫过敏反应(皮疹、发热、嗜酸性粒细胞增多)罕见;曾有报道一例由利培酮治疗诱发的自身免疫性肝炎病例,但大多数病例不具有自身免疫特征。 妊娠和哺乳期用药 ◉ 哺乳期用药概述 有限的信息表明,孕妇每日服用高达6毫克的利培酮,乳汁中药物浓度较低。据报道,婴儿通过母乳摄入利培酮后会出现镇静、生长发育迟缓、烦躁不安、震颤、异常肌肉运动和呼吸抑制等症状。由于关于利培酮在哺乳期应用的已发表经验较少,且缺乏长期随访数据,因此,尤其是在哺乳新生儿或早产儿时,可能更倾向于选择其他药物。对第二代抗精神病药物的系统评价得出结论,由于现有数据有限且利培酮与其他药物相比更容易分泌到乳汁中,因此在哺乳期,利培酮似乎应作为二线药物。一项安全性评分系统认为,在哺乳期谨慎使用利培酮是可行的。应监测婴儿的嗜睡、体重增长、震颤、呼吸频率、异常肌肉运动和发育里程碑,尤其是在同时使用其他抗精神病药物的情况下。 ◉ 对母乳喂养婴儿的影响 一位女性在哺乳期间每天服用 4 毫克利培酮。她的婴儿在9个月大之前的所有检查中均未发现发育异常。另一位母亲在哺乳期间每日服用6毫克利培酮。她的婴儿在12个月大之前的所有检查中均未发现发育异常。 两名分别每日服用4毫克和1.5毫克利培酮的女性,分别给她们3.3个月大和6周大的婴儿进行母乳喂养,婴儿的发育里程碑均正常,且未报告任何不良反应。 一名产后1周的妇女开始服用利培酮,每日2毫克,10天后增加至每日3毫克。她每天给婴儿哺乳6次。该婴儿接受了5周的住院治疗观察,儿科神经科医生评估其发育正常。未观察到婴儿出现镇静或其他不良反应。经过三个月的利培酮治疗,母亲和婴儿的健康状况良好。 一名婴儿在母亲每日服用1毫克利培酮治疗期间纯母乳喂养了三个月。儿科检查发现该婴儿无神经系统或身体异常,且互动正常。 在一项电话随访研究中,124名在哺乳期间服用苯二氮卓类药物的母亲报告了她们的婴儿是否有任何镇静迹象。一位每日服用0.75毫克利培酮、15毫克氟西泮、0.25毫克氯硝西泮(每日两次)和1毫克安非他酮的母亲报告说,她的母乳喂养婴儿出现了镇静现象。 一名被诊断患有精神分裂症的女性在妊娠晚期和产后(未说明哺乳时间)每日服用1.5毫克利培酮,同时哺乳她的足月婴儿。产后两周,由于症状复发,加用氟哌啶醇0.8毫克/天。在此剂量下,婴儿未出现不良反应。然而,由于症状复发,氟哌啶醇剂量增加至1.5毫克/天。三天后,婴儿出现过度镇静、喂养困难和运动迟缓。儿科评估未发现这些症状的医学原因。停止母乳喂养后,婴儿的症状在5天内完全消失。婴儿的症状可能由药物组合引起。 一项在印度一家住院母婴精神科病房进行的前瞻性队列研究,追踪了7名通过母乳接触利培酮的婴儿;大多数婴儿接受了部分补充治疗。其中一名婴儿的母亲服用利培酮4毫克和劳拉西泮2毫克,该婴儿出现镇静,停用劳拉西泮后镇静症状消失。一名母亲每日服用利培酮 4 mg、苯海索 2 mg 并接受电休克治疗的婴儿出现便秘。婴儿出院后接受了 1 至 3 个月的随访。一名婴儿体重发育迟缓,一名婴儿身高发育迟缓,一名婴儿智力发育迟缓,另一名婴儿运动和智力发育迟缓。 一名患有双相情感障碍的女性,睡前口服利培酮 2 mg,每 2 周肌注长效利培酮 50 mg,每日口服西酞普兰 20 mg,每日口服苯扎托品 0.5 mg。她怀孕后继续服用相同的药物。她的婴儿在妊娠 35 周时出生,并接受了母乳喂养(未说明喂养程度和持续时间)。婴儿16个月大时发育良好,各项发育指标均达标。 国家非典型抗精神病药物妊娠登记处登记的哺乳期服用第二代抗精神病药物的患者(n = 576)与未服用第二代抗精神病药物的哺乳期对照组患者(n = 818)进行了比较。在服用第二代抗精神病药物的患者中,60.4%同时服用两种或两种以上的精神药物。儿科病历回顾显示,无论婴儿是否接受第二代抗精神病药物单药治疗或联合治疗,均未发现不良反应。服用利培酮的女性人数未见报道。 一名早产儿出生时体重2.75公斤,孕周35周。由于呼吸窘迫,该婴儿出生后接受了2分钟的简易呼吸器辅助通气,并在出生后的前18小时内持续吸氧。婴儿出生后第二天开始母乳喂养。第12天,母亲开始服用利培酮,每日1毫克,用于治疗精神病发作。第13天,婴儿呼吸频率降至16次/分,无呼吸窘迫,遂给予持续气道正压通气(CPAP)12小时,之后逐渐撤机并开始配方奶喂养。第15天,母亲再次开始母乳喂养,但婴儿再次出现呼吸抑制。喂养方式改为在服用利培酮前挤出母乳,每次服药后6小时喂配方奶,之后再进行直接母乳喂养。接下来的两天未再出现呼吸抑制。婴儿于第24天出院,并被告知继续保持之前的喂养方式。呼吸抑制可能是由于乳汁中的利培酮引起的。 一位被诊断为未分化型精神分裂症的女性在5次妊娠期间每日服用4至5毫克利培酮和2毫克苯海索。她对每个婴儿进行20至24个月的母乳喂养。所有孩子均未出现不良发育后果。截至本文发表时,年龄最大的三个孩子(分别为26岁、23岁和22岁)已完成学业并就业,而年龄最小的两个孩子(分别为15岁和19岁)学业成绩良好。 ◉ 对哺乳和母乳的影响 服用利培酮的患者会出现血清催乳素水平升高、男性乳房发育和溢乳。在一例病例中,一名19岁男性在服用氟伏沙明期间出现了泌乳素水平正常的男性乳房发育症和溢乳。一项包含3项研究的荟萃分析发现,利培酮引起男性乳房发育症的风险是喹硫平的4.3倍。对于已建立泌乳的母亲,其泌乳素水平可能不会影响其哺乳能力。 一项研究将国家非典型抗精神病药物妊娠登记处登记的哺乳期服用第二代抗精神病药物的患者(n = 576)与主要诊断为重度抑郁症和焦虑症的对照组哺乳期患者(n = 818)进行了比较,对照组哺乳期患者通常接受选择性5-羟色胺再摄取抑制剂(SSRI)或选择性5-羟色胺和去甲肾上腺素再摄取抑制剂(SNRI)类抗抑郁药治疗,但未接受第二代抗精神病药物治疗。在服用第二代抗精神病药物的女性中,60.4%的人同时服用不止一种精神药物,而对照组女性的这一比例为24.4%。服用第二代抗精神病药物的女性中,59.3%的人报告“曾经母乳喂养过”,而对照组女性的这一比例为88.2%。产后3个月时,服用第二代抗精神病药物的女性中,23%的人仍在进行纯母乳喂养,而对照组女性的这一比例为47%。服用利培酮的女性人数未见报道。 ◈ 什么是利培酮? 利培酮是一种用于治疗精神疾病(如精神分裂症、双相情感障碍和抑郁症)的药物。它可以口服或注射给药。利培酮属于非典型或第二代抗精神病药物。利培酮的商品名包括Risperdal®、Risperdal Consta®和Perseris®。有时,当人们发现自己怀孕后,会考虑改变服药方式,甚至完全停药。然而,在改变服药方式之前,务必咨询您的医疗保健提供者。您的医疗保健提供者可以与您讨论治疗您病情的益处以及怀孕期间疾病未治疗的风险。 ◈ 我正在服用利培酮。它会影响我怀孕吗? 在某些人身上,利培酮可能会提高一种名为催乳素的激素水平。高水平的催乳素会抑制排卵(月经周期中卵巢释放卵子的过程)。这会使怀孕更加困难。如有任何疑虑,您的医疗保健提供者可以检测您的催乳素水平。 ◈ 服用利培酮会增加流产的风险吗? 流产很常见,任何妊娠都可能发生,原因多种多样。根据已审查的研究,预计利培酮不会增加流产的风险。 ◈ 服用利培酮会增加胎儿畸形的风险吗? 每次妊娠开始时都有3-5%的胎儿畸形风险。这被称为背景风险。根据已审查的研究,利培酮预计不会增加出生缺陷的风险,使其高于背景风险。 ◈ 孕期服用利培酮会增加其他妊娠相关问题的风险吗? 根据已审查的研究,利培酮可能导致低出生体重(出生时体重低于 5 磅 8 盎司 [2500 克])。利培酮可能导致孕妇体重增加和血糖问题,从而增加患妊娠期糖尿病的风险。更多关于妊娠期糖尿病的信息,请参阅我们的情况说明书:https://mothertobaby.org/fact-sheets/diabetes-pregnancy/。 ◈ 我需要在整个孕期服用利培酮,它会导致宝宝出生后出现戒断症状吗? 孕期服用某些药物可能会导致新生儿在出生后不久出现暂时性症状,这些症状有时被称为戒断反应。目前尚不清楚单独服用利培酮是否会增加新生儿出现戒断症状的风险。类似药物与戒断反应的风险相关,因此,在分娩前后接触过利培酮的婴儿应密切观察是否出现肌肉僵硬或无力、嗜睡、烦躁、震颤、呼吸困难和喂养困难等症状。大多数情况下,这些症状会在几天内自行消失,不会对健康造成长期影响。重要的是,您的医护人员应了解您正在服用利培酮,以便在出现症状时,您的宝宝能够得到最佳的护理。 ◈ 孕期服用利培酮是否会影响孩子未来的行为或学习能力? 目前尚无研究表明利培酮是否会导致孩子出现行为或学习问题。 ◈ 服用利培酮期间是否可以哺乳? 关于哺乳期间使用利培酮的信息有限。每日服用高达 6 毫克利培酮时,会在母乳中检测到少量利培酮。少数仅接触利培酮(每日剂量高达 6 毫克)的母乳喂养婴儿未报告副作用。如果您同时服用利培酮和其他药物,婴儿出现副作用的风险可能会更高。如果您怀疑婴儿出现任何症状(嗜睡、喂养困难、烦躁或异常动作),请联系孩子的医疗保健提供者。利培酮的产品标签建议哺乳期妇女不要使用此药。但使用利培酮的益处可能大于潜在风险。您的医疗保健提供者可以与您讨论使用利培酮以及最适合您的治疗方案。请务必就所有关于母乳喂养的问题咨询您的医疗保健提供者。 ◈ 如果男性服用利培酮,是否会影响生育能力(使伴侣怀孕的能力)或增加出生缺陷的风险? 服用利培酮可能会提高人体内的催乳素水平,这可能会影响生育能力。目前尚无研究表明利培酮是否会在背景风险的基础上增加出生缺陷的风险。一般来说,父亲或精子捐赠者接触到的药物不太可能增加怀孕的风险。更多信息,请参阅 MotherToBaby 网站上的“父亲接触”情况说明书:https://mothertobaby.org/fact-sheets/paternal-exposures-pregnancy/。 |
| 参考文献 | |
| 其他信息 |
治疗用途
抗精神病药;多巴胺拮抗剂;5-羟色胺拮抗剂 利培酮(Risperdal)适用于治疗精神分裂症。其疗效已在4项成人短期试验、2项青少年(13至17岁)短期试验和1项成人长期维持治疗试验中得到证实。/美国产品标签/ 利培酮与锂盐或丙戊酸盐联合治疗适用于治疗双相I型障碍相关的急性躁狂或混合发作。其疗效已在一项成人短期试验中得到证实。/美国产品标签/ 利培酮适用于治疗自闭症相关的易激惹症状,包括攻击他人、故意自伤、发脾气和情绪快速变化等症状。疗效已在3项针对儿童和青少年(5至17岁)的短期试验中得到证实。/美国产品标签包含/ 利培酮适用于治疗与I型双相情感障碍相关的急性躁狂或混合发作。疗效已在2项针对成人的短期试验和1项针对儿童和青少年(10至17岁)的短期试验中得到证实。/美国产品标签包含/ 药物警告 /黑框警告/ 警告:老年痴呆相关精神病患者死亡率增加。接受抗精神病药物治疗的老年痴呆相关精神病患者的死亡风险增加。利培酮(Risperdal)未获准用于治疗痴呆相关精神病患者。 与其他抗精神病药物(例如吩噻嗪类药物)一样,利培酮也与迟发性运动障碍有关。尽管有研究表明非典型抗精神病药物引起迟发性运动障碍的风险较低,但不同抗精神病药物引起迟发性运动障碍的潜力是否存在差异尚不清楚。在一项开放标签研究中,接受每日约8-9毫克口服利培酮至少1年的精神分裂症患者中,迟发性运动障碍的年发生率为0.3%。该综合征的患病率在老年患者(尤其是女性)中似乎最高。迟发性运动障碍的发生风险及其不可逆的可能性似乎会随着抗精神病药物治疗时间和累积剂量的增加而增加;然而,即使在相对较短的低剂量治疗后,该综合征也可能发生,尽管发生频率要低得多。神经阻滞剂恶性综合征(NMS)是一种潜在的致命症状群,已有服用抗精神病药物的患者报告出现该症状。NMS需要立即停药并进行强化对症和支持治疗。剂量相关性嗜睡是利培酮治疗中常见的副作用。在采用直接询问或检查表检测不良事件的研究中,每日口服16毫克利培酮的成年精神分裂症患者中约有8%报告出现嗜睡,而服用安慰剂的患者中这一比例为1%。 有关利培酮(共41条)的更多药物警告(完整)数据,请访问HSDB记录页面。 药效学 利培酮的主要作用是降低大脑中多巴胺能和血清素能通路活性,从而减轻精神分裂症和情绪障碍的症状。与大脑中的多巴胺D2受体相比,利培酮对血清素5-HT2A受体具有较高的结合亲和力。利培酮与D2受体的结合亲和力低于第一代抗精神病药物,后者与D2受体的结合亲和力非常高。与之前的抗精神病药物相比,利培酮能减轻锥体外系症状,这可能是由于其对多巴胺D2受体具有中等亲和力所致。长期以来,人们一直认为抗精神病药物主要作用于神经元或神经网络,包括突触网络。然而,本研究表明,抗精神病药物,尤其是利培酮,可通过抑制小胶质细胞活化发挥抗炎作用。因此,抗精神病药物可能通过减少小胶质细胞的炎症反应,从而抑制神经发生和少突胶质细胞生成,进而对精神分裂症患者产生潜在的治疗作用。这些结果可能为精神分裂症的治疗策略提供新的思路。能够抑制小胶质细胞活化的药物也可能对精神分裂症的治疗有益。为了进一步研究,应详细阐明利培酮对小胶质细胞活化的抑制作用的分子机制,并进行体内研究以验证目前的结果。[3] P-gp转运和抑制的机制基础已被深入研究多年。人们提出了多种假说来解释P-gp与其底物或抑制剂相互作用的分子机制。然而,由于P-gp上存在多个药物结合位点,建立一个普遍接受的模型来协调来自不同实验室的数据仍然是一个挑战。研究表明,P-gp上至少存在四个药物结合位点。这些位点可分为两类:转运位点,药物可在此跨细胞膜转运;以及调节位点,可改变P-gp的功能(Martin等,2000)。此外,一些药物可通过降低细胞内ATP供应和抑制P-gp ATPase活性来抑制P-gp活性(Batrakova等,2001)。考虑到利培酮/RSP和PALI似乎既是P-gp底物又是抑制剂,它们与其他底物竞争结合P-gp可能是其抑制P-gp的机制之一。然而,其他机制也不能排除,需要进一步研究来阐明RSP和PALI与P-gp相互作用的分子基础。[4]本研究未能从涉及多巴胺和/或5-HT受体拮抗作用的证据中获得关于注射利培酮的大鼠食物摄入量改变的最终解释。然而,利培酮(0.5 mg/kg)注射大鼠体重增加减少的部分原因可能是能量消耗增加,这可以从棕色脂肪组织(BAT)中UCP-1 mRNA表达的显著增加得到证实。在人类中,BAT存在于新生儿体内,但在成人体内含量减少,其作用也较小。73 这或许可以部分解释利培酮对啮齿动物和人类体重增加影响的差异。在本研究中,我们首次证实,利培酮注射可诱导大鼠白色脂肪组织(WAT)中瘦素mRNA的表达以及棕色脂肪组织(BAT)中UCP-1 mRNA的表达。然而,我们未能对这些表达升高给出合理的解释。因此,我们下一步的任务是阐明利培酮诱导脂肪组织中这些基因mRNA表达水平升高的机制。[6] |
| 分子式 |
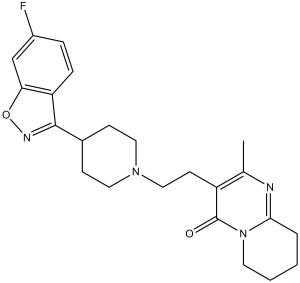
C23H27FN4O2
|
|
|---|---|---|
| 分子量 |
410.48
|
|
| 精确质量 |
410.211
|
|
| 元素分析 |
C, 67.30; H, 6.63; F, 4.63; N, 13.65; O, 7.80
|
|
| CAS号 |
106266-06-2
|
|
| 相关CAS号 |
Risperidone-d4; 1020719-76-9; Risperidone hydrochloride; 666179-74-4; Risperidone mesylate; 666179-96-0
|
|
| PubChem CID |
5073
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 沸点 |
572.4±60.0 °C at 760 mmHg
|
|
| 熔点 |
170°C
|
|
| 闪点 |
300.0±32.9 °C
|
|
| 蒸汽压 |
0.0±1.6 mmHg at 25°C
|
|
| 折射率 |
1.677
|
|
| LogP |
2.88
|
|
| tPSA |
64.16
|
|
| 氢键供体(HBD)数目 |
0
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
4
|
|
| 重原子数目 |
30
|
|
| 分子复杂度/Complexity |
731
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
FC1C([H])=C([H])C2=C(C=1[H])ON=C2C1([H])C([H])([H])C([H])([H])N(C([H])([H])C([H])([H])C2=C(C([H])([H])[H])N=C3C([H])([H])C([H])([H])C([H])([H])C([H])([H])N3C2=O)C([H])([H])C1([H])[H]
|
|
| InChi Key |
RAPZEAPATHNIPO-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C23H27FN4O2/c1-15-18(23(29)28-10-3-2-4-21(28)25-15)9-13-27-11-7-16(8-12-27)22-19-6-5-17(24)14-20(19)30-26-22/h5-6,14,16H,2-4,7-13H2,1H
|
|
| 化学名 |
3-[2-[4-(6-fluoro-1,2-benzoxazol-3-yl)piperidin-1-yl]ethyl]-2-methyl-6,7,8,9-tetrahydropyrido[1,2-a]pyrimidin-4-one
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 1 mg/mL (2.44 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 10.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1 mg/mL (2.44 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 10.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 1 mg/mL (2.44 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.4362 mL | 12.1809 mL | 24.3617 mL | |
| 5 mM | 0.4872 mL | 2.4362 mL | 4.8723 mL | |
| 10 mM | 0.2436 mL | 1.2181 mL | 2.4362 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
CLOZAPINE Response in Biotype-1
CTID: NCT04580134
Phase: Phase 4 Status: Recruiting
Date: 2024-08-28
|
|---|