| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
c-Met (IC50 = 5 nM); p-Met (IC50 = 3 nM)
The target of Savolitinib (AZD6094, HMPL-504) is mesenchymal-epithelial transition factor (c-Met), and it acts as a highly potent and selective inhibitor of c-Met. [1] Savolitinib (AZD6094, HMPL-504) is a selective c-Met inhibitor, and in gastric cancer cell lines with dysregulated c-Met, its EC50 values for inhibiting cell growth range from 0.6 nM/L to 12.5 nM/L [2] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:沃利替尼具有精细的激酶选择性和优异的效力。它在整个胃细胞系组中显示出高选择性,仅在 cMET 失调的细胞系中有效抑制细胞生长(EC50 值 0.6 nM/L-12.5 nM/L)。沃利替尼具有高膜渗透性,无需跨 Caco-2 细胞单层的外排转运,并且表现出可忽略不计的 P-gp 抑制 (IC50 > 17 μM)。沃利替尼在人肝微粒体中没有表现出显着的可逆或基于机制的 CYP 抑制,并且在人肝细胞中没有诱导 CYP1A2 和 CYP3A4。激酶测定:沃利替尼对于 c-Met 和 p-Met 的 IC50 值分别为 5 nM 和 3 nM。与 274 种其他激酶相比,它对 c-Met 表现出高选择性。细胞测定:孵育过夜后,用系列稀释的测试化合物在37℃下处理NCI-H441细胞1小时。然后除去培养基,并在 100 μL/孔裂解缓冲液(1% NP-40、20 mM Tris/pH 8.0、137 mM NaCl、10% 甘油、2 mM EDTA、1 mM 活化原钒酸钠、10 mg/mL 抑肽酶、10 mg/mL 亮肽素)。将含有细胞裂解物的板在-80℃下保存过夜。第二天,将板在冰上解冻,轻轻混合。将 25 μL/孔的裂解物添加到预先包被有抗 p-Met 抗体的检测板中,以检测 pc-Met 信号。 pc-Met 水平在 450 nm 和 570 nm 处测定。
1. 胃癌细胞系抗增殖活性:筛选22种胃癌细胞系以评估Savolitinib的抗增殖作用。结果显示,Savolitinib仅对c-Met失调的细胞系表现出强效的生长抑制作用,EC50值介于0.6 nM/L至12.5 nM/L;而对c-Met表达正常的胃癌细胞系无显著抑制效果[2] 2. c-Met信号通路药效学分析:将Hs746t胃癌细胞用0.1 μM Savolitinib处理1小时后制备细胞裂解液,进行蛋白质印迹(Western blot)分析。结果表明,Savolitinib可有效抑制c-Met(成熟型分子量145 kDa)的磷酸化,从而阻断c-Met信号通路的激活 [2] 3. 构效关系研究:合成一系列新型三唑并吡嗪类c-Met抑制剂并探究其构效关系,Savolitinib(研究中的化合物28)被鉴定为强效、选择性c-Met抑制剂,但参考文献[1]中未详细提供该化合物的具体体外酶活性或细胞活性数据[1] 4. 膜通透性与外排转运:Savolitinib在Caco-2细胞单层模型中表现出高膜通透性,A→B方向的表观渗透系数(Papp)为28×10⁻⁶ cm/s,且无外排转运现象;此外,Savolitinib对P-糖蛋白(P-gp)的抑制作用极弱,IC50值大于17 μM[3] 5. 体外代谢稳定性:评估Savolitinib在大鼠、犬、猴和人肝微粒体及S9组分中的代谢稳定性。在不同物种的肝微粒体和S9组分中检测到5种I相代谢产物,其中3种主要代谢产物(M1:去甲基化、M2:羟化、M3:单加氧)由CYP450酶和醛氧化酶等多种酶介导;大鼠的体外代谢特征和代谢产物谱与人类最相似[3] 6. CYP酶抑制/诱导作用:Savolitinib在人肝微粒体中未表现出显著的可逆性或机制性CYP酶抑制作用,且在人肝细胞中不诱导CYP1A2和CYP3A4的表达[3] |
| 体内研究 (In Vivo) |
沃利替尼在 U87MG 皮下异种移植模型中表现出剂量依赖性肿瘤生长抑制作用。在 3/3 cMET 失调的胃癌患者来源的肿瘤异种移植模型中,其治疗导致 c-MET 信号传导的药效学调节和有效的肿瘤停滞,但在胃癌控制模式中的活性可忽略不计。沃利替尼具有中等的血浆蛋白结合率(大鼠、狗和人为 60%∼70%;小鼠为 40%;猴为 80%),并且在大鼠的不同器官中分布广泛,其中肝脏和肾脏中的暴露量较高,与血浆水平相比,大脑、脊髓和睾丸中的水平较低。
1. 人胶质瘤异种移植模型抗肿瘤活性:Savolitinib在小鼠体内具有良好的药代动力学特性,且在裸鼠人胶质瘤异种移植模型中表现出良好的抗肿瘤活性[1] 2. Hs746t胃癌异种移植模型抗肿瘤活性:给荷有皮下Hs746t移植瘤的裸鼠(nu/nu)每日一次(qd)灌胃给予不同剂量的Savolitinib。结果显示,Savolitinib显著抑制肿瘤生长(P ≤ 0.001),但未详细说明具体肿瘤体积数据和剂量-效应关系;药效学分析表明,Savolitinib可抑制肿瘤组织中磷酸化c-Met水平,抑制率计算公式为:IR (%) = (1−给药组OD450/溶媒组OD450) × 100%,无具体数值报道[2] 3. 胃癌PDX模型抗肿瘤活性:给荷有人源胃癌组织移植瘤的裸鼠每日一次灌胃给予Savolitinib。在3种c-Met失调的胃癌PDX模型(SGC071、SGC184、SGC141)中,Savolitinib均能强效抑制肿瘤生长(P ≤ 0.001);而在c-Met低多体性的PDX模型(SGC070)中无显著活性(P ≥ 0.05);药效学分析证实,Savolitinib可调节肿瘤组织中磷酸化c-Met的表达(通过给药前后IHC染色评估)[2] 4. 与多西他赛联合治疗:在Hs746t异种移植模型和SGC184 PDX模型中,Savolitinib与多西他赛联合给药的抗肿瘤效果优于单药治疗(Hs746t模型P ≤ 0.001,SGC184模型P ≤ 0.05),未详细提供具体肿瘤生长曲线或消退率[2] 5. 大鼠体内分布:Savolitinib在大鼠体内广泛分布于各组织,肝、肾中暴露量较高,脑、脊髓和睾丸中的浓度远低于血浆水平[3] 6. 大鼠体内排泄:代谢是Savolitinib在大鼠体内的主要消除途径,原形药物经粪便、尿液和胆汁排泄的量不足给药剂量的2%;在大鼠血浆和排泄物中鉴定出16种I相代谢产物和8种II相代谢产物,其中M22(单加氧代谢产物M5的硫酸结合物)在所有检测基质中占主导地位;去甲基化生成M2并经尿液排泄也是重要消除途径[3] 7. 动物药代动力学参数: - 小鼠:口服吸收迅速(Tmax < 2.5 h),口服生物利用度27.2%,体内清除率(CL)11.0 mL/min/kg(低提取率),稳态分布容积(Vss)0.4 L/kg(中低分布)[3] - 大鼠:口服吸收迅速(Tmax < 2.5 h),口服生物利用度42.6%,CL 11.8 mL/min/kg(低提取率),Vss 1.4 L/kg(中低分布),在1~25 mg/kg剂量范围内呈线性药代动力学特征[3] - 犬:口服吸收迅速(Tmax < 2.5 h),口服生物利用度86.3%,CL 3.5 mL/min/kg(低提取率),Vss 1.4 L/kg(中低分布),在2~10 mg/kg剂量范围内呈线性药代动力学特征,食物对其药代动力学特征无显著影响[3] - 猴:口服吸收迅速(Tmax = 1.9 h),口服生物利用度仅1.9%,CL 17.2 mL/min/kg(高提取率),Vss 0.7 L/kg(中低分布);低生物利用度归因于首过提取效应过强[3] |
| 细胞实验 |
在 96 孔板中,NCI-H441 细胞以 15,000 个细胞/孔的密度接种在含有 10% FBS 的 RPMI-1640 培养基中。将细胞孵育一整夜,然后在 37°C 下用逐渐稀释的测试化合物处理一小时。除去培养基后,将细胞在每孔含有 100 μL 的裂解缓冲液中裂解,浓度如下:1% NP-40、20 mM Tris/pH 8.0、137 mM NaCl、10% 甘油、2 mM EDTA、1 mM 活化原钒酸钠、10 mg/mL 抑肽酶和 10 mg/mL 亮肽素。过夜后,将含有细胞裂解物的板储存在 -80°C 下。将板轻轻混合并于第二天在冰上解冻。为了检测 pc-Met 信号,将 25 μL/孔的裂解物添加到已预先涂有抗 p-Met 抗体的测定板中。 pc-Met 的测量在 450 和 570 nm 处进行。
1. 胃癌细胞增殖实验: - 步骤1:将22种胃癌细胞系以特定密度(未指定)接种至适宜培养板,在标准条件(温度、CO2浓度未提及)下培养至贴壁; - 步骤2:向培养基中加入不同浓度的Savolitinib,孵育一定时间(未指定); - 步骤3:采用细胞活力检测方法(未指定)测定细胞增殖率,计算各细胞系的EC50值;将结果与c-Met基因拷贝数(GCN)、c-Met蛋白IHC评分及细胞染色定位关联,分析c-Met失调与细胞对Savolitinib敏感性的关系[2] 2. c-Met磷酸化Western blot分析: - 步骤1:将Hs746t胃癌细胞在完全培养基中培养至所需汇合度(未指定); - 步骤2:用0.1 μM Savolitinib或PF-4217903(无关选择性c-Met抑制剂)处理细胞1小时; - 步骤3:用裂解液(组分未指定)裂解细胞制备裂解液,测定蛋白浓度(方法未指定); - 步骤4:取等量蛋白进行SDS-PAGE电泳(凝胶浓度未指定),转膜(膜类型未指定)后,用c-Met和磷酸化c-Met(成熟型,145 kDa)一抗孵育,再加入二抗;检测蛋白条带(检测方法未指定),分析Savolitinib对c-Met磷酸化的抑制作用[2] 3. Caco-2细胞通透性实验: - 步骤1:将Caco-2细胞接种于Transwell小室,培养至形成融合单层(培养时长、单层完整性验证方法未指定); - 步骤2:将Savolitinib加入Transwell小室的顶侧(A)或基底侧(B),37℃孵育特定时间(未指定); - 步骤3:在预设时间点收集对侧样品,测定Savolitinib浓度(检测方法未指定),计算A→B方向的表观渗透系数(28×10⁻⁶ cm/s),评估外排转运(无外排)[3] 4. 体外代谢稳定性实验: - 步骤1:制备大鼠、犬、猴和人的肝微粒体/S9组分(制备方法未指定),调整蛋白浓度至特定值(未指定); - 步骤2:将Savolitinib与肝微粒体/S9组分在辅因子(如CYP450代谢所需的NADPH)存在下37℃孵育不同时间(未指定); - 步骤3:加入淬灭剂(未指定)终止反应,采用色谱方法(未指定)分析样品,鉴定代谢产物(5种I相产物)并评估代谢稳定性;发现大鼠的代谢产物谱与人类最相似[3] |
| 动物实验 |
雌性无胸腺小鼠
\n1.0、2.5 和 10.0 mg/kg(口服);2.5 mg/kg(静脉注射) \口服给药/静脉注射 \n1.无胸腺裸鼠人胶质瘤异种移植模型: \n - 步骤 1:将特定数量的(未指定)人胶质瘤细胞(具体细胞系未指定)皮下植入无胸腺裸鼠(雌性/雄性,年龄未指定)体内。 \n - 步骤 2:肿瘤植入后,当肿瘤达到一定体积(未指定)时,将小鼠随机分为治疗组和对照组(组数未指定)。 \n - 步骤 3:治疗组给予Savolitinib(给药途径、剂量、频率未指定),对照组给予赋形剂。 \n - 步骤 4:定期监测肿瘤体积和小鼠体重(监测间隔未指定),以评估Savolitinib的抗肿瘤活性。未提供药物溶出度配方/赋形剂的详细信息[1] \n2.在裸鼠(nu/nu)中建立Hs746t胃癌异种移植模型: \n - 步骤1:将特定数量的Hs746t胃癌细胞(未具体说明)皮下注射到裸鼠(nu/nu)体内(每组7-8只小鼠)。 \n - 步骤2:当肿瘤形成后(具体体积未具体说明),每日一次(qd)灌胃给予不同剂量的Savolitinib(剂量未具体说明)。对照组接受赋形剂(未指定溶出配方)。 \n - 步骤 3:定期(未指定)测量肿瘤体积,并绘制随时间变化的曲线图,以评估抗肿瘤疗效(治疗组与对照组相比,P ≤ 0.001)。 \n - 步骤 4:进行药效学分析时,在给予Savolitinib后的不同时间点和剂量(未指定)收集肿瘤组织块,并制备肿瘤裂解液进行 ELISA 检测,以检测磷酸化 c-Met 水平。抑制率的计算公式为 IR (%) = (1−OD450 药物处理组/OD450 赋形剂) × 100% [2] \n3.裸鼠胃癌PDX模型: \n - 步骤1:将患者来源的胃肿瘤组织块皮下植入裸鼠(每组7-8只小鼠)体内,建立PDX模型(植入方法未具体说明)。 \n - 步骤2:待肿瘤形成后(具体体积未具体说明),每日一次(qd)灌胃给予Savolitinib,剂量未具体说明。对照组给予赋形剂(溶出方法未具体说明)。 \n - 步骤3:定期测量肿瘤体积(具体测量方法未具体说明),并绘制肿瘤体积随时间变化的曲线。 Savolitinib在3个c-Met扩增的PDX模型(SGC071、SGC184、SGC141,P ≤ 0.001)中诱导了强效的肿瘤抑制,但对SGC070无显著影响(P ≥ 0.05)。 \n - 步骤4:进行药效学分析时,在给药前和Savolitinib给药后2小时收集肿瘤组织,并通过IHC染色评估磷酸化c-Met的表达[2] \n4.异种移植/PDX模型中的联合治疗: \n - 步骤1:如上所述,在nu/nu小鼠中建立Hs746t异种移植或SGC184 PDX模型(组数未指定)。 \n - 步骤2:将小鼠随机分为四组:Savolitinib单药组(灌胃,每日一次,剂量未指定)、多西他赛单药组(给药途径:静脉注射,频率:每周一次,剂量未指定)、联合治疗组(两种药物按上述剂量/方案给药)和载体对照组。 \n - 步骤3:定期测量肿瘤体积(未指定),以评估联合治疗的协同作用(Hs746t P ≤ 0.001,SGC184 P ≤ 0.05)[2] \n5.在小鼠、大鼠、犬和猴体内进行的药代动力学研究: \n - 步骤 1:将动物(小鼠、大鼠、犬、猴;性别、年龄、体重未指定)分组(组数未指定),并根据需要进行禁食(用于口服给药)或非禁食(用于静脉给药)。 \n - 步骤 2:Savolitinib 以不同剂量(大鼠 1–25 mg/kg,犬 2–10 mg/kg)口服(灌胃)或静脉注射(剂量未指定)给药。将药物溶解于合适的溶剂中(未具体说明)。 \n - 步骤 3:给药后在预定时间点(未具体说明)采集血样,并分离血浆(方法未具体说明)。 \n - 步骤 4:采用经验证的分析方法(未具体说明)测定血浆中Savolitinib的浓度,并计算药代动力学参数(Tmax、生物利用度、CL、Vss)。对于犬,通过比较喂食组和空腹组来评估食物对药代动力学的影响(食物影响甚微)[3] \n6.大鼠体内分布和排泄研究: \n - 步骤 1:将大鼠(性别、年龄、体重未指定)以特定剂量(未指定)通过灌胃或静脉注射(途径未指定)给予Savolitinib。 \n - 步骤 2:为进行分布研究,在给药后特定时间点(未指定)处死大鼠,收集不同器官(肝脏、肾脏、脑、脊髓、睾丸等),进行匀浆处理(方法未指定),并测定Savolitinib浓度(方法未指定),以评估组织分布(肝脏/肾脏浓度高,脑/脊髓/睾丸浓度低)。 \n - 步骤 3:为进行排泄研究,在给予Savolitinib后,将大鼠置于代谢笼中收集粪便、尿液和胆汁(收集时间未指定)。测定了排泄物中母体药物及其代谢物的浓度(方法未具体说明),以计算排泄率(母体药物<剂量的2%)并鉴定代谢物(16种I期代谢物,8种II期代谢物)[3] |
| 药代性质 (ADME/PK) |
1. 吸收:
- Savolitinib 在小鼠、大鼠、狗和猴子中均显示出快速的口服吸收,Tmax < 2.5 小时(小鼠、大鼠、狗),Tmax = 1.9 小时(猴子)[3] - 口服生物利用度:27.2%(小鼠),42.6%(大鼠),86.3%(狗),1.9%(猴子)。猴子体内生物利用度低归因于首过提取过多[3] 2. 分布: - 血浆蛋白结合率:60%–70%(大鼠、犬、人),40%(小鼠),80%(猴)[3] - 在大鼠中,Savolitinib在不同器官中分布广泛,肝脏和肾脏暴露量高,而脑、脊髓和睾丸中的浓度与血浆水平相比非常低[3] - 稳态分布容积 (Vss):0.4 L/kg(小鼠),1.4 L/kg(大鼠),1.4 L/kg(犬),0.7 L/kg(猴),表明分布中等至低[3] 3. 代谢: - 体外:在大鼠、犬、猴和人的肝微粒体/S9组分中观察到五种I期代谢物;三种主要代谢物(M1:去甲基化,M2:羟基化,M3:单加氧)由CYP450和醛氧化酶介导。大鼠的代谢物谱与人类相似[3] - 体内(大鼠):在血浆和排泄物中共鉴定出16种I期代谢物和8种II期代谢物;M22(M5的硫酸盐结合物,一种单氧化代谢物)是主要代谢物。去甲基化为 M2 和尿液排泄是重要的消除途径 [3] 4. 排泄: - 在大鼠中,代谢是主要的消除途径,因为母体药物 Savolitinib 的粪便、尿液和胆汁排泄量占给药剂量的 < 2% [3] 5. 清除率: - 体内清除率 (CL):11.0 mL/min/kg(小鼠),11.8 mL/min/kg(大鼠),3.5 mL/min/kg(犬),17.2 mL/min/kg(猴)。小鼠、大鼠和犬的提取率较低,而猴的提取率则显著较高[3] 6. 线性药代动力学: - Savolitinib 在大鼠(剂量范围:1–25 mg/kg)和犬(剂量范围:2–10 mg/kg)中均表现出线性药代动力学特征[3] 7. 食物效应: - 食物对犬体内 Savolitinib 的药代动力学特征影响甚微[3] |
| 参考文献 | |
| 其他信息 |
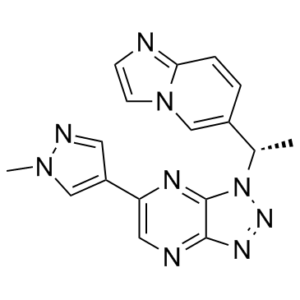
萨沃替尼属于三唑并吡嗪类化合物,其结构为1H-[1,2,3]三唑并[4,5-b]吡嗪,分别在1位和6位被(1S)-1-(咪唑并[1,2-a]吡啶-6-基)乙基和1-甲基-1H-吡唑-4-基取代。它是一种高选择性MET酪氨酸激酶抑制剂,已在中国获批用于治疗携带MET 14号外显子跳跃突变的晚期非小细胞肺癌。它既是c-Met酪氨酸激酶抑制剂,也是一种抗肿瘤药物。它属于吡唑类、三唑并吡嗪类和咪唑并吡啶类化合物。
萨沃替尼已用于多项临床试验,研究肿瘤、食物效应、胃癌、健康受试者和结直肠癌等疾病的治疗和健康服务。 萨沃替尼是一种口服生物利用度高的c-Met受体酪氨酸激酶抑制剂,具有潜在的抗肿瘤活性。萨沃替尼以ATP竞争性方式选择性地结合并抑制c-Met的活化,从而阻断c-Met信号转导通路。这可能导致c-Met蛋白过表达肿瘤细胞的生长受到抑制。c-Met编码肝细胞生长因子受体酪氨酸激酶,在肿瘤细胞增殖、存活、侵袭和转移以及肿瘤血管生成中发挥重要作用;这种蛋白质在多种癌症中过度表达或发生突变。 药物适应症 治疗肾脏肿瘤 治疗肺癌 1. 背景和发展:HGF/c-Met 信号通路与人类癌症有关,而泛 c-Met 抑制剂存在局限性。 Savolitinib(Volitinib)是一种新型、高效、选择性的小分子c-Met抑制剂,通过结构导向药物设计和构效关系研究开发而成[1]。 2. 中国胃癌中c-Met异常表达的发生率:在一项包含170例中国胃癌患者的研究中,c-MET基因扩增的发生率为6%,蛋白过表达的发生率为13%[2]。 3. 临床潜力:临床前研究表明,Savolitinib在c-Met异常表达的胃癌细胞系和PDX模型中具有显著的抗肿瘤活性,为其作为c-MET扩增胃癌患者的治疗选择进行临床研究提供了强有力的理论依据[2]。 4. 总体临床前特征:Savolitinib表现出良好的临床前PK/ADME特性,包括高膜渗透性和低P-gp值。抑制作用,无CYP酶抑制/诱导作用,在大鼠和犬中呈线性药代动力学,在小鼠、大鼠和犬中具有可接受的生物利用度[3] |
| 分子式 |
C17H15N9
|
|
|---|---|---|
| 分子量 |
345.36
|
|
| 精确质量 |
345.145
|
|
| 元素分析 |
C, 59.12; H, 4.38; N, 36.50
|
|
| CAS号 |
1313725-88-0
|
|
| 相关CAS号 |
|
|
| PubChem CID |
68289010
|
|
| 外观&性状 |
Off-white to yellow solid powder
|
|
| 密度 |
1.6±0.1 g/cm3
|
|
| 折射率 |
1.833
|
|
| LogP |
0.54
|
|
| tPSA |
91.61
|
|
| 氢键供体(HBD)数目 |
0
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
3
|
|
| 重原子数目 |
26
|
|
| 分子复杂度/Complexity |
505
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
N1(C2C(=NC([H])=C(C3C([H])=NN(C([H])([H])[H])C=3[H])N=2)N=N1)[C@@]([H])(C([H])([H])[H])C1C([H])=C([H])C2=NC([H])=C([H])N2C=1[H]
|
|
| InChi Key |
XYDNMOZJKOGZLS-NSHDSACASA-N
|
|
| InChi Code |
InChI=1S/C17H15N9/c1-11(12-3-4-15-18-5-6-25(15)10-12)26-17-16(22-23-26)19-8-14(21-17)13-7-20-24(2)9-13/h3-11H,1-2H3/t11-/m0/s1
|
|
| 化学名 |
3-[(1S)-1-imidazo[1,2-a]pyridin-6-ylethyl]-5-(1-methylpyrazol-4-yl)triazolo[4,5-b]pyrazine
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (6.02 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.08 mg/mL (6.02 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (6.02 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.8955 mL | 14.4776 mL | 28.9553 mL | |
| 5 mM | 0.5791 mL | 2.8955 mL | 5.7911 mL | |
| 10 mM | 0.2896 mL | 1.4478 mL | 2.8955 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04606771 | Active Recruiting |
Drug: Osimertinib + Savolitinib Drug: Savolitinib + Placebo |
Non-Small Cell Lung Cancer | AstraZeneca | September 28, 2020 | Phase 2 |
| NCT03091192 | Active Recruiting |
Drug: Savolitinib Drug: Sunitinib |
Carcinoma Kidney Diseases |
AstraZeneca | July 25, 2017 | Phase 3 |
| NCT03778229 | Recruiting | Drug: osimertinib Drug: savolitinib |
Carcinoma | AstraZeneca | January 9, 2019 | Phase 2 |
| NCT05261399 | Recruiting | Drug: Savolitinib Drug: Osimertinib |
Carcinoma Non-Small-Cell Lung |
AstraZeneca | August 3, 2022 | Phase 3 |
| NCT03833440 | Recruiting | Drug: Savolitinib Drug: DOCETAXEL |
Non-small Cell Lung Cancer | Assistance Publique Hopitaux De Marseille |
October 8, 2019 | Phase 2 |
Potent volitinib invitro anti‐proliferative activity correlates with dysregulation of cMET expression and pharmacodynamic activity in a gastric cancer cell line panel screen.Mol Oncol. 2015 Jan; 9(1): 323–333. |
|---|
Volitinib treatment results in anti‐tumor efficacy and pharmacodynamic modulation of cMET signaling in the cMET‐driven xenograft model, Hs746t.Mol Oncol. 2015 Jan; 9(1): 323–333. |
Volitinib displays antitumor efficacy in short duration efficacy studies using cMET‐dysregulated gastric cancer patient‐derived xenograft models.Mol Oncol. 2015 Jan; 9(1): 323–333. |
Volitinib enhances the efficacy of docetaxel in both standard and patient‐derived cMET‐driven xenograft models.Mol Oncol. 2015 Jan; 9(1): 323–333. |
|---|
J Med Chem.2014 Sep 25;57(18):7577-89. |