| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
ATR ( Ki = 13 nM ); ATM ( Ki = 16 μM ); DNA-PK ( Ki = 2.2 μM ); PI3Kγ ( Ki = 3.9 μM )
VE-821 targets ataxia telangiectasia mutated and Rad3 related (ATR) kinase (IC50 = 13 nM) [1] VE-821 targets ATR kinase (IC50 = 26 nM; selectivity over ATM: IC50 > 10 μM, DNA-PKcs: IC50 > 10 μM) [2] VE-821 targets ATR kinase (IC50 = 19 nM in pancreatic cancer cells) [3] VE-821 targets ATR kinase (IC50 = 22 nM in Myc-induced lymphoma cells) [4] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:VE-821 对 ATR 表现出优异的选择性,与相关 PIKKs ATM、DNA-PK、mTOR 和 PI3K 的交叉反应性极小(Kis 分别为 16 μM、2.2 μM、>1 μM 和 3.9 μM。VE-单独使用 821 可使大部分癌细胞群死亡,但它只能可逆地限制正常细胞的细胞周期进展,死亡或长期有害影响最小。VE-821 与顺铂治疗显示出最显着的协同作用。 821 抑制 H2AX 细胞生长,IC50 为 800 nM。激酶测定:使用放射磷酸盐掺入测定测试化合物抑制 ATR、ATM 或 DNAPK 激酶活性的能力。制备由适当的缓冲液、激酶和靶标组成的储备溶液向其中添加不同浓度的 DMSO 中的目标化合物,最终 DMSO 浓度为 7%。通过添加适当的 [γ-33P]ATP 溶液开始测定,并在 25 ℃ 下孵育。测定结束后,通过添加磷酸和 ATP 至终浓度分别为 100 mM 和 0.66μM,以达到所需的时间进程。将肽捕获在磷酸纤维素膜上,按照制造商的说明进行制备,并用 200 μL 100 mM 磷酸洗涤六次,然后添加 100 μL 闪烁混合物并在 1450 Microbeta 液体闪烁计数器上进行闪烁计数。使用 GraphPad Prism 软件分析剂量反应数据。细胞测定:用 10 μM VE-821 或 DMSO 预处理 HFL1 细胞,然后添加 200 μM 顺铂 (Cis)、1 μM 吉西他滨 (Gem)、100 μM 依托泊苷 (Etop) 或 5 Gy 电离辐射 (IR)、VE-821在所有条件下阻断 Chk1 Ser345 磷酸化,并在顺铂和吉西他滨治疗中抑制 H2AX 磷酸化。在 H23 癌细胞系中,VE-821 在生长抑制方面与顺铂显示出显着的协同作用。
在ATM缺陷(GM05849)和p53缺陷(H1299)癌细胞中,VE-821(0.5–10 μM)抑制细胞增殖,IC50值分别为1.2 μM和1.8 μM。它对ATM正常(GM0637)和p53正常(A549)细胞影响极小(IC50 > 10 μM)。在缺陷细胞中,它诱导G2/M期细胞周期阻滞和凋亡(Annexin V-FITC/PI染色),与γ-H2AX(DSB标志物)升高和ATR下游底物p-Chk1降低相关[1] - VE-821 具有强效ATR激酶抑制活性(IC50 = 26 nM)和高选择性:对ATM的选择性>380倍,对DNA-PKcs的选择性>380倍,在10 μM浓度下对其他26种激酶无显著抑制作用。在ATR依赖细胞系(U2OS)中,它以浓度依赖性方式阻断羟基脲(HU)诱导的Chk1磷酸化(p-Chk1)[2] - 在胰腺癌细胞系(PANC-1、MIA PaCa-2)中,VE-821(1–10 μM)单独使用时抑制增殖(IC50 = 4.5–6.8 μM)。与放疗(2–8 Gy)或吉西他滨(0.1–1 μM)联合使用时,它增强细胞毒性:4 Gy IR + 5 μM VE-821 使PANC-1细胞存活率降低约75%(单独IR组为30%);0.5 μM吉西他滨 + 5 μM VE-821 使凋亡率升高至约60%(单独吉西他滨组为15%)[3] - 在Myc诱导淋巴瘤细胞(Eμ-Myc)中,VE-821(2–8 μM)与BET溴结构域抑制剂(JQ1,0.5 μM)具有协同作用:联合处理诱导大量DNA损伤(γ-H2AX上调)、凋亡(半胱天冬酶-3/PARP切割)、衰老(SA-β-半乳糖苷酶阳性)和内质网应激(GRP78上调)。细胞活力降低约80%(单独VE-821组为25%,单独JQ1组为30%)[4] |
| 体内研究 (In Vivo) |
在胰腺癌皮下异种移植模型(裸鼠植入PANC-1细胞)中,腹腔注射VE-821(25 mg/kg/天)持续21天,较对照组抑制肿瘤生长约55%。与吉西他滨(10 mg/kg/周,静脉注射)联合使用时,进一步使肿瘤体积减少约80%,中位生存期从35天(对照组)延长至62天[3]
- 在Eμ-Myc淋巴瘤转基因小鼠中,口服VE-821(30 mg/kg/天)+ JQ1(50 mg/kg/天)持续14天,较单药治疗抑制肿瘤生长约70%(单独VE-821组为30%,单独JQ1组为35%)。肿瘤组织中γ-H2AX、切割型半胱天冬酶-3升高,p-Chk1降低[4] |
| 酶活实验 |
放射性磷酸盐掺入测定用于确定化合物(例如VE-821)抑制ATR、ATM或DNAPK激酶活性的能力。将适当的缓冲液、激酶和目标肽混合后,形成储备溶液。为了达到 7% 的最终 DMSO 浓度,将不同 DMSO 浓度的目标化合物添加到其中。添加适当的 [g-33P]ATP 溶液后,开始测定并在 25°C 下孵育。按照所需的时间进程,分别添加终浓度为 100 mM 和 0.66 μM 的磷酸和 ATP 来终止测定。在磷酸纤维素膜上制备肽,捕获,然后用 200 μL 100 mM 磷酸洗涤六次。接下来,添加 100 μL 闪烁混合物,并使用 1450 Microbeta 液体闪烁计数器对样品进行计数。 GraphPad Prism 软件用于分析剂量反应数据[2]。
重组人ATR激酶(与ATRIP结合)与Chk1衍生肽底物和ATP在激酶缓冲液中孵育。加入0.1 nM–10 μM的VE-821,混合物在30°C孵育60分钟。通过TR-FRET法(激发光340 nm,发射光665 nm)检测磷酸化肽段,计算抑制率,非线性回归确定IC50值[1] - 采用[γ-32P]ATP的ATR激酶活性实验:纯化的ATR-ATRIP复合物与组蛋白H2AX底物、[γ-32P]ATP和VE-821(0.01–50 nM)混合。37°C孵育30分钟后进行SDS-PAGE电泳和放射自显影,量化磷酸化H2AX的放射性以计算IC50[2] - 激酶选择性面板实验:VE-821(10 μM)与28种纯化激酶(包括ATM、DNA-PKcs、PI3K)及相应底物/ATP孵育。通过放射测量法或荧光法检测激酶活性,计算抑制百分比以评估选择性[2] |
| 细胞实验 |
将 MiaPaCa-2、PSN-1 和 Panc1 细胞 (5×104) 接种于 96 孔板中,4 小时后和 1 小时前用浓度逐渐增加的 VE-821 处理。暴露于单次 4 Gy 剂量的辐射。辐射后 72 小时更换培养基后,使用 Alamar Blue 测定法测定活力。让细胞增殖后,在第 10 天再次检查每种不同治疗方案的细胞活力。未处理(对照组)组的细胞活力和存活率已实现正常化 [3]。
细胞系从ATCC购买,并根据经销商的说明进行维护。细胞测定采用指数生长培养。使用免疫荧光显微镜(IF)分析H2AX磷酸化,将细胞固定在4%甲醛中,0.5% Triton X-100渗透,并用小鼠H2AX pS139抗体、AlexaFluor 488山羊抗小鼠抗体和Hoechst染色。然后使用BD Pathway 855生物成象仪和BD Attovision软件对细胞进行分析。采用CellTiter 96水细胞增殖(MTS)法分析细胞密度。细胞被镀在96孔板中并粘附过夜。第二天,按指定浓度加入化合物,终体积为200 μL,细胞孵育96 h,加入MTS试剂(40 μL), 1 h后,用SpectraMax Plus 384板读板仪测定490 nm处吸光度。采用Macsynergy软件评价协同作用和拮抗作用。[2] 细胞活力/凋亡检测:癌细胞(每孔5×103个)接种于96孔板,用VE-821(0.1–20 μM)单独处理或与IR/吉西他滨/JQ1联合处理48–72小时。CCK-8法检测活力;Annexin V-FITC/PI染色结合流式细胞仪检测凋亡[1,3,4] - 细胞周期分析:ATM/p53缺陷细胞用VE-821(3 μM)处理24小时,70%乙醇固定,PI/RNase溶液染色,流式细胞仪分析G2/M期积累情况[1] - Western blot分析:VE-821(1–10 μM)处理24–48小时的细胞裂解提取总蛋白。等量蛋白经SDS-PAGE电泳、转膜至PVDF膜,用抗ATR、p-ATR、Chk1、p-Chk1、γ-H2AX、半胱天冬酶-3、切割型半胱天冬酶-3、PARP、切割型PARP、GRP78或GAPDH(内参)抗体孵育,化学发光显影条带[1,2,3,4] - 克隆形成存活实验:胰腺癌细胞用VE-821(2.5–5 μM)处理1小时后,暴露于IR(2–8 Gy),接种于6孔板。14天后结晶紫染色克隆并计数,计算存活分数[3] - 衰老实验:Eμ-Myc细胞用VE-821 + JQ1处理72小时,甲醛固定,SA-β-半乳糖苷酶溶液染色,显微镜下计数衰老细胞(蓝色染色)[4] |
| 动物实验 |
胰腺癌异种移植模型:将PANC-1细胞(5×10⁶/只)皮下注射到4周龄雄性裸鼠体内。当肿瘤体积达到约100 mm³时,将小鼠分为4组(每组n=6):对照组、VE-821单药治疗组(25 mg/kg/天,腹腔注射)、吉西他滨单药治疗组(10 mg/kg/周,静脉注射)和联合治疗组。VE-821溶于5% DMSO + 95%生理盐水中;治疗持续21天。每3天测量一次肿瘤体积(长×宽²/2)和体重[3] - Eμ-Myc淋巴瘤模型:将6周龄雄性转基因Eμ-Myc小鼠(可触及肿瘤)随机分为4组(每组n=8):对照组、VE-821单药治疗组(30 mg/kg/天,口服)、JQ1单药治疗组(50 mg/kg/天,口服)和联合治疗组。VE-821溶于0.5% CMC溶液中;治疗持续14天。每2天测量一次肿瘤大小,并记录生存情况[4] |
| 毒性/毒理 (Toxicokinetics/TK) |
体外毒性:VE-821(浓度高达 20 μM)对正常人胰腺导管上皮细胞 (HPDE) 或正常淋巴细胞(存活率 >85% vs. 对照组)无显著细胞毒性[1,3]
- 体内急性毒性:小鼠单次腹腔注射VE-821(浓度高达 150 mg/kg)或口服(浓度高达 200 mg/kg)后,14 天内未出现死亡或严重毒性症状(嗜睡、体重减轻)[3,4] - 体内长期毒性:小鼠接受VE-821(25–30 mg/kg/天,持续 14–21 天)治疗后,与对照组相比,体重、肝功能(ALT、AST)或肾功能(BUN、肌酐)均无显著变化。肝脏、肾脏和心脏组织的组织学检查未发现异常病变[3,4] - 血浆蛋白结合率:VE-821在人血浆中的血浆蛋白结合率为93%,在小鼠血浆中的血浆蛋白结合率为90%(平衡透析试验)[2] |
| 参考文献 |
|
| 其他信息 |
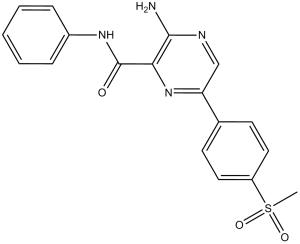
3-氨基-6-(4-甲基磺酰基苯基)-N-苯基-2-吡嗪甲酰胺是一种芳香酰胺。
DNA损伤剂是最常用的抗癌药物之一。然而,它们对大多数癌症的疗效有限。这可能归因于基因组维护网络——DNA损伤反应(DDR),该网络能够识别并修复受损的DNA。ATR是DDR的主要调节因子,也是一个极具吸引力的抗癌靶点。本文中,我们描述了一系列具有强效且选择性ATR抑制作用的氨基吡嗪类化合物的发现。化合物45对ATR的抑制常数Ki为6 nM,对相关激酶ATM或DNA-PK的选择性超过600倍,并且在细胞中以IC50为0.42 μM阻断ATR信号通路。利用该化合物,我们发现ATR抑制显著增强了DNA损伤剂在某些癌细胞而非正常细胞中诱导的细胞死亡。癌细胞和正常细胞之间这种不同的反应凸显了ATR抑制剂作为一种新型机制的巨大潜力,它有望显著提高许多现有药物和电离辐射的疗效。[2] 放射疗法和吉西他滨等DNA损伤药物常用于治疗胰腺癌。然而,这些治疗通常疗效有限。因此,提高胰腺癌患者的低生存率仍然是肿瘤学领域的一项重大挑战。抑制关键的DNA损伤反应激酶ATR被认为是一种提高肿瘤细胞对DNA损伤药物敏感性的有效方法,但特异性ATR抑制剂仍未研制成功。本文在体外研究了首个高选择性、高活性ATR抑制剂VE-821的增敏潜力。VE-821抑制了辐射和吉西他滨诱导的Chk1磷酸化,证实了其对ATR信号通路的抑制作用。 VE-821 持续显著增强了 PSN-1、MiaPaCa-2 和原代 PancM 胰腺癌细胞在常氧和缺氧条件下对放射线和吉西他滨的敏感性。VE-821 对 ATR 的抑制导致癌细胞放射诱导的 G2/M 期阻滞被抑制。VE-821 治疗后癌细胞放射存活率降低,同时伴有 DNA 损伤增加和同源重组修复抑制,分别表现为 γH2AX 和 53BP1 灶的持续存在以及 Rad51 灶的抑制。这些发现支持将 ATR 抑制作为一种提高标准癌症治疗疗效和治疗指数的新方法,适用于大部分胰腺癌患者。[3] 抑制溴结构域和末端外结构域 (BET) 家族的表观遗传阅读蛋白已被证明具有强大的抗肿瘤活性,这通常归因于转录抑制。本研究表明,两种结构不同的BET抑制剂(BETi)在亚致死浓度下即可干扰小鼠Myc诱导的淋巴瘤细胞的复制和细胞周期进程,而转录组基本保持不变。这种复制抑制与DNA损伤反应以及对上游复制应激传感器ATR抑制剂的敏感性增强相一致,这在体外和B细胞淋巴瘤小鼠模型中均有体现。机制上,ATR和BETi联合治疗可引起参与细胞死亡、衰老相关分泌途径、NF-κB信号通路和内质网应激的基因发生显著的转录变化。我们的数据表明,BETi可以增强ATR抑制剂引起的细胞应激和死亡。这表明,ATRi 可用于淋巴瘤的联合治疗,而无需使用基因毒性药物。[4] VE-821是一种合成的小分子 ATR 激酶抑制剂,旨在与 ATR 的 ATP 结合口袋结合并阻断其催化活性。[2] - 其作用机制涉及抑制 ATR 介导的 DNA 损伤修复,导致 DSB 积累、细胞周期阻滞和细胞凋亡——尤其是在 ATM/p53 缺陷或高复制应激的癌细胞中(例如,Myc 驱动的淋巴瘤、胰腺癌)[1,4] - VE-821通过靶向 ATR-Chk1 DNA 损伤反应通路,增强放疗和化疗(吉西他滨)在胰腺癌中的疗效,克服治疗耐药性。[3] - 与 BET 抑制剂(JQ1)的协同作用归因于 DNA 损伤、衰老和内质网应激的联合诱导。为Myc诱导的淋巴瘤提供潜在的治疗策略[4] |
| 分子式 |
C18H16N4O3S
|
|
|---|---|---|
| 分子量 |
368.41
|
|
| 精确质量 |
368.094
|
|
| 元素分析 |
C, 58.68; H, 4.38; N, 15.21; O, 13.03; S, 8.70
|
|
| CAS号 |
1232410-49-9
|
|
| 相关CAS号 |
|
|
| PubChem CID |
51000408
|
|
| 外观&性状 |
White to beige solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 沸点 |
568.4±50.0 °C at 760 mmHg
|
|
| 闪点 |
297.6±30.1 °C
|
|
| 蒸汽压 |
0.0±1.6 mmHg at 25°C
|
|
| 折射率 |
1.658
|
|
| LogP |
2.93
|
|
| tPSA |
126.91
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
4
|
|
| 重原子数目 |
26
|
|
| 分子复杂度/Complexity |
578
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
S(C([H])([H])[H])(C1C([H])=C([H])C(C2=C([H])N=C(C(C(N([H])C3C([H])=C([H])C([H])=C([H])C=3[H])=O)=N2)N([H])[H])=C([H])C=1[H])(=O)=O
|
|
| InChi Key |
DUIHHZKTCSNTGM-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C18H16N4O3S/c1-26(24,25)14-9-7-12(8-10-14)15-11-20-17(19)16(22-15)18(23)21-13-5-3-2-4-6-13/h2-11H,1H3,(H2,19,20)(H,21,23)
|
|
| 化学名 |
3-amino-6-(4-methylsulfonylphenyl)-N-phenylpyrazine-2-carboxamide
|
|
| 别名 |
VE-821; VE 821; 1232410-49-9; 3-Amino-6-(4-(methylsulfonyl)phenyl)-N-phenylpyrazine-2-carboxamide; VE 821; VE821; 3-Amino-6-[4-(methylsulfonyl)phenyl]-N-phenyl-2-pyrazinecarboxamide; BF884TQ935; 3-amino-6-(4-methylsulfonylphenyl)-N-phenylpyrazine-2-carboxamide; VE821
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|---|
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.7144 mL | 13.5718 mL | 27.1437 mL | |
| 5 mM | 0.5429 mL | 2.7144 mL | 5.4287 mL | |
| 10 mM | 0.2714 mL | 1.3572 mL | 2.7144 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
 VE-821 perturbs the irradiation-induced cell cycle checkpoint in pancreatic cancer cells.Cancer Biol Ther.2012 Sep;13(11):1072-81. |
 VE-821 radiosensitizes pancreatic tumor cells under hypoxic conditions.Cancer Biol Ther.2012 Sep;13(11):1072-81. |
VE-821 radiosensitizes pancreatic tumor cells.Cancer Biol Ther.2012 Sep;13(11):1072-81. |
|---|
 VE-821 sensitizes pancreatic cancer cells to gemcitabine treatment.Cancer Biol Ther.2012 Sep;13(11):1072-81. |
 VE-821 increases 53BP1 and γH2AX foci number and reduces Rad51 foci formation.Cancer Biol Ther.2012 Sep;13(11):1072-81. |